Слайд 2

Медь
Медь — элемент одиннадцатой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 29.
Обозначается символом Cu
Слайд 3

Физические свойства
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой.
Медь обладает высокой тепло и электропроводностью, занимает второе место по электропроводности после серебра.
Слайд 4

Нахождение в природе.
Медь встречается в природе как в соединениях, так и
в самородном виде. Нередко встречаются месторождения меди в осадочных породах — медистые песчаники и сланцы. Содержание меди в руде составляет от 0,3 до 1,0 %.
Слайд 5

Применение
Медь широко применяется в электротехнике для изготовления силовых кабелей, проводов или других проводников. Теплопроводимость меди
позволяет применять её в различных теплоотводных устройствах: радиаторах охлаждения,кондиционироввания и отопления. Медь широко используется для производства медных труб применяющихся для транспортировки жидкостей и газов.
Слайд 6

Медь широко используется для производства медных труб применяющихся для транспортировки жидкостей
и газов.
Слайд 7

Ювелирные сплавы
В ювелирном деле часто используются сплавы меди с золотом для увеличения
прочности изделий к деформациям и истиранию, так как чистое золото — очень мягкий металл и нестойко к этим механическим воздействиям.
Слайд 8

Медная кровля. Широко применяется медь в архитектуре. Кровли и фасады из
тонкой листовой меди из-за автозатухания процесса коррозии медного листа служат безаварийно по 100—150 лет.
Слайд 9

Влияние на экологию
При открытом способе добычи меди, после её прекращения карьер
становится источником токсичных веществ. Самое токсичное озеро в мире — Беркли Пит — образовалось в кратере медного рудника. Оно находится в Штате Монтана в США.
Слайд 10

Графит
Графи́т—уникальный самородный минерал, аллотропная модификация элемента углерода, наиболее устойчивая в земной
коре.
Слайд 11

Физические свойства
Цвет графита варьирует от железо-черного до стального серого с характерным
металлическим блеском. На ощупь минерал жирный, скользкий, пачкает пальцы и бумагу, при механическом воздействии расслаивается на отдельные чешуйчатые частицы. Именно это свойство графита позволяет применять его в карандашах.
По сравнению с алмазом графит обладает меньшей твердостью и плотностью, а также графит электропроводен. Его теплопроводность зависит от степени нагрева.
Графит обладает чрезвычайной огнеупорностью, его температура сгорания - 38500С
Слайд 12

Применение
в металлургии графит используется для производства тугоплавких тиглей, чехлов для термопар,
емкостей для кристаллизации. В литейном производстве графитовый порошок используется в качестве антипригарной присыпки, а также для смазывания литейных форм. Кроме производства карандашей, графит используется для изготовления красок и термостойких смазочных материалов, для наполнения пластмасс. Из коллоидно-графитовых смесей таких как графит С-1 изготавливают шлифовальные и полировочные пасты.
Слайд 13

Слайд 14

Слайд 15

Алмаз
Алма́з — минерал, кубическая аллотропная форма углерода. При нормальных условиях метастабилен, то есть может существовать неограниченно долго.
В вакууме или в инертном газе при повышенных температурах постепенно переходит в графит.
Формула С примесь N.
Слайд 16

Физические свойства
Главные отличительные черты алмаза — высочайшая среди минералов твёрдость (но в то же
время хрупкость), наиболее высокая теплопроводность среди всех твёрдых тел большой показатель преломления и дисперсия. Алмаз является диэлектриком. У алмаза очень низкий коэффициент трения по металлу на воздухе. Для алмаза также характерны самый высокий модуль упругости и самый низкий коэффициент сжатия.
Слайд 17

Алмазы подразделяются на ювелирные и технические. К первым относятся прозрачные, бесцветные
или слабо окрашенные разности более или менее крупных размеров; к техническим — тёмноокраминные разности и алмазы мелких размеров. В месторождениях, как правило, преобладают технические алмазы, реже встречаются ювелирные сорта.
















 Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Теория электролитической диссоциации
Теория электролитической диссоциации Мини-проект по дисциплине: Физико-химические методы исследования и техника лабораторных работ
Мини-проект по дисциплине: Физико-химические методы исследования и техника лабораторных работ Платина. Физические и химические свойства
Платина. Физические и химические свойства Электролит және бейэлектролит ерітінділердің коллигативті қасие
Электролит және бейэлектролит ерітінділердің коллигативті қасие Благородные металлы
Благородные металлы Технология оптического стекла
Технология оптического стекла Закономерности управления каталитическими процессами
Закономерности управления каталитическими процессами Характеристика элементов VI группы .Кислород. Озон
Характеристика элементов VI группы .Кислород. Озон Оксиды. 8 класс
Оксиды. 8 класс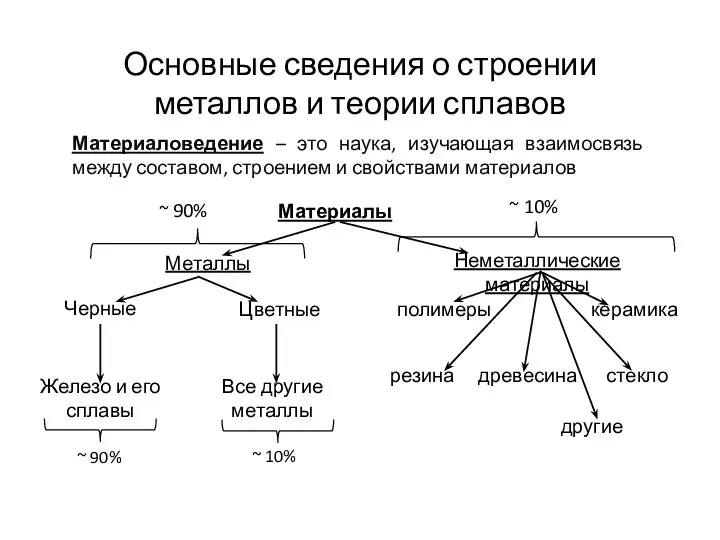 Основные сведения о строении металлов и теории сплавов
Основные сведения о строении металлов и теории сплавов Основы электрохимии. Электрохимические процессы
Основы электрохимии. Электрохимические процессы Ионное произведение воды. Водородный показатель
Ионное произведение воды. Водородный показатель Металдардың химиялық белсенділігі
Металдардың химиялық белсенділігі Измерение и оценка химического фактора. Лекция 9
Измерение и оценка химического фактора. Лекция 9 Алюминий и его соединения
Алюминий и его соединения Соединения азота. Оксиды азота
Соединения азота. Оксиды азота Молибденовые сплавы
Молибденовые сплавы Активационный анализ
Активационный анализ Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Современные химические технологии
Современные химические технологии Атом. Модели строения атома
Атом. Модели строения атома Введение в геохимию
Введение в геохимию Цитрусты жемістерді жерорта теңізінің жеміс шыбынынан, тұқымдық және азық-түліктік картопты картоп күйесіне қарсы бромды
Цитрусты жемістерді жерорта теңізінің жеміс шыбынынан, тұқымдық және азық-түліктік картопты картоп күйесіне қарсы бромды Химическое равновесие и условия его смещения
Химическое равновесие и условия его смещения Оксиды. Классификация. Получение. Свойства
Оксиды. Классификация. Получение. Свойства Органическая химия
Органическая химия Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение
Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение