Содержание
- 2. Тотығу түрлері. Оксидазды тотығу 2. Липидтердің пероксидті тотығуы (ЛПТ), Оксигеназды тотығу Пероксидазды тотығу 90%Оттек оксидазды тотығуға
- 3. Оксидазды тотығу=БТ Оттек молекуласы 4е- электронмен тотықсызданады. SН2+ ½ О2 S+ Н2О +Е субстрат МАҢЫЗЫ: 1.
- 4. ЛИПИДТЕРДІҢ ПЕРОКСИДТІ ТОТЫҒУЫ (ЛПТ) ЖӘНЕ ОНЫҢ РӨЛІ.
- 5. ПРООКСИДАНТТАР -ЛИПИДТЕРДІҢ ПЕРОКСИДТІ ТОТЫҒУЫН (ЛПТ) ТУҒЫЗАТЫН ЗАТТАР. АНТИОКСИДАНТТАР -ЛПТ ТЕЖЕЙТІН ЗАТТАР.
- 6. ЛПТ дегеніміз – майлардың, әсіресе мембранадағы фосфолипидтер құрамына кіретін көп қанықпаған май қышқылдарының (КҚМҚ) бос радикалдық
- 8. Бос радикал дегеніміз не? Сыртқы валенттік орбитасында жұптаспаған электроны бар атом немесе атом топтары. Свободные радикалы
- 9. КӨП ҚАНЫҚПАҒАН МАЙ ҚЫШҚЫЛДАРЫ (КҚМҚ) ( ВИТАМИН F, ЭССЕНЦИАЛДЫ МАЙ ҚЫШҚЫЛДАРЫ, АЛМАСТЫРЫЛМАЙТЫН МАЙ ҚЫШҚЫЛДАРЫ) С17Н31СООН-ЛИНОЛЬ 18
- 10. Животные – наиболее ценные среди них – жиры морской рыбы (содержат незаменимые ПНЖК) Растительные – содержат
- 11. Оттек молекуласы әр түрлі реакциялардан бір-бірден электронды қосып алып тотықсызданып оттектің активті формаларына (ОАФ) айналуы мүмкін.
- 14. +2Н+ Н2О2 + О2 О2 + ОН∙ - + ОН∙ (реакция Хабера-Вайса) + О2∙ - ОН
- 15. ОТТЕГlНlҢ АКТИВТl ФОРМАЛАРЫ (ОАФ) O2*- Супероксид-анион OH- Гидроксил радикалы NО- АЗОТ ОКСИДlНlН РАДИКАЛЫ ж/е т.б. LOO
- 16. НОСl- гипохлорит-анион O3 - озон LOOH (ГПЛ)-липидтер гидропероксиді 'O2 Синглетті оттек H2O2 Сутек асқын тотығы
- 17. Супероксидті радикал түзіледі: оттек ауыспалы валентті металдармен әрекеттескенде м\лы, Fe++ + О2 ? Fe+++ + О2•
- 18. Гидроксиль радикалы түзіледі: сутек асқын тотығынан (реакция Фентона): Fe++ + Н2О2 ? Fe+++ + ОН• +
- 20. Transition metal-catalyzed formation of free radicals X-H + Cu+2 → X• + H+ + Cu+ X-H
- 21. Бос радикалдар қайдан пайда болады?
- 22. ОАФ-ың түзілуіне әкелетін себептер: антиоксиданттық жүйенің жеткіліксіздігі, радиация сәулесі, шылым шегу, алкоголизм, қоршаған ортаның ластануы, қартаю,
- 23. ЛПТ реакциялары ОАФ әсерінен сатылы тізбекті реакция арқылы іске асады. 1-сатысы: тізбекті реакцияның басталуы – инициация.
- 24. л2-сатысы: Түзілген липид радикалы (L1∙) ары қарай оттек молекуласымен (О2) тез реакцияласып май қышқылының пероксид радикалын
- 25. Түзілген май қышқылының радикалы қайтадан 2-ші реакцияға одан кейін 3-ші реакцияға түсіп тағыда радикалдар түзіледі. Бұл
- 26. О•2 О2 L2Н О2 L3Н О2 L1Н L•1 L1OО• L•2 L2OО• L•3……….. L1OОН L2OОН КҚМҚ
- 27. Липидтердің пероксидті тотығуының алғашқы өнімі: ДИЕНДl КОНЪЮГАТТАР Аралық өнімдері: ГИДРОПЕРОКСИДТЕР Соңғы өнімдерінің бірі: МАЛОН ДИАЛЬДЕГИДl (МДА)
- 28. L1Н L•1 L1OО• L•2 L 2H L1OОН
- 30. ─Қалыпты жағдайда организмде Бос радикалды процесс жүреді ме? ─Үнемі, аз мөлшерде. Себебі, ағзадағы антиоксиданттық жүйе оны
- 31. ЛПТ не үшін керек? ЛПТ биологиялық маңызы: Биомембрананың өткізіштігін арттырады; Мембрананың липидтік құрамының жаңалануын қамтамасыз етеді;
- 32. Арахидон қышқылынан простагландиндер (ПГ) ж/е олардың туындыларын түзеді (простациклиндер, тромбоксандар, лейкотриендер); Ксенобиотиктер мен метаболизмнің улы өнімдерін
- 33. иммунды жүйенің қызметіне қатысады Бактерияларды жояды. М\ы, жедел қабыну кезінде лейкоциттер (әсіресе нейтрофилдер) НАДФН-ЦхР450-оксидаза жүйесі және
- 34. ФЕРМЕНТТІ СУПЕРОКСИДДИСМУТАЗА (СОД); КАТАЛАЗА; ГЛУТАТИОНРЕДУКТАЗА ГЛУТАТИОНПЕРОКСИДАЗА ФЕРМЕНТТІ ЕМЕС АНТИОКСИДАНТТАР Майда еритін витаминдер: А ж\е Е; С,Р
- 35. Супероксиддисмутаза катализдейтін реакция: О2- + О2- + 2Н+→ Н2О2+О2 Каталаза катализдейтін реакция: 2 Н2О2→2Н2О +О2 Глутатионпероксидаза
- 36. Н202 Fe2+ OH. Н20 Glu-SH NAD NADРH2 GSSG Каталаза Пероксидаза Глутатион редуктаза 02.- СОД
- 38. белоктардың SH тобына әсер етіп , оларың денатурациясын ж/е ферменттердің белсенділігін төмендетеді; жасуша мембранасының қызметтерін бұзады
- 39. БИОМЕМБРАНАДАҒЫ КҚМҚ-ын ыдыратып жасуша н/е органеллаларды зақымдайды, ЯДРО,МИТОХОНДРИЯ , БЕЛОК , НУКЛЕИН ҚЫШҚЫЛДАРЫ, ЛИПИДТЕР т.б. ЗАҚЫМДАЙТЫН
- 40. ОКИСЛИТЕЛЬНЫЙ СТРЕСС И ДЕСТРУКЦИЯ КЛЕТКИ
- 42. Бос радикалдар жасушаларға әсер етіп, олардың ДНҚ-сын, белоктарын, майларын зақымдайтын жоғары активті бөлшектер
- 43. Оксиданттық стресс және антиоксиданттық қорғаныс жүйесі
- 46. Антиоксиданттық система .
- 48. Aнтиоксиданттар Антиоксиданттар бос радикалға электронын беріп оларды нейтралдайды.
- 50. Избыток антиоксидантов вызывает прооксидантный эффект GluSH GS-SG α-Tocoferol α-Tocoferyl* Ascorbat Asc* АО АО* е* АФК NADH2
- 51. РЕГУЛЯЦИЯ
- 52. Витамин Е антиоксид ретінде Зақымдалған фосфолипидтер Бос радикал Қанықпаған майқышқылы Қос мембрана Нейтралданған бос радикал Витамин
- 53. C и E как Кo-Aнтиоксиданты Поскольку кислород реагирует с цепью ЖК, изменяется дипольный момент и это
- 54. C и E как Кo-Антиоксиданты (2) Липид Витамин Е Витамин Е удаляет пероксильный радикал и превращается
- 56. + 2 Н2О
- 57. ВОЗМОЖНО ЛИ ПРЕДОТВРАТИТЬ ИЛИ УДАЛИТЬ СШИВКИ? Вещества, используемые для предотвращения и удаления сшивок в коже. Карнозин
- 58. Оксигеназды тотығу эндоплазмалық ретикулум мембрансы (микросома) ж/е митохондрия мембранасының ішкі жағында жүреді. Оксигеназды тотығу 2 түрлі
- 59. Монооксигеназдық тотығуда оттектің бір атомы субстратпен байланысады ал 2-сі су молекуласын түзуге жұмсалады: RH+O2+NADPH2→ROH+H2O+ NADP+ Диоксигеназдық
- 60. Реакция микросомаларда, әсіресе залалсыздандыру бауырда жүреді. Мембранамен байланысқан НАДФН2, ФП ж\е цхР450 мультиферментті жүйе қатысады. Он
- 61. Оксигеназды тотығудың маңызы Бұл процестің қатысуымен Д витаминнің ауыспалы активті түрлері (1,25 (ОН)2Д3), стероидты гормондардың өт
- 62. Микросомальное окисление - совокупность реакций первой фазы биотрансформации ксенобиотиков и эндогенных соединений, катализирующихся ферментными системами мембран
- 65. Пероксидаздық тотығу Бұл процесс пероксисомаларда жүреді. Бұл процесте Н2О2 түзіледі. Пероксидаздық тотығуға АҚ-ның, биогенді аминдердің, пуриндердің
- 66. Пероксидаздық тотығу ксантиноксидаза Ксантин + Н2О + O2 --------------- несеп қышқылы + Н2О2 каталаза 2 Н2О2
- 68. Скачать презентацию
 Яды и химикаты
Яды и химикаты Водород
Водород Нахождение металлов в природе. Общие способы получения металлов. 9 класс
Нахождение металлов в природе. Общие способы получения металлов. 9 класс Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Общая характеристика элементов IБгруппы. Медь. Серебро. Золото
Общая характеристика элементов IБгруппы. Медь. Серебро. Золото Бальзам-ополаскиватель для волос
Бальзам-ополаскиватель для волос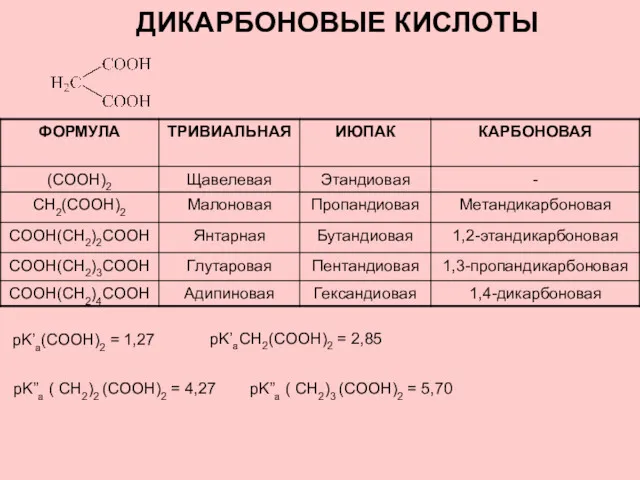 Дикарбоновые кислоты
Дикарбоновые кислоты Классы неорганических веществ (лекция № 4)
Классы неорганических веществ (лекция № 4) Химиядан сұрақтар
Химиядан сұрақтар Основное уравнение молекулярно-кинетической теории. Идеальный газ
Основное уравнение молекулярно-кинетической теории. Идеальный газ Белки. Аминокислоты
Белки. Аминокислоты Классификация органических соединений
Классификация органических соединений Общая характеристика неметаллов
Общая характеристика неметаллов Генетические ряды металлов, образующих нерастворимый гидроксид
Генетические ряды металлов, образующих нерастворимый гидроксид Бытовая химия
Бытовая химия Строение атома. 8 класс
Строение атома. 8 класс Білки (протеїни)
Білки (протеїни) Математические модели химических реакторов
Математические модели химических реакторов Класифікація, будова та номенклатура органічних сполук
Класифікація, будова та номенклатура органічних сполук Ферроқорытпа. Кремний және Хром
Ферроқорытпа. Кремний және Хром Йони. Йонний зв’язок, його утворення
Йони. Йонний зв’язок, його утворення Простые вещества (урок для 8 класса)
Простые вещества (урок для 8 класса) Кислоти. Фізичні властивості кислот
Кислоти. Фізичні властивості кислот Каталитические процессы нефтепереработки
Каталитические процессы нефтепереработки Молярная масса вещества
Молярная масса вещества Аррениус Сванте Август
Аррениус Сванте Август Розрахункові задачі. Розрахунки за хімічними рівняннями маси, об’єму, кількості речовини реагентів та продуктів. Хімія. 8 клас
Розрахункові задачі. Розрахунки за хімічними рівняннями маси, об’єму, кількості речовини реагентів та продуктів. Хімія. 8 клас Свойства растворов высокомолекулярных соединений
Свойства растворов высокомолекулярных соединений