Содержание
- 2. Периодическая система химических элементов Д.И. Менделеева
- 3. Ионная связь металл + неметалл Na + 11 ) ) ) 2 8 1 Cl +
- 4. Все вещества с ионной связью имеют немолекулярное строение Ионная кристаллическая решетка
- 5. Химическая связь, образованная посредством общих электронных пар, называется атомной или ковалентной Ковалентная химическая связь Ковалентная полярная
- 6. Ковалентная неполярная связь
- 7. Ковалентная неполярная связь Вариант 1 Структурная формула Н Н
- 8. Ковалентная неполярная связь F Вариант 1 Структурная формула + F
- 9. Ковалентная неполярная связь Вариант 1 Структурная формула
- 10. Ковалентная полярная связь
- 11. Ковалентная полярная связь
- 12. Ковалентная полярная связь Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. электроотрицательность
- 13. Ковалентная полярная связь Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. электроотрицательность
- 14. Ковалентная полярная связь Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. электроотрицательность
- 15. Ковалентная полярная связь Ряд неметаллов F, O, N, Cl, Br, S, C, P, Si, H. электроотрицательность
- 16. + + + + + + + + + + + + + + + +
- 17. Как определить вид связи в веществе? Определите природу химических элементов Если только металл только неметаллы металл
- 18. Определите вид связи в следующих веществах: Н2, Na, NaF, H2S, NH3, O2, Zn, CaS, Mg3N2, CH4,
- 19. Ионная Ковалентная неполярная Ковалентная полярная Металлическая Н2, Na, NaF, H2S, NH3, O2, Zn, CaS, Mg3N2, Al,
- 20. Химическую связь между атомами водорода одной молекулы (или её части) и атомами наиболее электоротрицательных элементов, имеющих
- 21. Водородная связь Межмолекулярная Возникает между молекулами Внутримолекулярная Возникает внутри молекулы
- 22. Межмолекулярная водородная связь 1)между молекулами воды
- 23. Межмолекулярная водородная связь 2)между молекулами аммиака
- 24. Межмолекулярная водородная связь 3)между молекулами спиртов (метанол, этанол, пропанол, этиленгликоль, глицерин)
- 25. Межмолекулярная водородная связь 4)между молекулами карбоновых кислот (муравьиная, уксусная) (димеры карбоновых кислот)
- 26. Внутримолекулярная водородная связь возникает 1)внутри молекул белков (водородная связь удерживает витки спирали пептидной молекулы)
- 28. Скачать презентацию
 Закономерности изменения свойств химических элементов
Закономерности изменения свойств химических элементов Характеристика элемента по его положению в периодической системе химических элементов (1)
Характеристика элемента по его положению в периодической системе химических элементов (1) Элементы подгруппы углерода
Элементы подгруппы углерода Полимеры. Структура и свойства
Полимеры. Структура и свойства Металлы побочных подгрупп. Марганец. Хром. (Лекция 15)
Металлы побочных подгрупп. Марганец. Хром. (Лекция 15)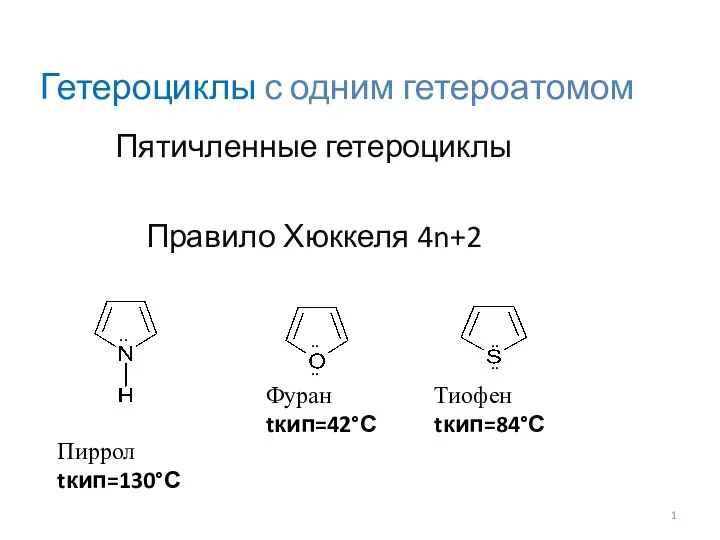 Гетероциклы с одним гетероатомом
Гетероциклы с одним гетероатомом Двойной электрический слой. Теория Гельмгольца
Двойной электрический слой. Теория Гельмгольца Химия в повседневной жизни
Химия в повседневной жизни Распространенные названия некоторых неорганических веществ
Распространенные названия некоторых неорганических веществ Радиоактивные элементы почв
Радиоактивные элементы почв Основные классы неорганических соединений. Химические свойства неорганических веществ
Основные классы неорганических соединений. Химические свойства неорганических веществ Химические свойства простых металлов, неметаллов и оксидов. Задание 6 по ЕГЭ
Химические свойства простых металлов, неметаллов и оксидов. Задание 6 по ЕГЭ Коллоидно-дисперсные системы
Коллоидно-дисперсные системы Теория сплавов
Теория сплавов Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Удобрения и их классификация
Удобрения и их классификация Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Теории происхождения нефти
Теории происхождения нефти Типы химических реакций
Типы химических реакций Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Карбоксильные соединения. Гидроксикислоты, кетонокислоты
Карбоксильные соединения. Гидроксикислоты, кетонокислоты Предельные углеводороды. Алканы. 10 класс
Предельные углеводороды. Алканы. 10 класс СОҢҒЫ СТ ДАЙЫНДЫҚ!
СОҢҒЫ СТ ДАЙЫНДЫҚ! Спирти. Феноли. Етери
Спирти. Феноли. Етери Минеральные вещества
Минеральные вещества Свинец
Свинец Строение атома. Лекция 2
Строение атома. Лекция 2 Химия өнеркәсібіндегі энергетикалық ресурстар
Химия өнеркәсібіндегі энергетикалық ресурстар