Содержание
- 2. ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯ МАКРОМОЛЕКУЛА: совокупность атомов или атомных групп, разных или одинаковых по химической природе,
- 3. Полимеры образуются в результате: Реакций (со)полимеризации и (со)поликонденсации мономеров; Полимераналогичных превращений в полимерах. (Со)Полимеризация - процесс
- 4. Основные понятия и определения курса Если строение повторяющегося звена совпадает по природе атомов, по количеству атомов,
- 5. Основные понятия и определения курса Составное повторяющееся звено (СПЗ) - наименьшее составное звено (атом или группа
- 6. гомополимеров: сополимеров: Основные понятия и определения курса Полипропилен (ПП) Полиэтилен (ПЭ) Полибутадиен (СКД) Бутадиен-нитрильный каучук (БНКС)
- 7. Основные понятия и определения курса Структурные элементы макромолекулы ПП Структурные элементы макромолекул
- 8. Основные понятия и определения курса
- 9. Основные понятия и определения курса где ММпол - молекулярная масса полимера Мзв - молекулярная масса повторяющегося
- 10. Олигомеры - соединения, построенные из повторяющихся мономерных единиц, при этом степень полимеризации невелика (олигос – немного),
- 11. Основные отличия от низкомолекулярных веществ
- 12. Адгезионные («клейкие») свойства полимеров
- 13. Основное фундаментальное свойство макромолекул – ГИГАНТСКАЯ АССИМЕТРИЯ
- 14. Из-за ассиметрии макромолекулы легко изгибаются и принимают различные пространственные формы, известные как конформации Следствие ассиметрии макромолекул
- 15. Основные отличия ВМС от НМС Способны существовать только в конденсированном (твердом или жидком) состоянии. Растворы полимеров
- 16. Процесс растворения полимера даже в «хорошем» растворителе через стадию набухания Сущность высокоэластической деформации полимеров Основные отличия
- 17. Классификация, строение, номенклатура, изомерия полимеров по происхождению 1. природные 2. искусственные 3. синтетические по геометрии основной
- 18. По происхождению Природные (натуральные) – полимеры, выделенные из сырья животного, растительного, микробиологического, минерального происхождения. Образуются в
- 19. Природные Классификация полимеров
- 20. Искусственные Синтетические Классификация полимеров
- 21. Органические Карбоцепные (полиэтилен, полистирол) Гетероцепные (полиамиды, полиэфиры) Элементоорганические (силоксаны, полифосфазены) Неорганические (полифосфаты, полисиликаты) Классификация полимеров по
- 22. Классификация полимеров по природе мономерного звена Органические Синтетические Карбоцепные (полиэтилен, полистирол) Основная цепь Боковые группы
- 23. Классификация полимеров по природе мономерного звена Органические Синтетические Гетероцепные (полиамиды, полиэфиры) найлон лавсан
- 24. Классификация полимеров по природе мономерного звена Элементоорганические (силоксаны, полифосфазены)
- 25. Классификация полимеров по природе мономерного звена Неорганические (полифосфаты, полисиликаты)
- 26. Термопластичные и термореактивные полимеры Термопластичные полимеры При нагревании плавятся. По достижении определенной температуры переходят в вязкие
- 27. Термореактивные полимеры При нагревании не плавятся. При достижении определенной температуры начинается разрыв полимерных цепей, сопровождающийся химическими
- 28. ХАРАКТЕРИЗУЕТСЯ: Структура (со)полимеров Параметры молекулярной структуры Параметр над- молекулярной структуры
- 29. Молекулярная структура полимеров Параметр: микроструктура макромолекул конфигурация звена – изомерная форма звена; конфигурация ближнего порядка –
- 30. в ненасыщенных полимерах в насыщенных полимерах цис- и транс- изомеры L- и D- изомеры плоскость зеркала
- 31. Виниловые полимеры “голова к хвосту” “хвост к хвосту” “голова к голове” Молекулярная структура полимеров участок цепи,
- 32. Диеновые полимеры 1,4 – 1,2 – 3,4 - (при наличии заместителя) Молекулярная структура полимеров
- 33. вдоль цепи L- и D- изомеры располагаются неупорядоченно вдоль цепи располагаются только L- или только D-
- 34. нерегулярного строения регулярного строения (атактические ) стереорегулярного строения (тактические) Способны к кристаллизации Не способны к кристаллизации
- 35. Влияние стереоизомерии на свойства полимеров изо-ПММА (Тст = 40°С); синдио-ПММА (Тст = 160°С); атактический-ПММА (Тст =
- 36. Молекулярная структура полимеров Дальний конфигурационный порядок (для сополимеров отражает характер присоединения последовательностей) блок-сополимеры, если соединяются в
- 37. Молекулярная структура полимеров Конфигурация цепи отражает геометрию макромолекулы линейные разветвленные сшитые (сетчатые) лестничные звездообразные Разветвленные полимеры
- 38. Конфигурация цепи Линейные Разветвленные Звездообразные Лестничные Сетчатые
- 39. Флуктуационная сетка в виде связанных между собой узлов Кристаллиты и кристаллы на их основе в виде
- 40. Элементы флуктуационной сетки: - макромолекулы в виде молекулярных клубков, узлы флуктуационной сетки (домены), проходные макромолекулы. Надмолекулярная
- 41. Ламель (кристаллит со сложенными цепями) – первичная надмолекулярная структура кристаллических полимеров Толщина ламелей (толщина складки) составляет
- 42. Аморфная прослойка: проходные цепи, петли, концы макромолекул. Проходные цепи участвуют в образовании нескольких ламелей, прочно связывают
- 43. Сферолит - трехмерное кристаллическое образование со сферической симметрией, состоит из фибриллярных кристаллитов, растущих из единого центра
- 44. ПОЛИДИСПЕРСНОСТЬ ПОЛИМЕРОВ –сущность явления Причины полидисперности: 1 – Случайный характер синтеза (если макромолекулы получены из мономера);
- 45. МОЛЕКУЛЯРНО-МАССОВЫЕ ХАРАКТЕРИСТИКИ ПОЛИМЕРОВ СРЕДНИЕ МОЛЕКУЛЯРНЫЕ МАССЫ -среднечисловая молекулярная масса Mn -средневесовая молекулярная масса Mw Числовая доля
- 46. ПОЛИДИСПЕРСНОСТЬ ПОЛИМЕРОВ –количественное описание коэффициент полидисперсности Полидисперсный образец Монодисперсный образец Kd ≥ 1 – коэффициент полидисперсности;
- 47. Методы определения молекулярной массы полимеров Центрифугирование поводят при больших скоростях, так что частицы, вначале равномерно распределены
- 48. Аналитическое центрифугирование Центрифугирование поводят при больших скоростях, так что частицы, вначале равномерно распределенные по всему объёму
- 49. Осмометрия. Осмос
- 50. Осмометрия Осмотическое давление возникает, когда растворитель и раствор полимера разделяются полупроницаемой мембраной, пропускающей молекулы растворителя, но
- 51. Осмометрический метод с - концентрация раствора ВМС, г/л; β - коэффициент, учитывающий гибкость и форму молекулы
- 52. ГПХ, пожалуй, единственный метод, позволяющий определить молекулярно-массовое распределение полимера При уменьшении Mw/Mn прочность и вязкость полимера
- 53. Механизм разделения по размерам
- 54. Механизм разделения основан на разнице в размерах
- 55. Механизм разделения по размерам Готовится разбавленный раствор полимера в элюенте и вводится в систему Колонка для
- 56. ГПХ. Схема установки Насос Хроматографическая колонка с определенными характеристиками Ввод полимера с неизвестной молекулярной массой элюент
- 57. Насос Ввод пробы колонки Детекторы Дегазатор ГПХ. Прибор
- 58. Вискозиметрический метод η и ηо — вязкости раствора и растворителя, t и t0 – соответствующие времена
- 59. Удельная вязкость Удельная вязкость показывает, насколько увеличилась вязкость раствора ВМС по сравнению с вязкостью растворителя: При
- 60. Приведенная вязкость Чтобы учесть влияние концентрации раствора (оценить, насколько велика удельная вязкость, отнесенная к единице концентрации
- 61. Характеристическая вязкость Поскольку ηпривед зависит от концентрации ВМС, приходится вводить еще одну величину - ηхар (собственную
- 62. Величина α зависит от формы макромолекул ( 0.5 В общем случае, с увеличением жесткости макромолекул величина
- 63. Уравнение Марка-Куна-Хаувинка К и а – постоянные для данной системы полимер-растворитель при постоянной температуре Как получить
- 64. Статическое рассеяние света
- 65. Метод светорассеяния для малых частиц 2Rg ≤ λ/10
- 66. Метод светорассеяния для крупных частиц 2Rg > λ/10 Диаграмма Зимма (двойная экстраполяция): θо = 0 tgα
- 67. Получение полимеров
- 68. РАДИКАЛЬНАЯ - активный центр - свободный радикал – частица с неспаренным электроном. (радикал роста, макрорадикал) КАТИОННУЮ
- 69. РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯ Основные стадии полимеризации: Инициирование Рост цепи Обрыв цепи Передача цепи Инициирование – включает 2
- 71. ИНИЦИИРОВАНИЕ Инициирование – превращение небольшой доли молекул мономера в активные центры под действием специально вводимых веществ
- 72. Рост цепи Реакционная способность мономера и макрорадикала определяется Сопряжением кратной связи с заместителем Полярностью заместителя Объёмом
- 73. МОНОМЕРЫ в радикальной полимеризации: Виниловые мономеры CH2=CH-X Винилиденовые мономеры CH2=C(X)-Y X, Y - алкил, галоген, COOH,
- 74. Обрыв цепи рекомбинация а) квадратичный диспропорционирование
- 75. б) обрыв на молекуле ингибитора стабильные радикалы, которые при взаимодействии с макрорадикалами, образуют неактивные молекулы (дифенилпикрилгидразил,
- 76. Передача цепи играет роль в регулировании длины материальной цепи (степени полимеризации) На растворитель (S) На мономер
- 77. Передача цепи играет роль в регулировании длины материальной цепи (степени полимеризации) На другую макромолекулу
- 78. МЕХАНИЗМ И КИНЕТИКА ПОЛИМЕРИЗАЦИИ Допущения, принимаемые для вывода кинетических уравнений полимеризации Малые конверсии мономера Pn >>1
- 79. КИНЕТИКА РАДИКАЛЬНОЙ ПОЛИМЕРИЗАЦИИ Поскольку мономер расходуется в основном на стадии роста, то скорость этой реакции совпадает
- 80. ДЛИНА КИНЕТИЧЕСКОЙ И МАТЕРИАЛЬНОЙ ЦЕПИ Кинетическая цепь ν – число молекул мономера, присоединившихся к одному образовавшемуся
- 81. Доля обрыва цепей диспропорционированием Доля обрыва цепей рекомбинацией 1-α
- 82. Степень полимеризации прямо пропорциональна М, обратно пропорциональна кв.корню из концентрации инициатора и обратно пропорциональна константе самопередачи
- 84. Инициирование: I2→ 2I∙ Вырожденная (деградационная) передача цепи на мономер, который превращается в неактивный аллильный радикал, неспособный
- 85. Полимеризация при термическом инициировании: Vин=Vo kин[M]2=ko[R∙]2 Полимеризация в присутствии ингибитора Vин=Vz kин[I]=kz[R∙][Z]
- 86. ПОЛИМЕРИЗАЦИЯ НА ГЛУБОКИХ КОНВЕРСИЯХ Стадии реакции обрыва: Диффузия центров масс индивидуальных макрорадикалов Сегментальная диффузия активных концов
- 87. Ионная полимеризация
- 88. Роль X – стабилизация аниона АНИОННАЯ ПОЛИМЕРИЗАЦИЯ Мономеры ВИНИЛОВЫЕ мономеры с электроноакцепторными заместителями X – нитрил,
- 89. АНИОННАЯ ПОЛИМЕРИЗАЦИЯ Основные стадии полимеризации: Инициирование Рост цепи Обрыв цепи Передача цепи Инициирование − присоединение к
- 90. ИНИЦИИРОВАНИЕ Анионная полимеризация Инициируют металлалкилы, алкоксиды и амиды металлов, щелочи и другие реагенты основного характера. При
- 91. Рост цепи Rn-B+ + M → Rn+1-B+ Rn- (B)+ Rn- ( B) + - B +
- 92. Реакции обрыва в анионной полимеризации 1. перенос гидрид-иона с конца растущей цепи на противоион (полимеризация акрилонитрила)
- 93. Полимеризация ненасыщенных углеводородов (стирол, диены) отсутствие реакций кинетического обрыва цепи при незначительной роли или полном отсутствии
- 94. Роль X – стабилизация катиона КАТИОННАЯ ПОЛИМЕРИЗАЦИЯ Мономеры а) ВИНИЛОВЫЕ мономеры с электронодонорными заместителями X –
- 95. КАТИОННАЯ ПОЛИМЕРИЗАЦИЯ Основные стадии полимеризации: Инициирование Рост цепи Обрыв цепи Передача цепи Инициирование – 1) образование
- 96. ИНИЦИИРОВАНИЕ Катионная полимеризация 1.протонодонорные кислоты H2SO4, H3PO4, HClO4 2. Инициирование комплексом катализатор–сокатализатор – кислоты Льюиса BF3,
- 97. Присоединение первичных активных частиц к мономеру K+ + M → KM+ Структура KM+ зависит от природы
- 98. Обрыв цепи При катионной полимеризации реакции обрыва и передачи цепи можно разделить условно, т.к. при обрыве
- 99. Передача на мономер играет важнейшую роль в катионной полимеризации
- 100. СОПОЛИМЕРИЗАЦИЯ – совместная полимеризация 2-х или более мономеров (классификация). Статистические сополимеры: в макромолекуле сополимера распределение мономерных
- 101. Сополимеризация Градиентные: состав макромолекулы изменяется непрерывно вдоль цепи ~ M1M1М2M1M1М1M1M2М1M1M2М2M1M1М2M2M2М2~ Блок-сополимеры: линейные макромолекулы с длинными (полимерными)
- 102. Различают : Мгновенную неоднородность, которая возникает в результате статистического характера реакций обрыва цепи. Конверсионную неоднородность, обусловленную
- 103. Композиционная неоднородность макромолекул сополимеров Эксплуатационные свойства бинарных сополимеров зависят от: среднего состава сополимера, композиционной неоднородности распределения
- 104. Реакция роста цепи ~M1* + M1 → ~M1M1* k11 ~M1* + M2 → ~M1M2* k12 ~M2*
- 105. k12[M1*][M2]= k21[M2*][M1] Допущения для вывода уравнения состава сополимера Pn >>1 (действительно реакция полимеризации) Реакционная способность M1*
- 106. Диаграмма составов сополимеров Если r1>1 и r2 Если r1 1, то сополимер обогащен звеньями М2 Если
- 107. Радикальная сополимеризация Значения r1 , r2 и состав сополимера обычно слабо зависят от природы растворителя и
- 108. Возможности контролируемой радикальной полимеризации Контроль скорости полимеризации и ММР Макромолекулярный дизайн: Контроль топологии макромолекул линейная звездообразная
- 109. Новые возможности радикальной полимеризации в контролируемом синтезе макромолекул Классическая радикальная полимеризация инициирование I → 2 R1
- 110. Псевдоживая (контролируемая) радикальная полимеризация Reversible-deactivation radical polymerization "Оживление" цепей и их участие в дальнейшем росте идёт
- 111. 1. Обратимое ингибирование Способы "оживления" макромолекул Стабильные радикалы радикал роста обратимо взаимодействует со стабильным или малоактивным
- 112. 2. Обратимый перенос атома Способы "оживления" макромолекул (ATRP)- англ.аббревиатура макрорадикал обратимо взаимодействует со специальной добавкой (катализатором)
- 113. псевдоживая полимеризация с обратимой передачей цепи (ОПЦ) по механизму присоединения – фрагментации reversible addition – fragmentation
- 114. 3. Обратимая передача цепи Способы "оживления" макромолекул радикал обратимо взаимодействует с агентом обратимой передачи цепи, содержащим
- 115. Поликонденсация
- 116. Сравнительные характеристики реакций полимеризации и поликонденсации полимеризация поликонденсация 1. цепная реакция присоединения активных центров (радикалов, анионов
- 118. Поликонденсация – процесс образования макромолекул в результате ступенчатого химического взаимодействия функциональных групп многофункциональных мономеров и n-меров,
- 119. СОПОЛИКОНДЕНСАЦИЮ (2 и более мономеров) простые полиэфиры полиамиды
- 120. полиамиды сложные полиэфиры
- 121. ИНТЕРСОПОЛИКОНДЕНСАЦИЮ (3 мономера) полиамиды
- 122. По топологии образующихся макромолекул поликонденсацию подразделяют на: ЛИНЕЙНУЮ (бифункциональные мономеры) ТРЕХМЕРНУЮ (полифункциональные мономеры)
- 123. По значению константы поликонденсационного равновесия K поликонденсацию подразделяют на: K = k1/k-1 равновесную (обратимую) неравновесную (необратимую)
- 124. Значения констант равновесия (К) для некоторых случаев поликонденсации Необратимая поликонденсация Обратимая поликонденсация
- 125. Побочные химические реакции , в результате которых функциональные группы утрачивают способность участвовать в реакции роста. 1.
- 126. Кинетика поликонденсации Для поликонденсации характерно исчезновение мономера уже на ранних стадиях процесса, когда молекулярная масса продукта
- 127. Кинетика поликонденсации Мономеры взяты в эквимолярных количествах Уравнение изменения концентрации функциональных групп: k – константа скорости
- 128. Необратимая поликонденсация:
- 129. Для обратимой гомополиконденсации предельная в данных условиях молекулярная масса определяется термодинамическими факторами, т.е. значением константы поликонденсационного
- 130. Факторы, влияющие на молекулярную массу поликонденсационных полимеров Глубина проведения процесса q (необратимая поликонденсация) Эквимольность реагирующих между
- 131. ПОЛИПРИСОЕДИНЕНИЕ Реакции проходят без выделения низкомолекулярного продукта !!! Полимочевины Полиуретаны
- 132. Основные классы поликонденсационных полимеров простые полиэфиры -C-O- сложные полиэфиры -C(=O)-O-
- 133. полиуретаны –NH-C(=O)-O- полиамиды –NH-C(=O)- полимочевины –NH-C(=O)-NH-
- 134. Некоторые конденсационные полимеры полиэтиленадипинат полиэтилентерефталат полиэтиленгликоль полиамид-6 (найлон-6, капрамид) полиамид-6,6 поли-пара-бензамид (Кевлар) полиуретаны полимочевины
- 135. Ароматические полиимиды: Полиэфиримиды: Термостойкие
- 136. Способы полимеризации 1. Полимеризации в блоке подвергаются жидкие мономеры в присутствии растворенных в них инициаторов. Такую
- 137. Способы полимеризации 2. Полимеризация в растворителях осуществляется в среде, растворяющей либо мономер и полимер, либо только
- 139. Скачать презентацию
 Химические превращения веществ
Химические превращения веществ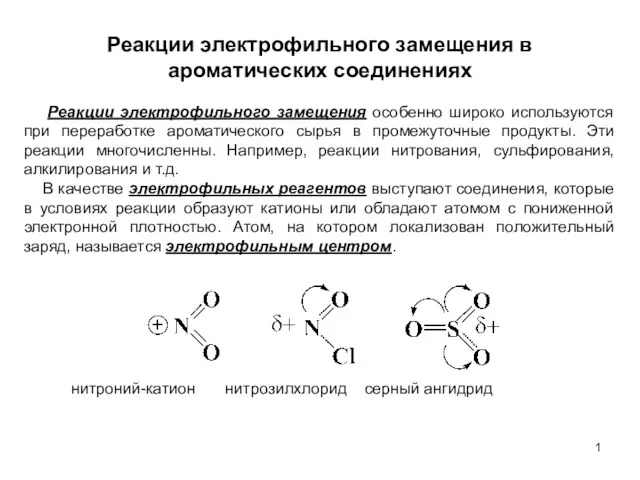 Реакции электрофильного замещения в ароматических соединениях. (Лекция 6)
Реакции электрофильного замещения в ароматических соединениях. (Лекция 6) Көмірсулар. Моносахаридтер. Жіктелуі. Гексозалар. Құрылысы
Көмірсулар. Моносахаридтер. Жіктелуі. Гексозалар. Құрылысы Минералдар
Минералдар Нитрид галлия. Основные свойства и применение. GaN и твердые растворы на его основе
Нитрид галлия. Основные свойства и применение. GaN и твердые растворы на его основе Классификация химических реакций
Классификация химических реакций ЕГЭ по химии. Анализ результатов решения (часть 2)
ЕГЭ по химии. Анализ результатов решения (часть 2) Химическое равновесие. Принцип Ле Шателье
Химическое равновесие. Принцип Ле Шателье Обратимость химических реакций. Обратимые и необратимые химические реакции. Химическое равновесие
Обратимость химических реакций. Обратимые и необратимые химические реакции. Химическое равновесие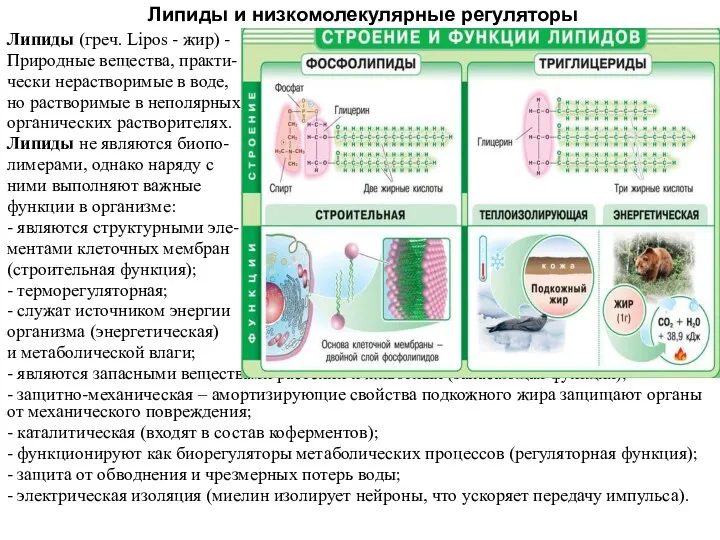 Липиды и низкомолекулярные регуляторы
Липиды и низкомолекулярные регуляторы Природный каучук
Природный каучук Свойства фосфора
Свойства фосфора Химия в повседневной жизни
Химия в повседневной жизни Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Электролиз – ОВ процесс
Электролиз – ОВ процесс Получение азотной кислоты
Получение азотной кислоты Алкены
Алкены Почва. Интегрированный урок по химии и географии
Почва. Интегрированный урок по химии и географии Коллигативные свойства растворов
Коллигативные свойства растворов Реакции SR в ряду алканов
Реакции SR в ряду алканов Періодичний закон. Хімія. 8 клас
Періодичний закон. Хімія. 8 клас Определение химического элемента на основании расчетов по химическим реакциям
Определение химического элемента на основании расчетов по химическим реакциям Дисперсные системы
Дисперсные системы Группы сходных химических элементов
Группы сходных химических элементов Бензол. Физические и химические свойства
Бензол. Физические и химические свойства Фосфор и его соединения
Фосфор и его соединения Химические элементы в организме человека
Химические элементы в организме человека Общая геология. Породообразующие минералы
Общая геология. Породообразующие минералы