Содержание
- 2. Обмен энергии
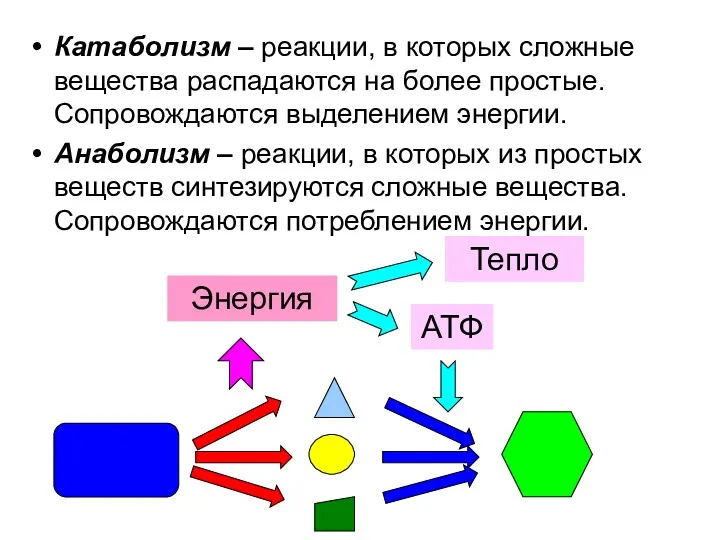
- 3. Катаболизм – реакции, в которых сложные вещества распадаются на более простые. Сопровождаются выделением энергии. Анаболизм –
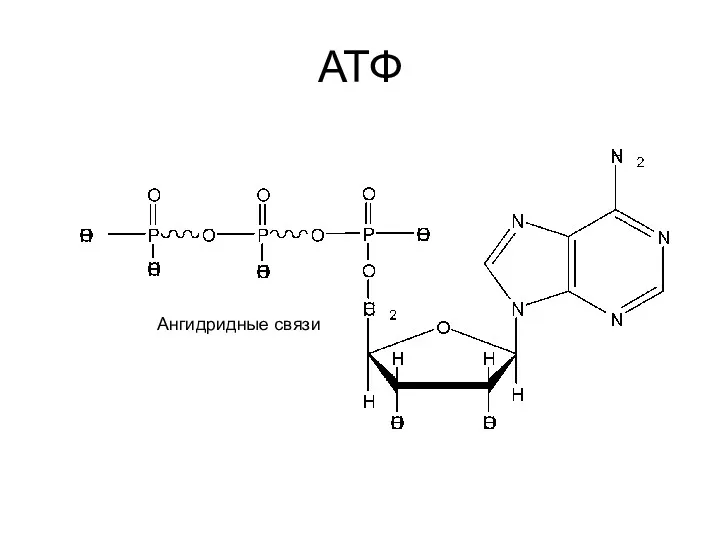
- 4. АТФ Ангидридные связи
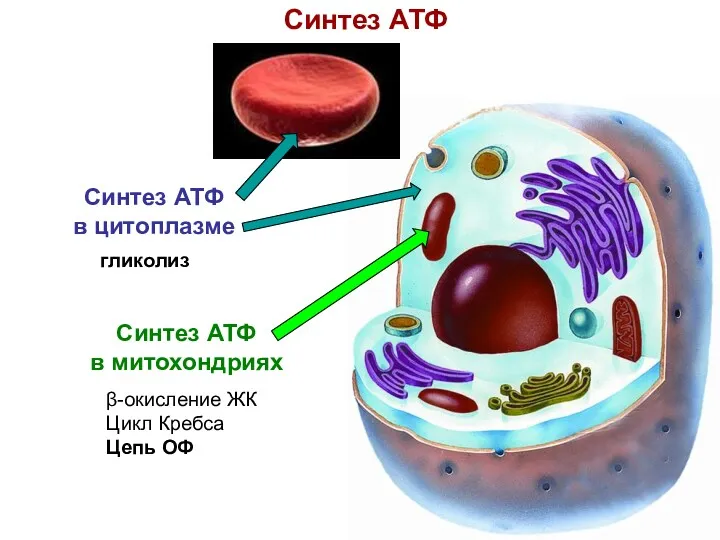
- 5. Синтез АТФ Синтез АТФ в митохондриях β-окисление ЖК Цикл Кребса Цепь ОФ Синтез АТФ в цитоплазме
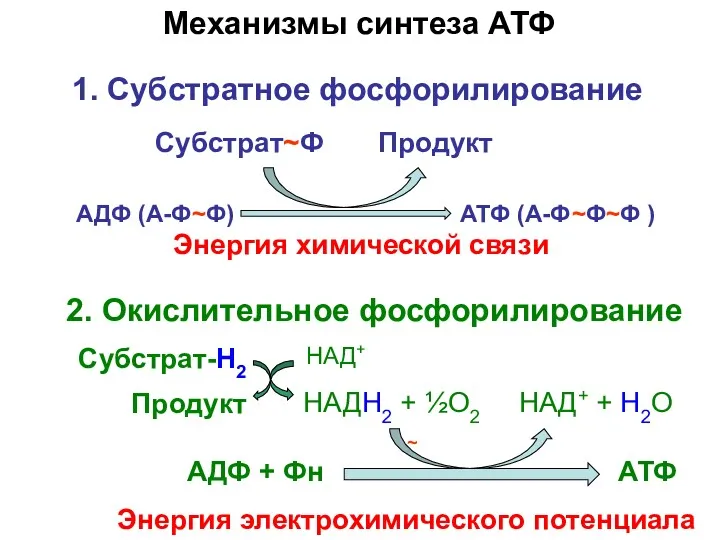
- 6. АДФ + Фн АТФ Механизмы синтеза АТФ Энергия электрохимического потенциала 2. Окислительное фосфорилирование АДФ (А-Ф~Ф) АТФ
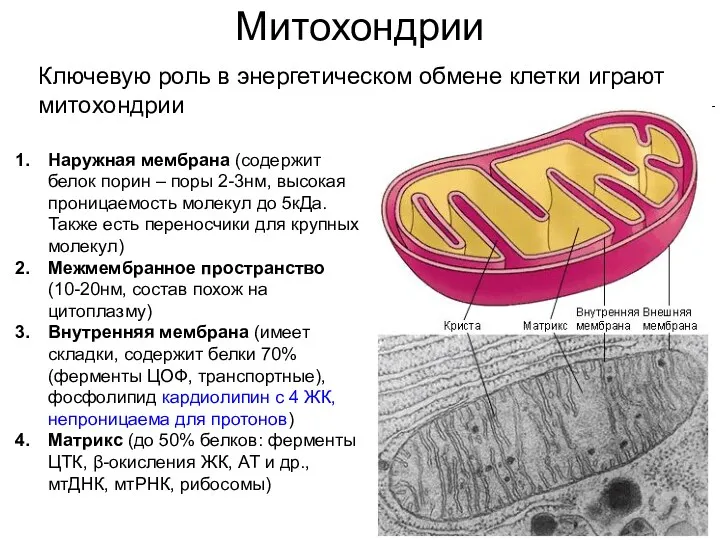
- 7. Митохондрии Ключевую роль в энергетическом обмене клетки играют митохондрии Наружная мембрана (содержит белок порин – поры
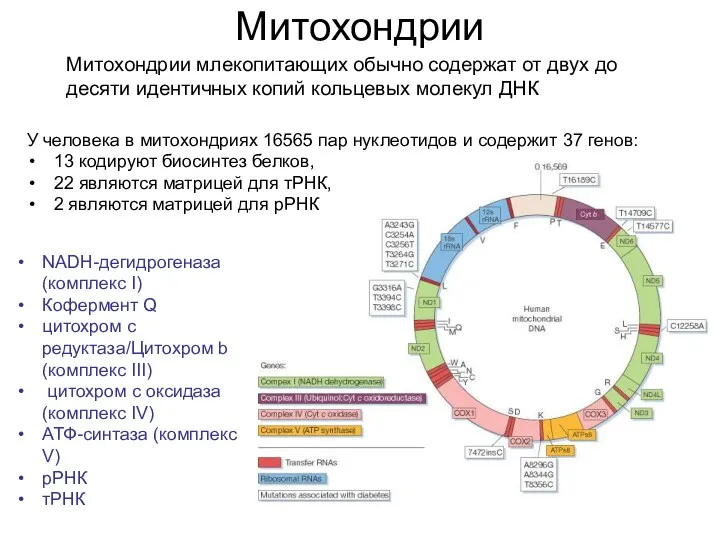
- 8. Митохондрии Митохондрии млекопитающих обычно содержат от двух до десяти идентичных копий кольцевых молекул ДНК NADH-дегидрогеназа (комплекс
- 9. История развития учения о биологическом окислении Антуан Лоран Лавуазье (1743 – 1794) – французский химик –
- 10. В конце XIX века русские исследователи А.Н. Бах и В.И. Палладин, работая независимо друг от друга,
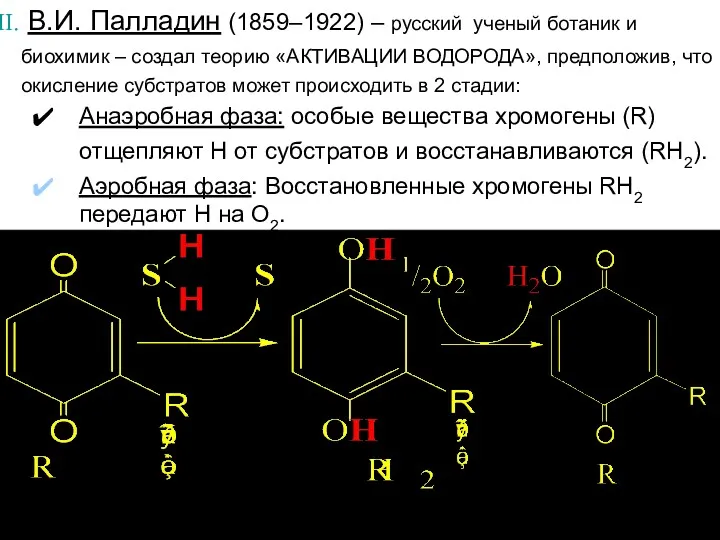
- 11. В.И. Палладин (1859–1922) – русский ученый ботаник и биохимик – создал теорию «АКТИВАЦИИ ВОДОРОДА», предположив, что
- 12. Отто Генрих Варбург открыл фермент(E) – цитохромоксидазу, работающую на заключительном этапе БО. Процесс БО представляет не
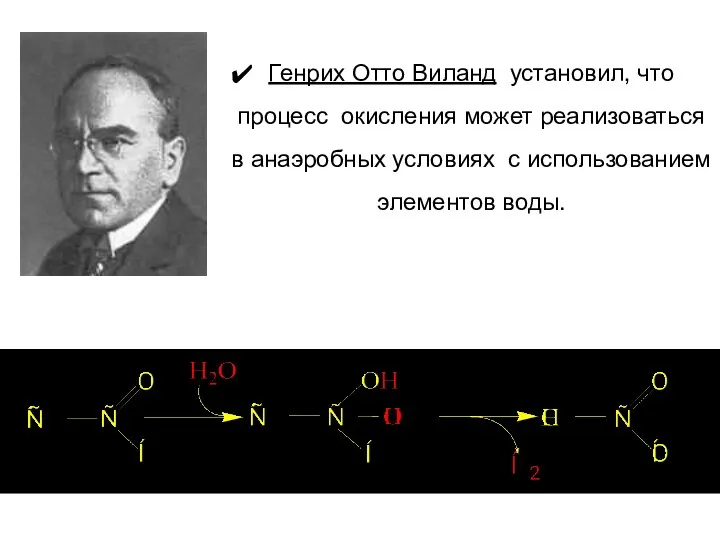
- 13. Генрих Отто Виланд установил, что процесс окисления может реализоваться в анаэробных условиях с использованием элементов воды.
- 14. Современные представления о биологическом окислении Согласно современной теории БО: окисление происходит как в аэробных, так и
- 15. Окислительно-восстановительные реакции (ОВР) – реакции, в которых меняется степень окисления субстрата за счет присоединения / отщепления:
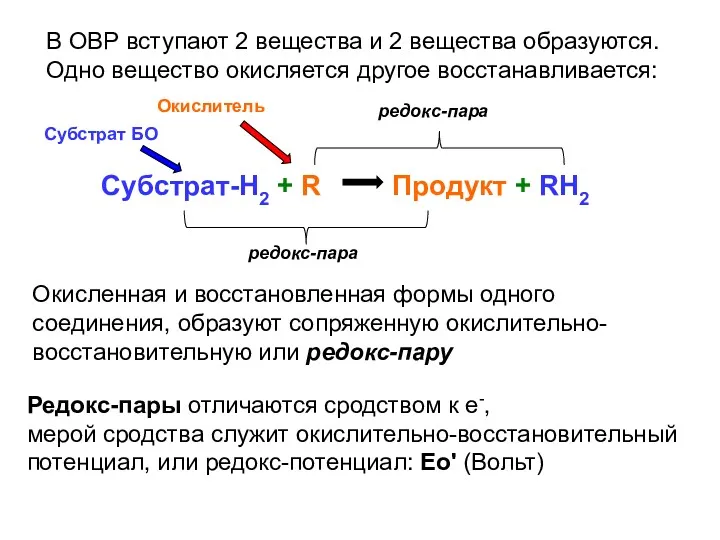
- 16. В ОВР вступают 2 вещества и 2 вещества образуются. Одно вещество окисляется другое восстанавливается: Субстрат-H2 +
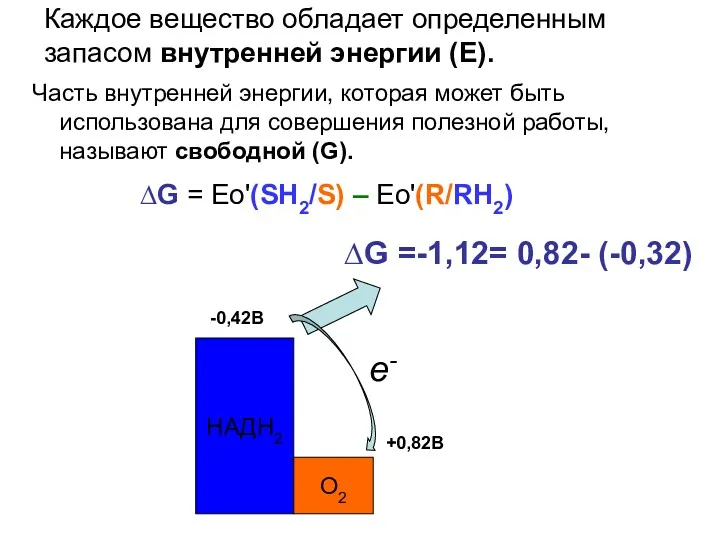
- 17. Каждое вещество обладает определенным запасом внутренней энергии (Е). Часть внутренней энергии, которая может быть использована для
- 18. Биологическое окисление (БО) - совокупность окислительно-восстановительных реакций в живых клетках. Особенности реакций БО: протекают в аэробных
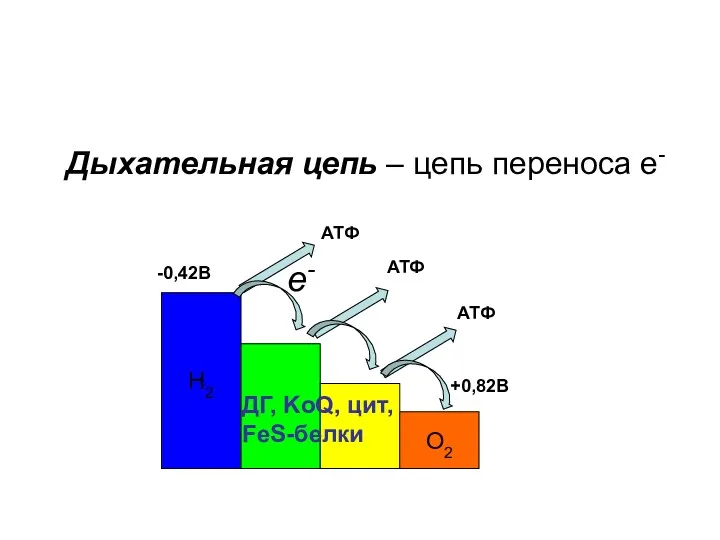
- 19. Дыхательная цепь – цепь переноса электронов. В переносе электронов от субстратов БО к О2 принимают участие:
- 20. -0,42В +0,82В Н2 О2 е- АТФ АТФ АТФ Дыхательная цепь – цепь переноса е- ДГ, KoQ,
- 21. В настоящее время выделено 4 основные пути использования О2 в организме: Оксидазный путь Функция: 90% О2
- 22. Диоксигеназный путь (Обеспечивает включение молекулы кислорода в молекулу субстрата) Функция: деградация АК; синтез новых веществ; Свободно-радикальный
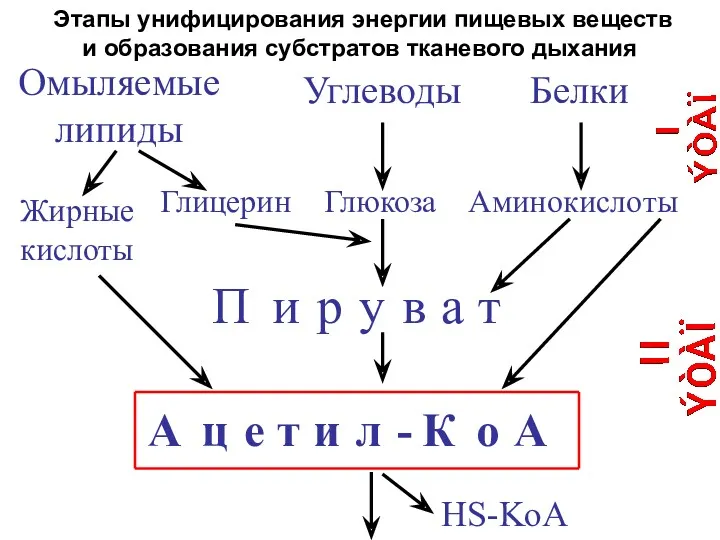
- 23. Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания Омыляемые липиды Углеводы Белки Глицерин Глюкоза
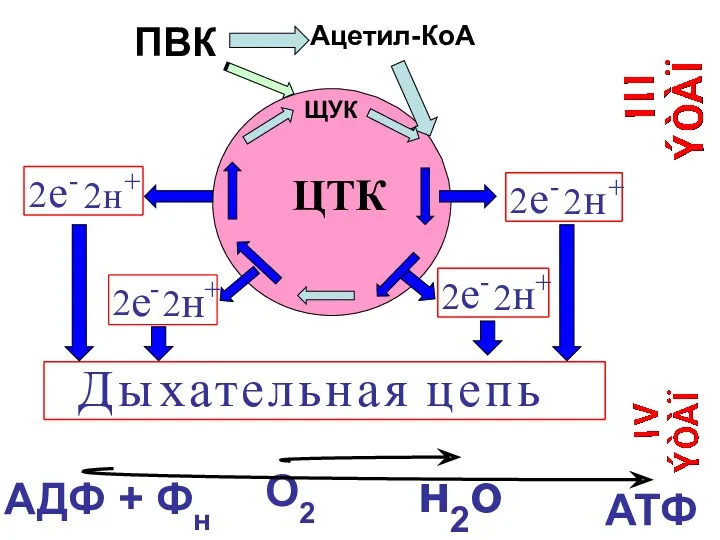
- 24. АДФ + Фн О2 н2о АТФ ЦТК Ацетил-КоА ЩУК ПВК
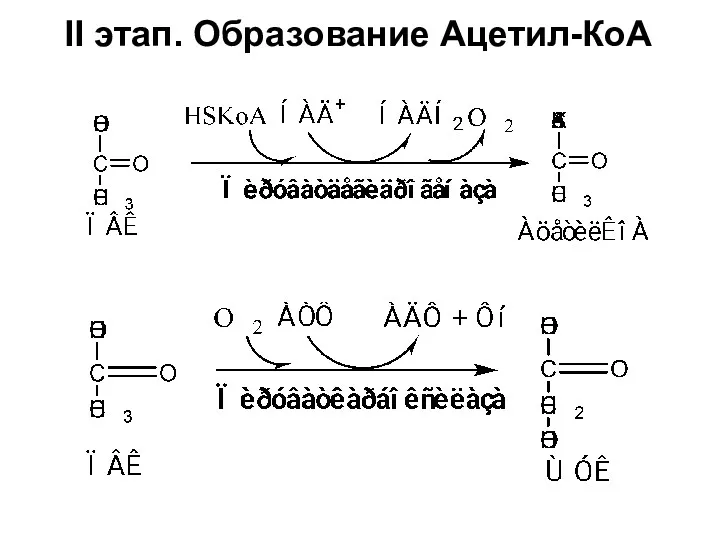
- 25. II этап. Образование Ацетил-КоА
- 26. ЦТК является процессом окисления Ацетил–КоА - универсального продукта катаболизма углеводов, белков и омыляемых липидов; ЦТК протекает
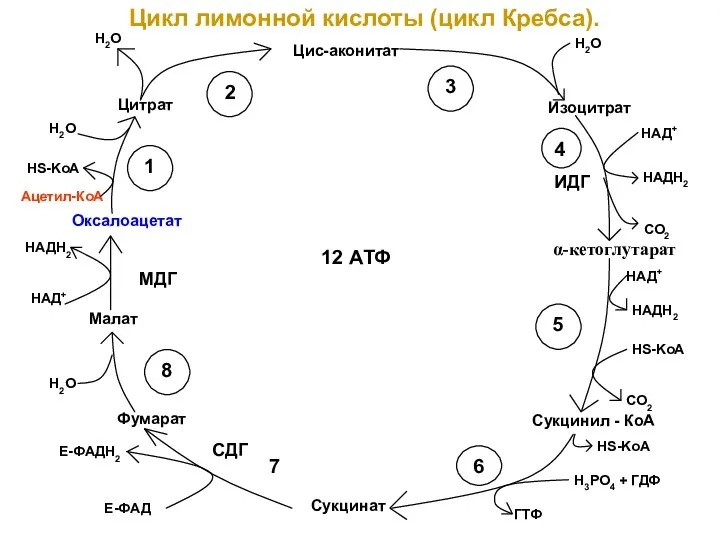
- 27. Цикл лимонной кислоты (цикл Кребса). Цис-аконитат Изоцитрат Сукцинил - КоА Сукцинат Цитрат Оксалоацетат Малат Фумарат 12
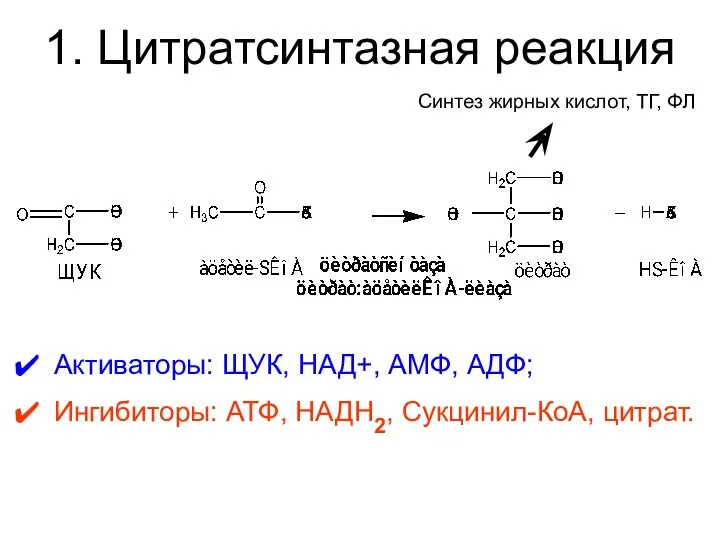
- 28. 1. Цитратсинтазная реакция Активаторы: ЩУК, НАД+, АМФ, АДФ; Ингибиторы: АТФ, НАДН2, Сукцинил-КоА, цитрат. Синтез жирных кислот,
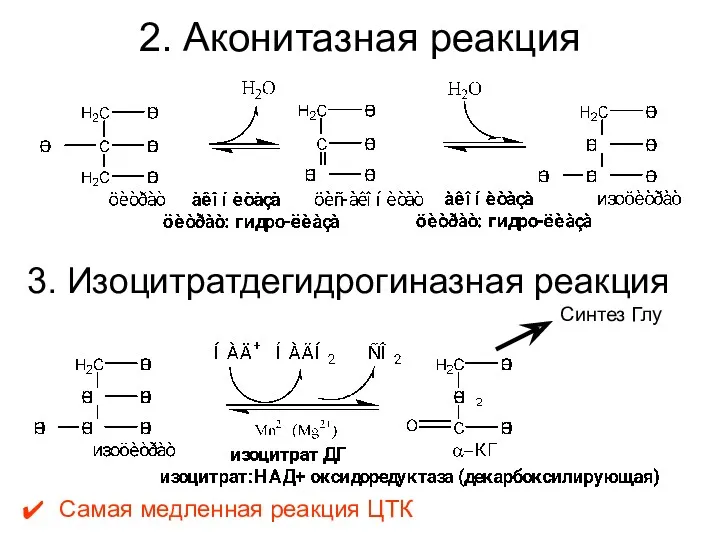
- 29. 2. Аконитазная реакция 3. Изоцитратдегидрогиназная реакция Самая медленная реакция ЦТК Синтез Глу
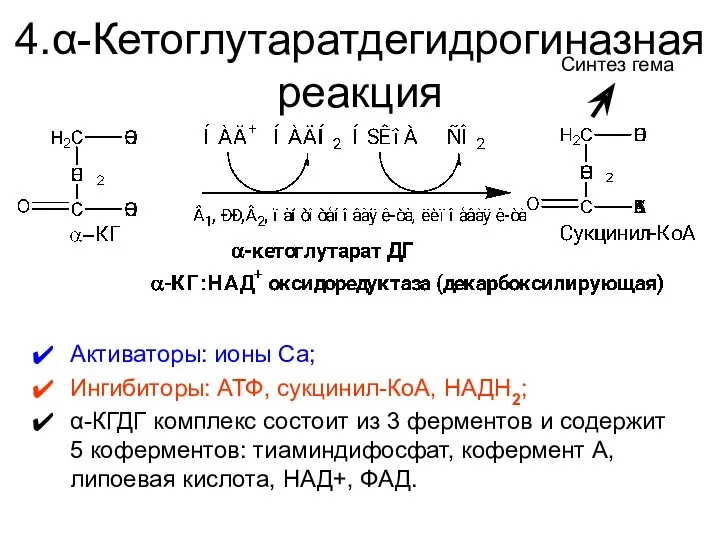
- 30. 4.α-Кетоглутаратдегидрогиназная реакция Активаторы: ионы Са; Ингибиторы: АТФ, сукцинил-КоА, НАДH2; α-КГДГ комплекс состоит из 3 ферментов и
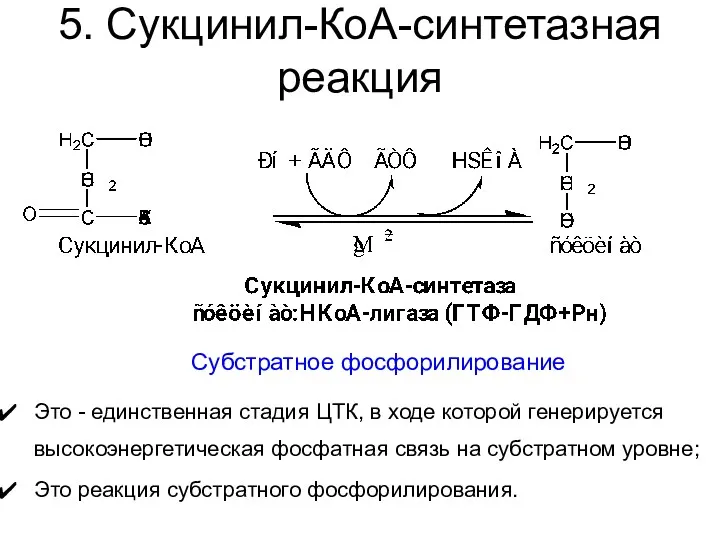
- 31. 5. Сукцинил-КоА-синтетазная реакция Это - единственная стадия ЦТК, в ходе которой генерируется высокоэнергетическая фосфатная связь на
- 32. 6. Сукцинатдегидрогиназная реакция СДГ является флавопротеином, состоящим из 2 субъединиц: Fe2S2 и Fe4S4, одна из которых
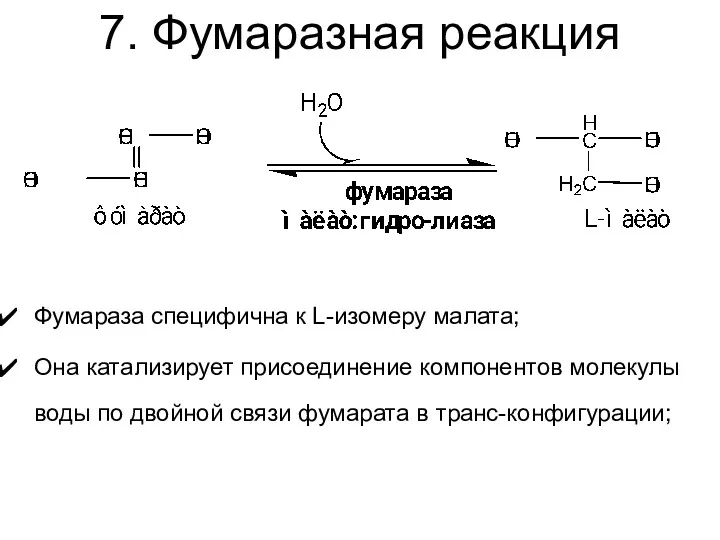
- 33. 7. Фумаразная реакция Фумараза специфична к L-изомеру малата; Она катализирует присоединение компонентов молекулы воды по двойной
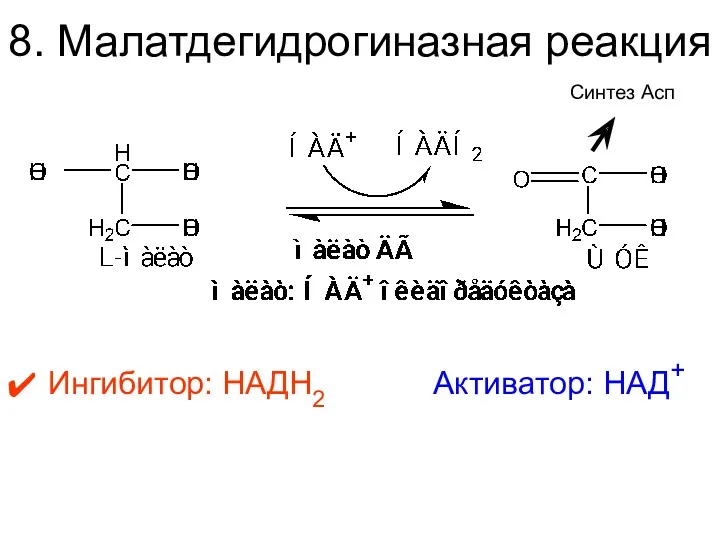
- 34. 8. Малатдегидрогиназная реакция Ингибитор: НАДН2 Активатор: НАД+ Синтез Асп
- 35. Энергетический баланс одного оборота ЦТК В 4 ОВР ЦТК образуются 3 НАДН2 и 1 ФАДН2, которые
- 36. Регуляция ЦТК Регуляторные (ключевые, лимитирующие) ферменты: Цитратсинтаза изоцитрат ДГ α-КГ ДГ СДГ Ингибирует – НАДН2 и
- 37. Стимулирует ЦТК гормон инсулин, а ингибирует – глюкагон O2 активирует ЦТК, переводя восстановленные формы НAДH2, ФAДH2
- 38. Биологическое значение ЦТК 1. образование водородных эквивалентов, которые в цепи ОФ обеспечивают синтез АТФ; 2. выполняет
- 39. IV этап. Окислительное фосфорилирование В 1966г. английский ученый Питер Денис Митчелл сформулировал хемиосмотическую гипотезу объясняющую принцип
- 40. цепь реакций, осуществляющихся в процессе дыхания, представляет собой последовательность сменяющих друг друга протонов и электронов. Белковые
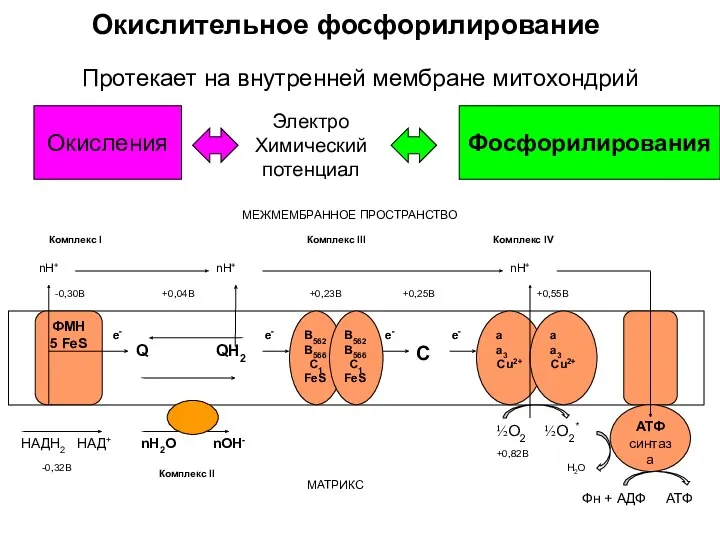
- 41. Окислительное фосфорилирование Q ½О2 ½О2* Н2О НАДН2 НАД+ nН+ е- QН2 nН2О nОН- nН+ АТФ синтаза
- 42. ФМН 5FеS ФАД FeS В562 В566 С1 FeS В562 В566 С1 FeS а а3 Сu2+ а
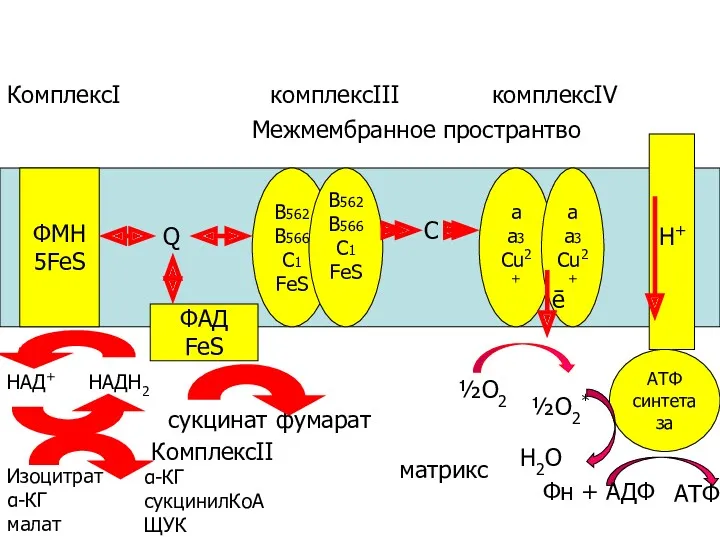
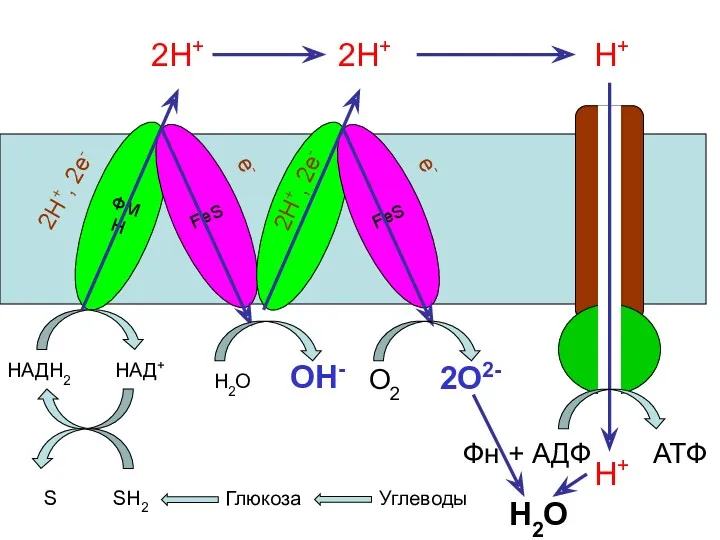
- 43. ФМН FeS НАДН2 НАД+ S SH2 Глюкоза Углеводы 2Н+, 2е- е- 2Н+ FeS 2Н+, 2е- е-
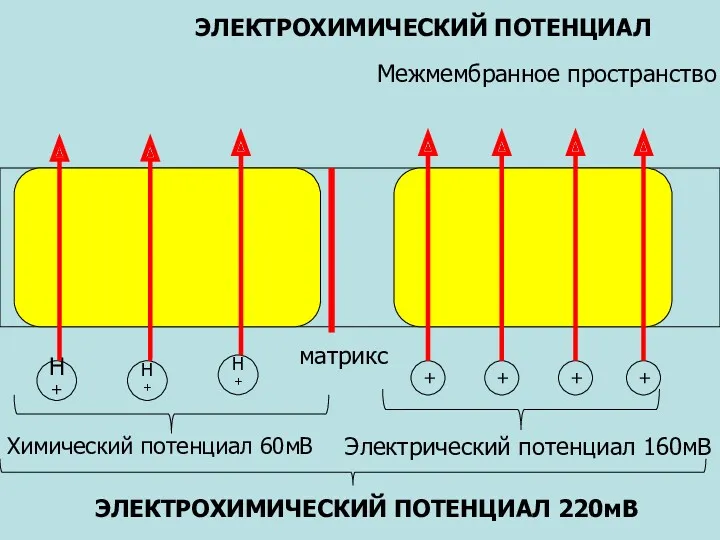
- 44. Н+ Н+ Н+ ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ Межмембранное пространство Химический потенциал 60мВ матрикс + + + + Электрический
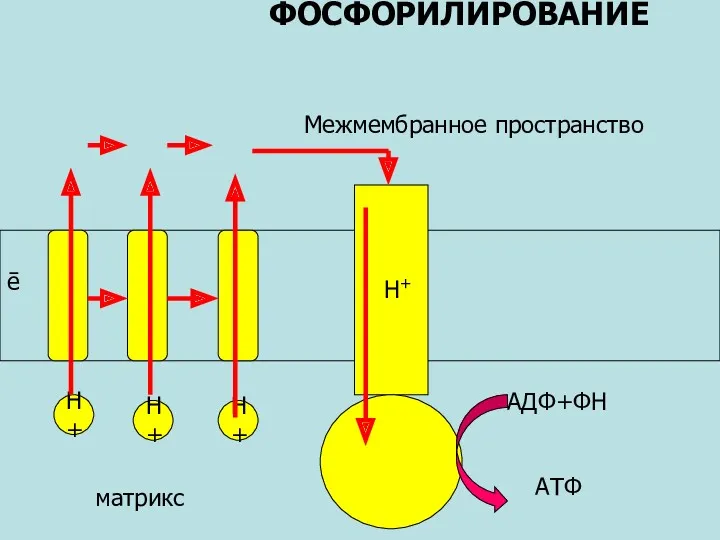
- 45. Н+ Н+ Н+ ē ФОСФОРИЛИРОВАНИЕ АДФ+ФН АТФ Н+ Межмембранное пространство матрикс
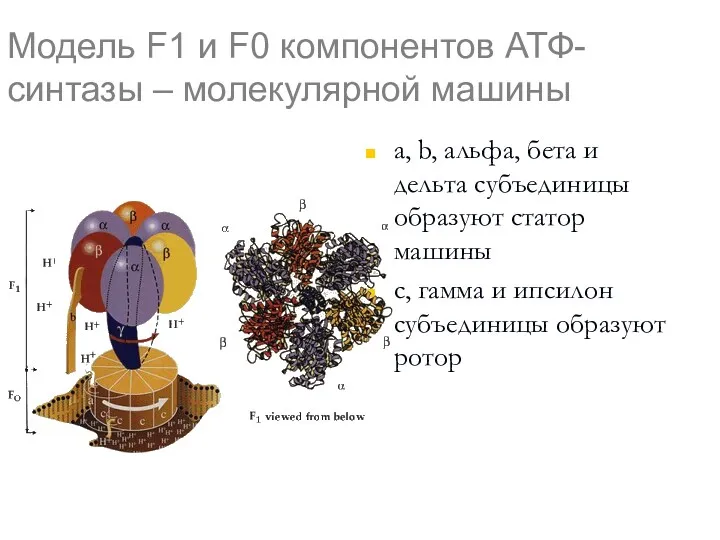
- 46. Модель F1 и F0 компонентов АТФ-синтазы – молекулярной машины a, b, альфа, бета и дельта субъединицы
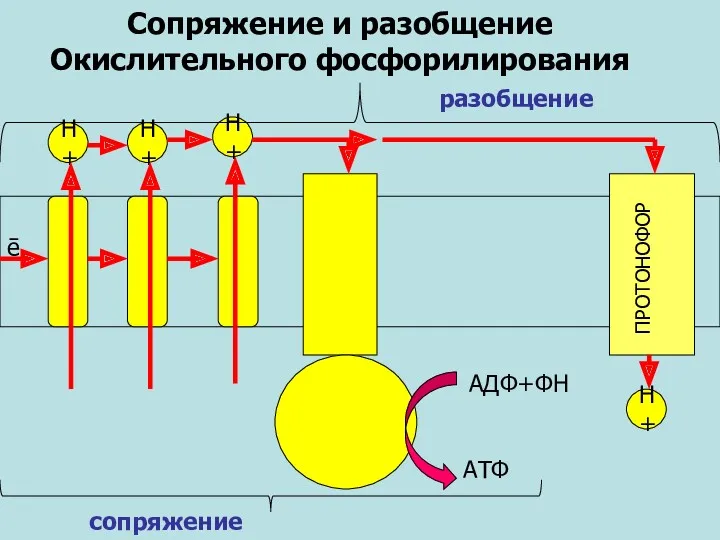
- 47. Н+ Н+ Н+ ē Сопряжение и разобщение Окислительного фосфорилирования АДФ+ФН АТФ сопряжение Н+ разобщение ПРОТОНОФОР
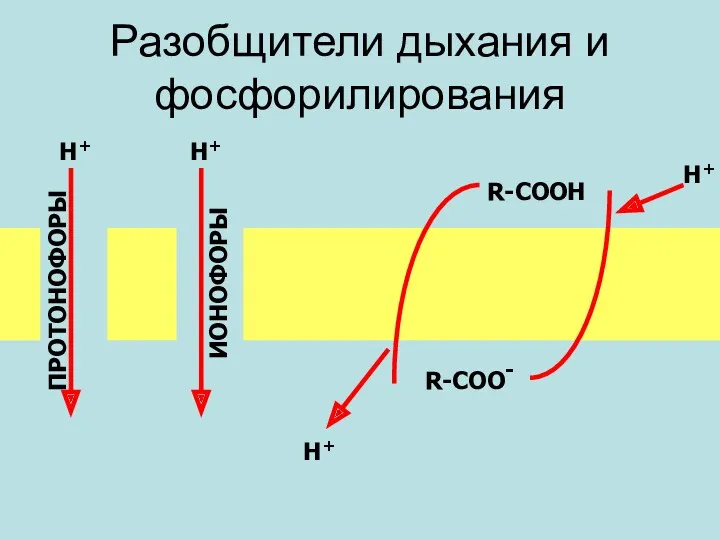
- 48. Разобщители дыхания и фосфорилирования R-СООН R-СОО- Н+ Н+ ПРОТОНОФОРЫ ИОНОФОРЫ Н+ Н+
- 49. 2,4-Динитрофенол 2,4-динитрофенол является классическим разобщителем окислительного фосфорилирования. При действии на митохондрии стимулирует их дыхание, но ингибирует
- 50. Дыхательный контроль - Зависимость интенсивности дыхания митохондрий от концентрации АДФ. В результате дыхательного контроля скорость синтеза
- 52. Скачать презентацию




















 Понятие об онтогенезе
Понятие об онтогенезе Метаболизм. Энергетический обмен
Метаболизм. Энергетический обмен Я і навакольны свет. Я і жывёльны свет (часть 1)
Я і навакольны свет. Я і жывёльны свет (часть 1) Любимые сад и огород. В.Н. Пастарнаков. Цикл: для начинающих. Часть 1. Посадка рассады
Любимые сад и огород. В.Н. Пастарнаков. Цикл: для начинающих. Часть 1. Посадка рассады מה ידוע לך על תולעי משי?
מה ידוע לך על תולעי משי? Основные направления эволюционного процесса
Основные направления эволюционного процесса Размножение цветковых растений
Размножение цветковых растений Бұршақтар, қалақайлар, шамшаттар тұқымдастарына сипаттама
Бұршақтар, қалақайлар, шамшаттар тұқымдастарына сипаттама Теория И.П. Павлова о типах высшей нервной деятельности
Теория И.П. Павлова о типах высшей нервной деятельности Красная Книга
Красная Книга Моногибридное скрещивание
Моногибридное скрещивание Микроэволюция. Популяция эволюцияның элементарлық өлшем бірлігі
Микроэволюция. Популяция эволюцияның элементарлық өлшем бірлігі Концепции современного естествознания
Концепции современного естествознания Царство грибы
Царство грибы Строение белков
Строение белков Цестодозы жвачных
Цестодозы жвачных Мы в ответе за тех, кого приручили
Мы в ответе за тех, кого приручили Селекция растений. 11 класс
Селекция растений. 11 класс Выделение. Мочевыделительная система. 8 класс
Выделение. Мочевыделительная система. 8 класс Мышцы человека
Мышцы человека Тип Хордовые. Подтип Бесчерепные. Подтип Черепные (Позвоночные)
Тип Хордовые. Подтип Бесчерепные. Подтип Черепные (Позвоночные) Многообразие живых организмов. Царства живой природы
Многообразие живых организмов. Царства живой природы Презентация по теме: Экологические группы птиц
Презентация по теме: Экологические группы птиц Презентация Органоиды клетки часть 1
Презентация Органоиды клетки часть 1 Критерии к лабораторной работе по биологии
Критерии к лабораторной работе по биологии Новый урок биологии с Марусей
Новый урок биологии с Марусей Протерозойская эра
Протерозойская эра Ферменттер
Ферменттер