Содержание
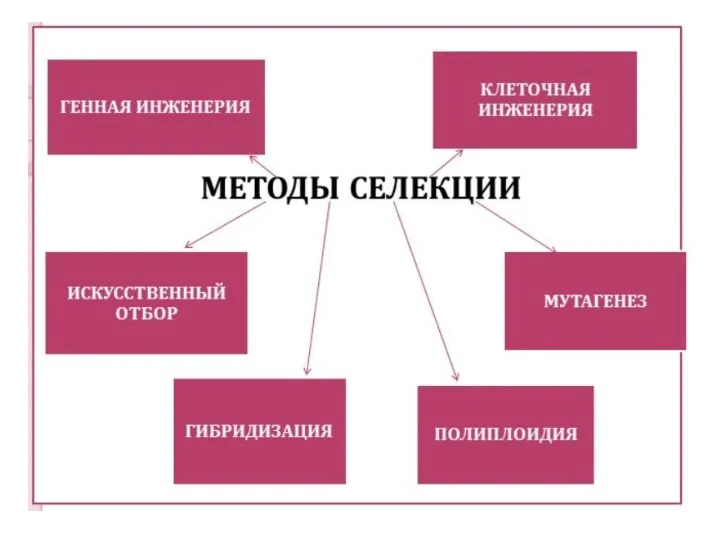
- 2. Основные методы селекции и биотехнологии
- 4. Порода, сорт и штамм – это популяция организмов, искусственно созданная человеком, которая характеризуется специфическим генофондом, наследственно
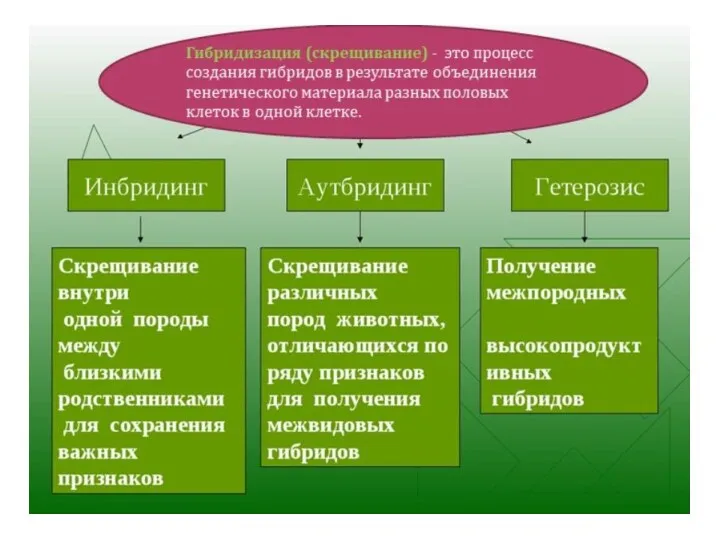
- 11. Гибридизация –искусственное скрещивание различных по признакам особей с целью выявления характера наследования признаков, получения новых сочетаний
- 12. Аутбридинг – неродственное скрещивание (внутривидовое и межвидовое), отдаленная гибридизация. Неродственное скрещивание организмов, относящихся к разным линиям
- 13. AAbbCCdd х aaBBccDD AaBbCcDd Гетерозис –мощное развитие признаков (ускорение роста, увеличение размеров, повышение жизнестойкости и плодовитости)
- 15. Мул – гибрид лошади и осла
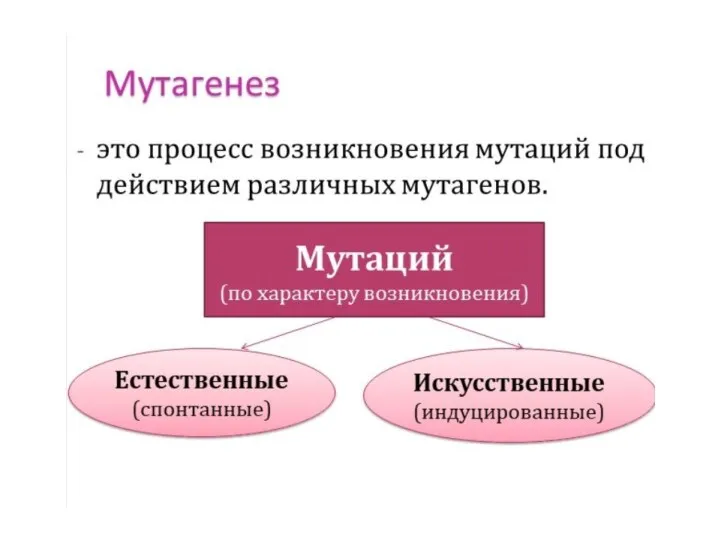
- 19. Искусственный мутагенез Получение мутаций, контролируемых человеком 1927г. – американский генетик Меллер открыл искусственный мутагенез. Воздействовал на
- 27. Современная биотехнология — это наука о генно-инженерных и клеточных методах создания и использования генетически трансформированных биологических
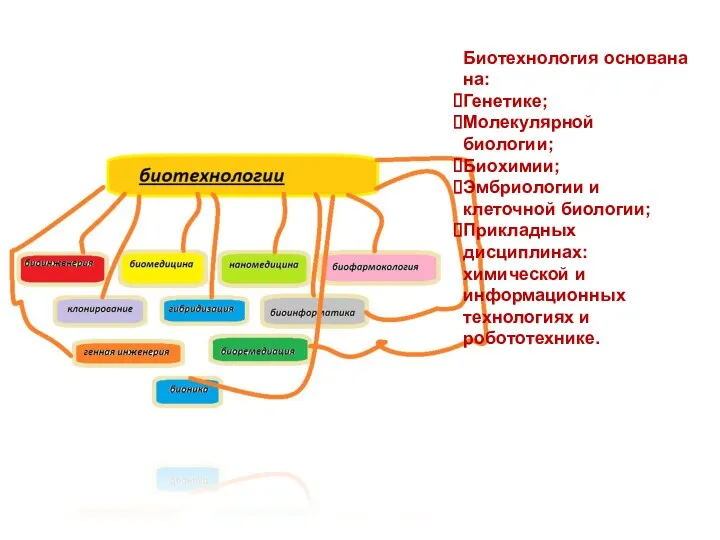
- 28. Биотехнология основана на: Генетике; Молекулярной биологии; Биохимии; Эмбриологии и клеточной биологии; Прикладных дисциплинах: химической и информационных
- 29. Значение биотехнологии: получение продуктов питания, кормовых добавок и ценных кормовых белков, лекарственных препаратов и средств диагностики,
- 30. Разделы биотехнологии Промышленная биотехнология (биотехнологические производства, использующие преимущественно микроорганизмы). Клеточная инженерия (культивирование растительных и животных клеток).
- 31. Промышленная биотехнология Фармацевтическая биотехнология (вакцины, ферменты, инсулин, интерфероны, витамины, антибиотики, биодеградируемые пластмассы, биосовместимые материалы, тест-системы). Сельскохозяйственная
- 32. Использование бактерий в биотехнологии: Производство кисломолочных продуктов Квашение овощей Силосование травы Производство витаминов, гормонов, фенрментов Первой
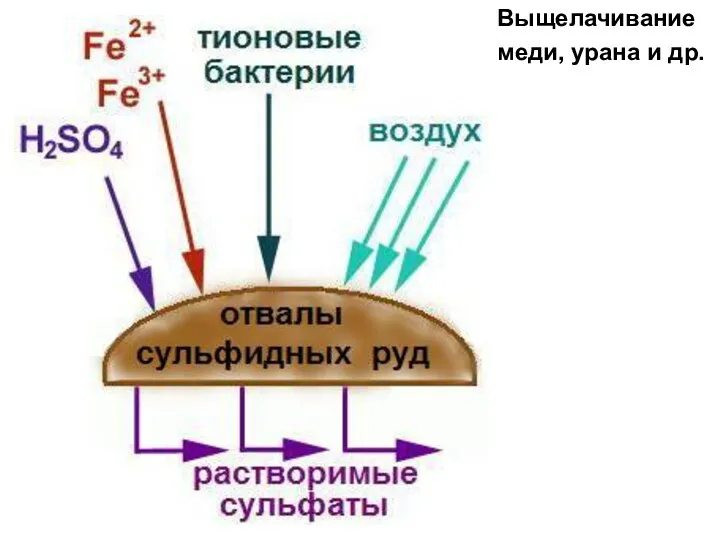
- 33. Выщелачивание меди, урана и др.
- 34. «Грибные» биотехнологические продукты Антибиотики (пенициллин и др.). Ферменты (амилазы, протеазы, целлюлаза и др.) Органические кислоты: лимонная,
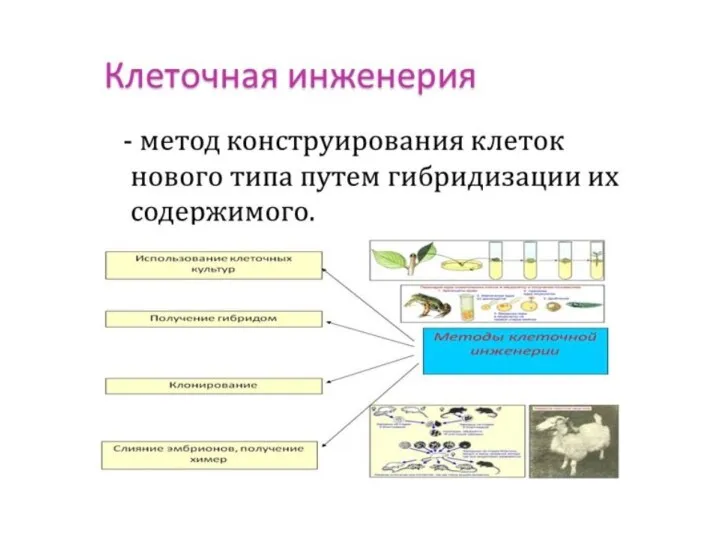
- 36. Клеточная инженерия — метод конструирования клеток нового типа на основе их культивирования на питательной среде, гибридизации
- 37. Клеточная инженерия конструирование клеток нового типа; создание химер агрегационным или инъекционным методом (генетическая мозаичность химер не
- 38. Клонирование Растений, грибов и микроорганизмов – бесполое размножение зачатками многоклеточными или одноклеточными Животных – многоплодность за
- 39. Клон - точная копия? Точное воспроизведение растения, животного или человека невозможно. Новый организм обязательно будет отличаться
- 40. Клеточная инженерия растений Ускоренное клональное микроразмножение растений, позволяющее из одного экспланта получать до 1 млн. растений
- 41. Культуры растительных клеток в суспензиях Растения: женьшень, раувольфия змеиная, наперстянка шерстистая и пурпурная, диоскорея дельтовидная, воробейник,
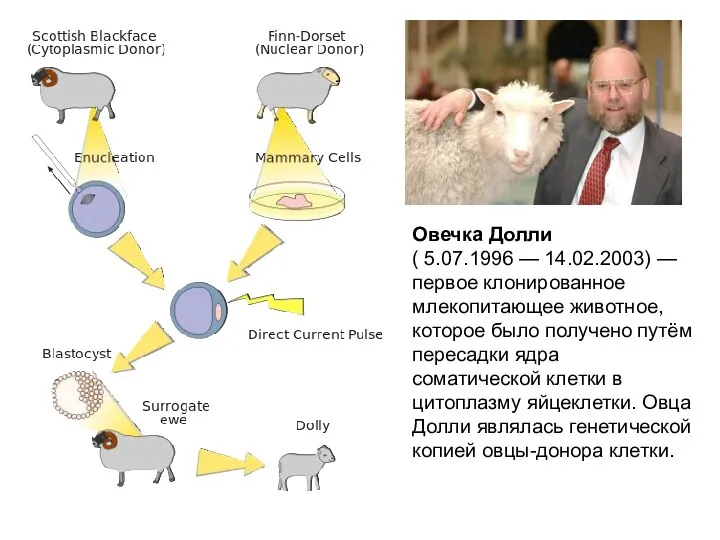
- 42. Овечка Долли ( 5.07.1996 — 14.02.2003) — первое клонированное млекопитающее животное, которое было получено путём пересадки
- 43. Первые клонированные животные 1996 — овечка Долли 1997 — мышь 1998 — корова 1999 — козёл
- 44. Клеточная инженерия человека Экстракорпоральное оплодотворение (ЭКО); Криоконсервация эмбрионов; Многолетнее ведение культур клеток человека; Культивирование фибробластов и
- 45. Достижения в области изучения и терапевтического использования стволовых клеток Испанские хирурги провели первую в мире трансплантацию
- 46. Создание iPS-клеток iPS-клетки (Induced Pluripotent Stem cells)- индуцированные плюрипотентные стволовые клетки. Основной метод перепрограммирования для получения
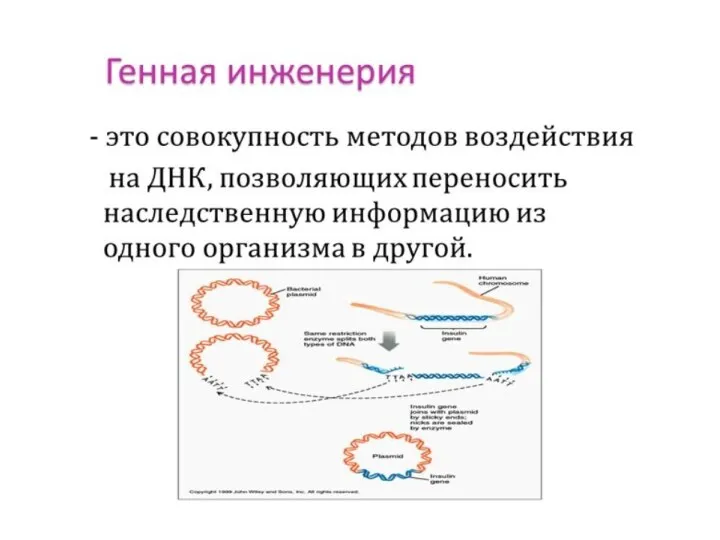
- 48. Генная инженерия — это отрасль молекулярной биологии и генетики, задачей которой является конструирование генетических структур по
- 49. Переносу генов предшествует кропотливая работа по выявлению нужного гена в геноме организма - донора (вируса, бактерии,
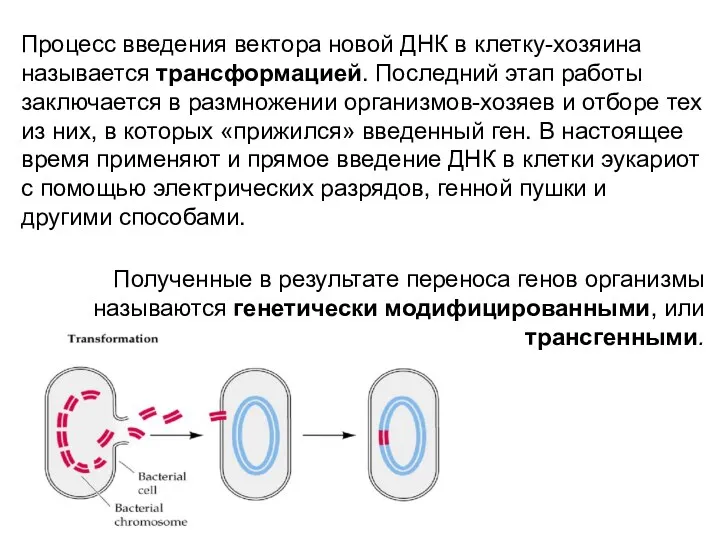
- 50. Процесс введения вектора новой ДНК в клетку-хозяина называется трансформацией. Последний этап работы заключается в размножении организмов-хозяев
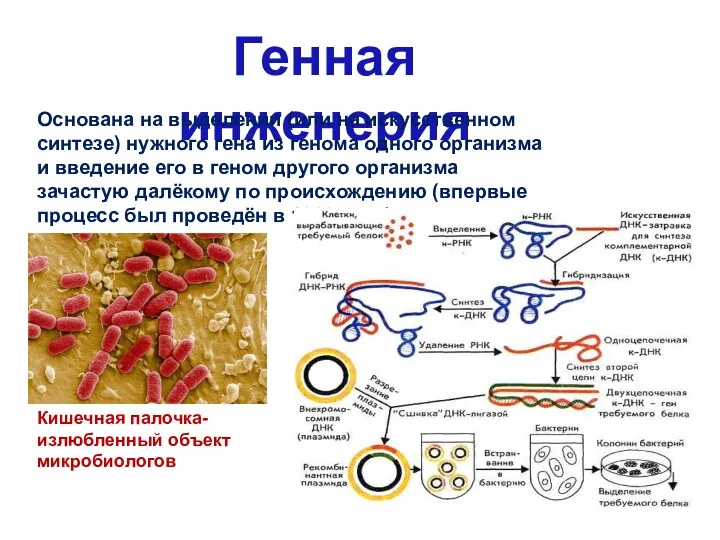
- 51. Генная инженерия Основана на выделении (или на искусственном синтезе) нужного гена из генома одного организма и
- 52. Генная инженерия Конструирование рекомбинантных молекул ДНК, внедрение селективных и репортёрных генов; Генетическая паспортизация; Диагностика генетических заболеваний;
- 53. История становления генной инженерии конструирование специальных штаммов кишечной палочки для промышленного производства человеческих гормонов – инсулина
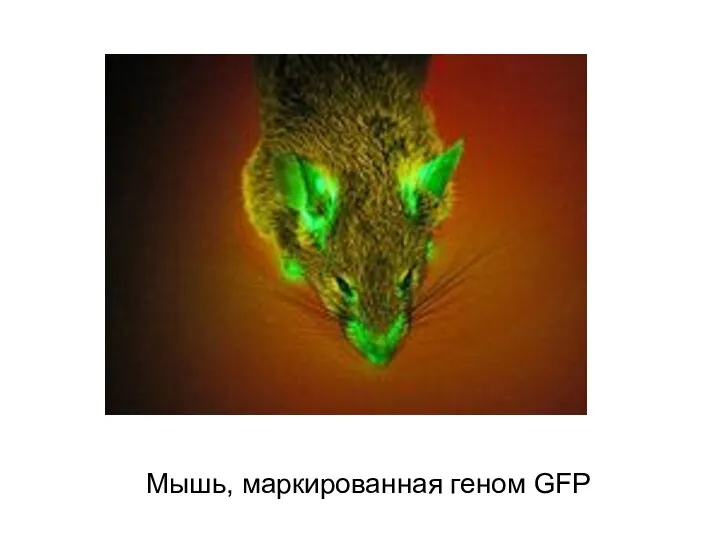
- 54. Мышь, маркированная геном GFP
- 55. Широко используются для прижизненного мечения белков, органелл и клеток генетические флуоресцирующие маркеры типа GFP (зелёные) и
- 56. «Светящиеся» ткани у трансгенных кур
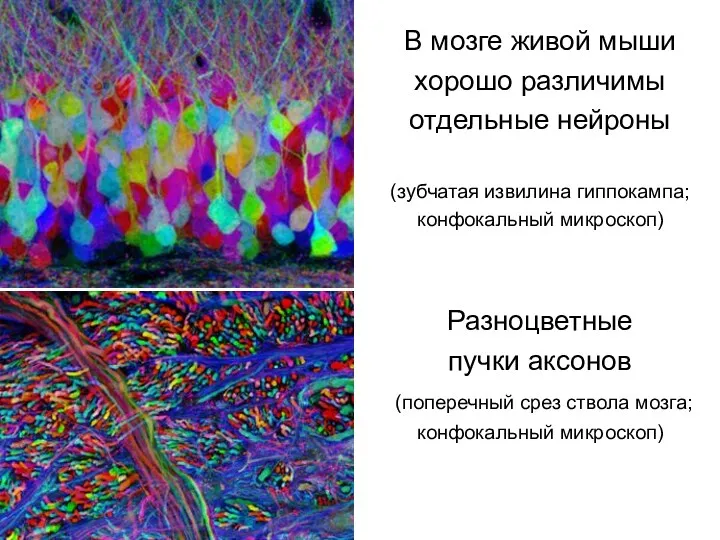
- 57. В мозге живой мыши хорошо различимы отдельные нейроны (зубчатая извилина гиппокампа; конфокальный микроскоп) Разноцветные пучки аксонов
- 58. «Светящиеся» рыбки данио рерио (GloFish) стали первым общедоступным генетически модифицирован-ным домашним животным.
- 59. Методы введения генов в клетку При помощи векторов (бактериальные плазмиды, вирусы, транспозоны и др.). Прямое введение
- 60. «Генная пушка» Метод биологической баллистики является одним из самых эффективных методов трансформации растений, особенно однодольных (кукуруза,
- 61. Генная пушка
- 62. Введение генов животным Лучшие векторы созданы на основе ретровирусов (вирус лейкоза мышей и др.). Ретровирусы обеспечивают
- 63. Фетальная генотерапия животных Введение генетической конструкции в зиготу или эмбрион на ранней стадии развития. Трансгенные животные
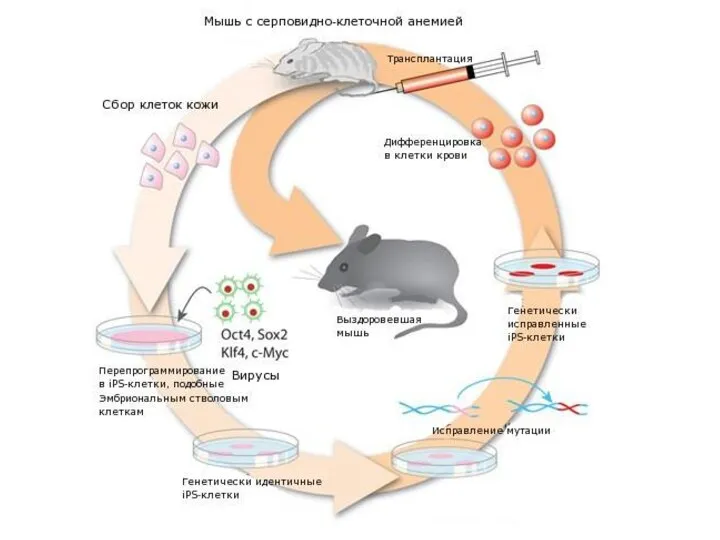
- 64. Соматическая генотерапия животных в 2007 г. мыши, больные человеческой серповидноклеточной анемией, были вылечены с помощью перепрограммированных
- 66. В 2008 г. биологи Гарвардского университета сумели перепрограммировать взрослые клетки в эмбриональные непосредственно в живом организме,
- 67. Успехи генетической инженерии в экспериментах над приматами Доказана возможность «вживления» искусственно модифицированного гена в ткани взрослых
- 68. Соматическая генотерапия человека Амавроз Лебера - врождённая слепота. Инъекция вектора с геном, кодирующим светочувствительный пигмент, в
- 69. Применение генной инженерии в сельском хозяйстве Первые трансгенные растения (растения табака со встроенными генами из микроорганизмов)
- 70. Первые трансгенные продукты появились в продаже в США в 1994 г. томаты «Flavr Savr» с замедленным
- 71. Трансгенный хлопчатник В 1997 году в Китае начали выращивать трансгенный хлопчатник, в геном которого был вставлен
- 72. В XXI веке начала развиваться «метаболическая инженерия» - получение организмов, содержащих ценные белки, модифицированные полисахариды, вакцины,
- 73. Значение биотехнологии для развития селекции, сельского хозяйства, микробиологической промышленности, сохранения генофонда планеты Прогресс биотехнологии позволил совершить
- 74. Культивирование клеток растений на фоне высоких концентраций солей и других соединений позволяет сократить сроки выведения новых
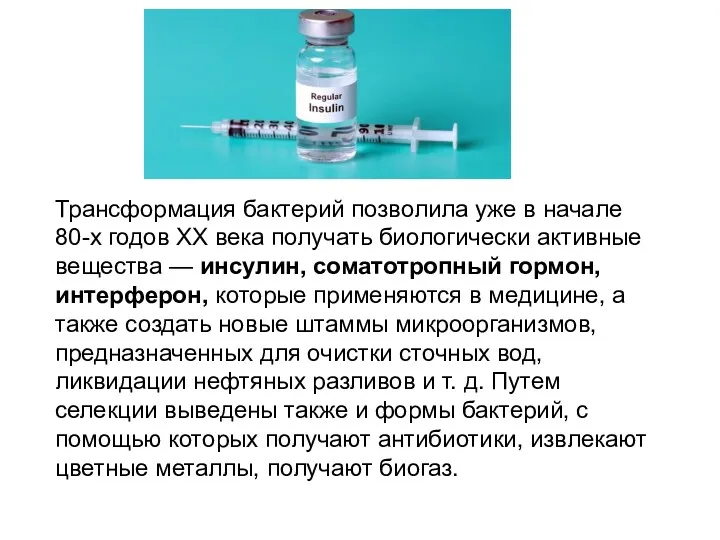
- 75. Трансформация бактерий позволила уже в начале 80-х годов ХХ века получать биологически активные вещества — инсулин,
- 76. Успехи в выведении трансгенных животных В 1980-х гг. фирма «AquaBounty» (Массачусетс) впервые ввела в икринки атлантического
- 78. Скачать презентацию




























































 Основи ембріології
Основи ембріології Выделение веществ как важнейший процесс жизнедеятельности организмов. 6 класс
Выделение веществ как важнейший процесс жизнедеятельности организмов. 6 класс Вегетативная нервная система
Вегетативная нервная система презентация по биологии Ароморфозы и идиоадаптации
презентация по биологии Ароморфозы и идиоадаптации Мир динозавров
Мир динозавров Өсімдіктердің көптүрлілігі
Өсімдіктердің көптүрлілігі Выделение у растений и животных
Выделение у растений и животных Використання мутагегезу в селекції польових культур
Використання мутагегезу в селекції польових культур Отряд Приматы
Отряд Приматы Цитология. Методологические подходы
Цитология. Методологические подходы Биология наука о жизни
Биология наука о жизни Физиология растений. Лекция 2
Физиология растений. Лекция 2 Моногибридное скрещивание
Моногибридное скрещивание Внешнее строение и разнообразие листьев
Внешнее строение и разнообразие листьев Радіобіологія організму людини і тварин. Радіочутливість тканин і органів організму людини і тварин
Радіобіологія організму людини і тварин. Радіочутливість тканин і органів організму людини і тварин Международный день птиц
Международный день птиц Лесные животные. Часть 1 Медведь
Лесные животные. Часть 1 Медведь Полет птиц
Полет птиц Немембранные и двумембранные органоиды
Немембранные и двумембранные органоиды Скелет конечностей
Скелет конечностей Растения влажных экваториальных лесов
Растения влажных экваториальных лесов Поведінка риб
Поведінка риб Типы внешнего проявления болезней
Типы внешнего проявления болезней Первая помощь при солнечном и тепловом ударе
Первая помощь при солнечном и тепловом ударе Нервная система. Строение и функции НС, спинного мозга, головного мозга
Нервная система. Строение и функции НС, спинного мозга, головного мозга Индивидуальное развитие организмов – онтогенез
Индивидуальное развитие организмов – онтогенез Экология микроорганизмов - среды обитания и временного сохранения. Микроорганизмы - биодеструкторы. Лекция 5
Экология микроорганизмов - среды обитания и временного сохранения. Микроорганизмы - биодеструкторы. Лекция 5 Большие и маленькие улиточки
Большие и маленькие улиточки