Содержание
- 2. Смысл изучения биохимии: - понимание причинно-следственных связей - база для других предметов – физиологии, патофизиологии, фармакологии,
- 3. 1. Т.Т. Березов, Б.Ф. Коровкин. Биологическая химия: Учебник. - 4-е издание - М.: Медицина, 2007. 2.
- 4. Ленинджер А., Основы биохимии, тт. 1-3, М.: Мир, 1985 Марри Р., Греннер Д., Мейес П., Родуэлл
- 5. БЕЛКИ. СТРУКТУРА И ФУНКЦИИ
- 6. Белки - полимерные молекулы, в которых мономерами служат аминокислоты. В составе белков в организме человека встречают
- 7. Элементный состав белков практически одинаковый: С (50-54%), Н(8%), О (22%), N (15-17%) и S (0.3-2.5%) или
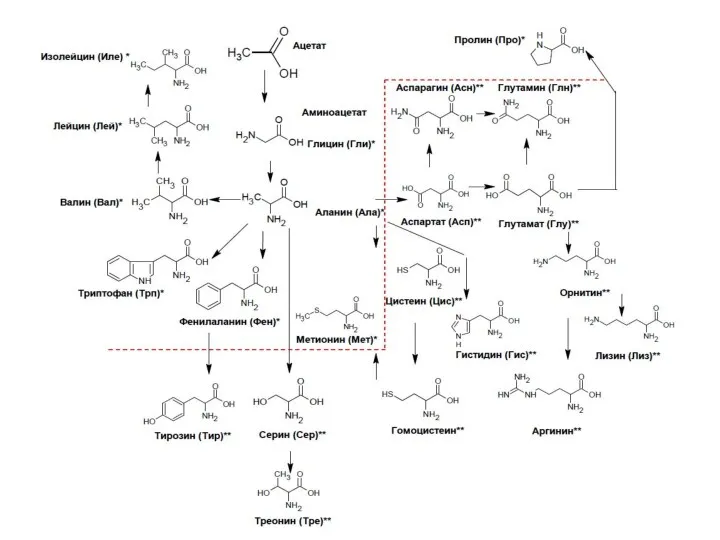
- 8. Для животных и человека 10 из 20-ти АМК должны поступать с пищей и являются незаменимыми: валин,
- 9. Строение и свойства аминокислот
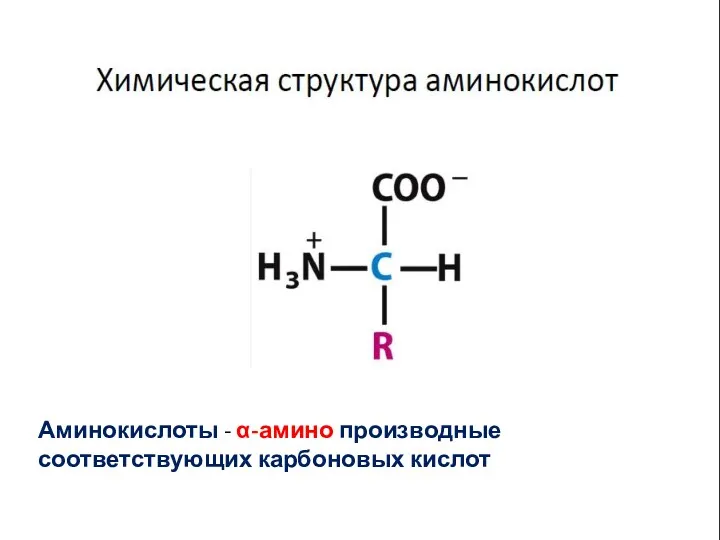
- 10. Аминокислоты - α-амино производные соответствующих карбоновых кислот
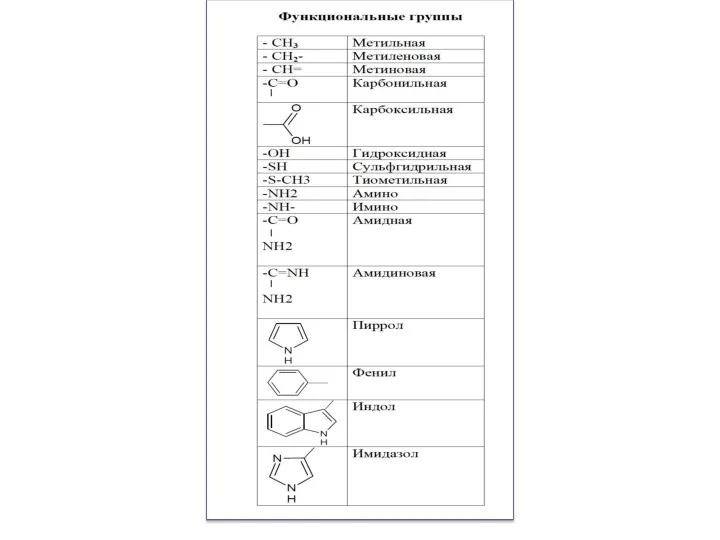
- 13. В составе алифатических радикалов АМК могут находиться функциональные группы, придающие им специфические свойства: карбоксильная (-СООН), амино
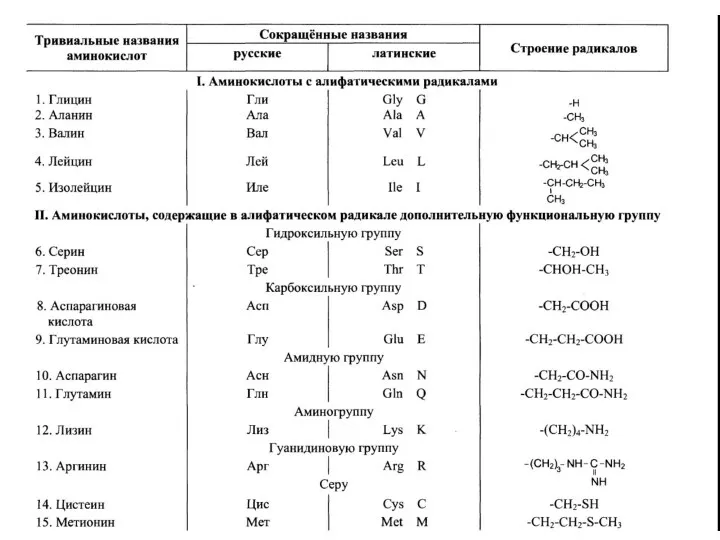
- 14. Названия аминокислот можно построить по заместительной номенклатуре, но обычно используют тривиальные названия
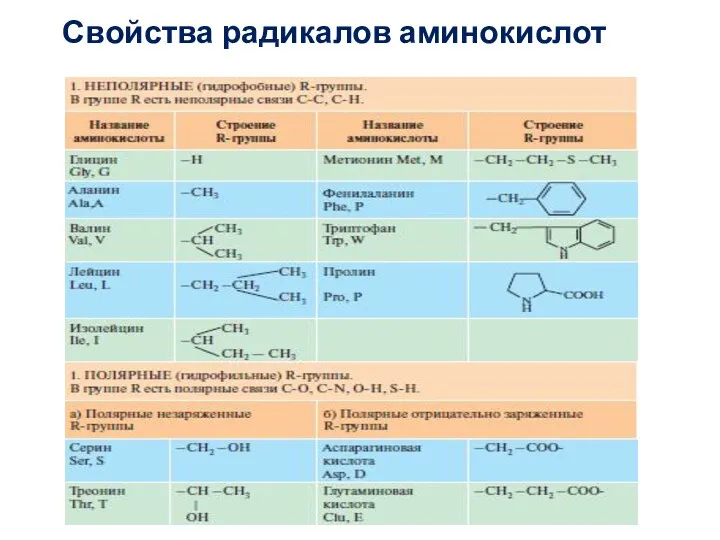
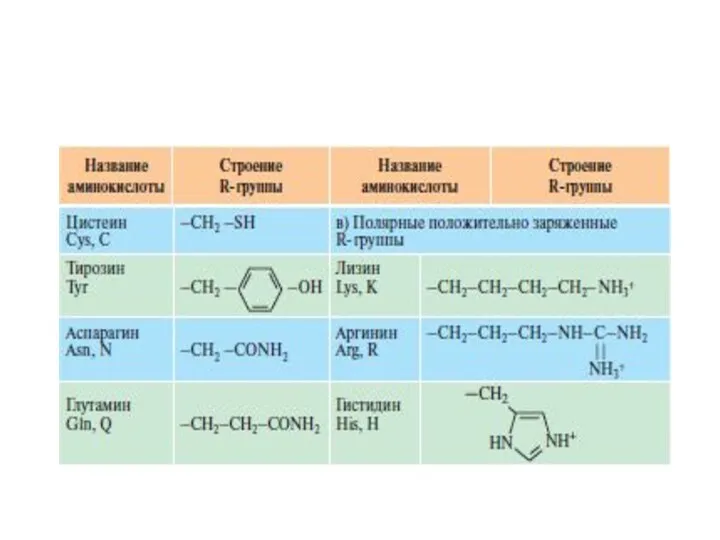
- 15. Свойства радикалов аминокислот
- 17. Для записи аминокислотных остатков в молекулах пептидов и белков используют трёхбуквенные сокращения их тривиальных названий, а
- 18. Протеиногенные АМК содержат ассиметричный С и относятся к изомерам L-ряда. D-изомеры встречаются редко, в частности, в
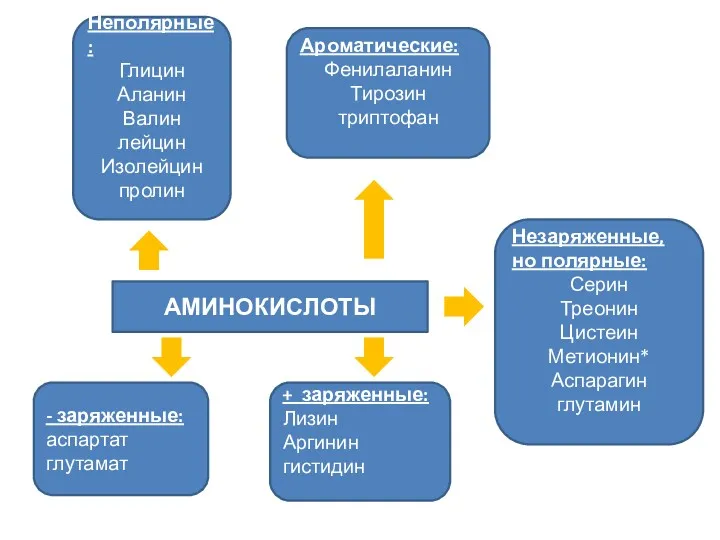
- 19. АМИНОКИСЛОТЫ Неполярные: Глицин Аланин Валин лейцин Изолейцин пролин Ароматические: Фенилаланин Тирозин триптофан Незаряженные, но полярные: Серин
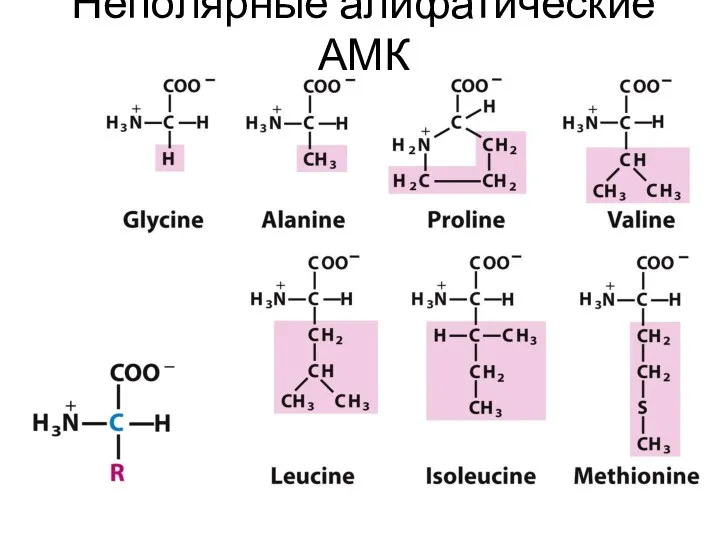
- 20. Неполярные алифатические АМК
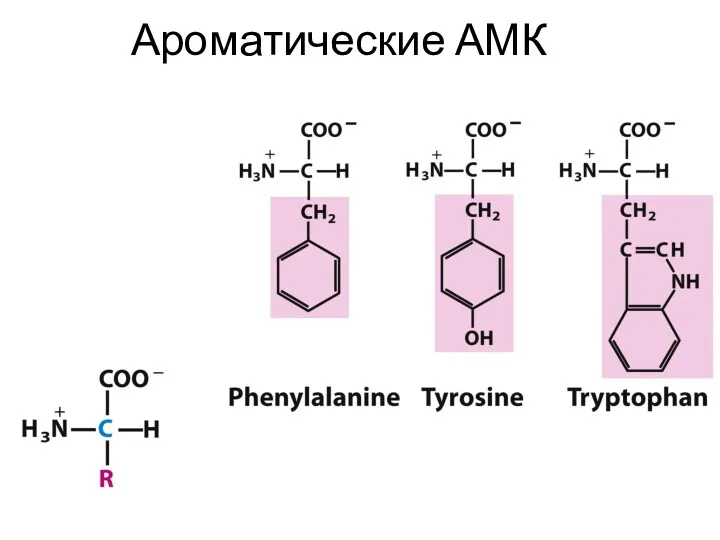
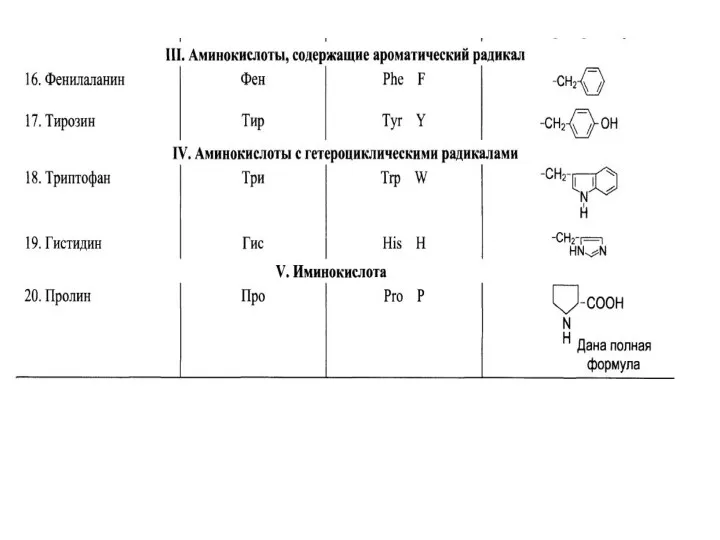
- 21. Ароматические АМК
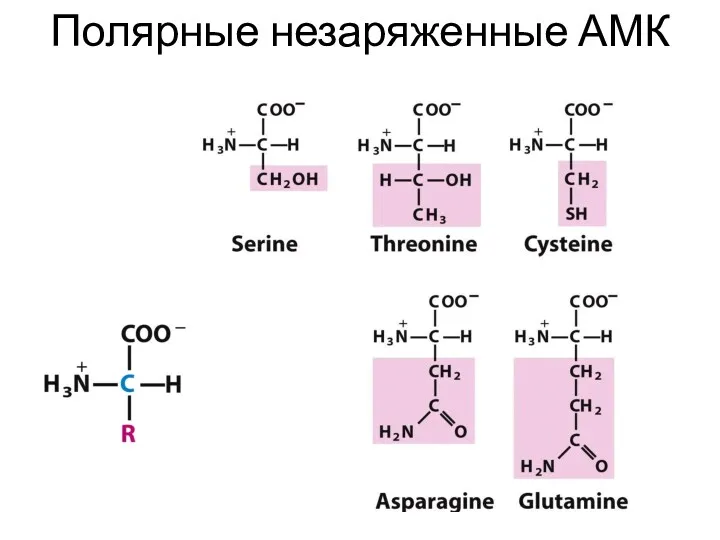
- 22. Полярные незаряженные АМК
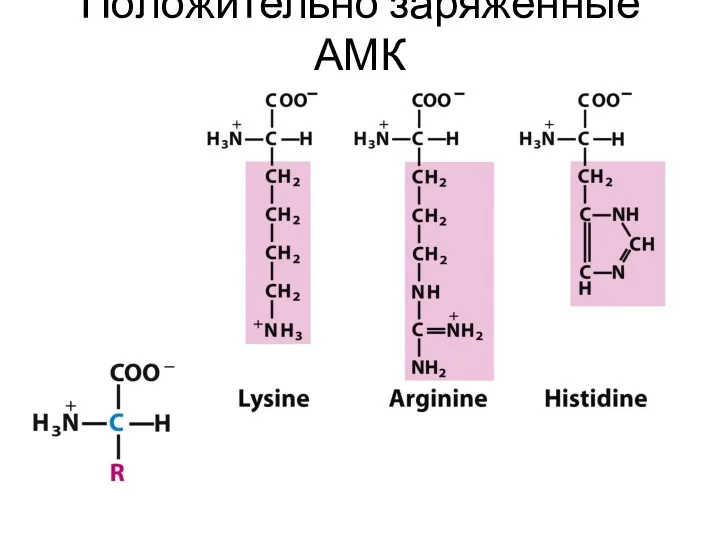
- 23. Положительно заряженные АМК
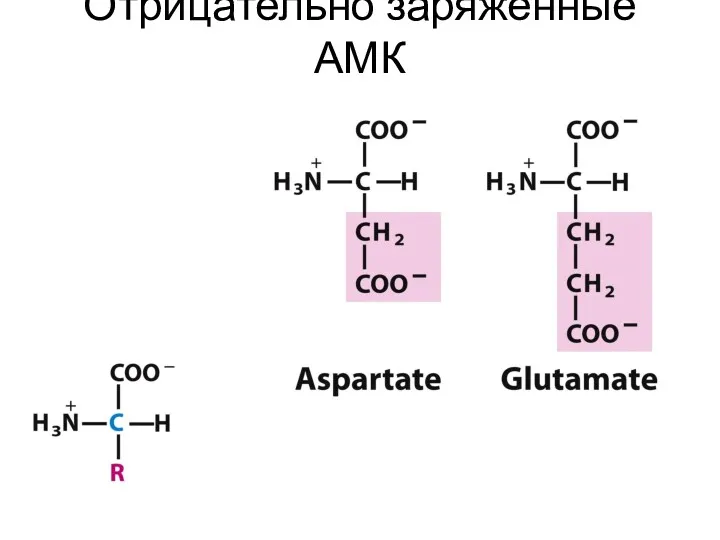
- 24. Отрицательно заряженные АМК
- 28. Все 20 аминокислот в белках организма человека можно сгруппировать по способности их радикалов растворяться в воде.
- 29. Аминокислоты с неполярными радикалами К неполярным (гидрофобным) АМК относят радикалы, имеющие алифатические углеводородные цепи (радикалы аланина,
- 30. Аминокислоты с полярными незаряженными радикалами Радикалы этих АМК лучше, чем гидрофобные радикалы, растворяются в воде, так
- 31. Аминокислоты с полярными отрицательно заряженными радикалами К этой группе относят аспарагиновую и глутаминовую аминокислоты, имеющие в
- 32. Наибольшей растворимостью в воде обладают полярные заряженные радикалы аминокислот
- 33. Аминокислоты с полярными положительно заряженными радикалами Дополнительную положительно заряженную группу в радикале имеют лизин и аргинин.
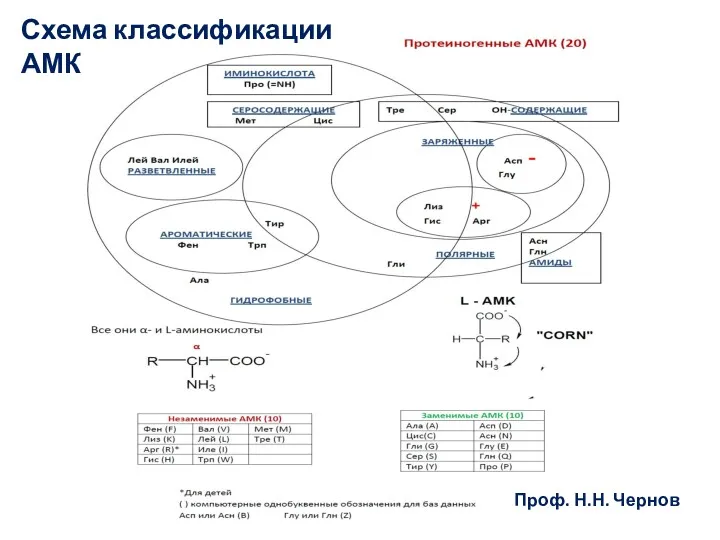
- 34. Схема классификации АМК Проф. Н.Н. Чернов
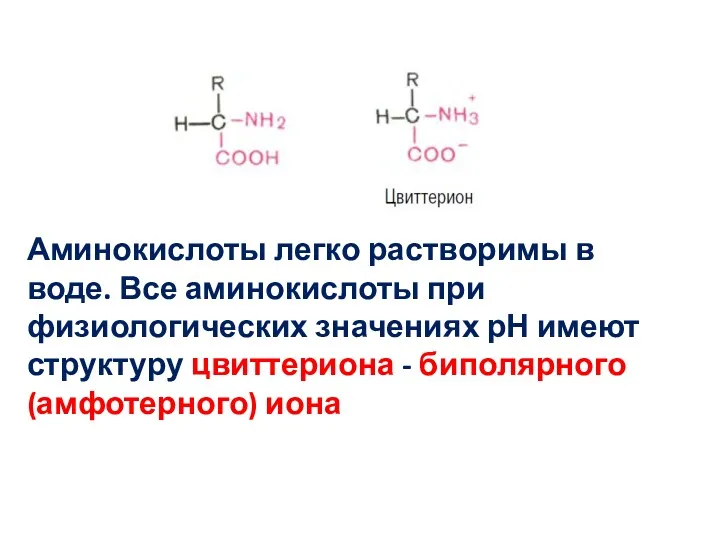
- 35. Аминокислоты легко растворимы в воде. Все аминокислоты при физиологических значениях рН имеют структуру цвиттериона - биполярного
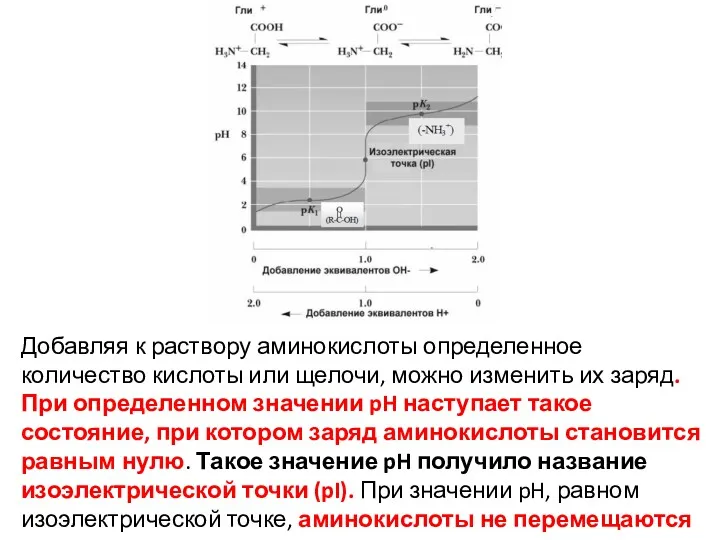
- 36. Добавляя к раствору аминокислоты определенное количество кислоты или щелочи, можно изменить их заряд. При определенном значении
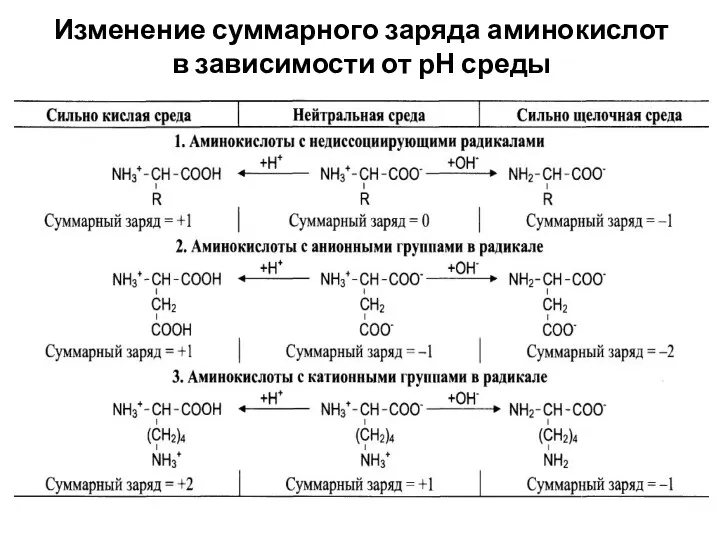
- 37. Изменение суммарного заряда аминокислот в зависимости от рН среды
- 38. При нейтральных значениях рН все кислотные (способные отдавать Н+) и все основные (способные присоединять Н+) функциональные
- 39. Изменение суммарного заряда аминокислот в зависимости от рН среды
- 40. Модифицированные аминокислоты, присутствующие в белках Непосредственно в синтезе белков организма человека принимают участие только 20 перечисленных
- 41. Введение дополнительных функциональных групп в структуру аминокислот придаёт белкам свойства, необходимые для выполнения ими специфических функций.
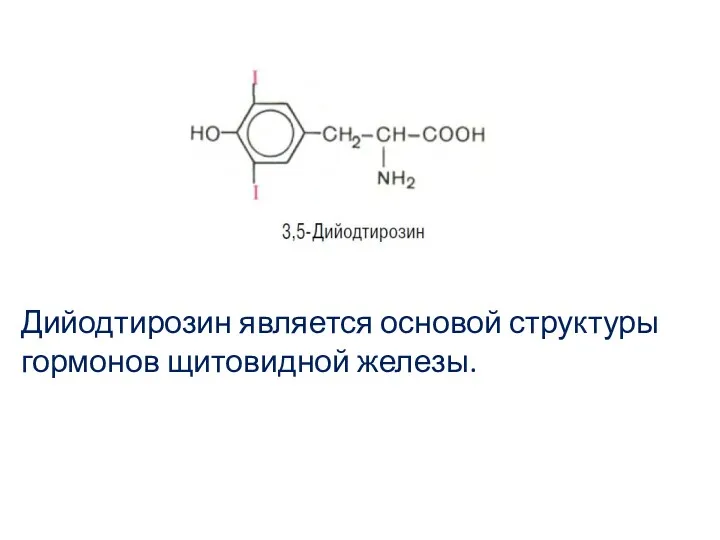
- 42. Дийодтирозин является основой структуры гормонов щитовидной железы.
- 43. Ряд α-аминокислот выполняет важные функции в обмене веществ, хотя и не входит в состав белков, в
- 44. Химические реакции, используемые для обнаружения аминокислот Способность аминокислот вступать в те или иные химические реакции определяется
- 45. Универсальные реакции: Биуретовая реакция (реакция на наличие пептидной связи в беках и олигопептидах) Сиреневая окраска Нингидриновая
- 47. Скачать презентацию


























 Рыбы реки Ирень
Рыбы реки Ирень Презентация к уроку биологии 7 класс
Презентация к уроку биологии 7 класс ип: Моллюски. Класс: Брюхоногие.(7 класс)
ип: Моллюски. Класс: Брюхоногие.(7 класс) Тип Моллюски
Тип Моллюски Уровни организацииживой материи
Уровни организацииживой материи Энергетикалық алмасудың маңызы
Энергетикалық алмасудың маңызы Ракообразные. Внешнее строение. Внутреннее строение
Ракообразные. Внешнее строение. Внутреннее строение Одноклеточные животные
Одноклеточные животные Почва экологический фактор. Проблемы загрязнения и деградации
Почва экологический фактор. Проблемы загрязнения и деградации Презентация проверка домашнего задания по теме: Общая характеристика Класса Моллюски
Презентация проверка домашнего задания по теме: Общая характеристика Класса Моллюски Микробиология зерновых продуктов
Микробиология зерновых продуктов Грибы – паразиты зерновых
Грибы – паразиты зерновых Значение опорно-двигательного аппарата, его состав. Строение костей
Значение опорно-двигательного аппарата, его состав. Строение костей Вирусы. Строение вируса. Типы капсидов
Вирусы. Строение вируса. Типы капсидов Животные Пермского периода
Животные Пермского периода Животные национальные символы стран мира
Животные национальные символы стран мира Сон. Функції сну
Сон. Функції сну Углеводы и их биологическая роль
Углеводы и их биологическая роль Введение в методы анализа продуктов биотехнологии
Введение в методы анализа продуктов биотехнологии Физиология центральной нервной системы
Физиология центральной нервной системы бесполое размножение организмов
бесполое размножение организмов Тип Кишечнополостные. Биология. 7 класс
Тип Кишечнополостные. Биология. 7 класс Части лесной зоны
Части лесной зоны Животные Антарктиды
Животные Антарктиды От семечки до цветка
От семечки до цветка Продукты пчеловодства
Продукты пчеловодства Необычные рыбы
Необычные рыбы Вегетативное размножение растений
Вегетативное размножение растений