Содержание
- 2. Сложные белки - протеиды Сложные белки классифицируются по характеру простетической группы: Хромопротеиды ( к ним относятся
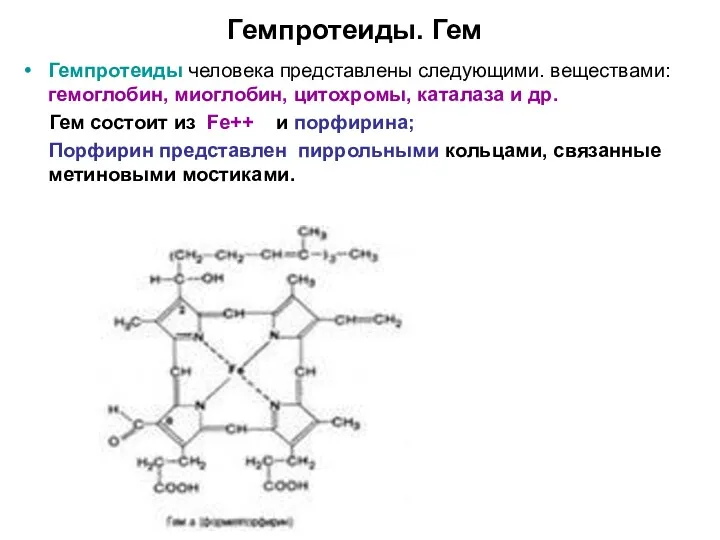
- 3. Гемпротеиды. Гем Гемпротеиды человека представлены следующими. веществами: гемоглобин, миоглобин, цитохромы, каталаза и др. Гем состоит из
- 4. Гемоглобин Молекула гемоглобина А представлена: 4 гема связаны с попарноодинаковыми пептидными цепями 2L = 2β Синтез
- 5. Источники гема Пищевые продукты - (экзогенный путь) не имеет значения. В пищевом рационе в составе продуктов
- 6. Синтез гема Синтез de novo – источник гема!!! Место синтеза все ткани (не имеет значения), основное
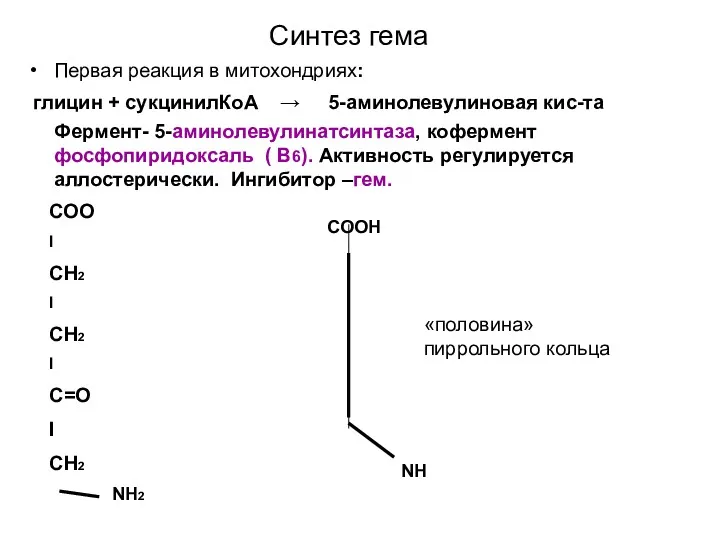
- 7. Синтез гема Первая реакция в митохондриях: глицин + сукцинилКоА → 5-аминолевулиновая кис-та Фермент- 5-аминолевулинатсинтаза, кофермент фосфопиридоксаль
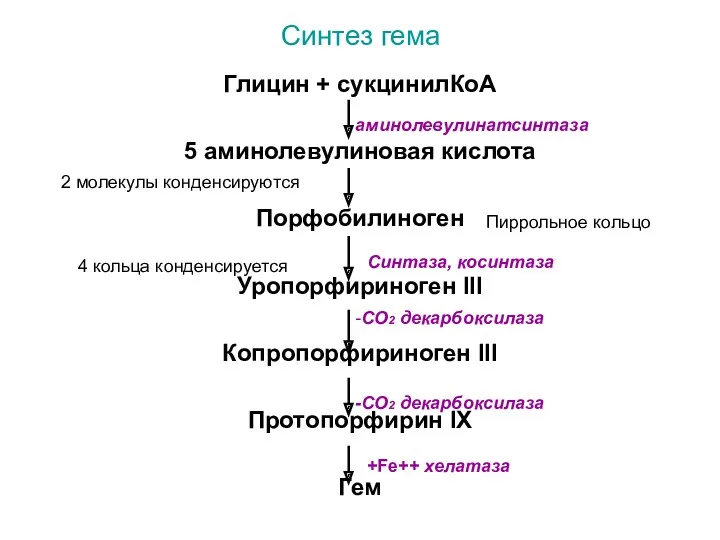
- 8. Синтез гема Глицин + сукцинилКоА 5 аминолевулиновая кислота Порфобилиноген Уропорфириноген III Копропорфириноген III Протопорфирин IХ Гем
- 9. Нарушения синтеза гема Порфирии - (порфирин – пурпурный(греч.) сопровождаются накоплением в крови порфириногенов и их окисленных
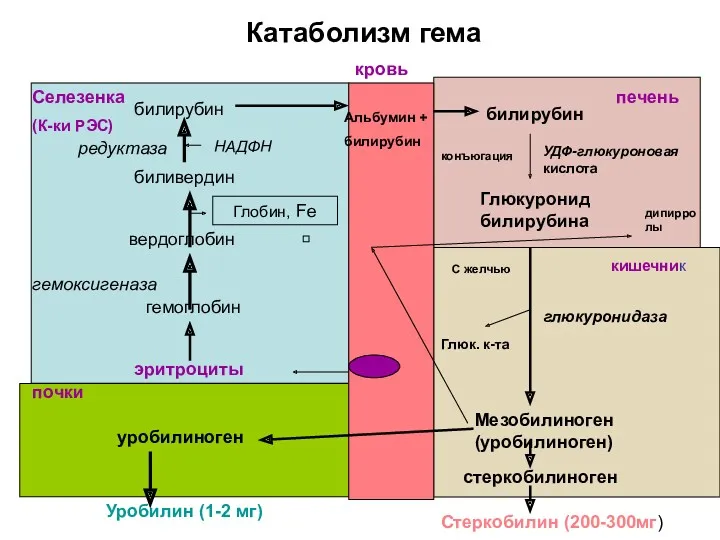
- 10. Катаболизм гема Селезенка (К-ки РЭС) почки печень кишечник эритроциты вердоглобин биливердин билирубин гемоглобин Глобин, Fe Альбумин
- 11. Билирубин – основной метаболит гема (гидрофобный) В норме в крови общего билирубина до 20 мкмоль/л Свободный
- 12. Метаболизм нуклеотидов
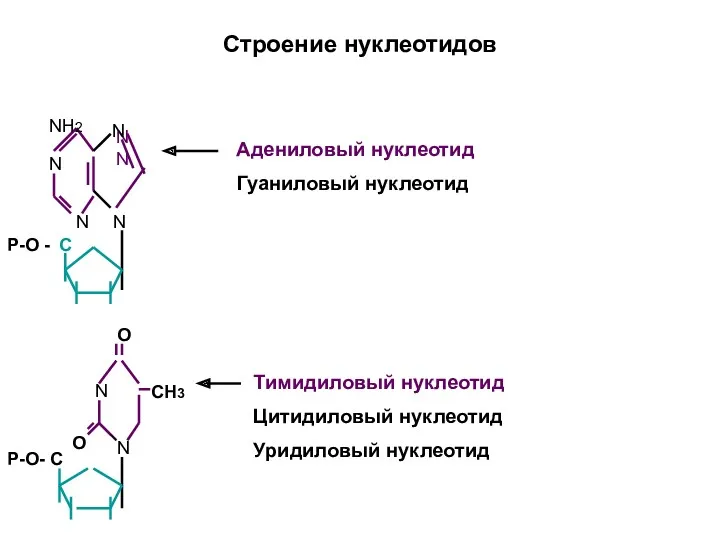
- 13. Строение нуклеотидов N N NN N N C P-O - N N P-O- C NH2 CH3
- 14. Метаболизм нуклеотидов – (простетическая группа нуклеопротеидов) Значение нуклеотидов: Мономеры нуклеиновых кислот – ДНК и РНК; Нуклеотиды-
- 15. Источники нуклеотидов 1. Биосинтез de novo (практически во всех тканях) !!!! 2. Повторный синтез из готовых
- 16. Превращение нуклеопротеидов пищи в ЖКТ нуклеопротеиды HCL Пепсин - желудок Трипсин - 12 перстная кишка Нуклеиновые
- 17. Биосинтез нуклеотидов de novo !!! Азотистые основания синтезируются из низкомолекулярных предшественников Рибозы- источник - пентозофосфатный путь;
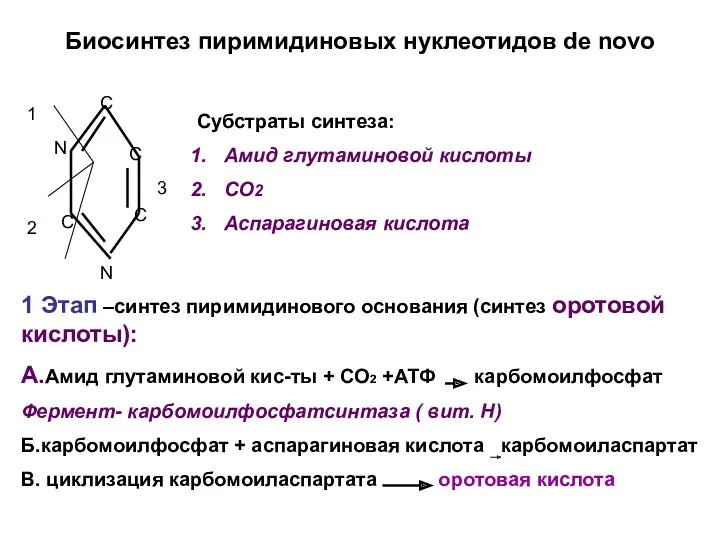
- 18. Биосинтез пиримидиновых нуклеотидов de novo N N C C C C 1 2 3 Субстраты синтеза:
- 19. Биосинтез пиримидиновых нуклеотидов N N C=O CH C-COOH O=C Оротовая кислота -сформированное пиримидиновое кольцо 2 этап:
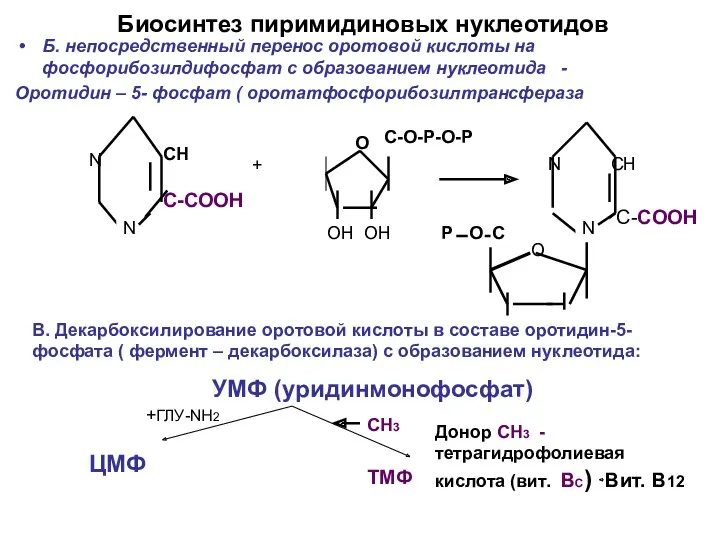
- 20. Биосинтез пиримидиновых нуклеотидов Б. непосредственный перенос оротовой кислоты на фосфорибозилдифосфат с образованием нуклеотида - Оротидин –
- 21. Нарушение синтеза пиримидиновых нуклеотидов Оротацидурия ( генетически обусловленное) Энзимдефекты- оротатфосфорибозилтрансфераза, декарбоксилаза; «Пиримидиновый голод»- мегалобластичес- кая анемия
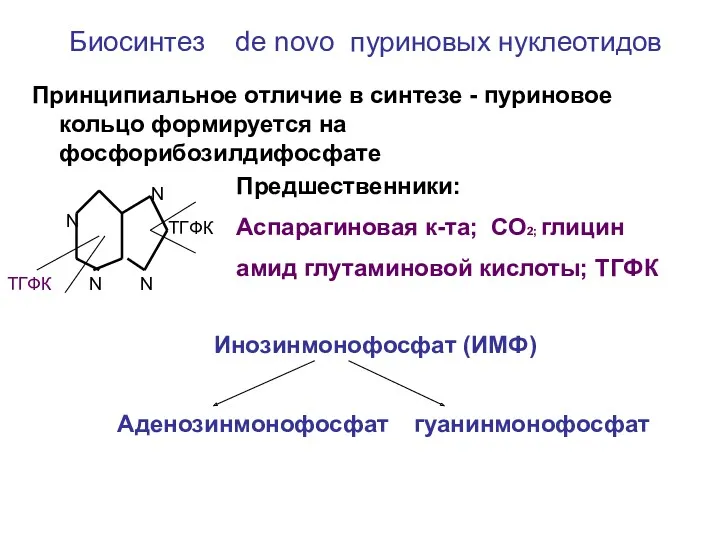
- 22. Биосинтез de novo пуриновых нуклеотидов Принципиальное отличие в синтезе - пуриновое кольцо формируется на фосфорибозилдифосфате N
- 23. Катаболизм пуриновых нуклеотидов 1 Этап: распад нуклеотида в тканях до азотистого основания, рибозы(дезокси-),фосфорная кислота. Ферменты :
- 25. Скачать презентацию














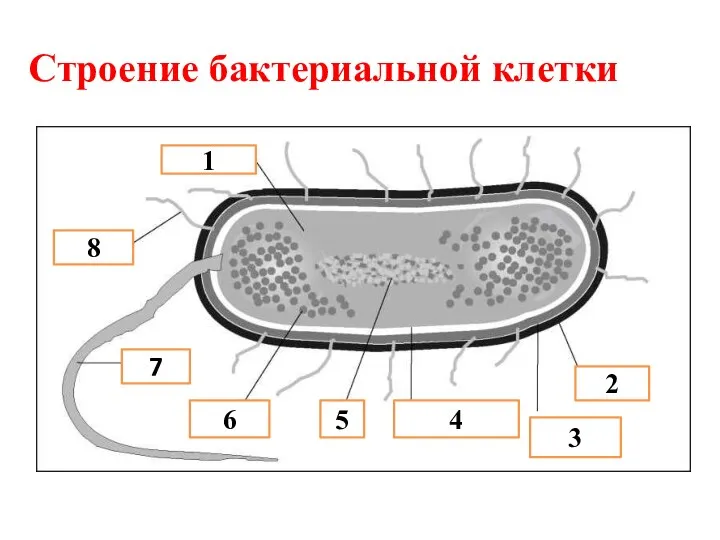 Строение бактериальной клетки
Строение бактериальной клетки Пингвин – необычная птица
Пингвин – необычная птица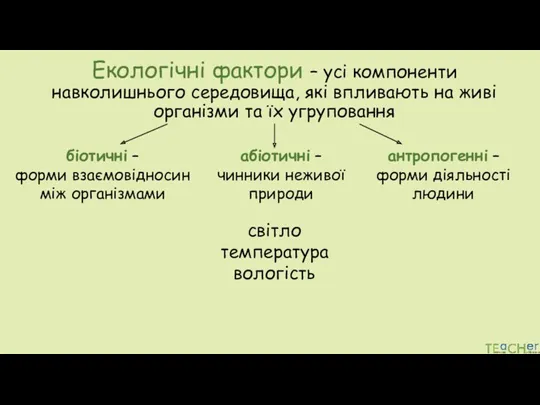 Екологічні фактори. Форми біотичних зв’язків
Екологічні фактори. Форми біотичних зв’язків Визажистика. Строение лица
Визажистика. Строение лица Физические процессы в биологических мембранах. Лекция 8
Физические процессы в биологических мембранах. Лекция 8 Презентация кабинета биологии
Презентация кабинета биологии Млекопитающие различных экосистем
Млекопитающие различных экосистем Строение сердечнососудистой системы
Строение сердечнососудистой системы Бесполое размножение
Бесполое размножение Везикулярлық тасымалдау
Везикулярлық тасымалдау Совы. Виды
Совы. Виды Животные крайнего Севера
Животные крайнего Севера Сауын сиырды азықтандыру
Сауын сиырды азықтандыру Презентация к уроку биологии 6 кл.
Презентация к уроку биологии 6 кл. Практична робота №1. Виявлення прикладів пристосування до способу життя у комах
Практична робота №1. Виявлення прикладів пристосування до способу життя у комах Факторы влияющие на качество молока. Лекция 4
Факторы влияющие на качество молока. Лекция 4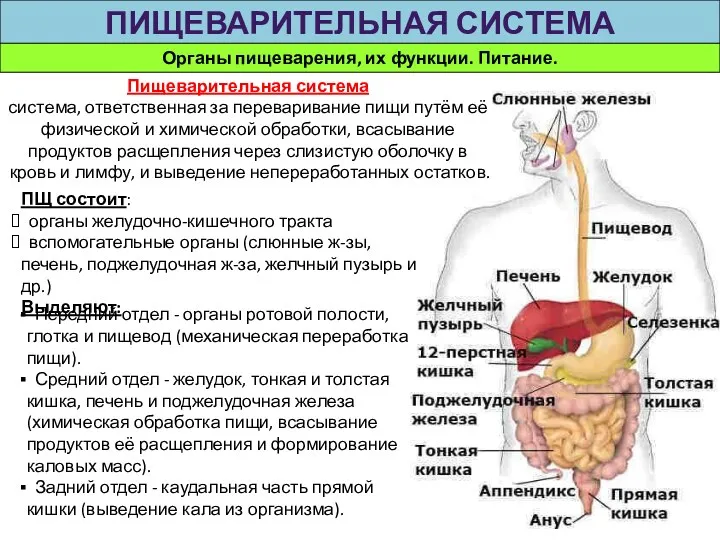 Органы пищеварения, их функции. Питание. Пищеварительная система
Органы пищеварения, их функции. Питание. Пищеварительная система Амфібії. 7 клас
Амфібії. 7 клас Насекомые луга
Насекомые луга Otters. Выдры
Otters. Выдры Детская неврология. Анатомия и физиология нервной системы. (Часть 1)
Детская неврология. Анатомия и физиология нервной системы. (Часть 1) нервно - гуморальная регуляция организма
нервно - гуморальная регуляция организма Нервная система
Нервная система Возможности и особенности человеческого глаза
Возможности и особенности человеческого глаза Разнообразие растительного мира. Семейство Норичниковые
Разнообразие растительного мира. Семейство Норичниковые Cистема кровообращения
Cистема кровообращения Моё увлечение - конный спорт
Моё увлечение - конный спорт Как питаются разные животные?
Как питаются разные животные?