Слайд 2

В процессе эволюции сформировались различные типы азотистого обмена, которые классифицируются по
основному конечному продукту:
1) аммониотелический тип, главный конечный продукт — аммиак (рыбы);
2) урикотелинеский тип, главный конечный продукт — мочевая кислота (рептилии, птицы);
3) уреотелический тип, главный конечный продукт — мочевина (млекопитающие).
Слайд 3
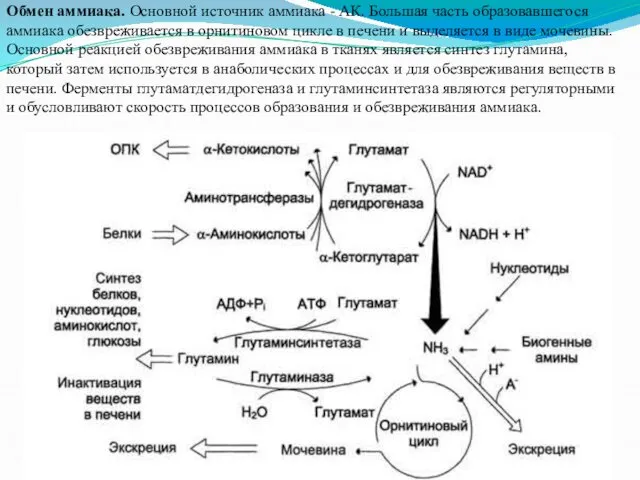
Обмен аммиака. Основной источник аммиака - АК. Большая часть образовавшегося аммиака
обезвреживается в орнитиновом цикле в печени и выделяется в виде мочевины. Основной реакцией обезвреживания аммиака в тканях является синтез глутамина, который затем используется в анаболических процессах и для обезвреживания веществ в печени. Ферменты глутаматдегидрогеназа и глутаминсинтетаза являются регуляторными и обусловливают скорость процессов образования и обезвреживания аммиака.
Слайд 4
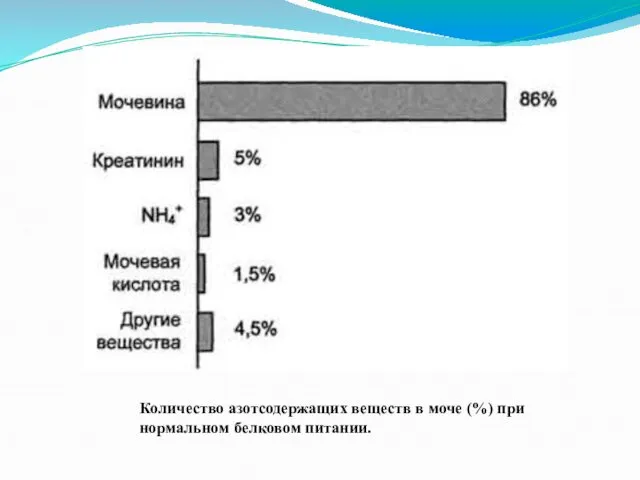
Количество азотсодержащих веществ в моче (%) при нормальном белковом питании.
Слайд 5

поступление аммиака из кишечника в портальную вену
Слайд 6
Слайд 7

Функции аммиака
Аммиак вовлекается (непосредственно или через глутамин) в синтез многих компонентов
организма: заменимые аминокислоты, пурины, пиримидины, аминосахара и т. д.
Слайд 8

Аммиак - токсичное соединение. Даже небольшое повышение его концентрации оказывает неблагоприятное
действие на организм, и прежде всего на ЦНС. Так, повышение концентрации аммиака в мозге до 0,6 ммоль вызывает судороги. К симптомам гипераммониемии относят тремор, нечленораздельную речь, тошноту, рвоту, головокружение, судорожные припадки, потерю сознания. В тяжёлых случаях развивается кома с летальным исходом.
Механизм токсического действия аммиака на мозг и организм в целом, очевидно, связан с действием его на несколько функциональных систем.
Аммиак легко проникает через мембраны в клетки и в митохондриях сдвигает реакцию, катализируемую глутаматдегидрогеназой, в сторону образования глутамата:
α-Кетоглутарат + NADH + Н+ + NH3 → Глутамат + NAD+.
Уменьшение концентрации α-кетоглутарата вызывает:
угнетение обмена аминокислот (реакции транса-минирования) и, следовательно, синтеза из них нейромедиаторов (ацетилхолина, дофамина и др.);
гипоэнергетическое состояние в результате снижения скорости ЦТК.
Слайд 9

Недостаточность α-кетоглутарата приводит к снижению концентрации метаболитов ЦТК, что вызывает ускорение
реакции синтеза оксалоацетата из пирувата, сопровождающейся интенсивным потреблением СО2. Усиленное образование и потребление диоксида углерода при гипераммониемии особенно характерны для клеток головного мозга.
Повышение концентрации аммиака в крови сдвигает рН в щелочную сторону (вызывает алкалоз). Это, в свою очередь, увеличивает сродство гемоглобина к кислороду, что приводит к гипоксии тканей, накоплению СО2 и гипоэнергетическому состоянию, от которого главным образом страдает головной мозг.
Высокие концентрации аммиака стимулируют синтез глутамина из глутамата в нервной ткани (при участии глутаминсинтетазы):
Глутамат + NH3 + АТФ → Глутамин + АДФ + Н3Р04.
Накопление глутамина в клетках нейроглии приводит к повышению осмотического давления в них, набуханию астроцитов и в больших концентрациях может вызвать отёк мозга. Снижение концентрации глутамата нарушает обмен аминокислот и нейромедиаторов, в частности синтез ϒ-аминомасляной кислоты (ГАМК), основного тормозного медиатора. При недостатке ГАМК и других медиаторов нарушается проведение нервного импульса, возникают судороги.
Ион NH4+ практически не проникает через цитоплазматические и митохондриальные мембраны. Избыток иона аммония в крови способен нарушать трансмембранный перенос одновалентных катионов Na+ и К+, конкурируя с ними за ионные каналы, что также влияет на проведение нервных импульсов.
Слайд 10
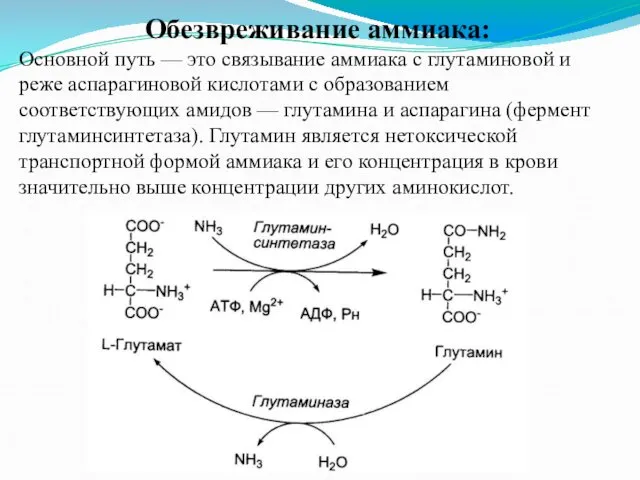
Обезвреживание аммиака:
Основной путь — это связывание аммиака с глутаминовой и реже
аспарагиновой кислотами с образованием соответствующих амидов — глутамина и аспарагина (фермент глутаминсинтетаза). Глутамин является нетоксической транспортной формой аммиака и его концентрация в крови значительно выше концентрации других аминокислот.
Слайд 11
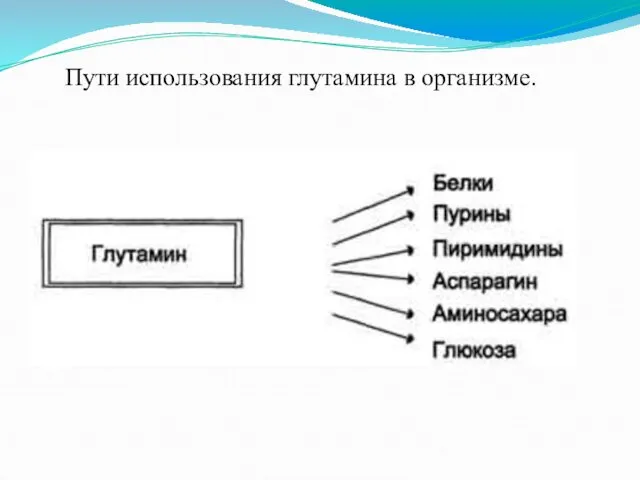
Пути использования глутамина в организме.
Слайд 12
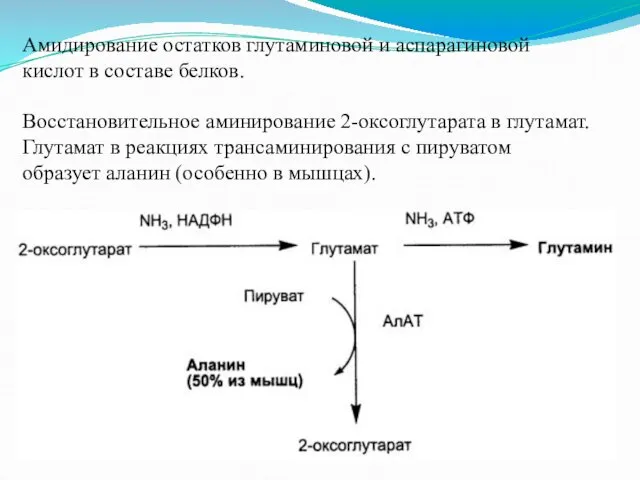
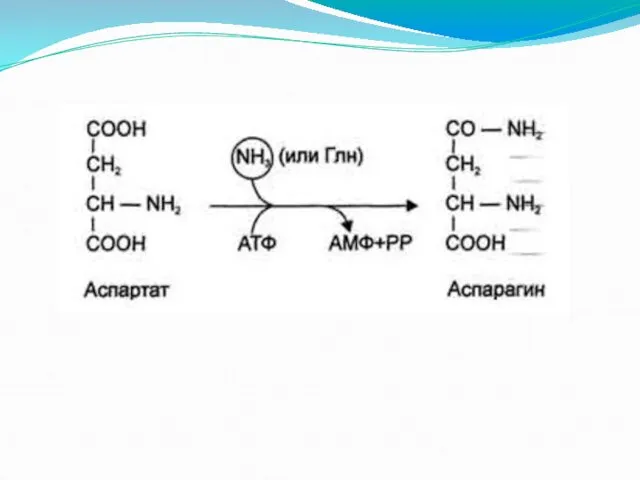
Амидирование остатков глутаминовой и аспарагиновой кислот в составе белков.
Восстановительное аминирование 2-оксоглутарата
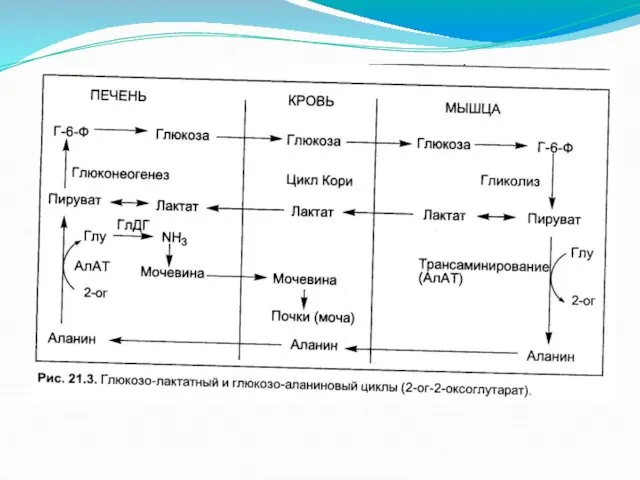
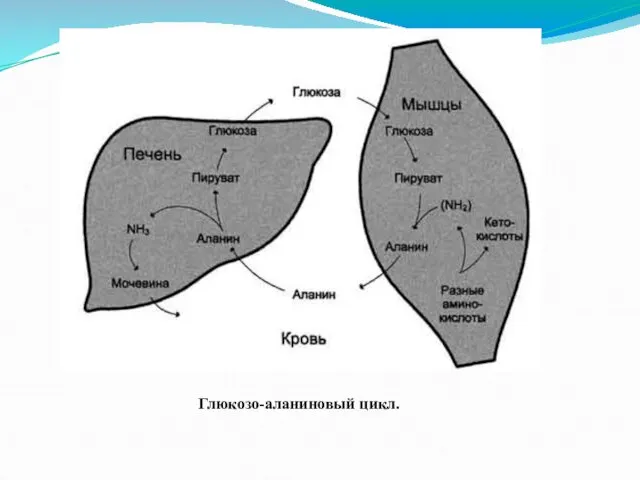
в глутамат. Глутамат в реакциях трансаминирования с пируватом образует аланин (особенно в мышцах).
Слайд 13
Слайд 14
Слайд 15
Слайд 16
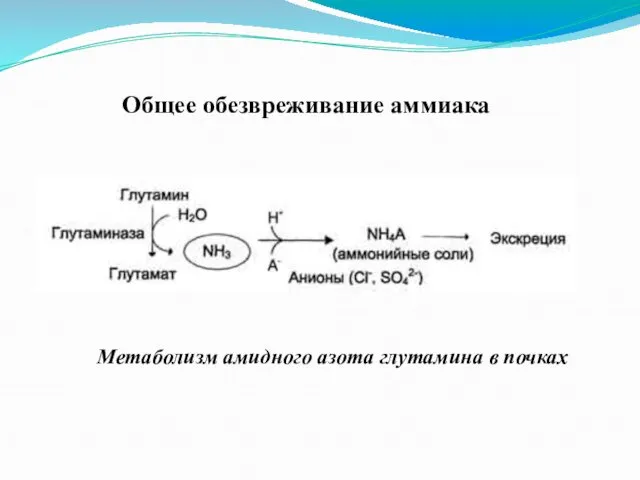
Метаболизм амидного азота глутамина в почках
Общее обезвреживание аммиака
Слайд 17
Слайд 18
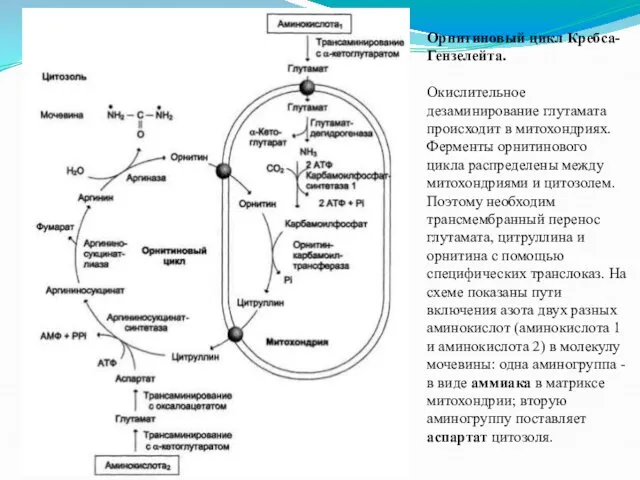
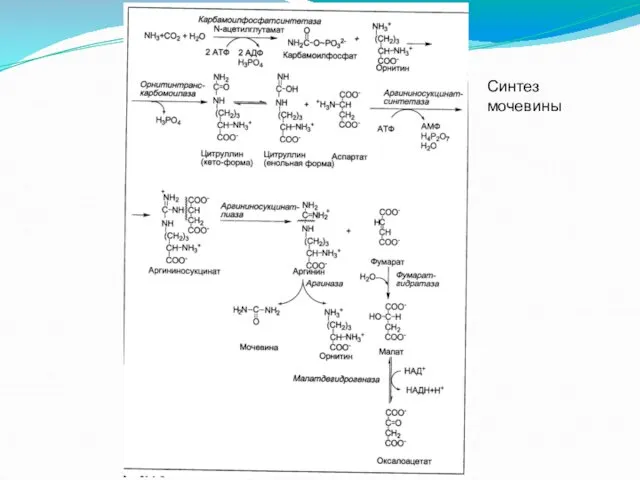
Орнитиновый цикл Кребса-Гензелейта.
Окислительное дезаминирование глутамата происходит в митохондриях. Ферменты орнитинового
цикла распределены между митохондриями и цитозолем. Поэтому необходим трансмембранный перенос глутамата, цитруллина и орнитина с помощью специфических транслоказ. На схеме показаны пути включения азота двух разных аминокислот (аминокислота 1 и аминокислота 2) в молекулу мочевины: одна аминогруппа - в виде аммиака в матриксе митохондрии; вторую аминогруппу поставляет аспартат цитозоля.
Слайд 19
Слайд 20
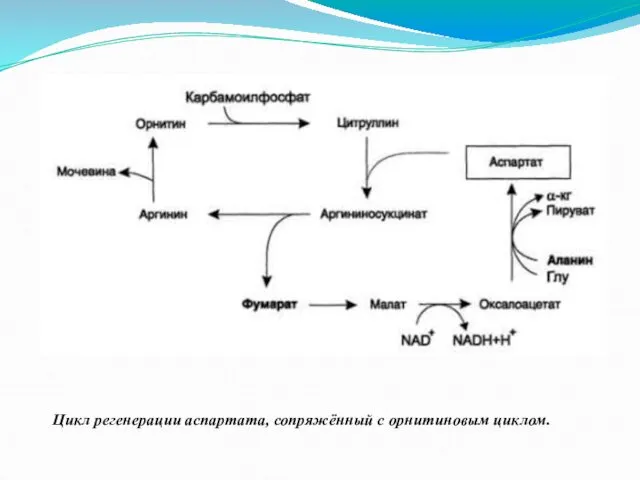
Цикл регенерации аспартата, сопряжённый с орнитиновым циклом.
Слайд 21

Орнитиновый цикл в печени выполняет 2 функции:
превращение азота аминокислот в
мочевину, которая экскретируется и предотвращает накопление токсичных продуктов, главным образом аммиака;
синтез аргинина и пополнение его фонда в организме.
Регуляторные стадии процесса - синтез карбамоилфосфата, синтез цитруллина и заключительная стадия, катализируемая аргиназой.
Эффективность работы орнитинового цикла при нормальном питании человека и умеренных физических нагрузках составляет примерно 60% его мощности. Запас мощности необходим для избежания гипераммониемии при изменениях количества белка в пище. Увеличение скорости синтеза мочевины происходит при длительной физической работе или длительном голодании, которое сопровождается распадом тканевых белков. Некоторые патологические состояния, характеризующиеся интенсивным распадом белков
Слайд 22
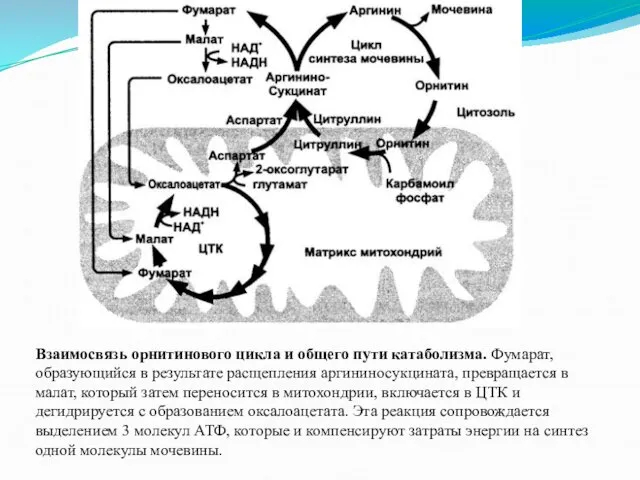
Взаимосвязь орнитинового цикла и общего пути катаболизма. Фумарат, образующийся в результате
расщепления аргининосукцината, превращается в малат, который затем переносится в митохондрии, включается в ЦТК и дегидрируется с образованием оксалоацетата. Эта реакция сопровождается выделением 3 молекул АТФ, которые и компенсируют затраты энергии на синтез одной молекулы мочевины.
Слайд 23
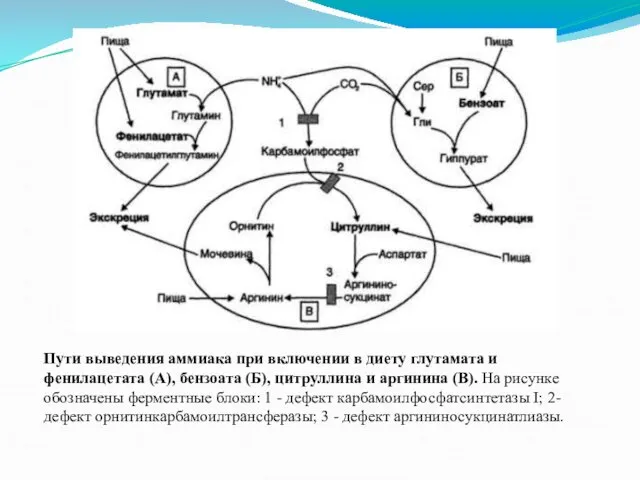
Пути выведения аммиака при включении в диету глутамата и фенилацетата (А),
бензоата (Б), цитруллина и аргинина (В). На рисунке обозначены ферментные блоки: 1 - дефект карбамоилфосфатсинтетазы I; 2-дефект орнитинкарбамоилтрансферазы; 3 - дефект аргининосукцинатлиазы.
Слайд 24
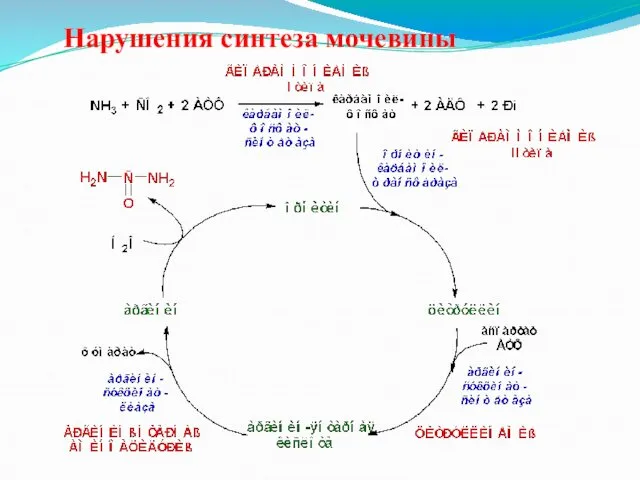
Нарушения синтеза мочевины
Слайд 25
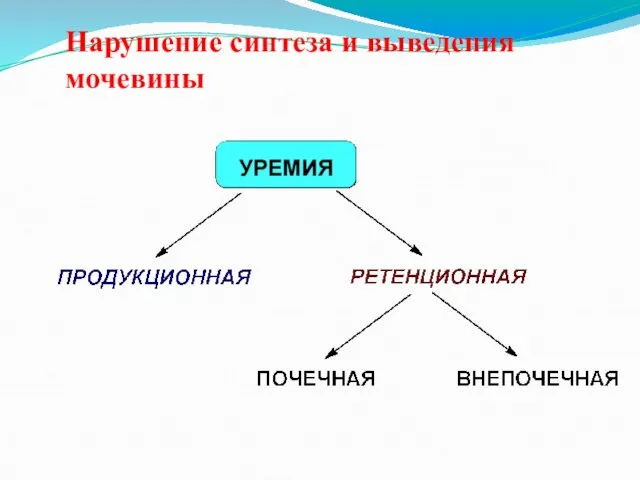
Нарушение синтеза и выведения мочевины
Слайд 26

Количество азотсодержащих веществ в моче (%) при нормальном белковом питании
Слайд 27

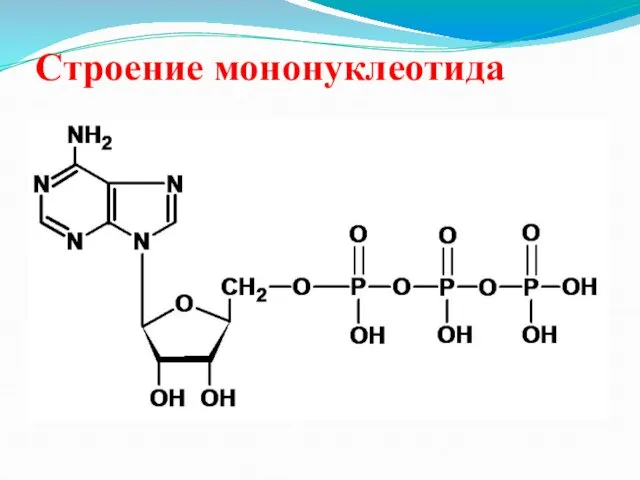
Синтез и распад пуриновых и пиримидиновых оснований
Слайд 28
Слайд 29
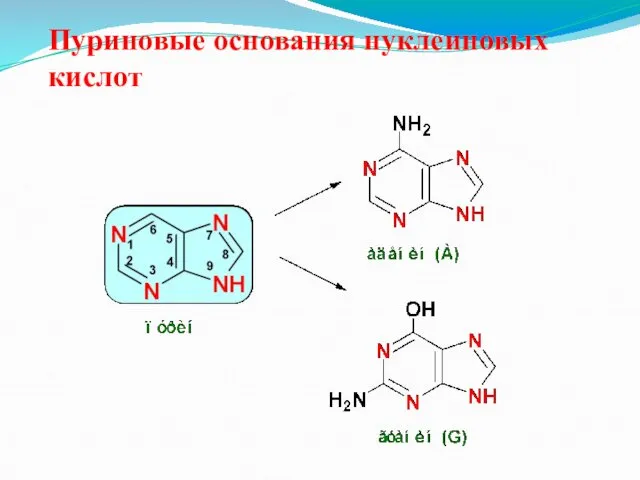
Пуриновые основания нуклеиновых кислот
Слайд 30
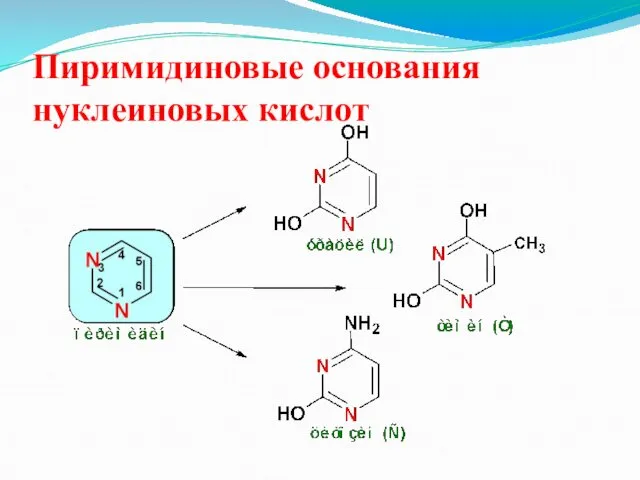
Пиримидиновые основания нуклеиновых кислот
Слайд 31
Слайд 32
Слайд 33
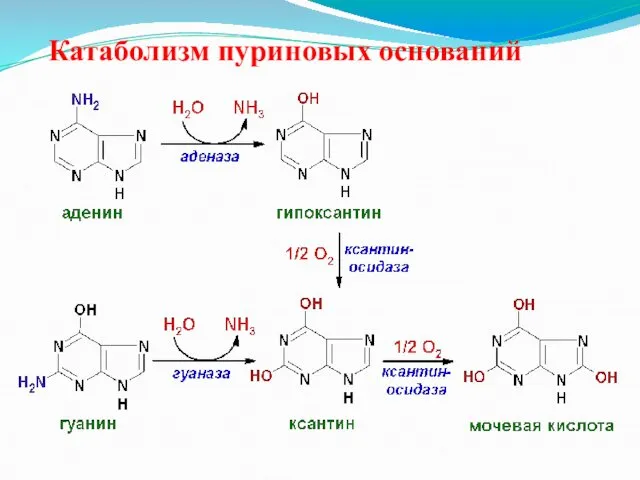
Катаболизм пуриновых оснований
Слайд 34
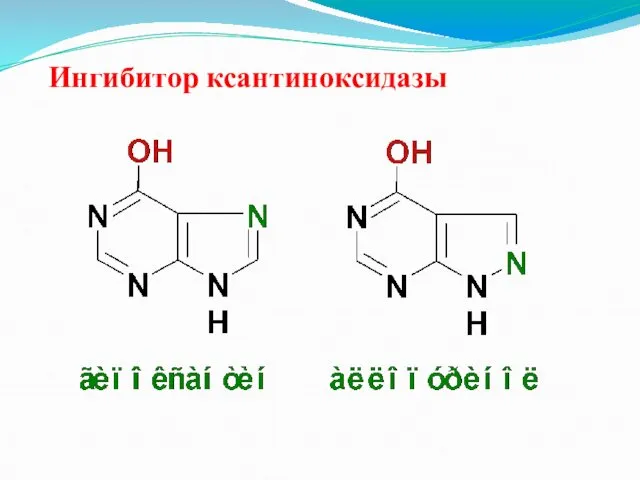
Ингибитор ксантиноксидазы
Слайд 35
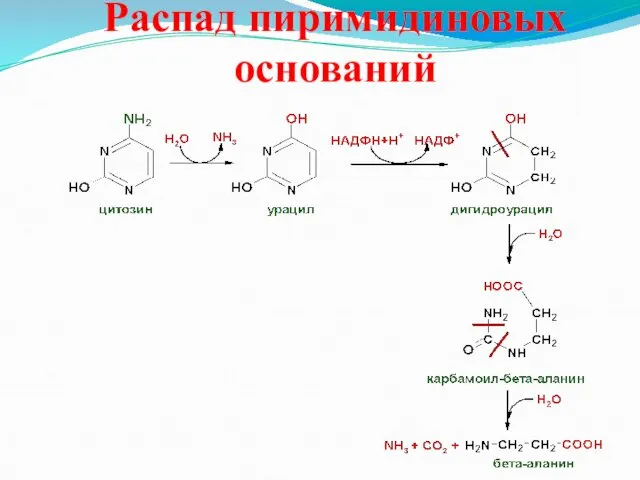
Распад пиримидиновых оснований
Слайд 36
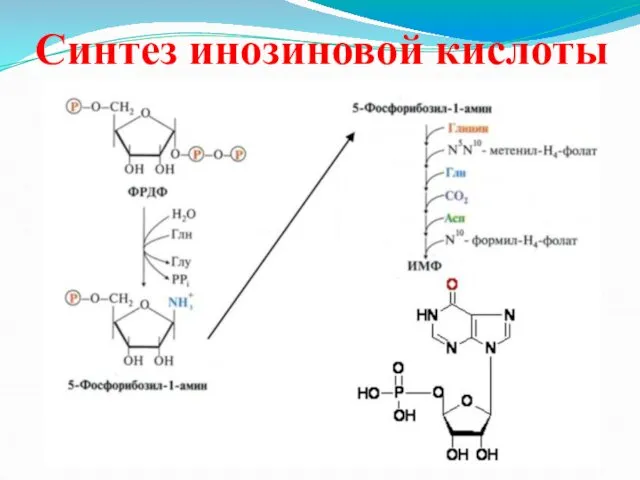
Синтез инозиновой кислоты
Слайд 37
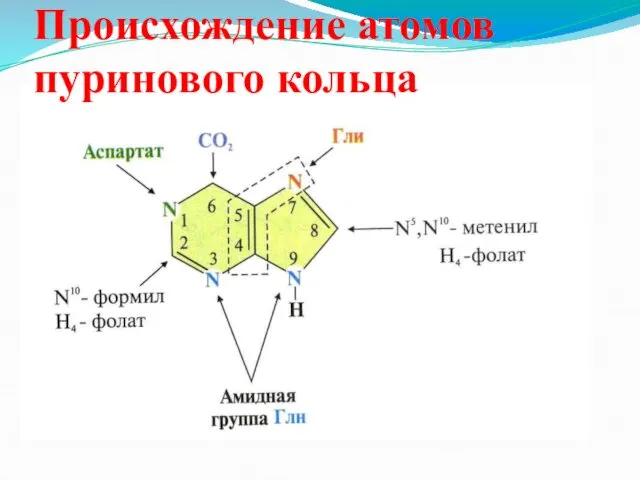
Происхождение атомов пуринового кольца
Слайд 38
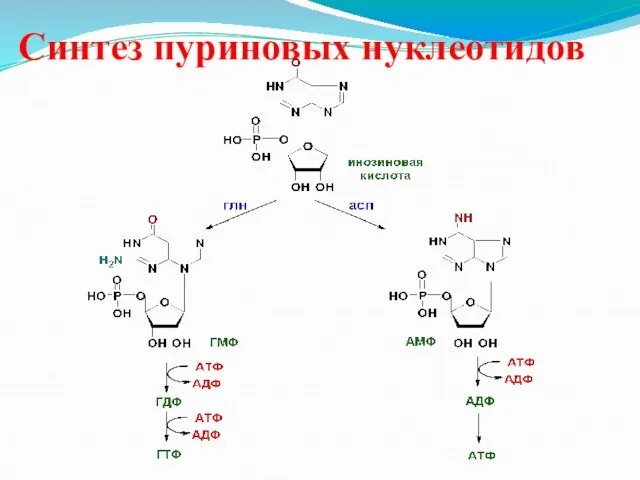
Синтез пуриновых нуклеотидов
Слайд 39
Слайд 40
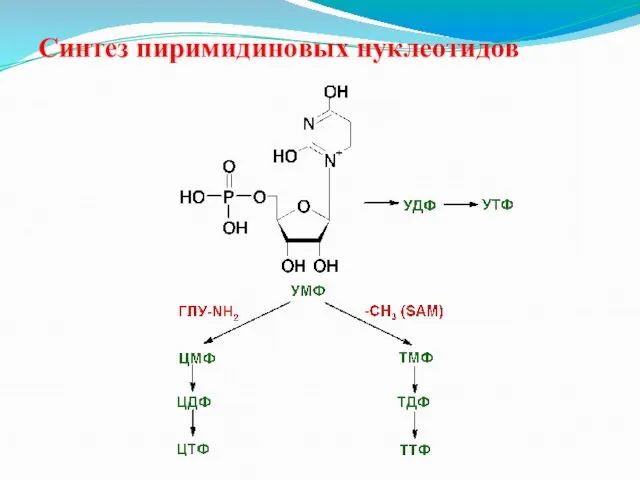
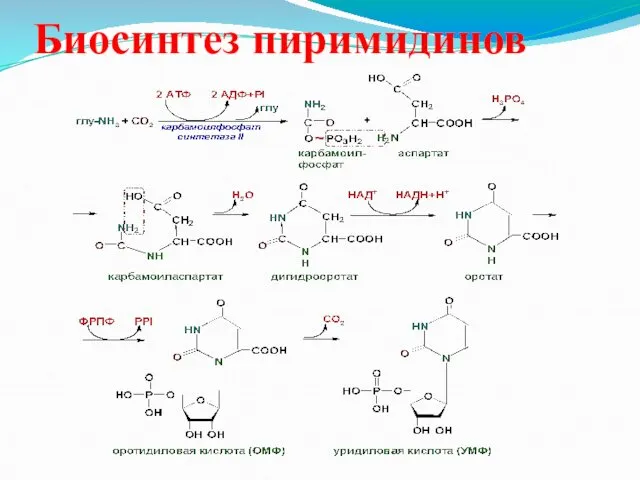
Синтез пиримидиновых нуклеотидов
Слайд 41
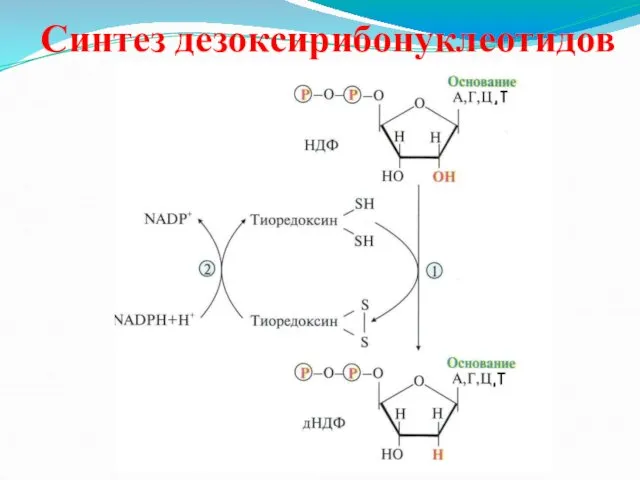
Синтез дезоксирибонуклеотидов
Слайд 42
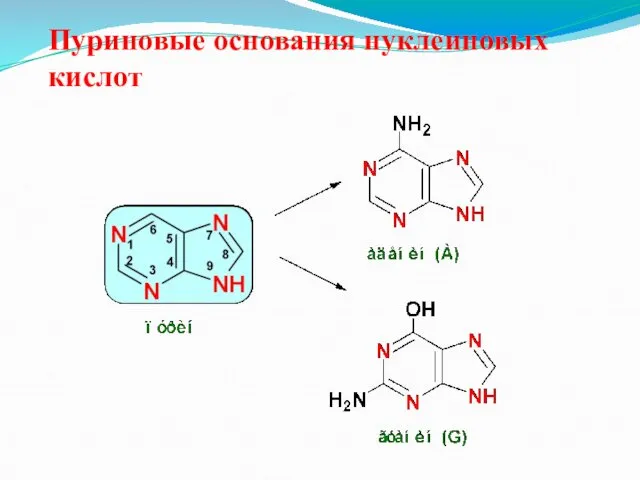
Пуриновые основания нуклеиновых кислот
Слайд 43
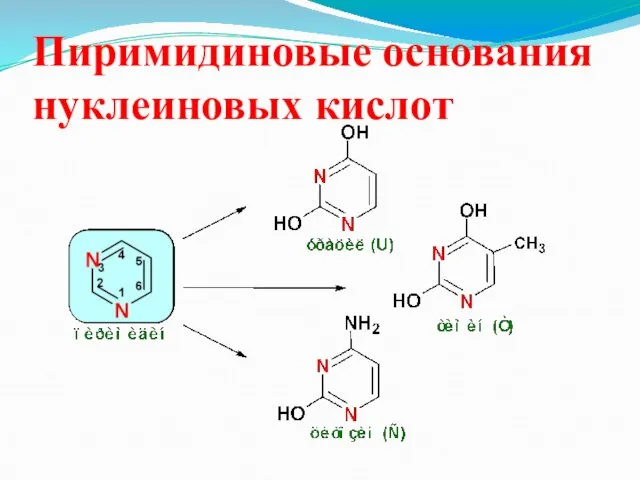
Пиримидиновые основания нуклеиновых кислот
Слайд 44
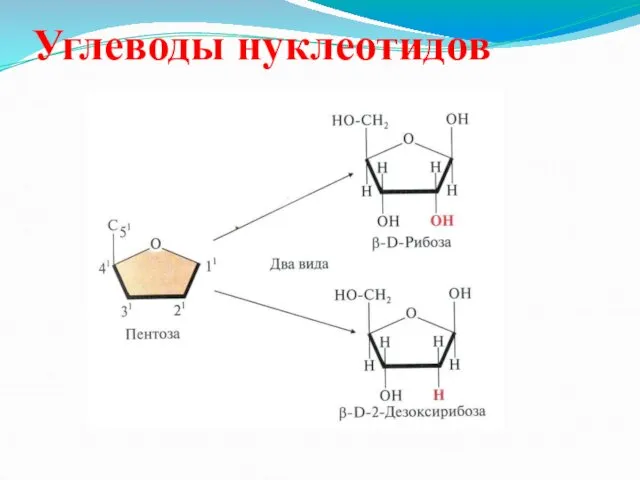
Слайд 45
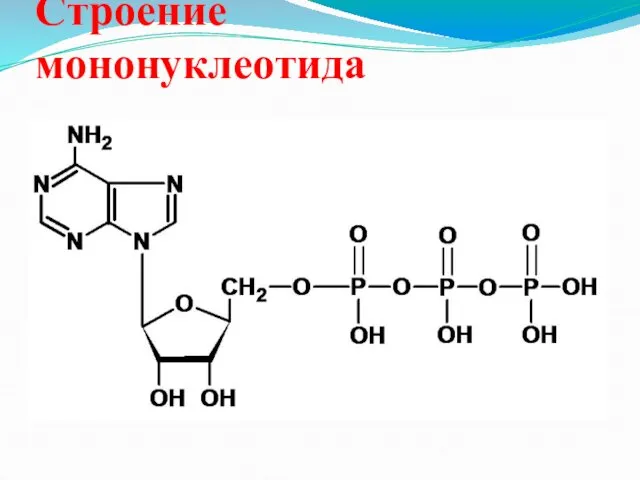












































 Проект Выращивание микрозелени
Проект Выращивание микрозелени Приспособленность организмов к среде обитания
Приспособленность организмов к среде обитания Зоопсихология. Методы зоопсихологических исследований
Зоопсихология. Методы зоопсихологических исследований Животные и растения России. Белка и пион
Животные и растения России. Белка и пион Corynebacterium Erysipelothrix & Listeria
Corynebacterium Erysipelothrix & Listeria Углеводы. Функции углеводов
Углеводы. Функции углеводов Грибы-паразиты
Грибы-паразиты Роль пчелы
Роль пчелы Стихи, загадки, песни про птиц
Стихи, загадки, песни про птиц Сүйектің байланысу түрлері
Сүйектің байланысу түрлері ГМО в нашей жизни
ГМО в нашей жизни Мышечная и нервная ткани. Лекция № 4
Мышечная и нервная ткани. Лекция № 4 Родительское поведение животных
Родительское поведение животных Плодовые овощи
Плодовые овощи Семейство куньих. Горностай
Семейство куньих. Горностай Половая система человека
Половая система человека Подцарство Простейшие
Подцарство Простейшие Значение и биология пчёл
Значение и биология пчёл Микроорганизімдер систематикасы
Микроорганизімдер систематикасы Биологический словарь
Биологический словарь Генетика микроорганизмов
Генетика микроорганизмов о вреде мобильных телефонов
о вреде мобильных телефонов Череп. Общий обзор
Череп. Общий обзор Организм как целостная система
Организм как целостная система Пингвины
Пингвины Опасная флора и фауна
Опасная флора и фауна Стрекозы. Виды стрекоз
Стрекозы. Виды стрекоз Методика фитоценотических или геоботанических исследований
Методика фитоценотических или геоботанических исследований