Содержание
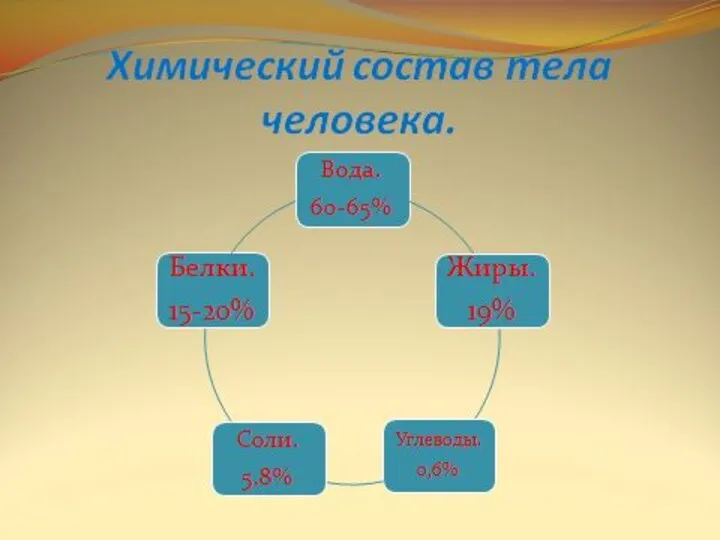
- 4. Химический состав Основные химические элементы, входящие в состав белков С(углерод) – 50% O(кислород) – 17-24% H(водород)
- 5. Строение аминокислот Общая формула: - основная группа - кислотная группа - радикал
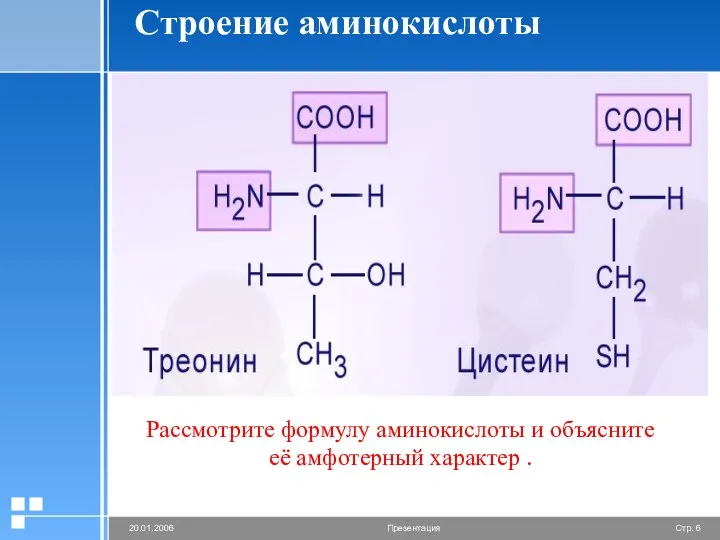
- 6. Строение аминокислоты Рассмотрите формулу аминокислоты и объясните её амфотерный характер .
- 7. Данилевский Александр Яковлевич. Предположение о том, что белки состоят из остатков аминокислот, связанных пептидной связью, было
- 8. Пептидная связь Соединение молекул аминокислот: Рассмотрите схему образования дипептида. Какие атомы образовали молекулу воды в результате
- 9. Реакции получения полимеров, которые сопровождаются образованием побочного низкомолекулярного продукта, например воды, называются реакциями поликонденсации. Давайте докажем
- 10. Биуретовая реакция. Приливаем в пробирку 2 мл. раствора белка. Добавляем 2 мл. раствора гидроксида натрия, затем-
- 11. Полимер, состоящий из аминокислот
- 12. БЕЛКИ. ПРОТЕИНЫ. ПРОТЕИДЫ. Белки – это макромолекулы, биополимеры, полипептиды. Белки – это самые сложные молекулы. Протеины
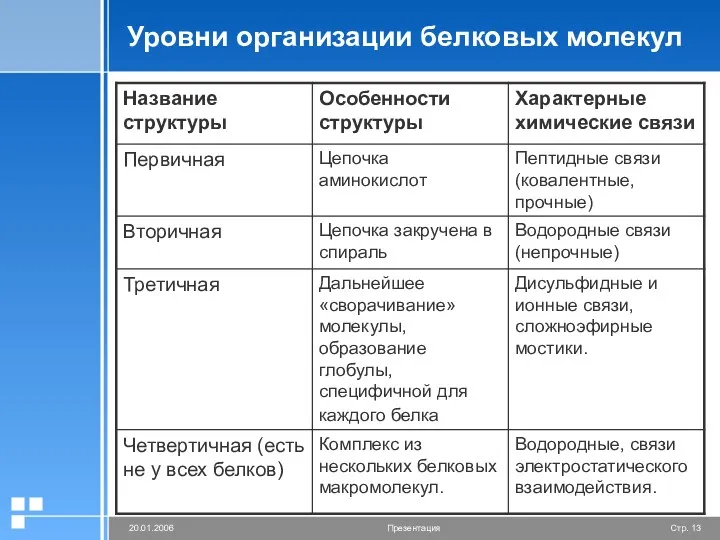
- 13. Уровни организации белковых молекул
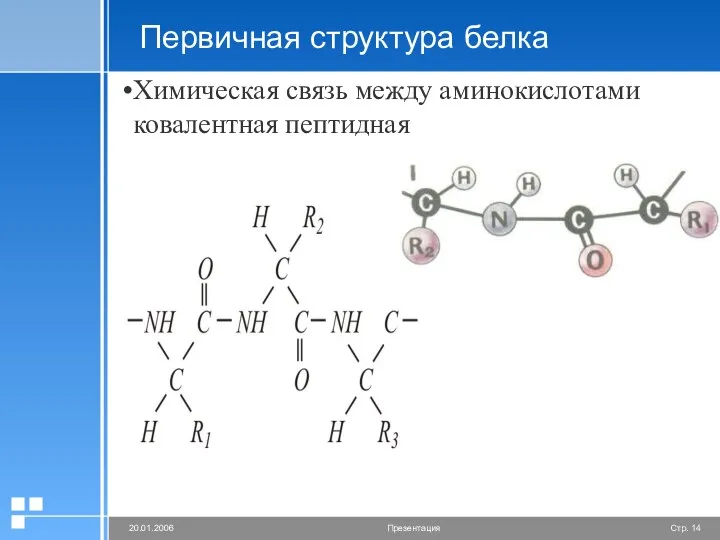
- 14. Первичная структура белка Химическая связь между аминокислотами ковалентная пептидная
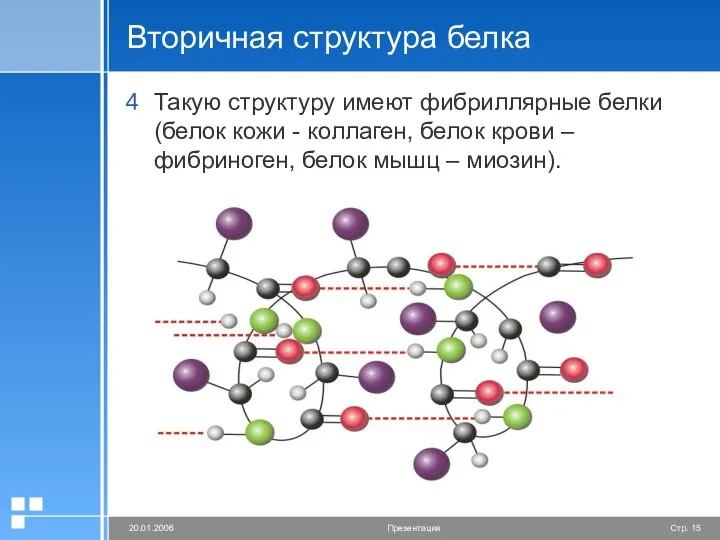
- 15. Вторичная структура белка Такую структуру имеют фибриллярные белки (белок кожи - коллаген, белок крови – фибриноген,
- 16. Типы вторичной структуры белка. Существует 3 типа вторичной структуры. Альфа- спираль – это пептидная цепь штопорообразно
- 17. Третичная структура белка Это многократно скрученная спираль, глобула. Такую структуру имеют глобулярные белки (альбумины, глобулины).
- 18. Четвертичная структура белка Четыре глобулы связанные атомом железа имеет белок гемоглобин.
- 19. Денатурация – это изменение вторичной, третичной и четвертичной структуры белковой макромолекулы под влиянием внешних факторов (температуры,
- 20. КИСЛОТНЫЙ ГИДРОЛИЗ ПРОТЕКАЕТ ПРИ ДЕЙСТВИИ 25% РАСТВОРОВ СЕРНОЙ ИЛИ СОЛЯНОЙ КИСЛОТЫ В ТЕЧЕНИИ 12-48 ЧАСОВ. ПРИ
- 22. ГОРЕНИЕ. БЕЛКИ ПРИ СЖИГАНИИ ОБРАЗУЮТ АЗОТ, УГЛЕКИСЛЫЙ ГАЗ, ВОДУ И НЕКОТОРЫЕ ДРУГИЕ ВЕЩЕСТВА. ГОРЕНИЕ СОПРОВОЖДАЕТСЯ ХАРАКТЕРНЫМ
- 23. КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ. ЭТО ЦВЕТНАЯ РЕАКЦИЯ НА БЕЛКИ,СОДЕРЖАЩИЕ АРОМАТИЧЕСКИЕ АМИНОКИСЛОТЫ. ЧАСТЬ ИХ ЯВЛЯЕТСЯ НЕЗАМЕНИМЫМИ ДЛЯ ЧЕЛОВЕКА. ОПРЕДЕЛИМ
- 24. Свойства белков. Денатурация. Ренатурация. Гидролиз. Горение. Цветные реакции.
- 25. Классификация белков. По растворимости: Водорастворимые Солерастворимые Спирторастворимые Нерастворимые По конформационной структуре: Фибриллярные Глобулярные По химическому строению:
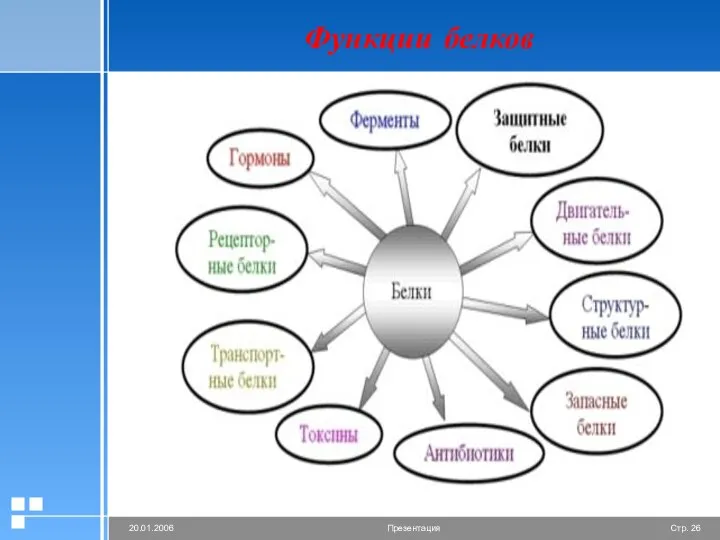
- 26. Функции белков
- 27. Функции белков в клетке
- 29. Скачать презентацию




















 Витамины. Естественные и искусственные витамины
Витамины. Естественные и искусственные витамины Цитология. Клеточная теория. Строение клетки
Цитология. Клеточная теория. Строение клетки Курс подготовки к ЕГЭ по биологии
Курс подготовки к ЕГЭ по биологии Теории возникновения жизни на Земле
Теории возникновения жизни на Земле Деление клетки. Митоз
Деление клетки. Митоз Пора года - лето
Пора года - лето Тестирование по теме Цветок. Соцветие
Тестирование по теме Цветок. Соцветие Тип Плоские черви
Тип Плоские черви Насекомые. Отряд перепончатокрылые
Насекомые. Отряд перепончатокрылые Время посева и глубина заделки семян
Время посева и глубина заделки семян Ядовитые растения
Ядовитые растения Бассүйек кұрылысы, оның милық және беттік бөліктері
Бассүйек кұрылысы, оның милық және беттік бөліктері Митоз. Деление клеток организма
Митоз. Деление клеток организма Плоды. Классификация.
Плоды. Классификация.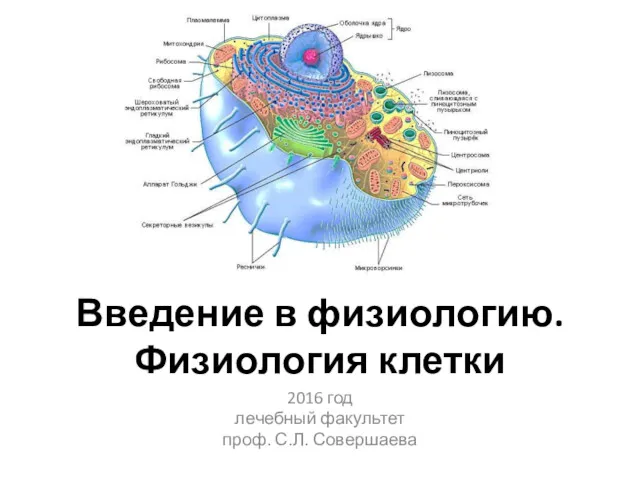 Введение в физиологию. Физиология клетки
Введение в физиологию. Физиология клетки Генетика. Решение задач
Генетика. Решение задач Сборник заданий № 25 с ответами. ЕГЭ по биологии
Сборник заданий № 25 с ответами. ЕГЭ по биологии Гидротермические условия для выращивания растений
Гидротермические условия для выращивания растений Основные популяционные показатели
Основные популяционные показатели Снежный барс (Ирбис)
Снежный барс (Ирбис) Дневные хищные, совы, куриные
Дневные хищные, совы, куриные Как появился человек на Земле
Как появился человек на Земле Лекарственные растения Мангистауской области
Лекарственные растения Мангистауской области Надкласс II. Рыбы
Надкласс II. Рыбы Cell Structure end Function
Cell Structure end Function Деревья
Деревья Medical Academy Named after S. I. Georgievsky of Crimea
Medical Academy Named after S. I. Georgievsky of Crimea Увеличительные приборы. 6 класс. Урок № 3
Увеличительные приборы. 6 класс. Урок № 3