Содержание
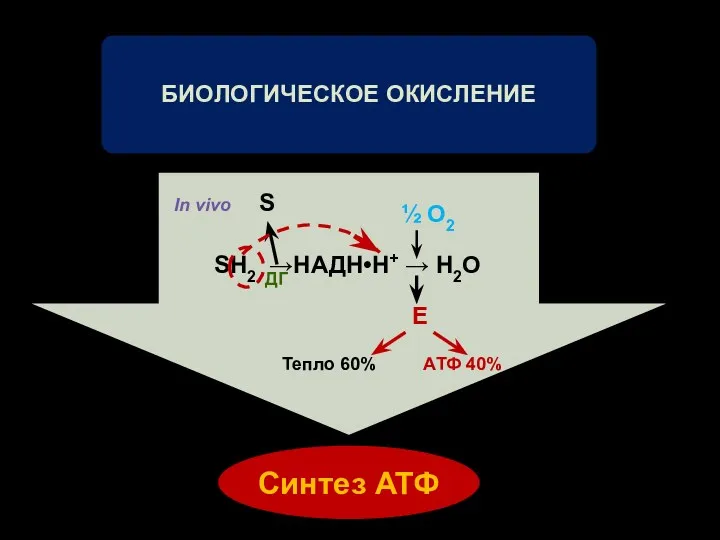
- 2. SН2 →НАДН•Н+ → Н2О S ½ О2 Е Тепло 60% АТФ 40% ДГ In vivo
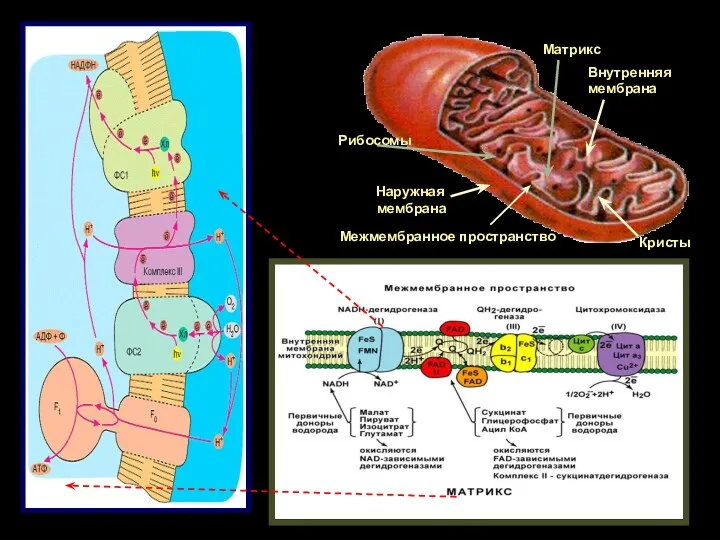
- 3. Наружная мембрана Внутренняя мембрана Кристы Межмембранное пространство Рибосомы Матрикс
- 4. Современная теория биологического окисления Путем отнятия водорода от окисляемого субстрата – митохондриальное окисление и внемитохондриальное окисление
- 5. Типы окисляемых субстратов Субстраты 1 типа (углеводородные) – сукцинат, ацетил-КоА. ∆G = 150 кДж/моль. Это меньше,
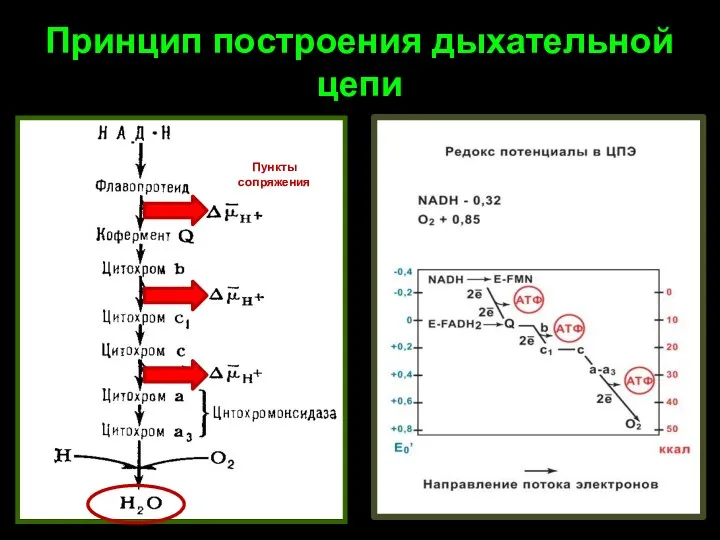
- 6. Принцип построения дыхательной цепи Пункты сопряжения
- 7. Полная дыхательная цепь Комплекс I – НАДН-КоQ (убихинон) – оксидоредуктаза, обеспечивает передачу е- от НАДН+Н+ к
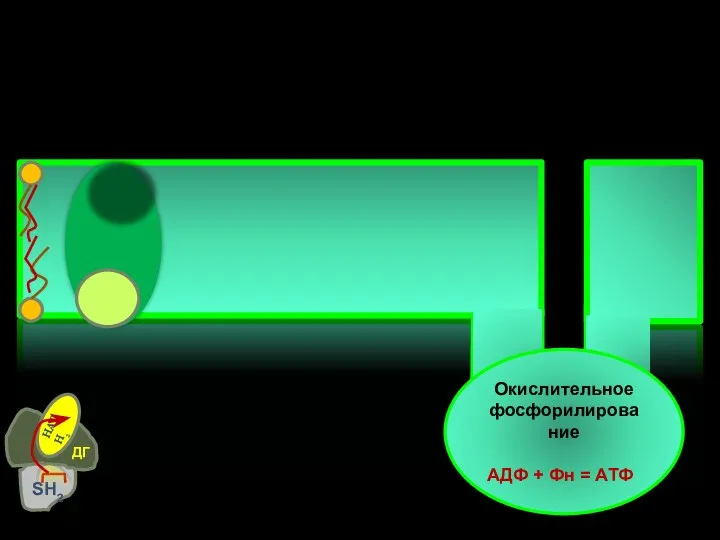
- 8. Окислительное фосфорилирование АДФ + Фн = АТФ SH2 НАДН2 ДГ ФМНН2 -е FeS 2е- 1е- Q10
- 9. Последовательность переносчиков определяется их способностью отдавать электроны окислителю, т.е. стандартным восстановительным потенциалом Е0 (редокс-потенциалом). Редокс-потенциал численно
- 10. Дыхательная цепь
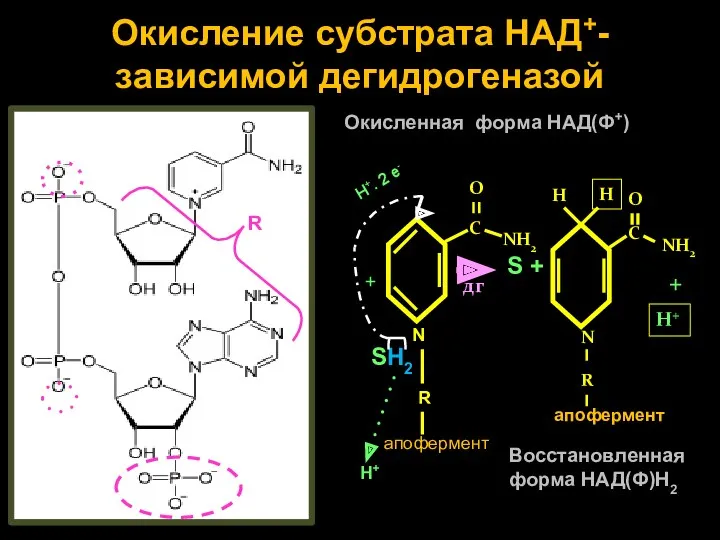
- 11. Окисление субстрата НАД+- зависимой дегидрогеназой Окисленная форма НАД(Ф+) SH2 R N R апофермент С О NH2
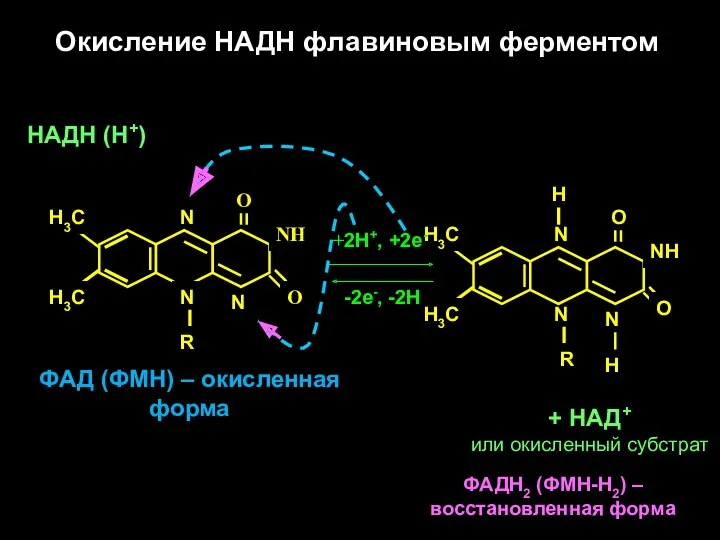
- 12. Н3С Н3С N R N N O NH O Н3С Н3С N R N N O
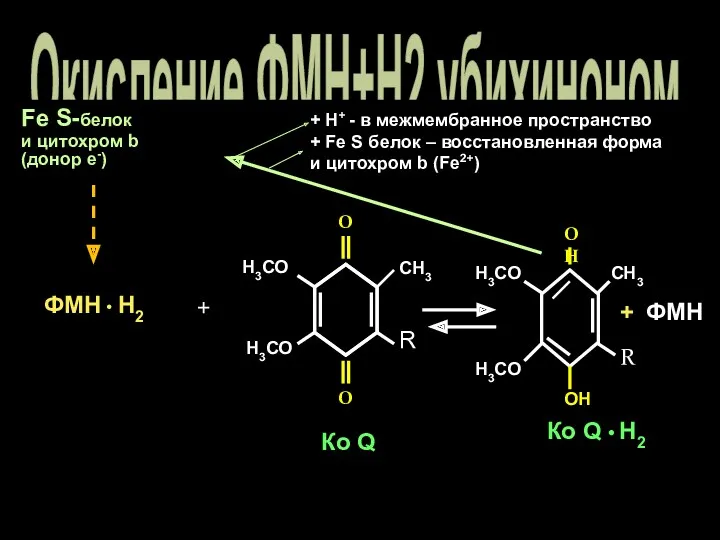
- 13. Окисление ФМН+Н2 убихиноном Fe S-белок и цитохром b (донор е-) О О СН3 R Н3СО Н3СО
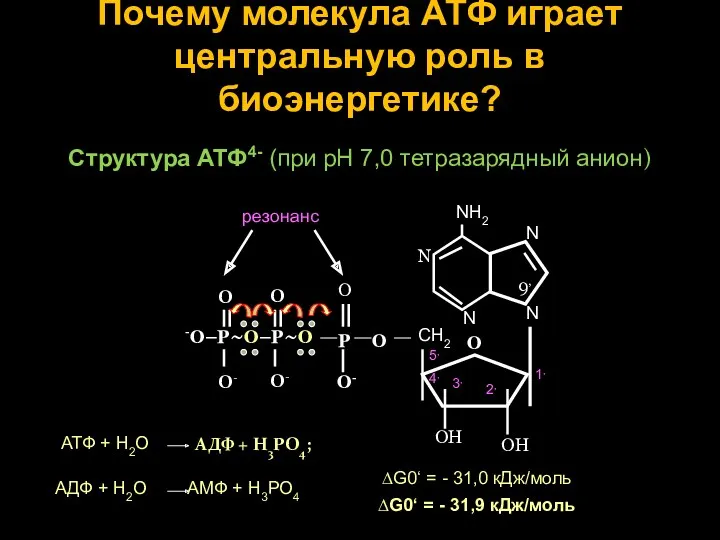
- 14. Почему молекула АТФ играет центральную роль в биоэнергетике? Структура АТФ4- (при рН 7,0 тетразарядный анион) N
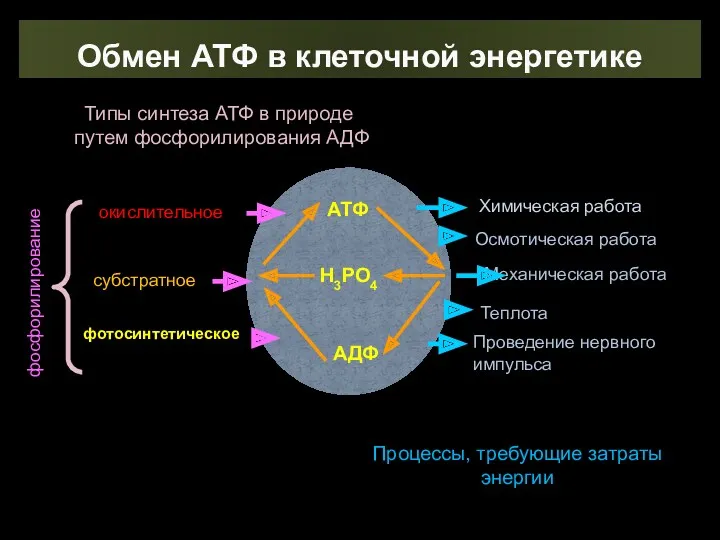
- 15. Обмен АТФ в клеточной энергетике АТФ Н3РО4 АДФ фосфорилирование окислительное субстратное фотосинтетическое Химическая работа Осмотическая работа
- 16. Окислительное фосфорилирование – это синтез АТФ из АДФ и неорганического фосфата, сопряженный с переносом протонов и
- 17. Окислительное фосфорилирование Это сопряжение двух клеточных процессов: Экзергонической реакции окисления восстановительных молекул (НАДН•Н+ или ФАДН2) Эндергонической
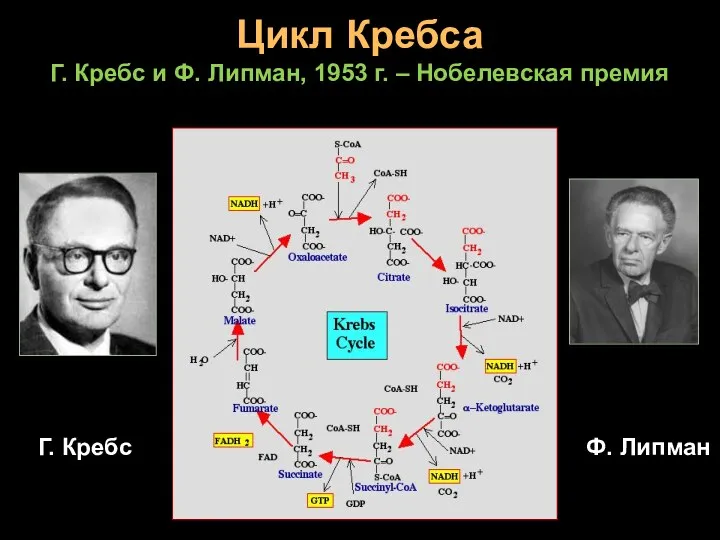
- 18. Цикл Кребса Г. Кребс и Ф. Липман, 1953 г. – Нобелевская премия Г. Кребс Ф. Липман
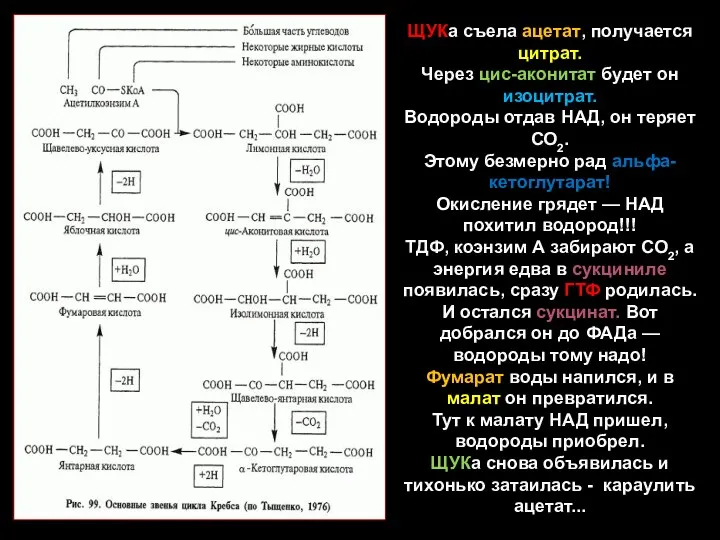
- 19. ЩУКа съела ацетат, получается цитрат. Через цис-аконитат будет он изоцитрат. Водороды отдав НАД, он теряет СО2.
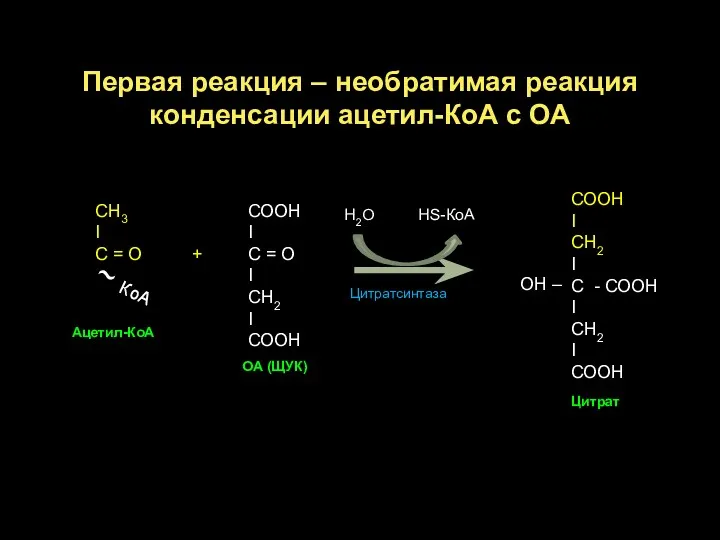
- 20. Первая реакция – необратимая реакция конденсации ацетил-КоА с ОА СН3 I С = О + ~
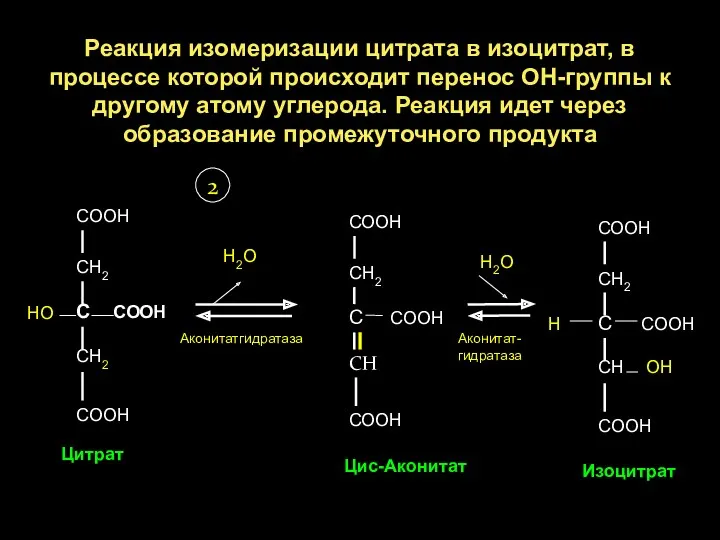
- 21. Реакция изомеризации цитрата в изоцитрат, в процессе которой происходит перенос ОН-группы к другому атому углерода. Реакция
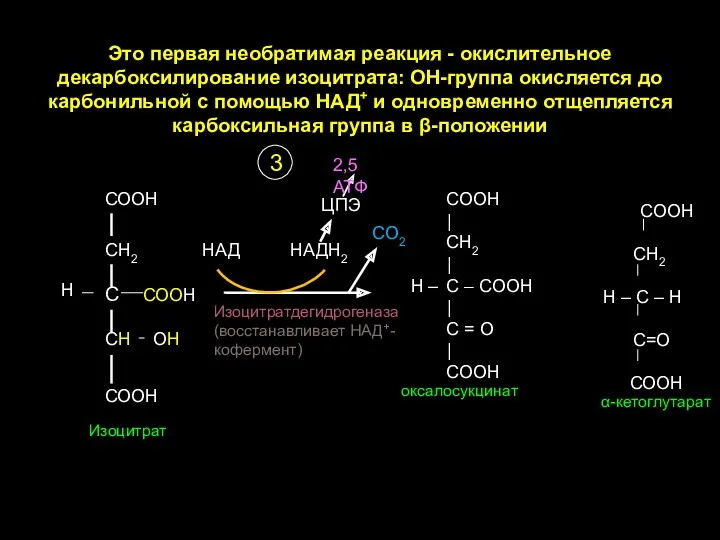
- 22. Это первая необратимая реакция - окислительное декарбоксилирование изоцитрата: ОН-группа окисляется до карбонильной с помощью НАД+ и
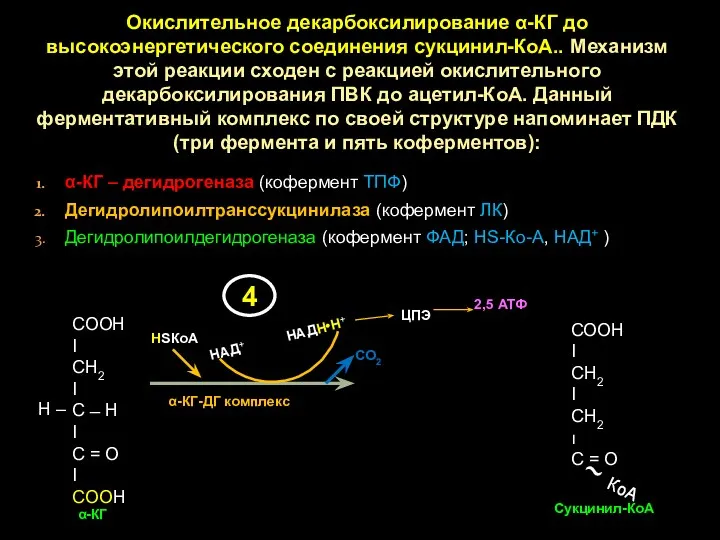
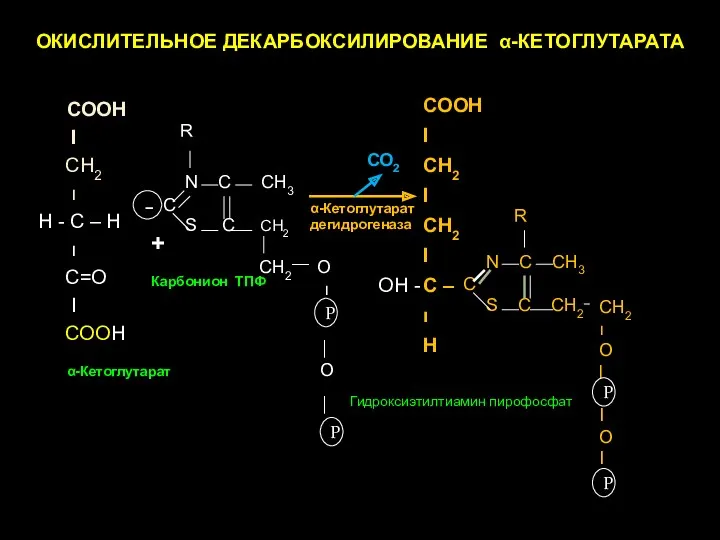
- 23. Окислительное декарбоксилирование α-КГ до высокоэнергетического соединения сукцинил-КоА.. Механизм этой реакции сходен с реакцией окислительного декарбоксилирования ПВК
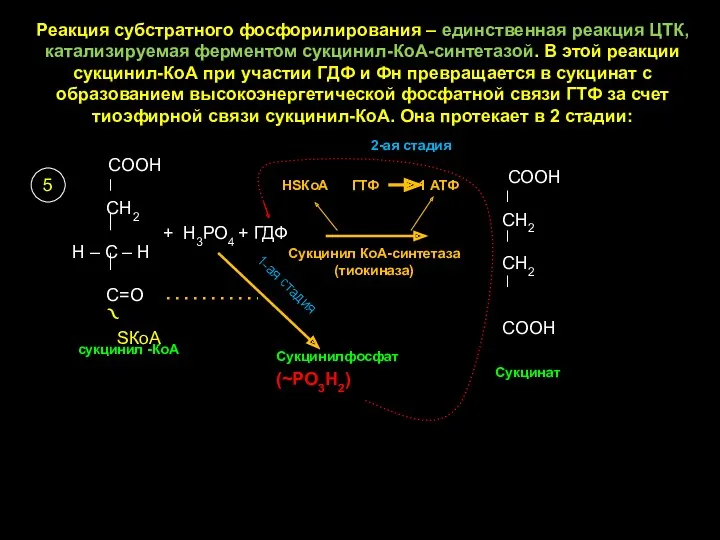
- 24. Реакция субстратного фосфорилирования – единственная реакция ЦТК, катализируемая ферментом сукцинил-КоА-синтетазой. В этой реакции сукцинил-КоА при участии
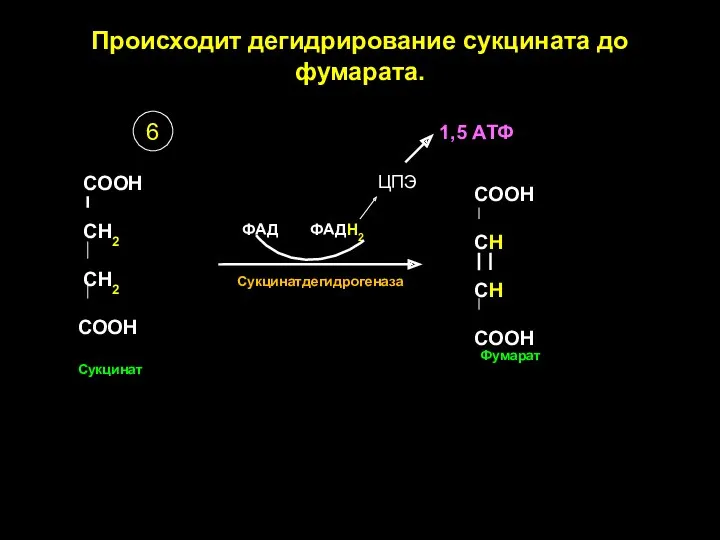
- 25. Происходит дегидрирование сукцината до фумарата. СООН СН2 СН2 СООН Сукцинат СООН СН СН СООН Сукцинатдегидрогеназа ФАД
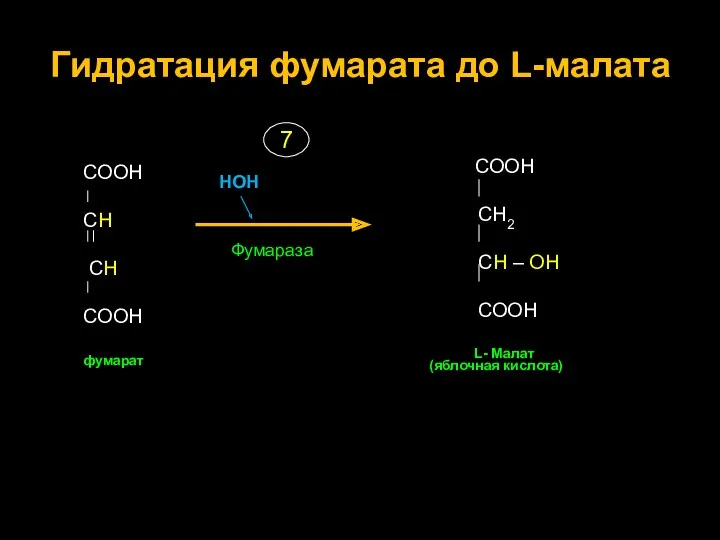
- 26. Гидратация фумарата до L-малата СООН СН СН СООН фумарат Фумараза НОН СООН СН2 СН – ОН
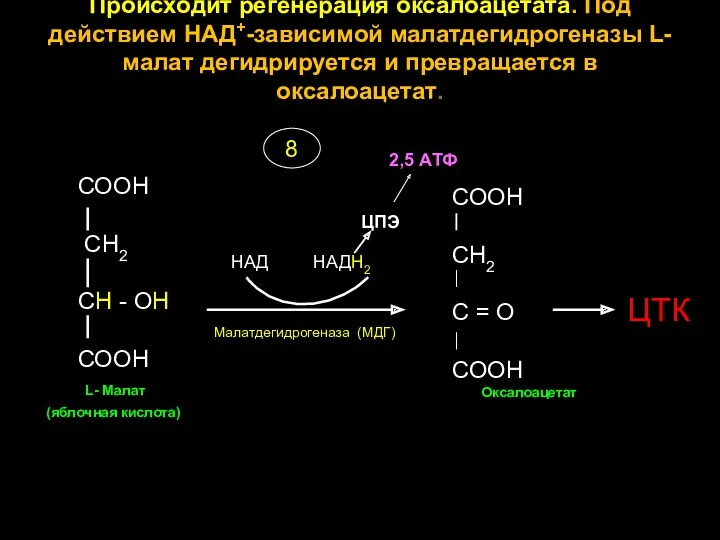
- 27. Происходит регенерация оксалоацетата. Под действием НАД+-зависимой малатдегидрогеназы L-малат дегидрируется и превращается в оксалоацетат. СООН СН2 СН
- 28. Стехиометрия ЦЛК: 3 НАДН2 ЦПЭ 2,5 (3) АТФ х3 =8,5 АТФ 1 ФАДН2 ЦПЭ 1,5 (2)
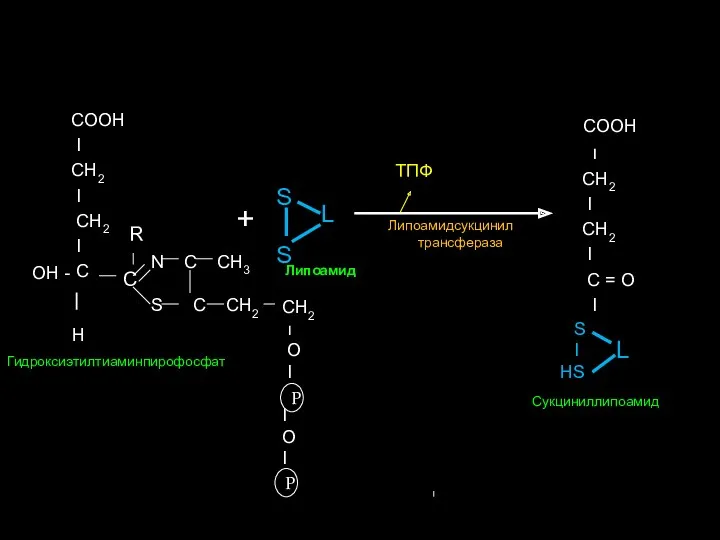
- 29. СООН I СН2 I СН2 I С – ı Н + СН2 О ı Р О
- 30. СООН I СН2 I СН2 I С СН2 ı О I I О I Р Р
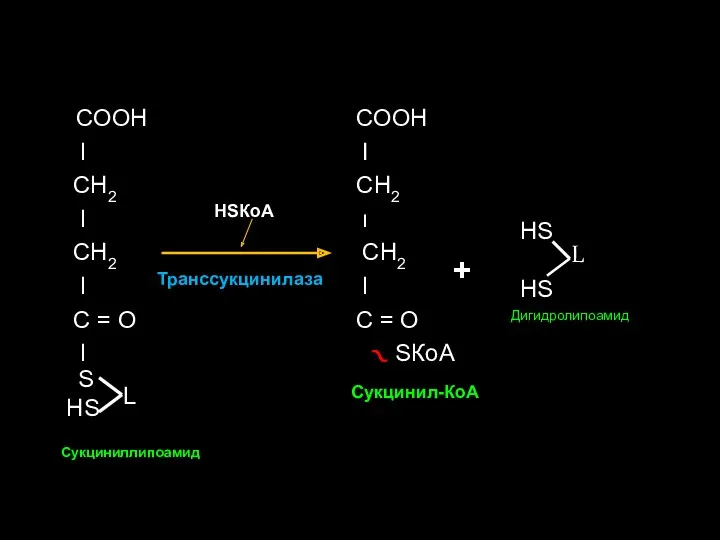
- 31. СООН l СН2 l СН2 l С = О l S НS L Сукциниллипоамид НSКоА СООН
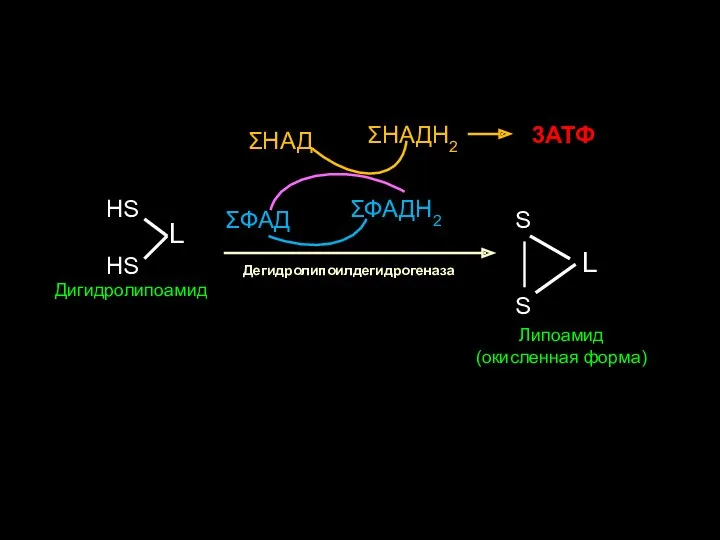
- 32. Дегидролипоилдегидрогеназа Дигидролипоамид L L Липоамид (окисленная форма)
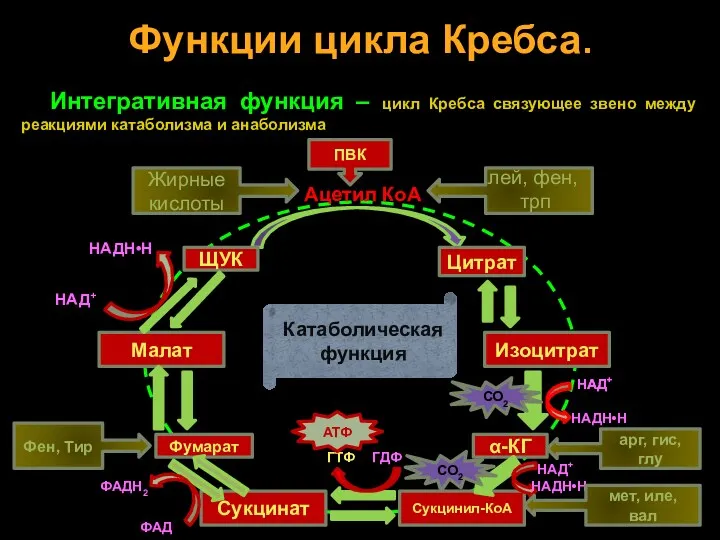
- 33. Интегративная функция – цикл Кребса связующее звено между реакциями катаболизма и анаболизма Функции цикла Кребса. Катаболическая
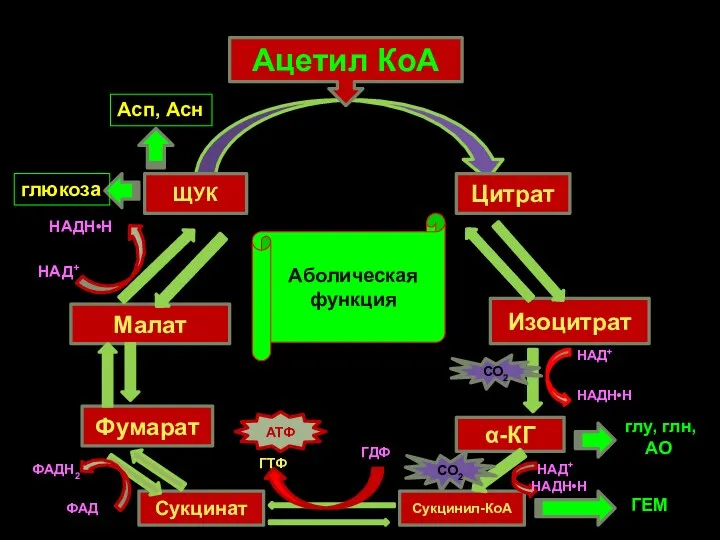
- 34. Аболическая функция Ацетил КоА ЩУК Цитрат Изоцитрат α-КГ НАДН•Н СО2 Сукцинил-КоА НАД+ НАДН•Н СО2 Сукцинат Фумарат
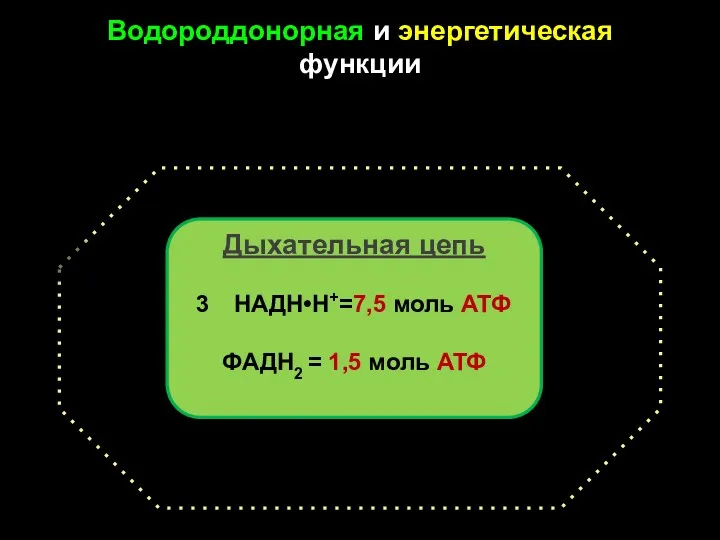
- 35. Водороддонорная и энергетическая функции Дыхательная цепь НАДН•Н+=7,5 моль АТФ ФАДН2 = 1,5 моль АТФ Малат Фумарат
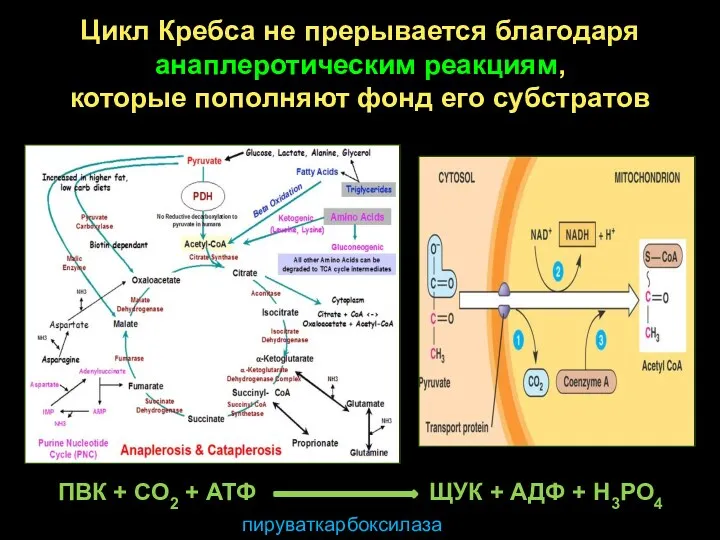
- 36. Цикл Кребса не прерывается благодаря анаплеротическим реакциям, которые пополняют фонд его субстратов ПВК + СО2 +
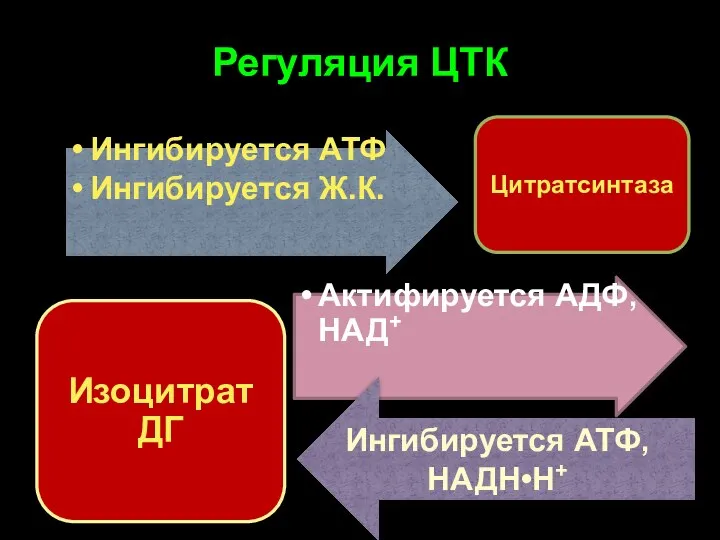
- 37. Регуляция ЦТК Ингибируется АТФ, НАДН•Н+
- 39. Скачать презентацию








 Развитие органического мира
Развитие органического мира Поведінка тварин
Поведінка тварин Методическая разработка урока Главные направления эволюции с применением Case-технологии
Методическая разработка урока Главные направления эволюции с применением Case-технологии Рослини і тварини України, які походять з інших материків і частин Євразії
Рослини і тварини України, які походять з інших материків і частин Євразії Животный и растительный мир Красной книги Республики Коми
Животный и растительный мир Красной книги Республики Коми Урок природоведения 5 класс Свойства воды
Урок природоведения 5 класс Свойства воды Центры происхождения культурных растений и домашних животных
Центры происхождения культурных растений и домашних животных Мир РНК. Роль РНК в современном мире
Мир РНК. Роль РНК в современном мире Развитие систем регуляции организма человека
Развитие систем регуляции организма человека Как звери готовятся к зиме
Как звери готовятся к зиме Центры подкрепления, прилежащее ядро. Кора больших полушарий: механизмы обучения; гиппокамп
Центры подкрепления, прилежащее ядро. Кора больших полушарий: механизмы обучения; гиппокамп Улы жыландар
Улы жыландар Растения
Растения Потребности человека
Потребности человека Методические материалы
Методические материалы Тип Членистоногие Класс Паукообразные
Тип Членистоногие Класс Паукообразные Витамины
Витамины Высшая нервная деятельность человека. 8 класс
Высшая нервная деятельность человека. 8 класс Теория абиогенеза (биохимической эволюции)
Теория абиогенеза (биохимической эволюции) Земноводні України
Земноводні України Algologiya. Suv o’tlar to’g’rida umumiy ma’lumot
Algologiya. Suv o’tlar to’g’rida umumiy ma’lumot Презентация По страницам Красной Книги
Презентация По страницам Красной Книги Мышцы туловища
Мышцы туловища Влияние факторов внешней среды на микроорганизмы
Влияние факторов внешней среды на микроорганизмы Строение кожи
Строение кожи Цветок. Строение и значение цветка
Цветок. Строение и значение цветка Немного о кошках
Немного о кошках Жизнь животных зимой
Жизнь животных зимой