Содержание
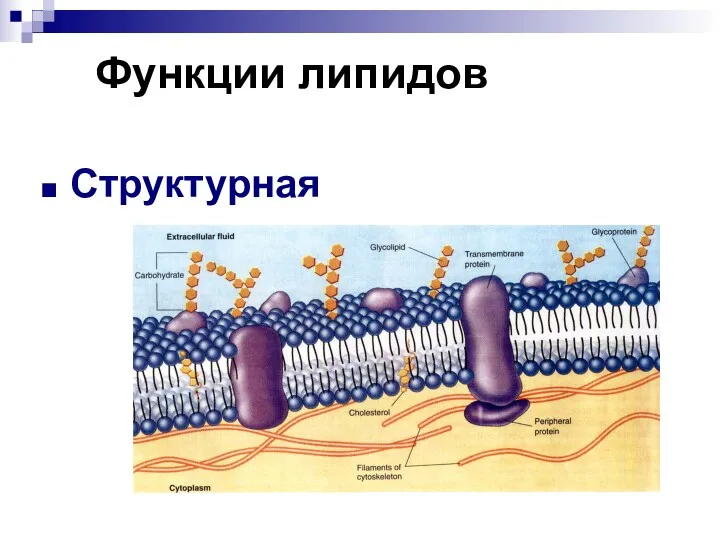
- 2. Функции липидов Структурная
- 3. Функции липидов Защитная (аммортизация) Запасающая Энергетическая 1 г жира 38,9 кДж Е
- 4. Функции липидов Теплоизоляция Источник метаболической воды 1 г жира 1,1 г Н2О Регуляторная Специфические ff витаминов,
- 5. Тест на гениальность… Самые умные, попробуйте ответить на вопросы: Как можно использовать липосомы? Почему у верблюда
- 6. Гиганты в мире молекул понятие о мономерах, структурных звеньях, полимерах…
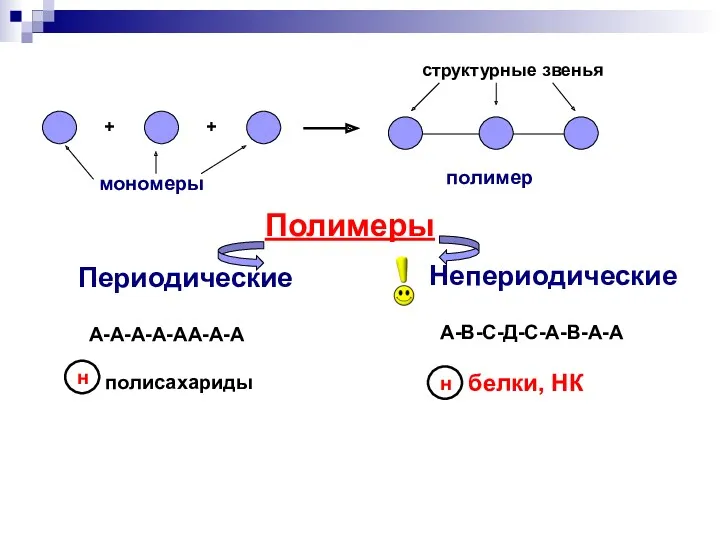
- 7. + + мономеры полимер структурные звенья Полимеры Периодические А-А-А-А-АА-А-А полисахариды н Непериодические А-В-С-Д-С-А-В-А-А белки, НК н
- 8. Белки
- 9. Белки - Непериодические полимеры, мономером которых является аминокислота
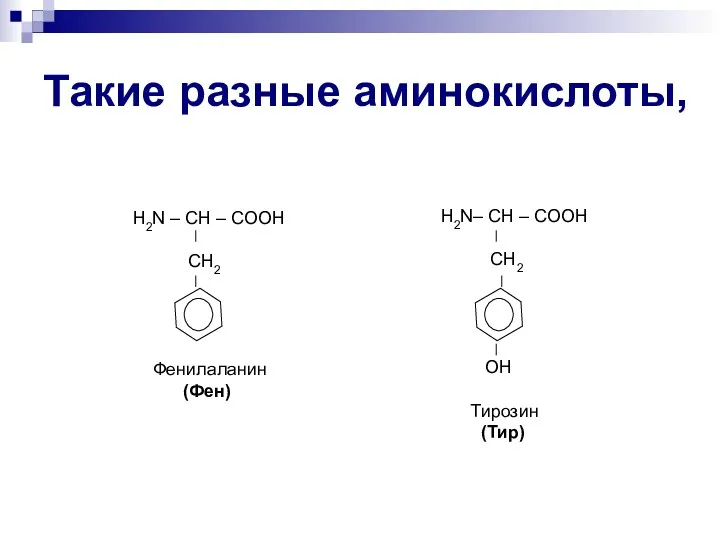
- 10. Такие разные аминокислоты, Н2N – CH – COOH СН2 Фенилаланин (Фен) Н2N– CH – COOH СН2
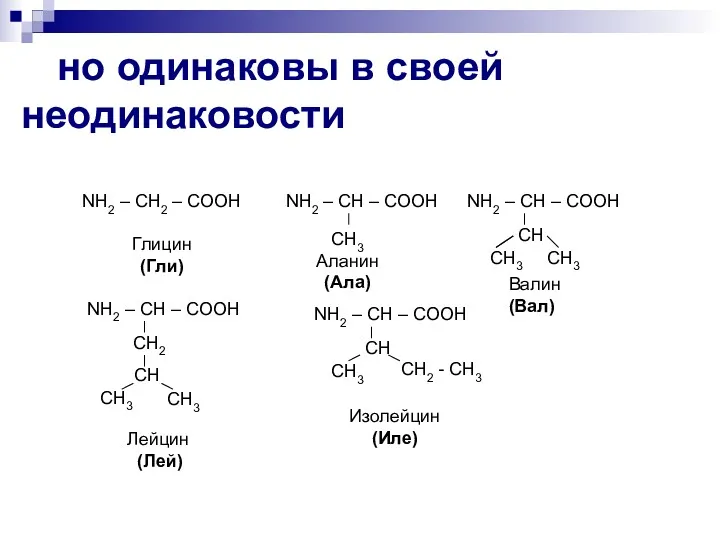
- 11. но одинаковы в своей неодинаковости NH2 – CH2 – COOH Глицин (Гли) NH2 – CH –
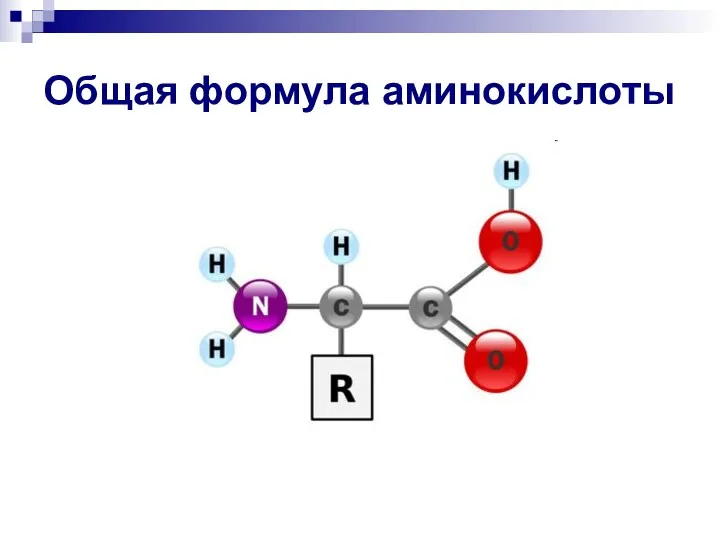
- 12. Общая формула аминокислоты
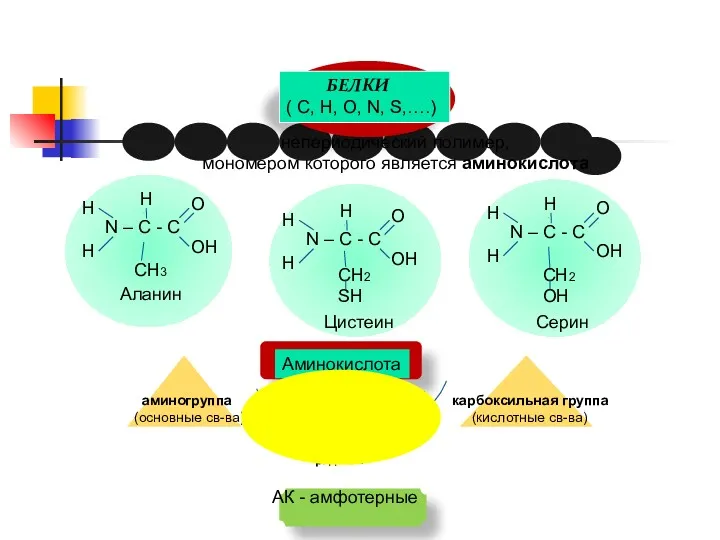
- 13. БЕЛКИ ( С, Н, О, N, S,….) непериодический полимер, мономером которого является аминокислота СН3 Аланин СН2
- 14. Главное – система… АК (по R): Неполярные Полярные Заряженные АК (по отношению к Н2О) Гидрофильные? Гидрофобные?
- 15. Невозможно забыть… АК (по способностити синтезироватьсяся в организме) Незаменимые: Вал, Лей, Иле, Лиз, Мет, Три, Тре,
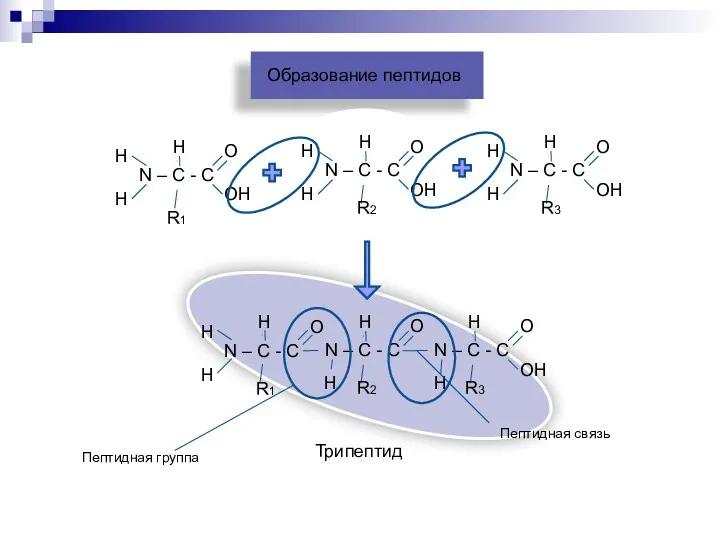
- 16. Образование пептидов R1 R2 R3 R1 R2 R3 Трипептид Пептидная связь Пептидная группа
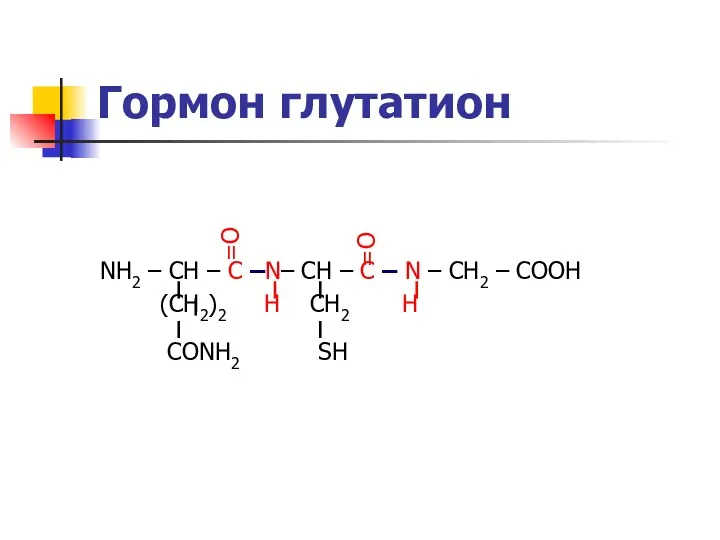
- 17. Гормон глутатион NH2 – CH – С –N– CH – C – N – CH2 –
- 18. Великое берет начало с малого Сир Публий, I в. до.н.э.
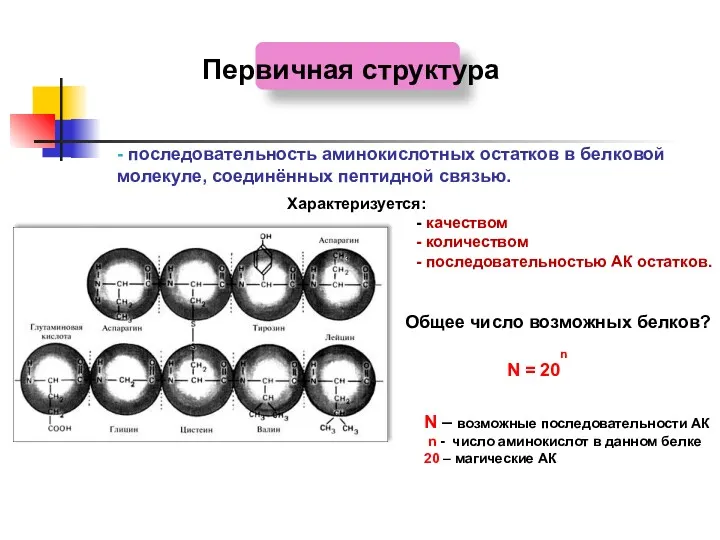
- 19. Первичная структура - последовательность аминокислотных остатков в белковой молекуле, соединённых пептидной связью. Характеризуется: - качеством -
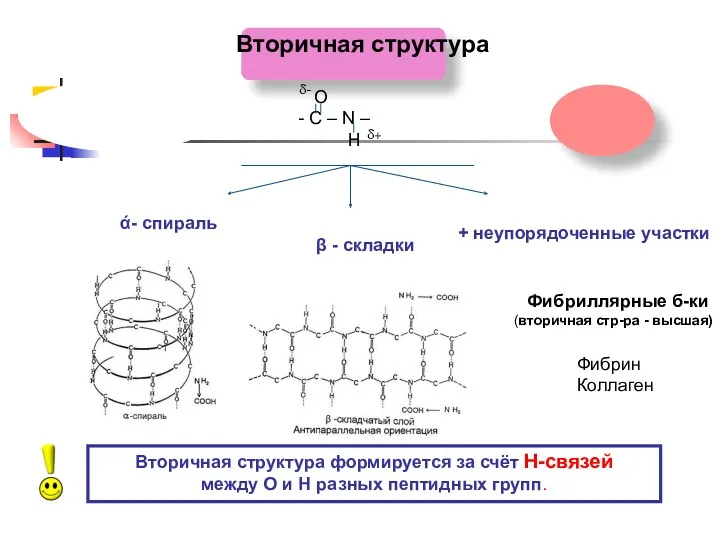
- 20. Вторичная структура О С – N – Н δ+ δ- ά- спираль β - складки +
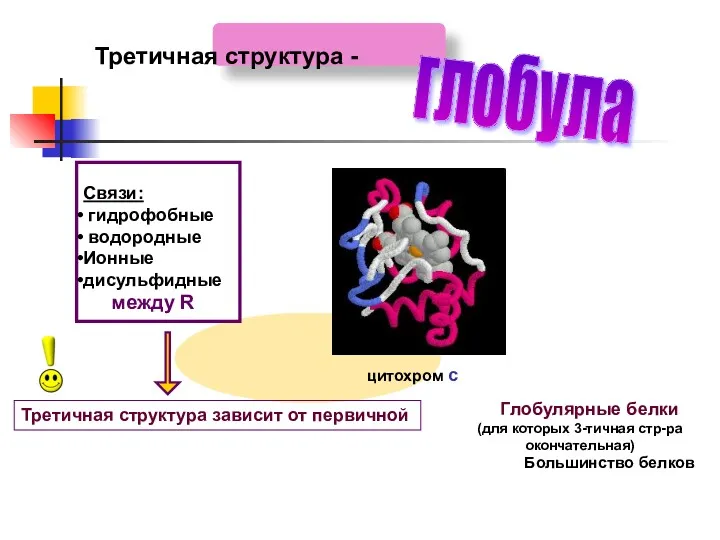
- 21. Связи: гидрофобные водородные Ионные дисульфидные между R Третичная структура - Третичная структура зависит от первичной Глобулярные
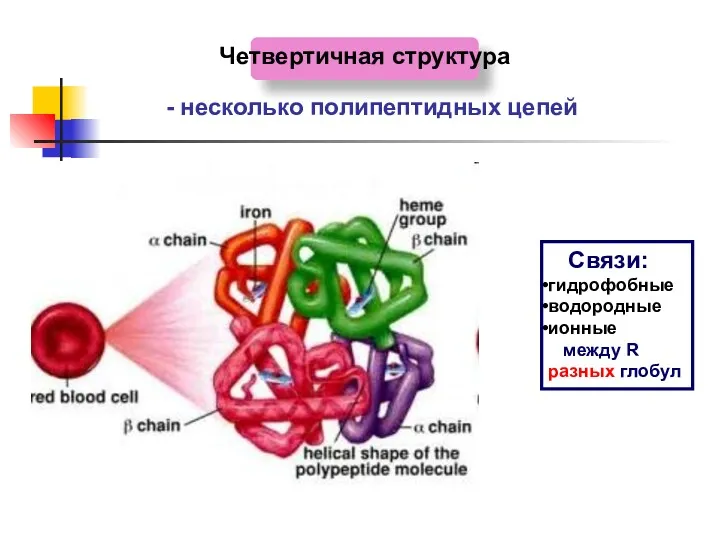
- 22. Четвертичная структура - несколько полипептидных цепей Связи: гидрофобные водородные ионные между R разных глобул
- 23. От простого к сложному
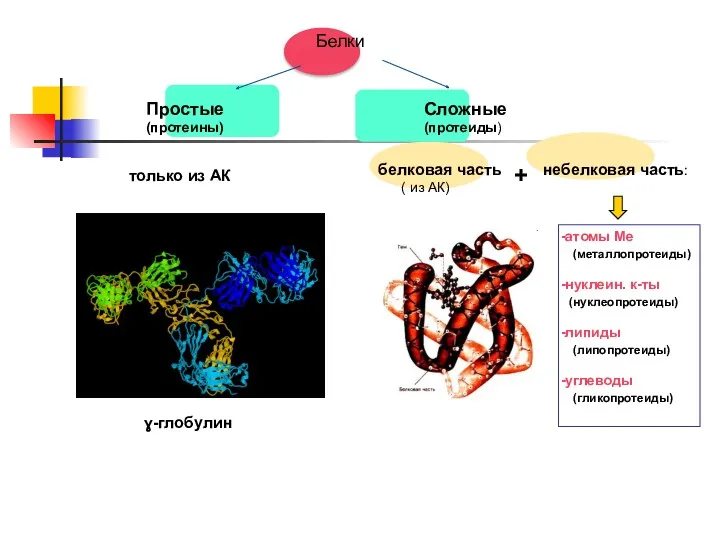
- 24. Белки Простые (протеины) Сложные (протеиды) только из АК белковая часть ( из АК) небелковая часть: атомы
- 26. Скачать презентацию










 Почему осенью осыпаются листья
Почему осенью осыпаются листья Среды жизни и места обитания животных. Взаимосвязь животных в природе
Среды жизни и места обитания животных. Взаимосвязь животных в природе Эмбриогенез амфибий
Эмбриогенез амфибий Обобщающий урок – КВН Общее знакомство с цветковыми растениями Клеточное строение растительного организма
Обобщающий урок – КВН Общее знакомство с цветковыми растениями Клеточное строение растительного организма Индивидуальное развитие человека, или онтогенез
Индивидуальное развитие человека, или онтогенез презентация ГМО
презентация ГМО Клеточные. Эукариоты. Царство Животные. Подцарство Позвоночные. Тип Хордовые. Подтип Черепные. Класс Земноводные
Клеточные. Эукариоты. Царство Животные. Подцарство Позвоночные. Тип Хордовые. Подтип Черепные. Класс Земноводные Внешнее строение листа
Внешнее строение листа Органеллы клетки
Органеллы клетки Жизненные циклы растений
Жизненные циклы растений Животные весной
Животные весной Методы микробиологического исследования
Методы микробиологического исследования Анатомия человека
Анатомия человека Грибы-паразиты
Грибы-паразиты Биологическая роль алюминия в организме человека
Биологическая роль алюминия в организме человека Система виділення. Механізми утворення сечі
Система виділення. Механізми утворення сечі Слагаемые биотехнологического производства
Слагаемые биотехнологического производства Эволюция (1 часть)
Эволюция (1 часть) Наследственность и среда. Тема 3
Наследственность и среда. Тема 3 Природные опасности. Ядовитые животные и растения
Природные опасности. Ядовитые животные и растения Механика и энергетика мышц
Механика и энергетика мышц Семейства: Костенцовые, Гиполеписовые, Многоножковые, Сальвиниевые, Ужовниковидные, Сосновые, Кипарисовые, Эфедровые
Семейства: Костенцовые, Гиполеписовые, Многоножковые, Сальвиниевые, Ужовниковидные, Сосновые, Кипарисовые, Эфедровые Пищевые потребности прокариот
Пищевые потребности прокариот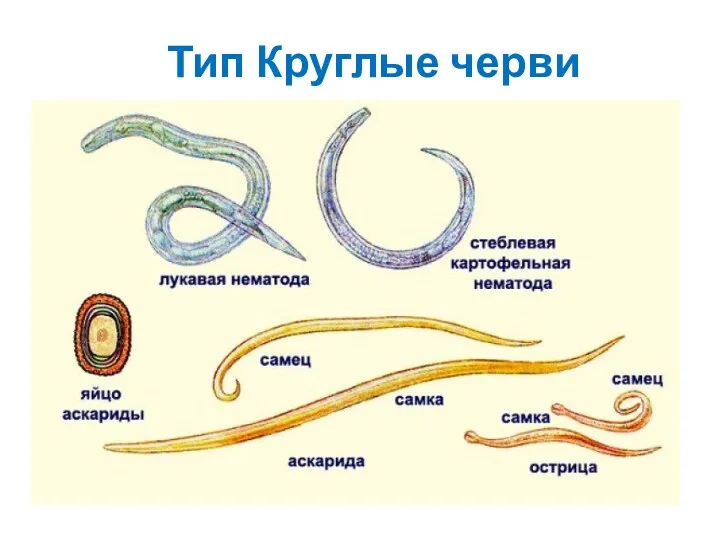 Тип Круглые черви
Тип Круглые черви Разбор заданий ВПР 5 класс
Разбор заданий ВПР 5 класс Мышцы . Лекция 3
Мышцы . Лекция 3 Самые - самые растения
Самые - самые растения Общая биология. Вводная 10 класс
Общая биология. Вводная 10 класс