Содержание
- 2. Световые реакции фотосинтеза Улавливание световой энергии, передача энергии на специализированные структуры - реакционные центры (РЦ). Осуществляет:
- 3. Энергия фотона ε = hv h - константа Планка, v - частота волны. Скорость фотона c=
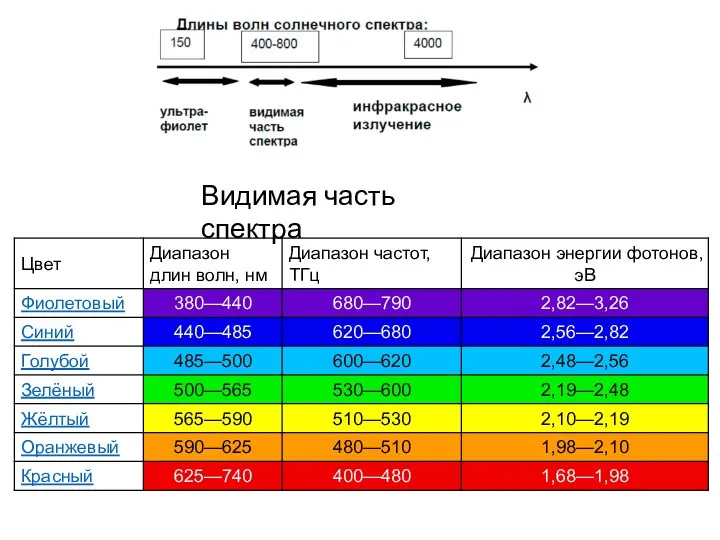
- 4. Видимая часть спектра
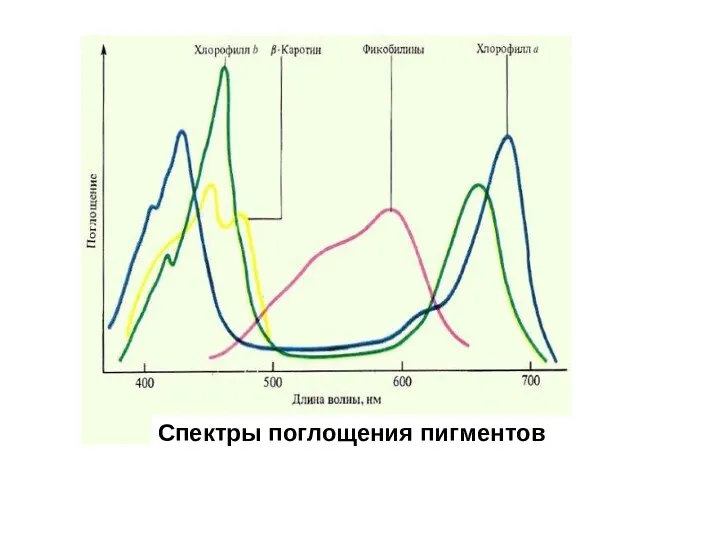
- 5. Спектры поглощения пигментов
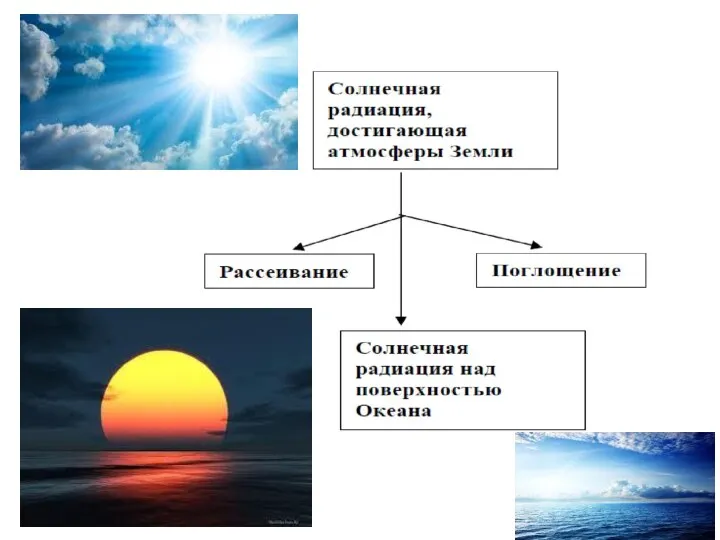
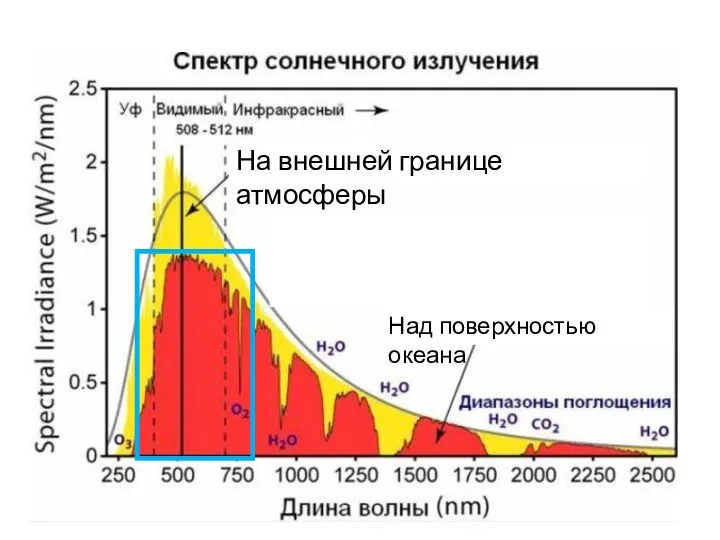
- 7. На внешней границе атмосферы Над поверхностью океана
- 8. В любой молекуле электроны (ē) расположены на орбиталях (S, p. d, f и т.д.). На каждой
- 9. ē могут переходить на более высокий энергетический уровень (ε1), если (а) там есть вакансия; (б) ē
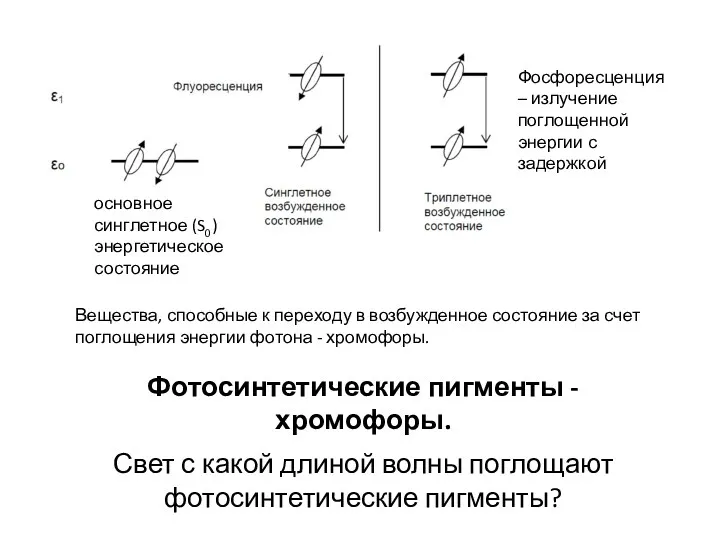
- 10. Вещества, способные к переходу в возбужденное состояние за счет поглощения энергии фотона - хромофоры. Фотосинтетические пигменты
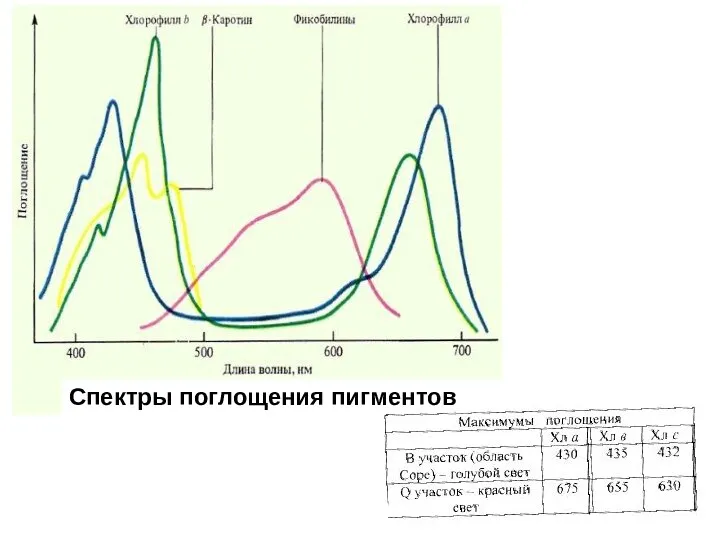
- 11. Спектры поглощения пигментов
- 12. Пигментный состав Prasinophyceae
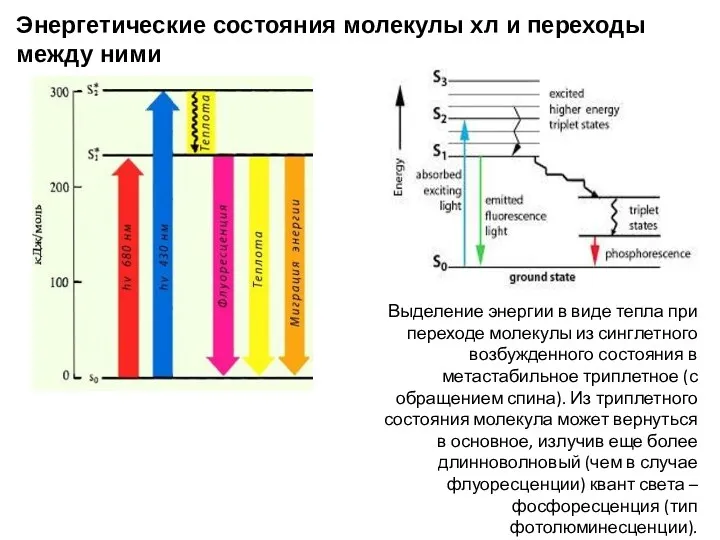
- 13. Энергетические состояния молекулы хл и переходы между ними Выделение энергии в виде тепла при переходе молекулы
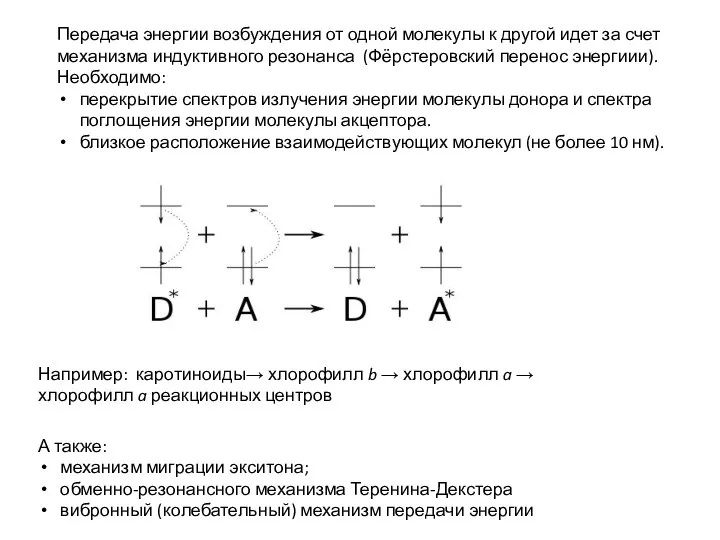
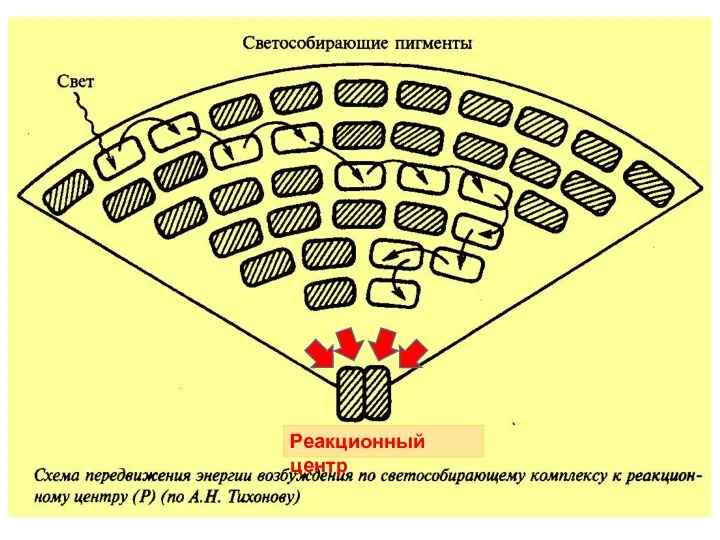
- 14. Передача энергии возбуждения от одной молекулы к другой идет за счет механизма индуктивного резонанса (Фёрстеровский перенос
- 15. Реакционный центр
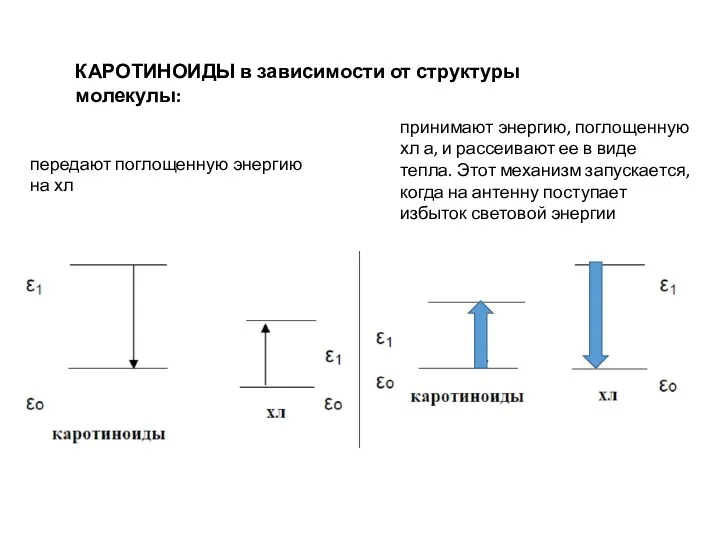
- 16. КАРОТИНОИДЫ в зависимости от структуры молекулы: передают поглощенную энергию на хл принимают энергию, поглощенную хл а,
- 17. По ССК (антенне) в РЦ передается только ЭНЕРГИЯ возбуждения, электрон НЕ передается Что происходит в РЦ?
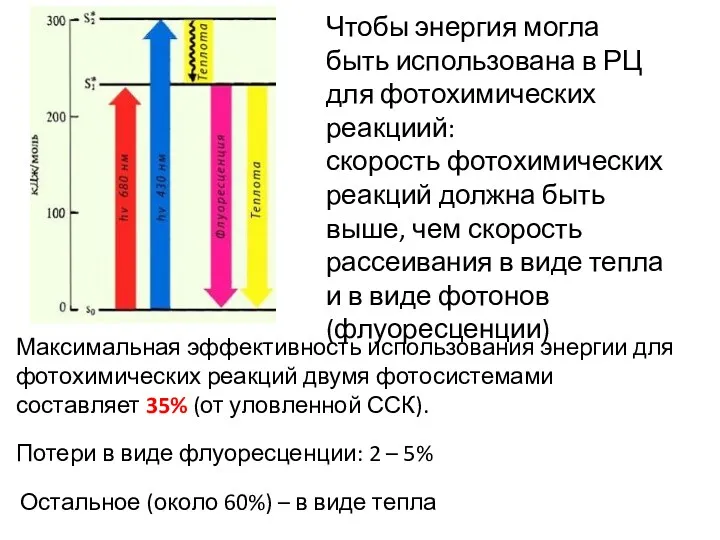
- 18. Чтобы энергия могла быть использована в РЦ для фотохимических реакциий: скорость фотохимических реакций должна быть выше,
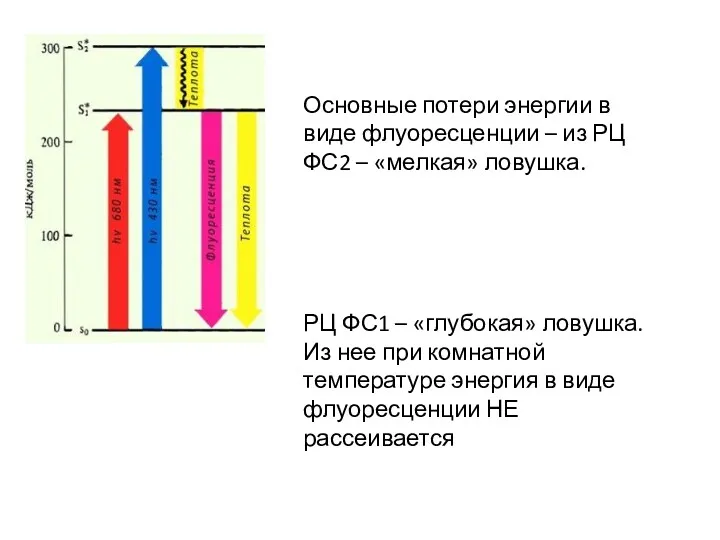
- 19. Основные потери энергии в виде флуоресценции – из РЦ ФС2 – «мелкая» ловушка. РЦ ФС1 –
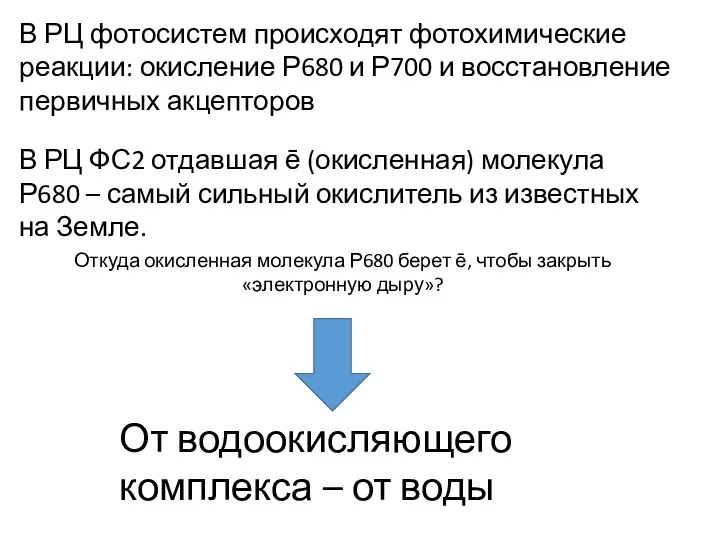
- 20. В РЦ ФС2 отдавшая ē (окисленная) молекула Р680 – самый сильный окислитель из известных на Земле.
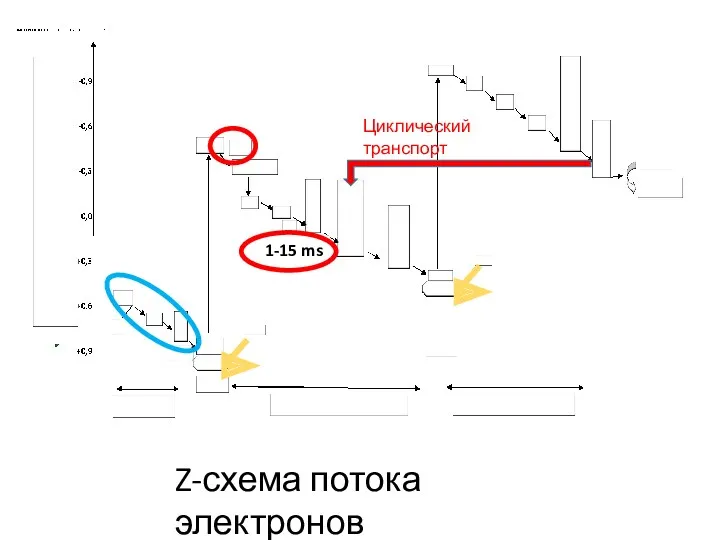
- 21. 1-15 ms Z-схема потока электронов Циклический транспорт
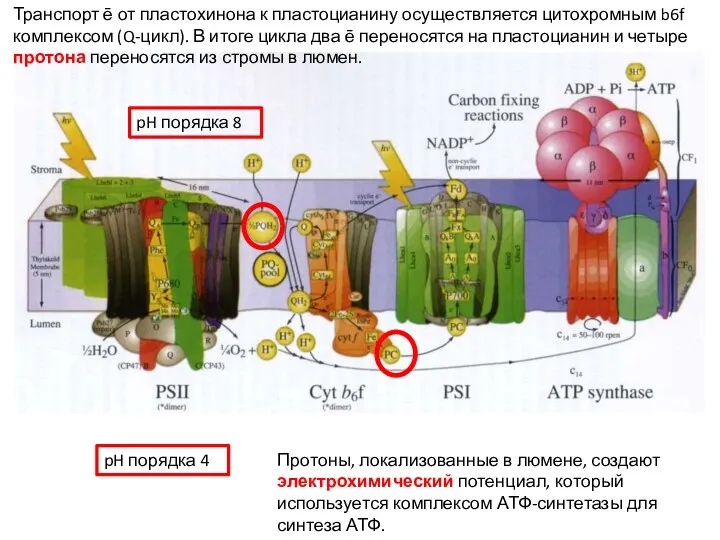
- 22. Протоны, локализованные в люмене, создают электрохимический потенциал, который используется комплексом АТФ-синтетазы для синтеза АТФ. Транспорт ē
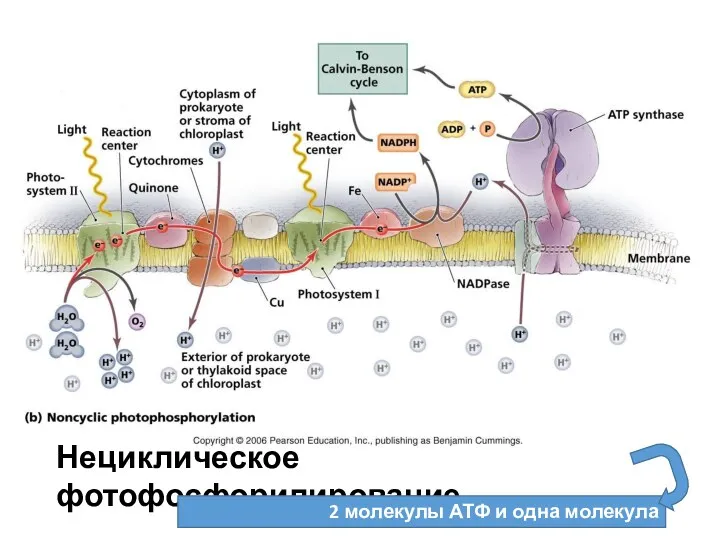
- 23. Нециклическое фотофосфорилирование 2 молекулы АТФ и одна молекула восстановителя
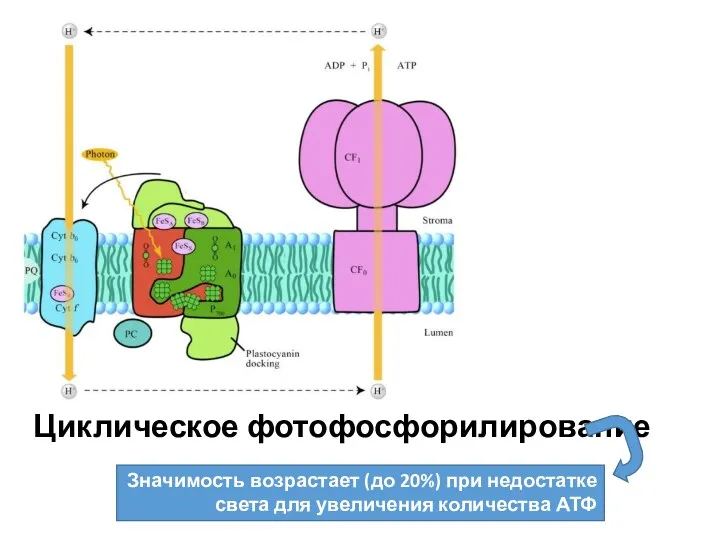
- 24. Циклическое фотофосфорилирование Значимость возрастает (до 20%) при недостатке света для увеличения количества АТФ
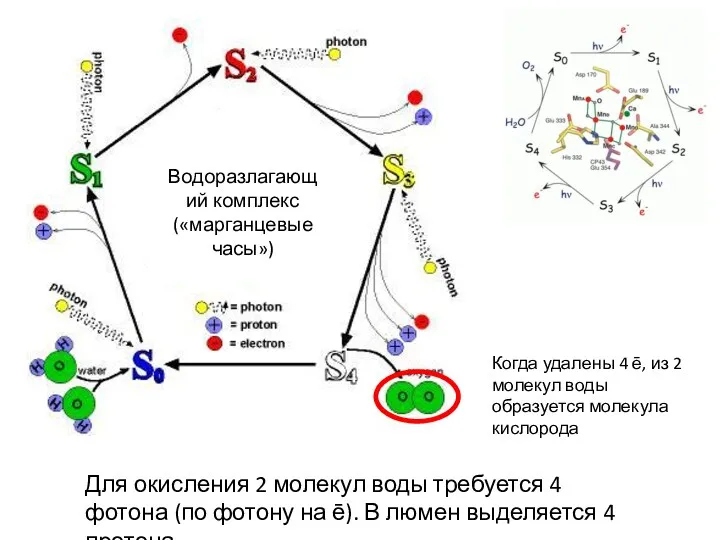
- 25. Водоразлагающий комплекс («марганцевые часы») Для окисления 2 молекул воды требуется 4 фотона (по фотону на ē).
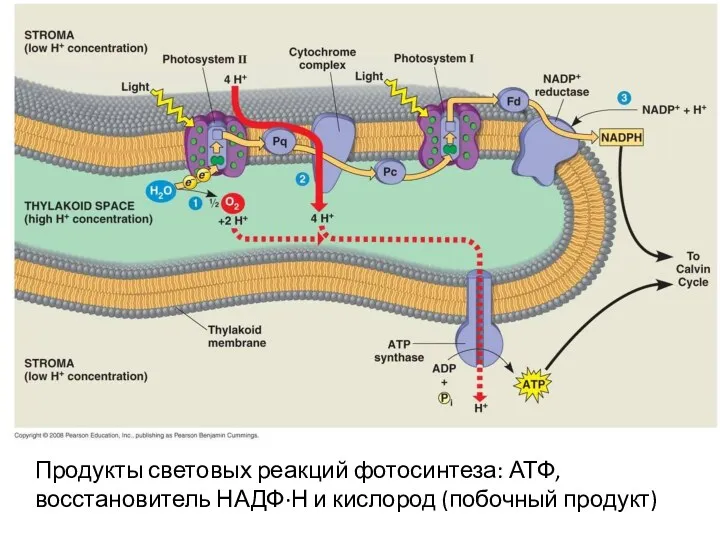
- 26. Продукты световых реакций фотосинтеза: АТФ, восстановитель НАДФ·Н и кислород (побочный продукт)
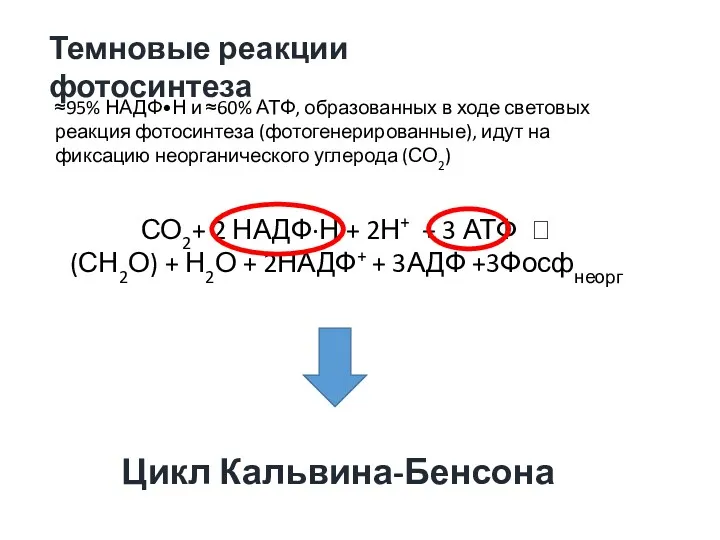
- 27. ≈95% НАДФ•Н и ≈60% АТФ, образованных в ходе световых реакция фотосинтеза (фотогенерированные), идут на фиксацию неорганического
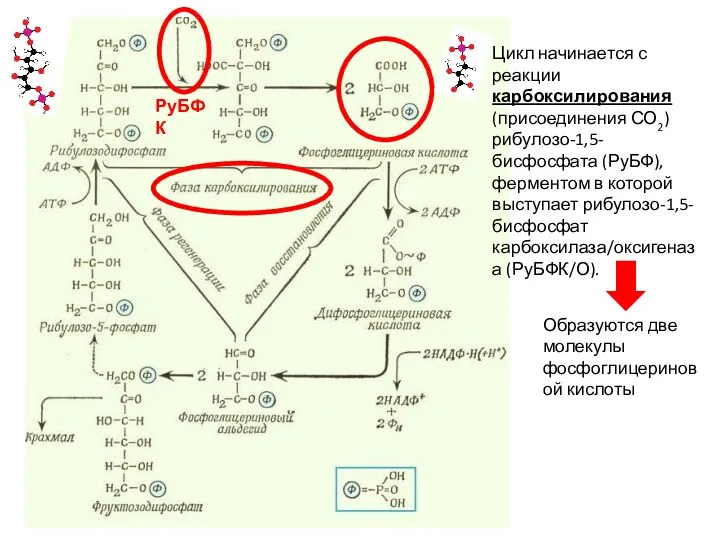
- 28. Цикл начинается с реакции карбоксилирования (присоединения СО2) рибулозо-1,5-бисфосфата (РуБФ), ферментом в которой выступает рибулозо-1,5-бисфосфат карбоксилаза/оксигеназа (РуБФК/О).
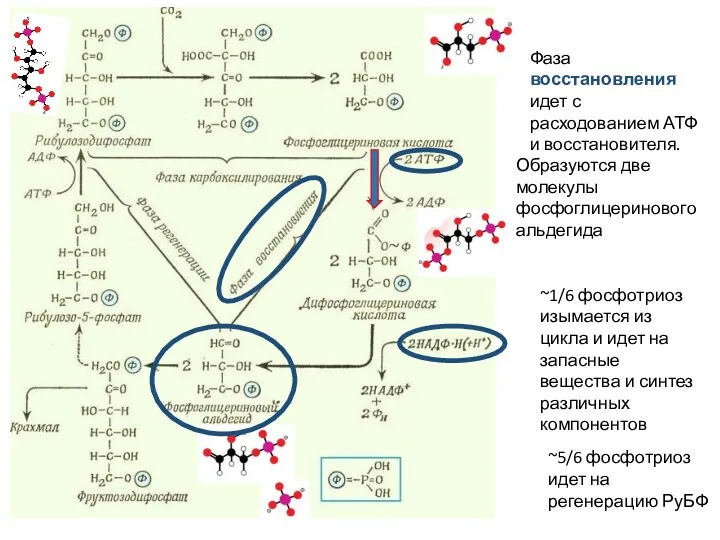
- 29. ~1/6 фосфотриоз изымается из цикла и идет на запасные вещества и синтез различных компонентов ~5/6 фосфотриоз
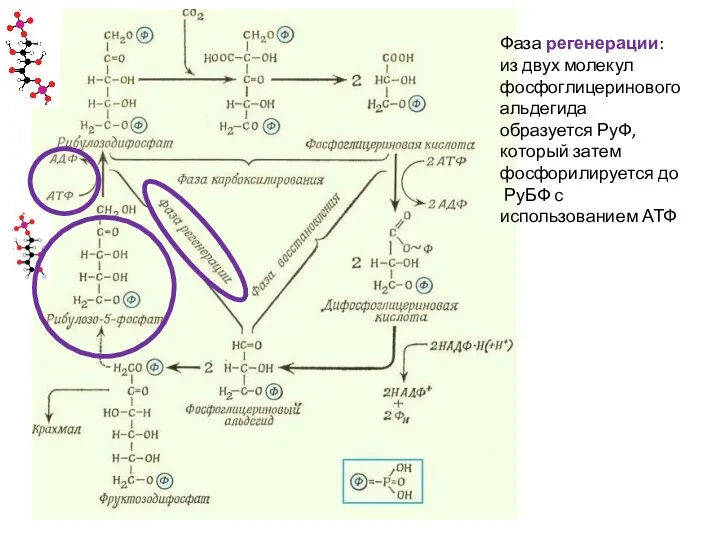
- 30. Фаза регенерации: из двух молекул фосфоглицеринового альдегида образуется РуФ, который затем фосфорилируется до РуБФ с использованием
- 31. Ферменты цикла Кальвина-Бенсона Реакции цикла и ферменты, их катализирующие, могут быть разделены на три основные группы:
- 32. Звено, лимитирующее скорость функционирования цикла Кальвина-Бенсона Субстраты цикла – СО2 (субстрат РуБФК/О) и фотогенерированные АТФ и
- 33. (3) Если и СО2, и свет не лимитируют. Скорость работы всего цикла будет ограничиваться максимально возможной
- 34. Первый шаг в фиксации неорганического углерода: СО2+РуБФ, катализируется РуБФК/О откуда берется? В водном растворе при взаимодействии
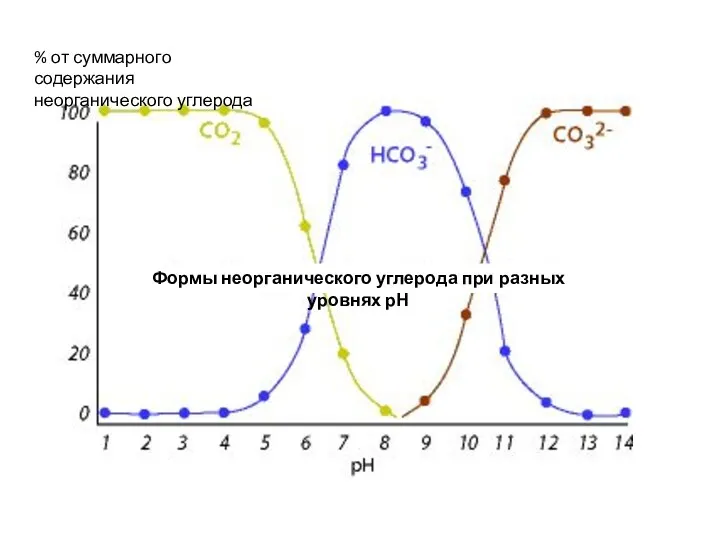
- 35. Формы неорганического углерода при разных уровнях рН % от суммарного содержания неорганического углерода
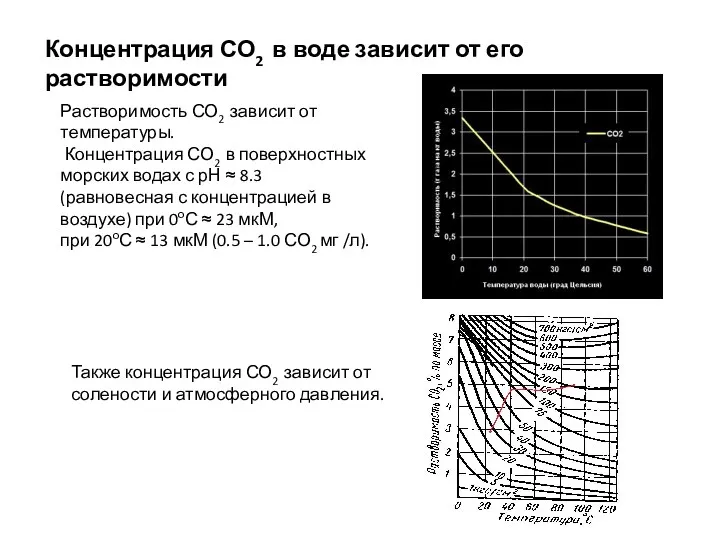
- 36. Растворимость СО2 зависит от температуры. Концентрация СО2 в поверхностных морских водах с рН ≈ 8.3 (равновесная
- 37. Концентрация бикарбонатов существенно больше, чем углекислого газа. Но! для иона НСО3- клеточная мембрана непроницаема для РуБК/О
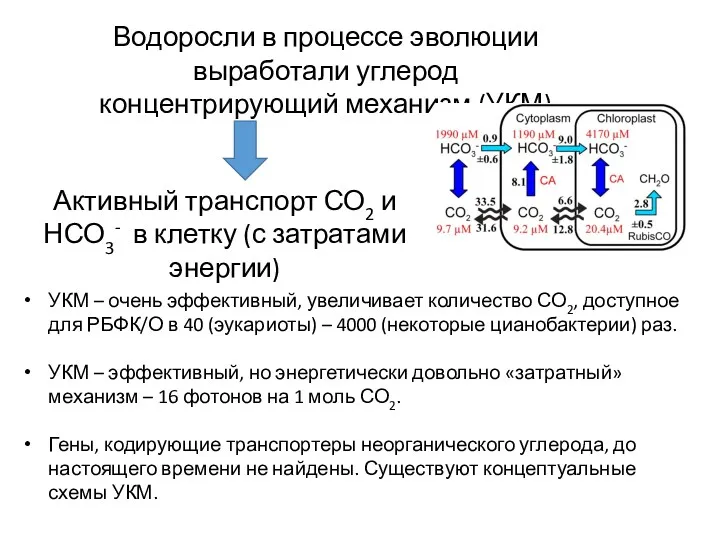
- 38. Водоросли в процессе эволюции выработали углерод концентрирующий механизм (УКМ) Активный транспорт СО2 и НСО3- в клетку
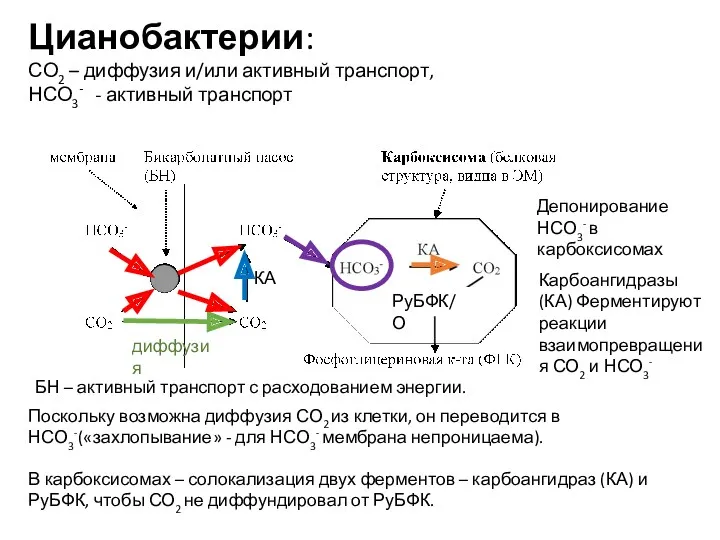
- 39. Цианобактерии: СО2 – диффузия и/или активный транспорт, НСО3- - активный транспорт Поскольку возможна диффузия СО2 из
- 40. Карбоангидразы есть внеклеточные и внутриклеточные. Внутриклеточные КА сконцентрированы в местах локализации РуБФК/О, для обеспечения РуБФК/О субстратом
- 41. Карбоангидразы (КА): В молекуле есть Zn. Высокая скорость оборота – до 600 000/сек. Km = 5
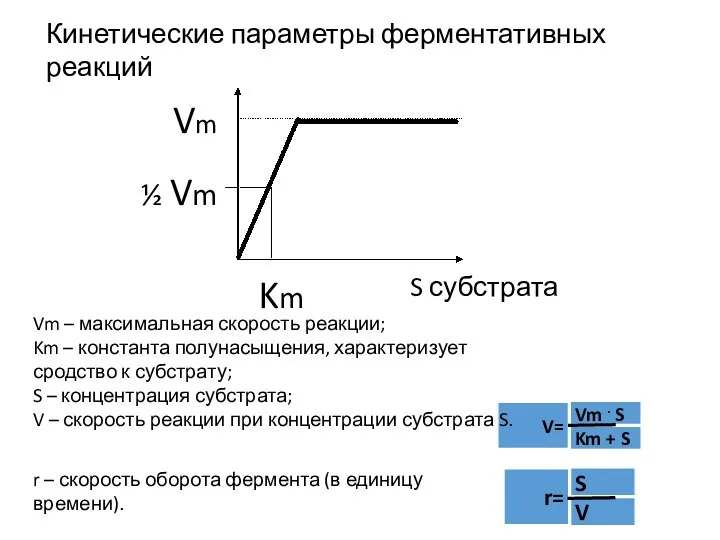
- 42. Кинетические параметры ферментативных реакций Vm Km ½ Vm S субстрата Vm – максимальная скорость реакции; Km
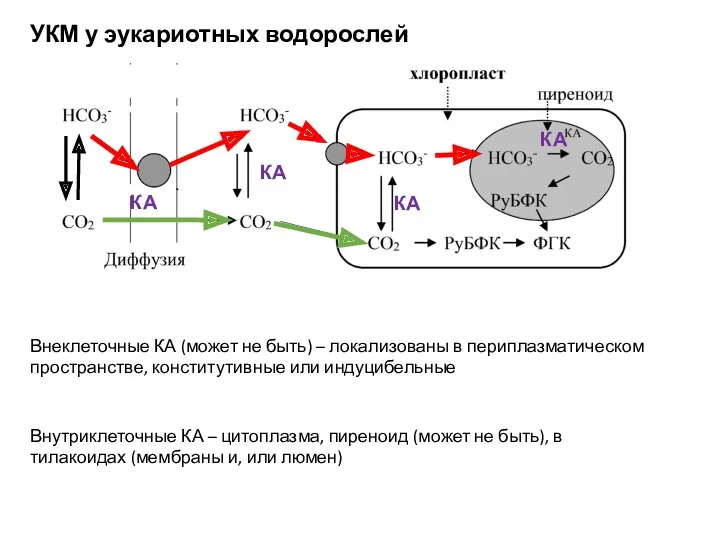
- 43. УКМ у эукариотных водорослей Внутриклеточные КА – цитоплазма, пиреноид (может не быть), в тилакоидах (мембраны и,
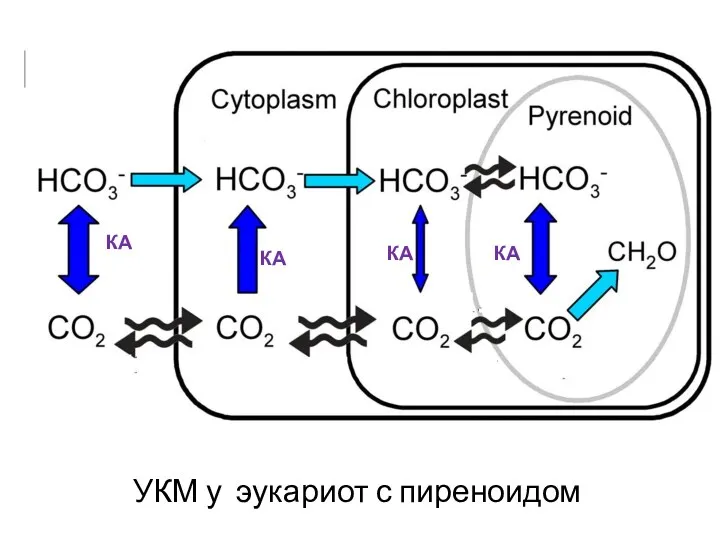
- 44. УКМ у эукариот с пиреноидом КА КА КА КА
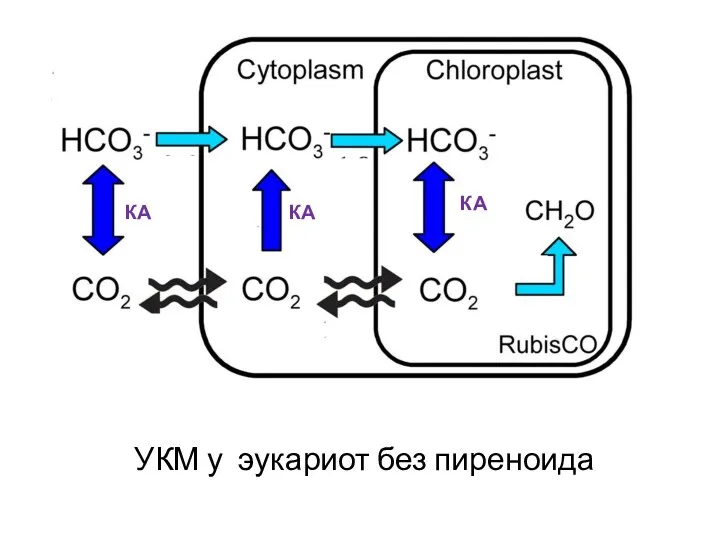
- 45. УКМ у эукариот без пиреноида КА КА КА
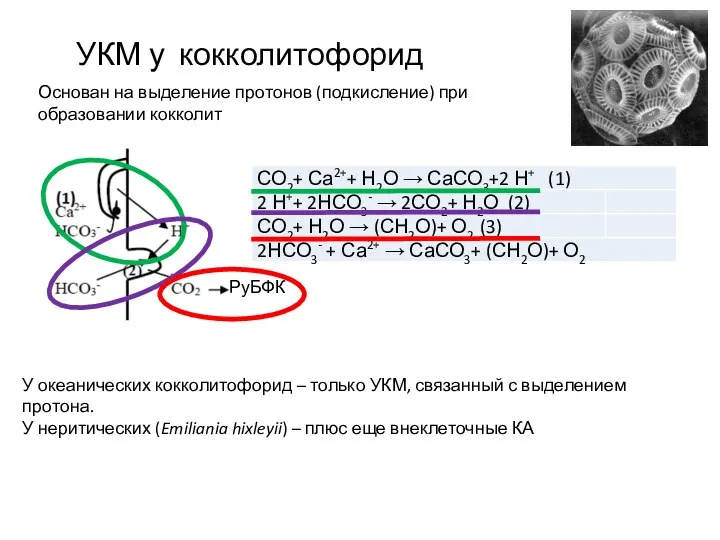
- 46. УКМ у кокколитофорид Основан на выделение протонов (подкисление) при образовании кокколит У океанических кокколитофорид – только
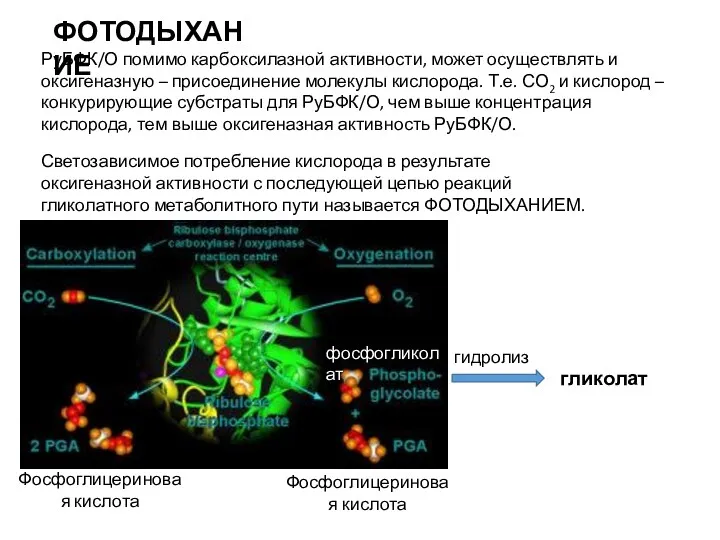
- 47. фосфогликолат Светозависимое потребление кислорода в результате оксигеназной активности с последующей цепью реакций гликолатного метаболитного пути называется
- 48. Выделение гликолата в виде экзометаболитов – результат фотодыхания. Как правило, у водорослей фотодыхание незначительное, у наземных
- 49. (2) Выработка углерод концентрирующего механизма, включая выработку активного транспорта НСО3- (более обильной в водной среде формы
- 50. МОЛЕКУЛЯРНАЯ СТРУКТУРА ФОТОСИНТЕТИЧЕСКОГО АППАРАТА И РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ ФОТОСИНТЕЗА На следующей лекции:
- 52. Скачать презентацию















 Половое размножение животных
Половое размножение животных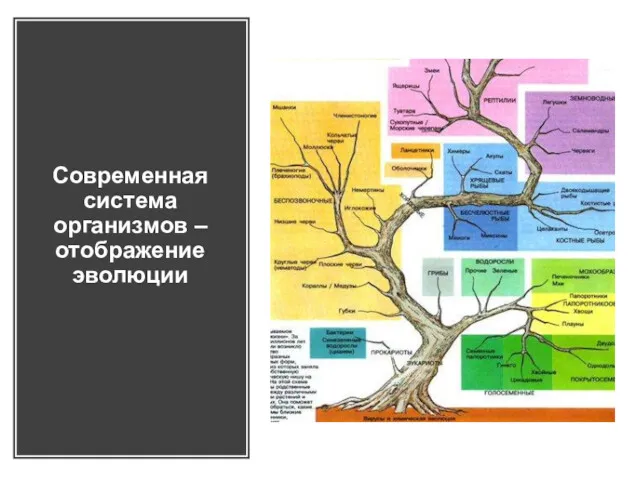 Современная система организмов – отображение эволюции
Современная система организмов – отображение эволюции Сүт және сүт өнімдерінің ішек микрофлорасына әсері
Сүт және сүт өнімдерінің ішек микрофлорасына әсері Химический состав клетки. Неорганические вещества клетки. Глава 1
Химический состав клетки. Неорганические вещества клетки. Глава 1 Семейства: Костенцовые, Гиполеписовые, Многоножковые, Сальвиниевые, Ужовниковидные, Сосновые, Кипарисовые, Эфедровые
Семейства: Костенцовые, Гиполеписовые, Многоножковые, Сальвиниевые, Ужовниковидные, Сосновые, Кипарисовые, Эфедровые Класифікація кормів
Класифікація кормів Семейство растений пасленовые
Семейство растений пасленовые Кровеносная система
Кровеносная система Насекомые-вредители растений
Насекомые-вредители растений Cells. Muscle cells
Cells. Muscle cells конспект урока по биологии 8 класс с мультимедийной презентацией Пищеварительная система
конспект урока по биологии 8 класс с мультимедийной презентацией Пищеварительная система ОПРЕДЕЛЕНИЕ ХРОНОБИОТИПА УЧАЩИХСЯ
ОПРЕДЕЛЕНИЕ ХРОНОБИОТИПА УЧАЩИХСЯ Фотосинтез. 9 класс
Фотосинтез. 9 класс Урок по теме Клетка - универсальная единица жизни.
Урок по теме Клетка - универсальная единица жизни. Презентация, конспект урока, карточки - задания к уроку биологии для 6 класса на тему Фотосинтез.
Презентация, конспект урока, карточки - задания к уроку биологии для 6 класса на тему Фотосинтез. Углеводы
Углеводы Жизненный цикл клеток
Жизненный цикл клеток Приспособленность живых организмов к среде обитания
Приспособленность живых организмов к среде обитания Схема строения Protozoa на примере амебы
Схема строения Protozoa на примере амебы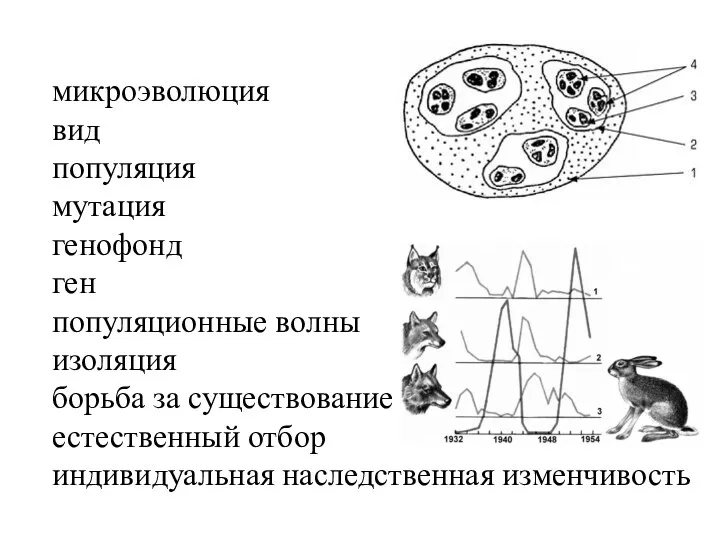 Видообразование. Пути и способы видообразования
Видообразование. Пути и способы видообразования Презентация Здоровье – ключ к успеху
Презентация Здоровье – ключ к успеху Осмос құбылысы
Осмос құбылысы Поняття про середовище існування
Поняття про середовище існування Introduction to artificial intelligence
Introduction to artificial intelligence Состав, структура, свойства ДНК. (Лекция 2)
Состав, структура, свойства ДНК. (Лекция 2) Биологическая активность ксенобиотиков
Биологическая активность ксенобиотиков Млекопитающие отряда приматы
Млекопитающие отряда приматы Современная система селекции растений и семеноводства
Современная система селекции растений и семеноводства