Содержание
- 2. Термодинамика (от греч. Therme — тепло + Dynamis — сила) — раздел физики, изучающий соотношения и
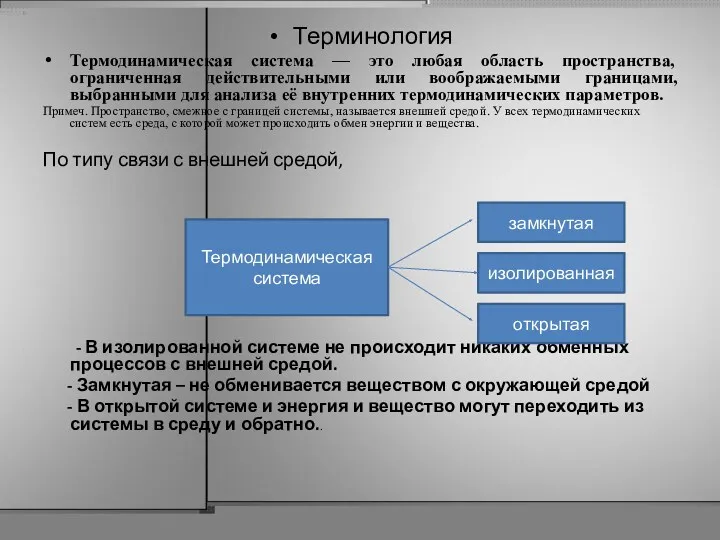
- 3. Терминология Термодинамическая система — это любая область пространства, ограниченная действительными или воображаемыми границами, выбранными для анализа
- 4. Состояние термодинамической системы определяется физическими свойствами вещества. Температура, давление, объем, внутренняя энергия, энтальпия и энтропия —
- 5. ЭНЕРГИЯ (от греч. energeia - действие - деятельность), общая количественная мера различных форм движения материи. Различным
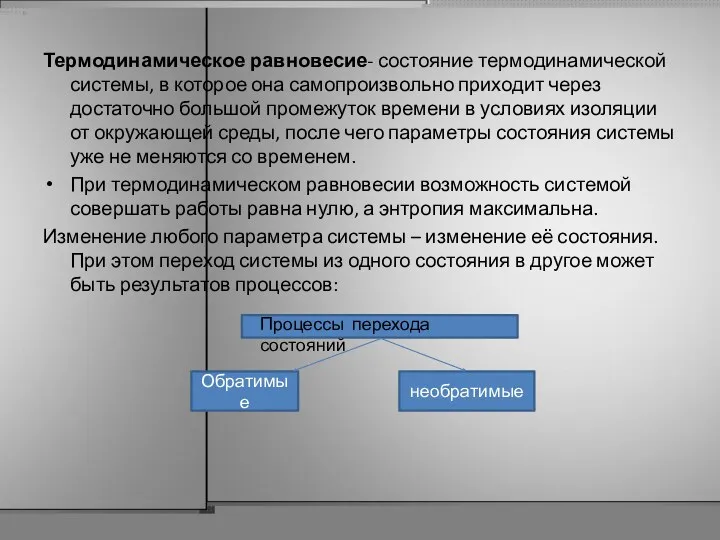
- 6. Термодинамическое равновесие- состояние термодинамической системы, в которое она самопроизвольно приходит через достаточно большой промежуток времени в
- 7. Обратимые и необратимые термодинамические процессы Если в результате процесса состояние системы не изменяется, то такой процесс
- 8. Необратимые т/д процессы – называют такие процессы, которые могут самопроизвольно протекать только в одном определённом направлении.
- 9. Диссипация энергии Диссипация энергии, - у физических систем переход части энергии упорядоченного процесса (например, электрической энергии)
- 10. Внутренняя энергия Внутренняя энергия - энергия тела, зависящая только от его внутреннего состояния. Понятие В. э.
- 11. Биологические системы –открытые системы, в них постоянно происходит процесс обмена энергией с внешней средой. Внутренние метаболические
- 12. Механизмы трансформации энергии в биоструктурах связаны с конформационными превращениями особых макромолекулярных комплексов, таких, как реакционные центры
- 13. ТЕРМОДИНАМИКА НЕОБРАТИМЫХ ПРОЦЕССОВ В БИОЛОГИЧЕСКИХ СИСТЕМАХ ВБЛИЗИ РАВНОВЕСИЯ В классической термодинамике рассматриваются главным образом равновесные состояния
- 14. Первый закон термодинамики «Изменение внутренней энергии (dU) тела (системы) при переходе из одного состояния в другое
- 15. где работа (А) dА = pdV + dAmax (2) Или dQ = dU + pdV +
- 16. Виды работы совершаемой в живых организмах: 1. химическая –синтез органических веществ (ВМС из низкомолекулярных и т.п.)
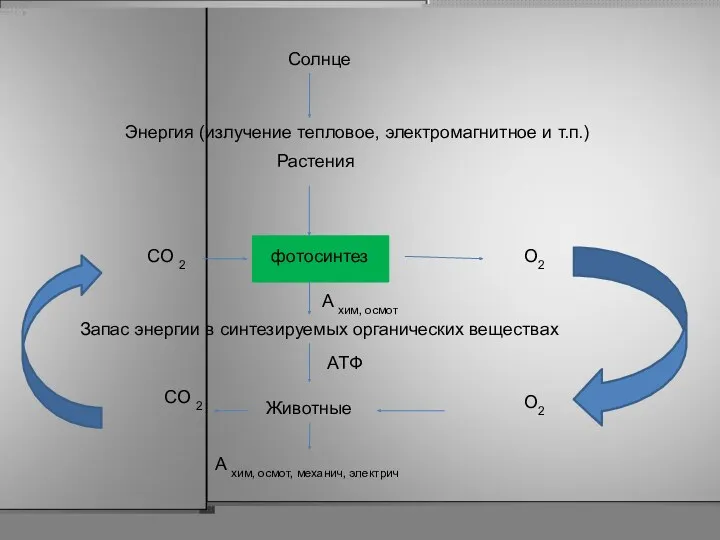
- 17. Солнце Энергия (излучение тепловое, электромагнитное и т.п.) Растения фотосинтез СО 2 Запас энергии в синтезируемых органических
- 18. АТФ + Н2O АДФ + Н3 PO4 + Q (8.5 ккал) Q (теплота) первичная (обмен веществ)
- 19. Энтальпия. Закон Гесса Образование теплоты у гомойотермных животных в покое: 50 % в органах брюшной полости
- 20. ! При физиологических условиях существует равенство между первичной и вторичной теплотой! При патологии – воспаление-происходит разобщение
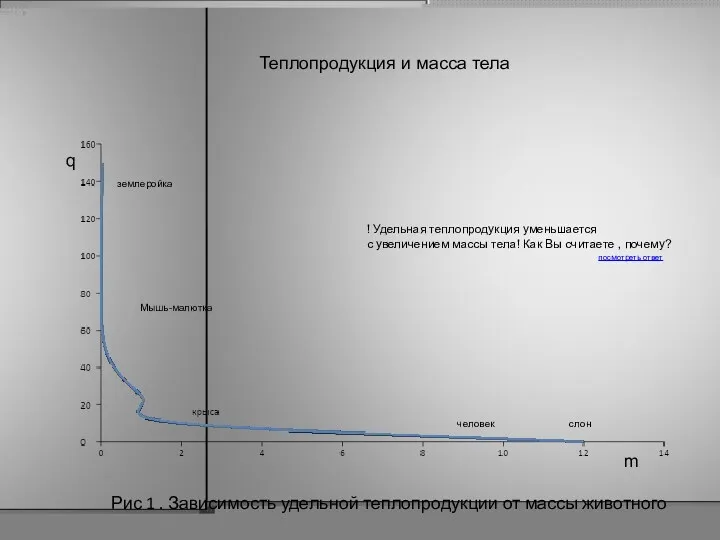
- 21. а-количество клеток b- площадь поверхности Отсюда, удельная теплопродукция (q):
- 22. Рис 1 . Зависимость удельной теплопродукции от массы животного q m землеройка слон человек ! Удельная
- 23. Энтальпия Живые организмы – открытые термодинамические системы, существуют в условиях постоянства давления и температуры. В этих
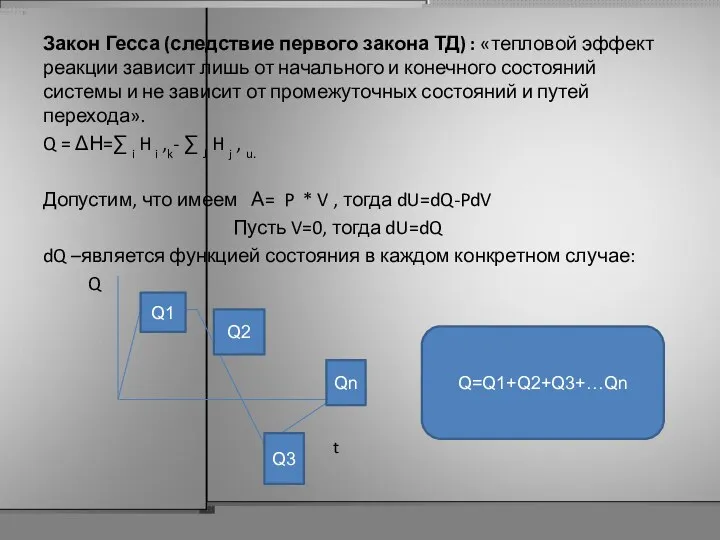
- 24. Закон Гесса (следствие первого закона ТД) : «тепловой эффект реакции зависит лишь от начального и конечного
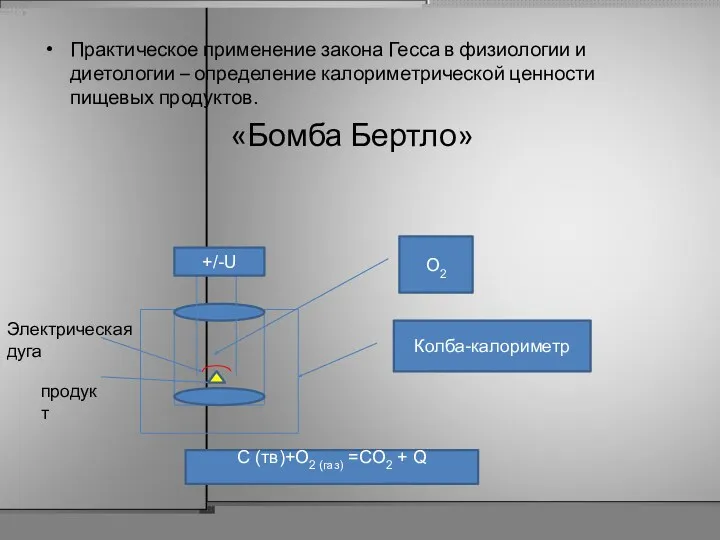
- 25. Практическое применение закона Гесса в физиологии и диетологии – определение калориметрической ценности пищевых продуктов. «Бомба Бертло»
- 26. Второй закон термодинамики (Клаузиуса): «Невозможен процесс, единственным результатом которого являлась бы передача тепла от более холодного
- 27. I – закон не говорит о направлении пути самопроизвольного процесса. Возможность протекания Т/Д процессов их направленность
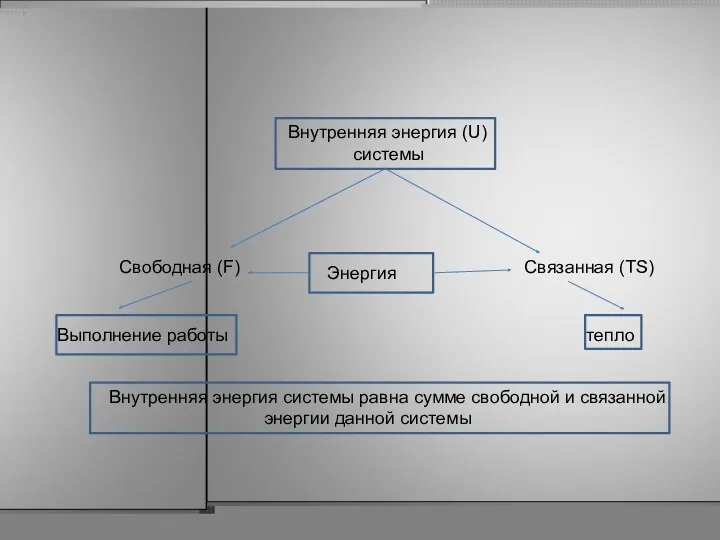
- 28. Внутренняя энергия системы равна сумме свободной и связанной энергии данной системы Внутренняя энергия (U) системы Свободная
- 29. При T = const, связанная энергия определяется энтропией.., отсюда чем больше энтропия, тем больше связанной энергии…,
- 30. Обобщая вышесказанное с позиций Второго закона Т/Д: «Любой самопроизвольный процесс в изолированной системе приводит к уменьшению
- 31. Математически Второй закон термодинамики может быть выражен: d Q T 0 dS = Знак больше относится
- 32. Максимально полезная работа, совершаемая системой А макс – связана с термодинамическими функциями свободной энергии: F =
- 33. Применительно к биохимическим реакциям, изменения объема и давления незначительны: dF=-SdT-pdv dG=-SdT+vdp=dF+pdv+vdp Δ F ≈ ΔG Таким
- 34. При этом dA = 0. В этом случае система деградирована и не способна совершать работу. Для
- 35. Таким образом, эволюционный критерий направленности необратимых изменений в изолированных системах, заключается в том что они всегда
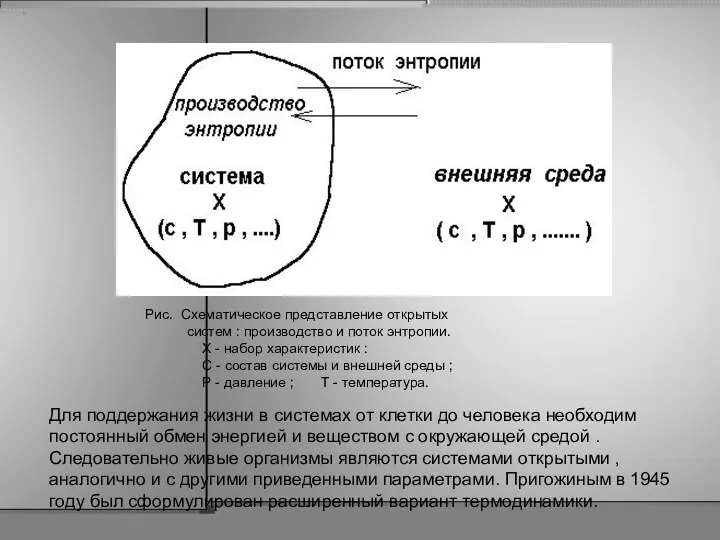
- 36. ОБЩАЯ ХАРАКТЕРИСТИКА ОТКРЫТЫХ СИСТЕМ. Открытые системы - это термодинамические системы, которые обмениваются с окружающими телами (
- 37. Для поддержания жизни в системах от клетки до человека необходим постоянный обмен энергией и веществом с
- 38. Рассмотрим свойства организма как -термодинамически - открытой системы, в которой протекают химические реакции. Биохимические реакции на
- 39. Энтропия в организме может оставаться постоянной величиной или увеличиваться или уменьшаться, если поток отрицательной энтропии из
- 40. Потенциально, возможно состояние когда скорость производства энтропии внутри системы равна скорости поступления энтропии из среды: dSi=
- 41. ДИССИПАТИВНЫЕ СИСТЕМЫ Каждая система состоит из элементов (подсистем) . Эти элементы находятся в определенном порядке и
- 42. Формирование структур при необратимых процессах должно сопровождаться качественным скачком (фазовым переходом) при достижении в системе критических
- 43. Чтобы начать формирование структуры , отдача энтропии должна превысить некоторое критическое значение . В сильно неравновесном
- 44. Пространственные , временные или пространственно-временные структуры , которые могут возникать вдали от равновесия в нелинейной области
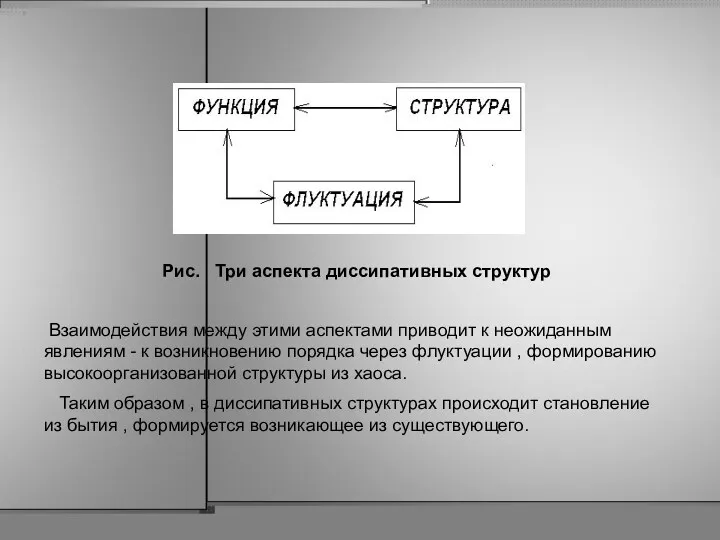
- 45. Рис. Три аспекта диссипативных структур Взаимодействия между этими аспектами приводит к неожиданным явлениям - к возникновению
- 46. Соотношения Онзагера В организме имеет место сопряжение многих химических и физико-химических процессов. При этом соотношение между
- 47. Пусть имеем два взаимодействующих процесса (J1 X 1 ) и (J2 X 2 ). Тогда потоки
- 48. Пусть имеем два взаимодействующих процесса (J1 X 1 ) и (J2X2 ). Тогда, J1 = L11X1+L12X2
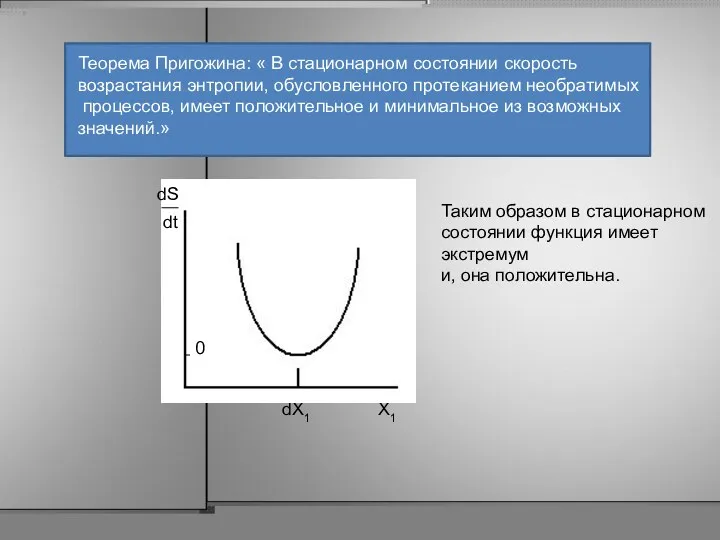
- 49. Теорема Пригожина: « В стационарном состоянии скорость возрастания энтропии, обусловленного протеканием необратимых процессов, имеет положительное и
- 50. Итак, состояние всякой линейной открытой системы с независящими от времени краевыми условиями всегда изменяется в направлении
- 51. В живых системах, как считается, можно приравнять диссипативную функцию к интенсивности теплопродукции, а следовательно, интенсивности дыхания
- 52. Против теоремы Пригожина–Виам выдвинуто два основных возражения: 1) считается, что эта теория все же недостаточно проверены
- 53. Согласно термодинамической теории Пригожина – Виам, можно считать, что процесс развития, роста и старения организмов представляет
- 54. Дополнительная литература 1. Базаров И.П. Термодинамика. - М.: Высшая школа, 1991 г. 2. Гленсдорф П. ,
- 55. Спасибо, за внимание !
- 57. Скачать презентацию












































 Животные Антарктиды
Животные Антарктиды Рефлексы головного мозга
Рефлексы головного мозга Палеонтология, как наука
Палеонтология, как наука Введение в дисциплину Цитология, гистология, эмбриология. Лекция 1
Введение в дисциплину Цитология, гистология, эмбриология. Лекция 1 Lapbook: использование на уроках биологии
Lapbook: использование на уроках биологии Важность правильного питания
Важность правильного питания The cell Vesicular nucleus in liver cells
The cell Vesicular nucleus in liver cells Африканская улитка – гигантская Ахатина
Африканская улитка – гигантская Ахатина Разнообразие лис. Всё о лисах
Разнообразие лис. Всё о лисах Animals. Food chain
Animals. Food chain Отряды насекомых. Таракановые. Прямокрылые. Отряд Уховёртки. Подёнки
Отряды насекомых. Таракановые. Прямокрылые. Отряд Уховёртки. Подёнки Структура и функции органоидов клетки (10 класс)
Структура и функции органоидов клетки (10 класс) Жасушаларды жасанды ортады өсіру жағдайлары
Жасушаларды жасанды ортады өсіру жағдайлары Таємниці мітозу
Таємниці мітозу Отдел Моховидные, особенности строения и жизнедеятельности. Значение мхов
Отдел Моховидные, особенности строения и жизнедеятельности. Значение мхов Полезные и лекарственные растения Зауралья
Полезные и лекарственные растения Зауралья Методы цитологии. Клеточная теория
Методы цитологии. Клеточная теория Быть здоровым – это здорово
Быть здоровым – это здорово Размножение и развитие растений
Размножение и развитие растений зимующие-птицы
зимующие-птицы Летние задания по биологии. 5 класс
Летние задания по биологии. 5 класс Онтогенез. Развитие насекомых
Онтогенез. Развитие насекомых Биологиялық ырғақ
Биологиялық ырғақ Ветеринарно-санитарная экспертиза рыбы и рыбных продуктов
Ветеринарно-санитарная экспертиза рыбы и рыбных продуктов Красная Книга Белгородской области. Редкие птицы Белгородской области
Красная Книга Белгородской области. Редкие птицы Белгородской области Домашний питомец, кот Мурзик
Домашний питомец, кот Мурзик Опорно-двигательный аппарат животных и человека
Опорно-двигательный аппарат животных и человека Рекордсмени в природі
Рекордсмени в природі