Содержание
- 2. Оттектің активті формалары Стресс жағдайда оттектің активті формалары түзіледі. ОАФ-ға оттектің аз мөлшері анлғанға қарамастан (2—5%),
- 3. Оттек барлық тірі ағзалардың құрамына кіреді. Негізгі жағдайында оттекте екі қосылмаған электрондары бар, басқаша айтқанда, ол
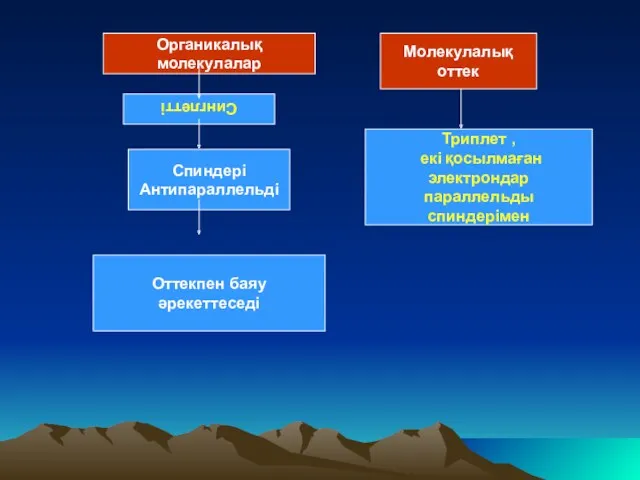
- 4. Органикалық молекулалар Спиндері Антипараллельді Оттекпен баяу әрекеттеседі Молекулалық оттек Триплет , екі қосылмаған электрондар параллельды спиндерімен
- 5. Классификация электронных состояний молекулы основывается на ряде признаков, из к-рых, прежде всего, следует отметить мулътиплетностъ и
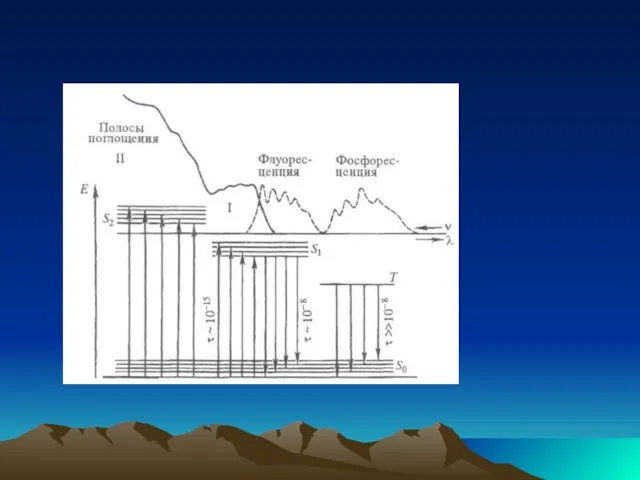
- 7. Спектры испускания. Многоатомные молекулы в конденсир. фазе способны заметно испускать свет лишь при переходах из S1
- 8. Молекулалық оттек негізгі күйінде триплет болып келеді. Ол екі қосылмаған электрондары бар спиндері параллельды, олар әр
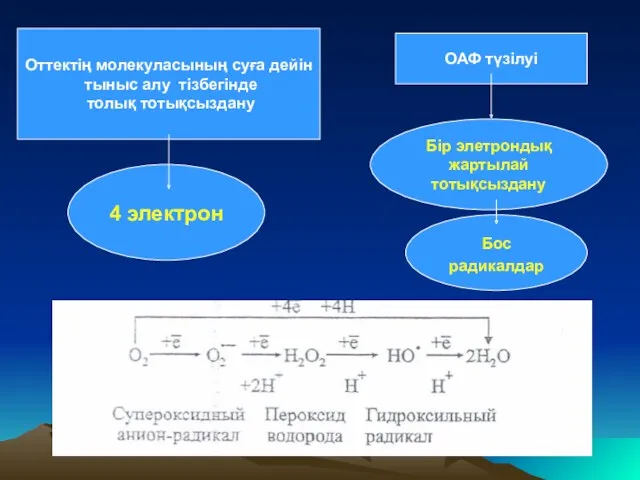
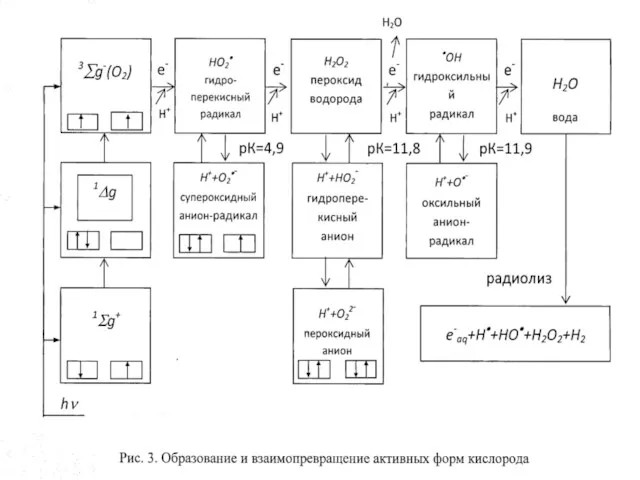
- 9. Оттектің молекуласының суға дейін тыныс алу тізбегінде толық тотықсыздану 4 электрон ОАФ түзілуі Бір элетрондық жартылай
- 10. Ұлпаларда ОАФ аз мөлшерде болады. Н2О2 -10-8 моль/л, О2*- - 10-11 моль/л, НО*- - 10-11 моль/л.
- 11. ОАФ-РЫ БИОМОЛЕКУЛАЛАРДЫ ЗАҚЫМДАНУДА Молекулалық оттек өз өзінен бақыланбайтын химиялық реакцияларға қатспайды, оны ативтендіру үшін ферменттік процестер
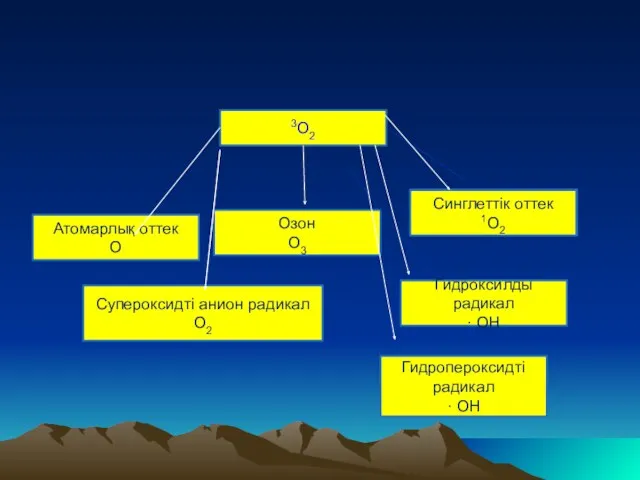
- 12. · 3О2 Атомарлық оттек О Озон О3 Синглеттік оттек 1О2 Супероксидті анион радикал О2 Гидроксилды радикал
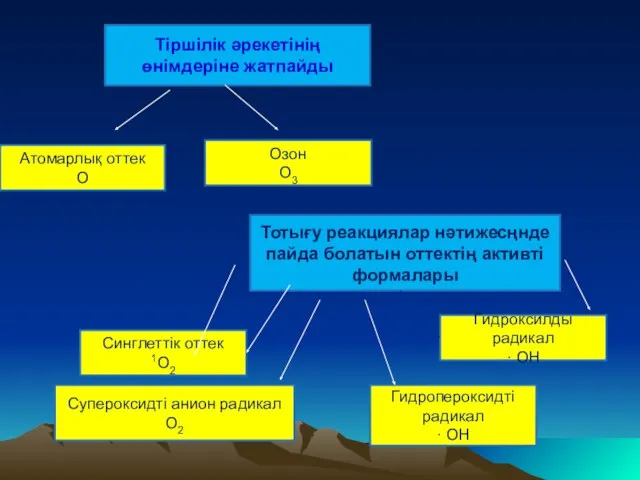
- 13. Тiршiлiк әрекетiнiң өнiмдерiне жатпайды Атомарлық оттек О Озон О3 Супероксидті анион радикал О2 Гидроксилды радикал ·
- 14. Оттектің аткивті формалары (ОАФ) – қысқа өмір сүретін активті реакцияларға жоғары қабілетті оттектің формалары, олар оттектің
- 15. ОАФ түзілунің бірнеше жолдары бар.Олар аэробты метаболизмде , егер тыныс алу тізбегінде оттек толық тотықсызданбаса.жанама өнімдер
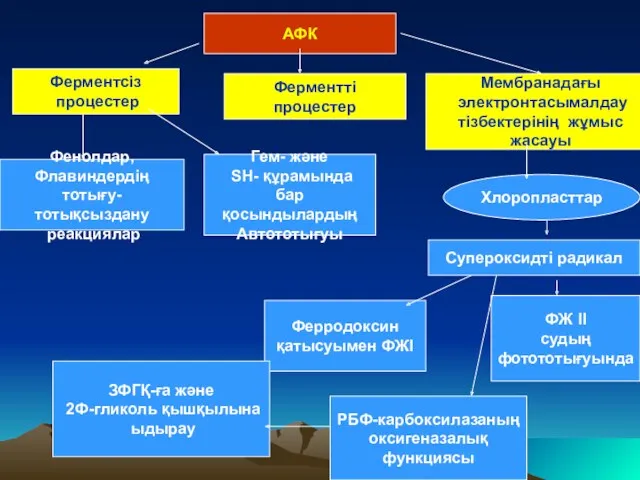
- 16. АФК Ферментсіз процестер Фенолдар, Флавиндердің тотығу- тотықсыздану реакциялар Гем- және SН- құрамында бар қосындылардың Автототығуы Ферментті
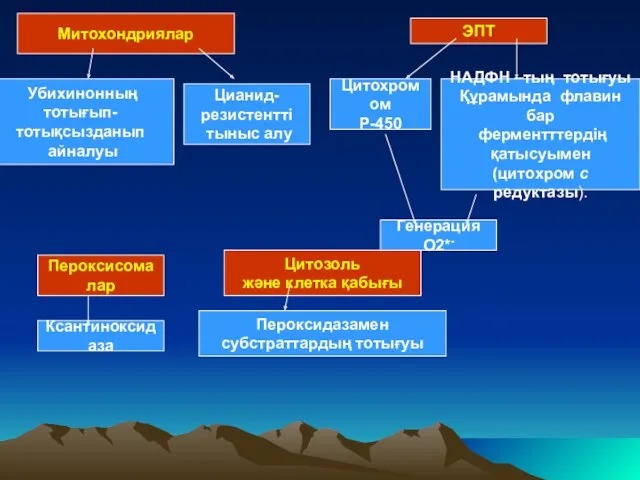
- 17. Митохондриялар Убихинонның тотығып- тотықсызданып айналуы Цианид- резистентті тыныс алу ЭПТ Цитохромом Р-450 Генерация О2*- НАДФН –тың
- 18. Бос радикал сыртқы орбитальда электроны бар бөлік. Ол бөлікті мынадай белгілейді «·».
- 19. Супероксидті анион радикал О2- Оттектің бір электрондық тотықсыздануының өнімі – протонданған формадағы гидропероксидті радикал ионданған формадағы
- 20. Супероксид анион-радикал және басқа ОАФ клетканың әр түрлі құрылымдарында түзіледі. Олар ферментсіз (фенолдардың, хинондардың, құрамында SH-топтары
- 21. Cупероксидті анион-радикалдың түзілуі құрамында флавин бар ксантиноксидаза, сияқты ферменттің қатысуымен, микросомдық мионооксигеназалар, тотықсызданған флавиндердің және хинондардың
- 22. Митохондрии являются главным источником создания супероксидных анионов в клетках. В ходе транспорта электронов к молекулярному кислороду,
- 23. Бос радикалда сыртқы орбитальда. қосылмаған электрон болады Супероксид анион радикал ол тотықсызданудың бірінші өнімі, оның протонданған
- 24. Молекулалық оттектен басқа, олар мембраналардан жақсы өтеді, супероксидті радикалдың заряды бар, ол су молеклаларымен қоршалып тұрады,
- 25. АФК-ның генерациясында молекулалық оттектің күн сәуесінің әсерінен фотодиссиоциацияның нәтижесінде пайда болған озон маңызды роль ойнайды. Озон
- 26. Н2O2 Ол орташа тотықтырғыш болып саналады. Валенттігін ауыстыратын металдар болмаса ол тұрақты болады. Бәрақ оның өмірі
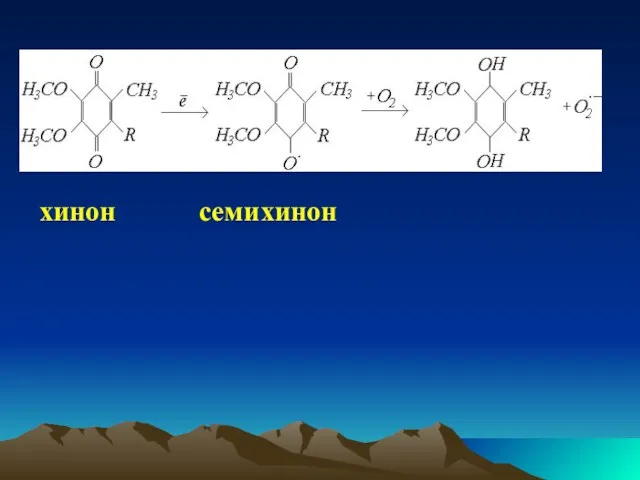
- 27. Cупероксид анион-радикалдың түзілуі құрамында флавин бар ксантиноксидаза, сияқты ферменттің қатысуымен, микросомдық мионооксигеназалар, тотықсызданған флавиндердің және хинондардың
- 28. хинон семихинон
- 30. Бірақ ең көп супероксидтер митохондриядағы және хлоропласттағы электрон тасымалдаушы тізбектің жұмысында түзіледі. Супероксид оттектің хлоропластта тотықсыздануының
- 31. - Клеткалық қабығында оттектің радикалдары пайда болады. Ол өсімдіктің иммундық реакцияларында, клетка қабығындағы , оның ұзарғаныныда
- 32. Оттектің басқа радикалдарынан және синглетті оттектен айырмашылығы - оның ең маңызыды қасиеті - салыстырмалы өмір сүру
- 33. Бір электрон және екі протондар супероксид радикалға қосылғанда сутектің асқын тотығыпайдаболады (Н202 + Сутектің асқын тотығы
- 35. Осы ОАФның өмір сүру ұзақтығы 1 мс, сондықтан ол түзілген жерден біраз жерге диффузяланады. Асқын тотыңтың
- 36. Хлоропластта сутектің асқын тотығы фото тыныс алуда түзіледі, гликолат гликолаоксидазамен тотыққынада, онда Н2О2 ол каталазамен ыдырайды.
- 37. Сутектің асқын тотығы супероксидтің хлоропласттағы және митохондриядағы тотықсыздандырғыштармен әрекеттескенде пайда болады : аскорбатпен, ферредоксинмен. Оны супероксидтің
- 38. Фентон реакциясы: Сутектің асқын тотығының токсикалық әсері осымен белгіленеді Хабера-Вайса реакциясы: ,
- 39. ГИДРОКСИЛ РАДИКАЛ ОН. Келесі бір электрондық тотықсызданған нәтижесінде гидроксил радикал түзіледі ОН. Ол қатты тотықтырғыш болып
- 40. Гидроксил радикал клетканың ішінде миграция жасалмайды, себебі ол тез биомолекулаларымен реакцияға түседі. Оның негізгі көзі Фентон
- 41. Гидроксил радикал клетканың ішінде миграция жасамайды, себебі ол тез биомолекулаларымен реакцияға түседі. ОН-тың негізгі көзі -
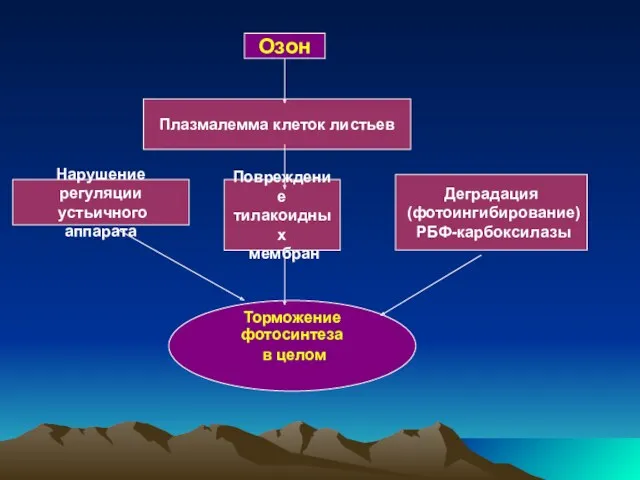
- 42. Озон жапырақтың клеткалық плазмалеммасымен байланысады, леп тесіктердің реттелуін бұзады, тилакоидтық мембрананы зақымдайды, РБФ-карбоксилазаны деградацияға ұшыратады, соңында
- 43. Озон Плазмалемма клеток листьев Нарушение регуляции устьичного аппарата Повреждение тилакоидных мембран Деградация (фотоингибирование) РБФ-карбоксилазы Торможение фотосинтеза
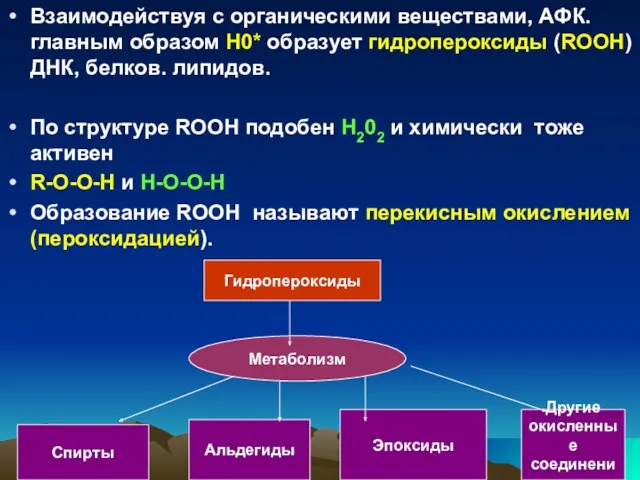
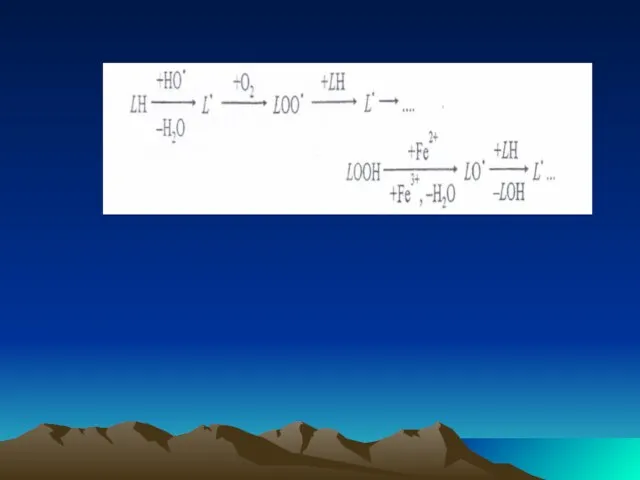
- 44. ROOH-тың түзілуін асқын тотығу деп атайды Метаболизм барысында гидропероксидтер спирттерге, альдегидтерге, эпоксидтерге айналады. Липидтерде /L/ полиқанықпаған
- 45. Взаимодействуя с органическими веществами, АФК. главным образом Н0* образует гидропероксиды (RООН) ДНК, белков. липидов. По структуре
- 46. Реакция LООН с Fе2+ ведет к разветвлению цепи. Далее образуются диеновые (триеновые) коньюгаты жирных кислот, а
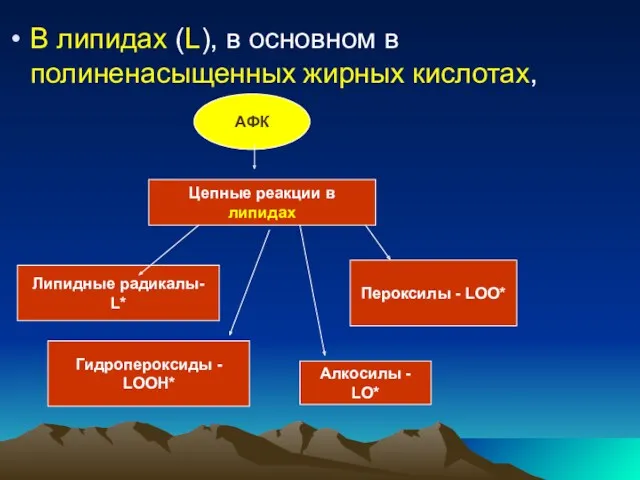
- 47. В липидах (L), в основном в полиненасыщенных жирных кислотах, АФК Цепные реакции в липидах Липидные радикалы-
- 49. Синглетті оттек 1О2 Оның түзілуі жарық реакциялармен байланысты. Жарықтың 1 квантын сіңіргенде пигмент-сенсибилизаор /хлорофилл/ синглеттік қозу
- 50. Синглетті оттек (1О2), фотототығуда пайда болады фотосенсибилизаторлар - флавины, гематопорфирин, хлорофилл и др., бар жағдайда және
- 51. Осы процестің ең басты қорғаныс механизмі бета-каротин, ол синглетті оттекті триплетті жағдайға өткізеді. Бірақ су мен
- 52. Молекулы пигмента в виде синглета или триплета. сталкиваясь с 02, основное состояние которого триплетно, передают на
- 53. ОАФ биологиялық маңызы Қалыпты жағдайда ОАФ және липидтердің асқын тотығы пайда болатыны белгілі. Патологиялық салдар ОАФ
- 54. Тотығу стресс нуклеин қышқылдарды, белоктарды, липидтерді зақымдайды. Супероксид анион-радикал митохондряның ішкі мембранасында орналасады, митохондрияның ДНҚсының қасында,
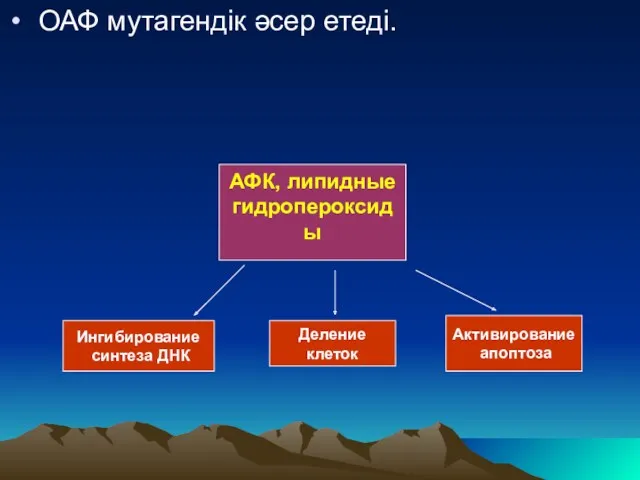
- 55. ОАФ мутагендік әсер етеді. АФК, липидные гидропероксиды Ингибирование синтеза ДНК Деление клеток Активирование апоптоза
- 56. Окислительные модификации белков, вызванные АФК, включают не только изменение аминокислотных остатков. Это может быть и нарушение
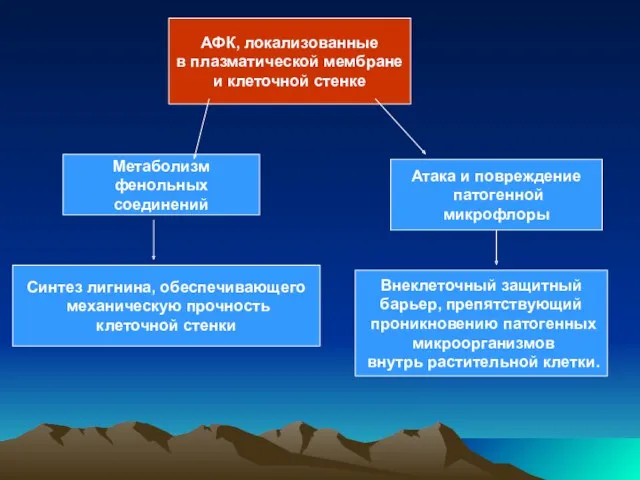
- 57. АФК, локализованные в плазматической мембране и клеточной стенке Атака и повреждение патогенной микрофлоры Метаболизм фенольных соединений
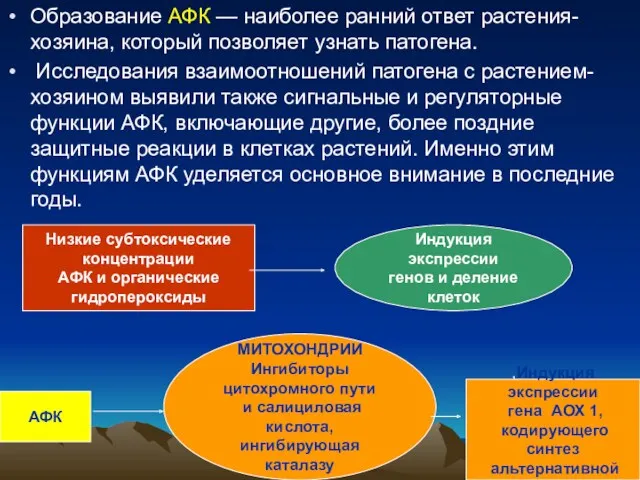
- 58. Образование АФК — наиболее ранний ответ растения-хозяина, который позволяет узнать патогена. Исследования взаимоотношений патогена с растением-хозяином
- 59. Накопление в клетке вторичных посредников — циклонуклеотидов: цАМФ и цГМФ, стимулирует образование АФК. У животных цГМФ
- 60. МЕХАНИЗМЫ ЗАЩИТЫ Способы снижения образования активных форм кислорода Торможение образования супероксид-аниона возможно путем уменьшения в клетке
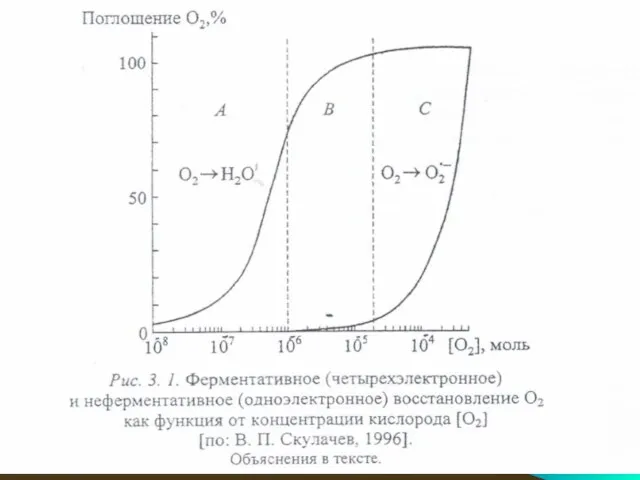
- 61. Концентрация кислорода. обеспечивающая половину максимальной скорости ферментативного восстановления (02 → Н20), принята равной 3•10-7 моль/л. Скорость
- 63. В области В цитохромоксидаза насыщена кислородом, но его недостаточно для обеспечения заметной скорости образования супероксид-аниона. Очевидно,
- 64. Известно несколько способов снижения уровня кислорода в клетке. Активация цианидрезистентной альтернативной оксидазы в ЭТЦ митохондрий. В
- 65. Утечка ионов водорода. Г. Биверс и Б. Чанс установили, что образование Н2О2 митохондриям клеток животных в
- 66. Открывание пор в мембране митохондрий. Если система утечки протонов оказывается недостаточной, включается более радикальный путь, ведущий
- 68. Скачать презентацию























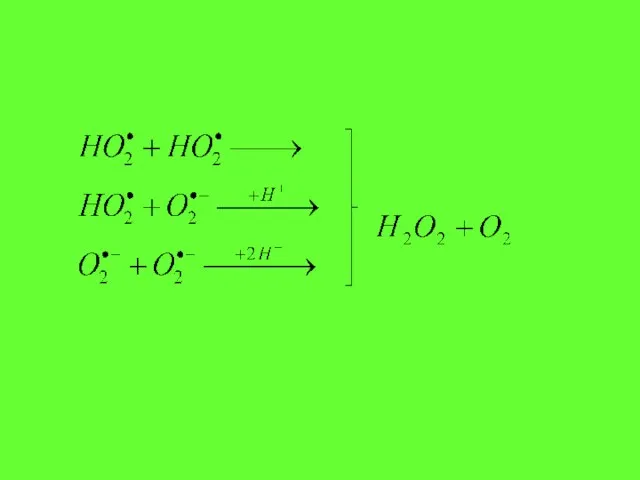
























 Семейство лилейные, отдел цветковые или покрытосеменные
Семейство лилейные, отдел цветковые или покрытосеменные Комнатные растения (часть 2)
Комнатные растения (часть 2) Цитологические основы наследственности
Цитологические основы наследственности What is the engine of our body machine
What is the engine of our body machine Птицы
Птицы У Чёрного моря
У Чёрного моря Вредители питомников и молодняков. (Лекция 5)
Вредители питомников и молодняков. (Лекция 5) Ткани растений
Ткани растений Изучение биоритмов человека – их влияние на жизнедеятельность
Изучение биоритмов человека – их влияние на жизнедеятельность Кормовая и сахарная свёкла
Кормовая и сахарная свёкла Сана және өзіндік сана
Сана және өзіндік сана Растительный и животный мир Республики Удмуртия
Растительный и животный мир Республики Удмуртия Интересные растения
Интересные растения Жасуша ядросы
Жасуша ядросы Бидай. Бидайдың зиянкестері
Бидай. Бидайдың зиянкестері Значение бактерий в природе и жизни человека
Значение бактерий в природе и жизни человека Устройство речевого аппарата
Устройство речевого аппарата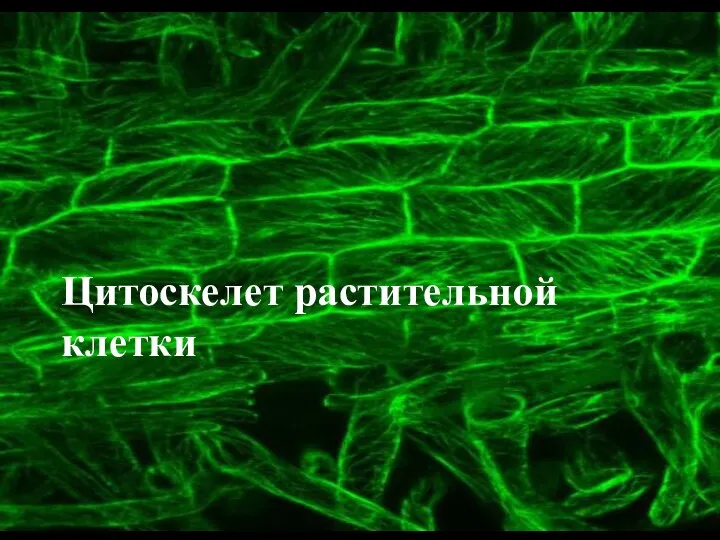 Цитоскелет растительной клетки
Цитоскелет растительной клетки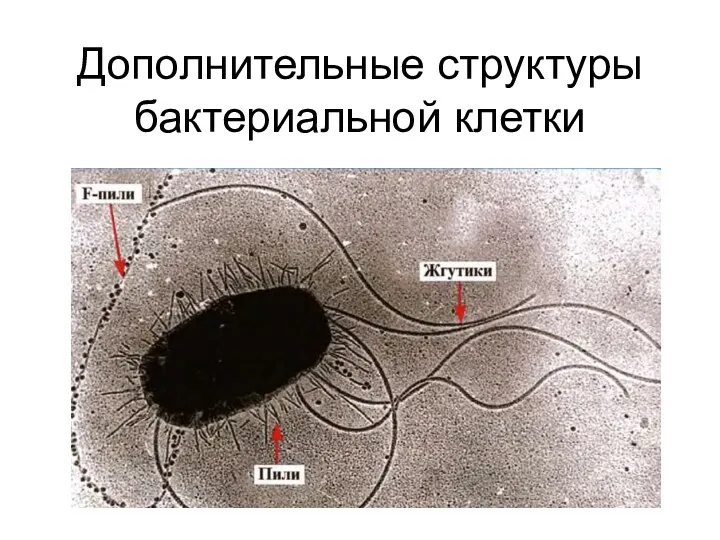 Дополнительные структуры бактериальной клетки
Дополнительные структуры бактериальной клетки Влияние факторов внешней среды на онтогенез
Влияние факторов внешней среды на онтогенез Морфология эпителиальной ткани
Морфология эпителиальной ткани Продолговатый мозг. Черепно-мозговые нервы (IX - XII)
Продолговатый мозг. Черепно-мозговые нервы (IX - XII) Сүт және сүт өнідерінің тағамдық биологиялық құндылығы мен қауіпсіздігі
Сүт және сүт өнідерінің тағамдық биологиялық құндылығы мен қауіпсіздігі Индивидуальное развитие цветковых растений
Индивидуальное развитие цветковых растений Генная инженерия: новые возможности и проблемы
Генная инженерия: новые возможности и проблемы Клонирование
Клонирование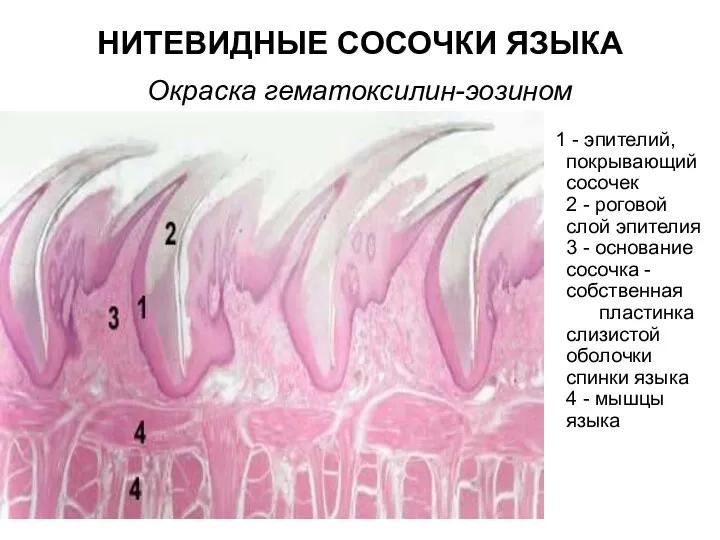 Нитевидные сосочки языка. Окраска гематоксилин-эозином
Нитевидные сосочки языка. Окраска гематоксилин-эозином Птицы Челябинской области
Птицы Челябинской области