Содержание
- 2. План 13.1 Введение . Биологическая роль 13.2 Классификация. Стереоизомерия 13.3 Пентозы. Гексозы 13.4 Цикло-оксо таутомерия 13.5
- 3. 13.1. Введение. Биологическая роль Важной составной частью всех живых организмов являются углеводы. На долю углеводов приходится
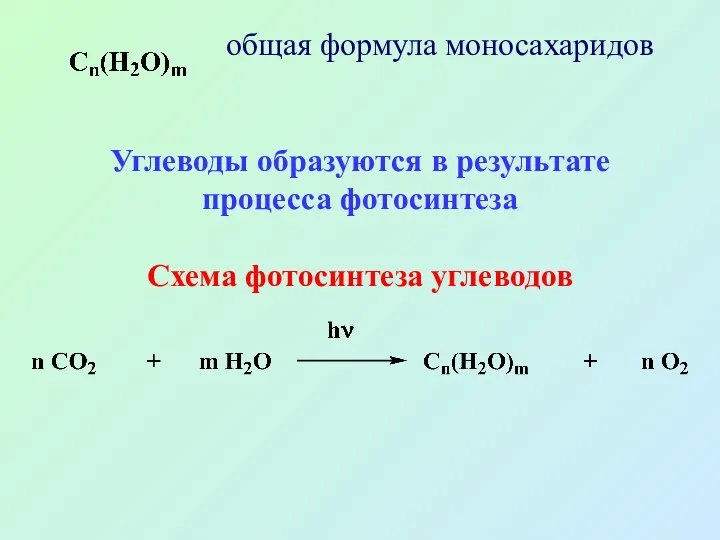
- 4. общая формула моносахаридов Углеводы образуются в результате процесса фотосинтеза Схема фотосинтеза углеводов
- 5. Биологическая роль углеводов Энергетическая функция, 1 г углеводов – 16,9 кДж 2. Углеводы – запасный питательный
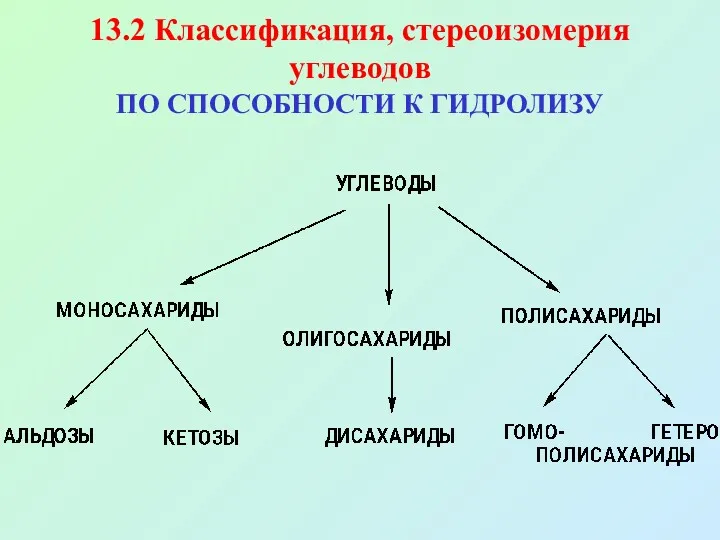
- 6. 13.2 Классификация, стереоизомерия углеводов ПО СПОСОБНОСТИ К ГИДРОЛИЗУ
- 7. Классификация углеводов В зависимости от функциональной группы различают альдозы ( содержат альдегидную группу и кетозы (содержат
- 8. Классификация углеводов ПО ЧИСЛУ АТОМОВ УГЛЕРОДА 3 С триозы 4 С тетрозы 5 С пентозы 6
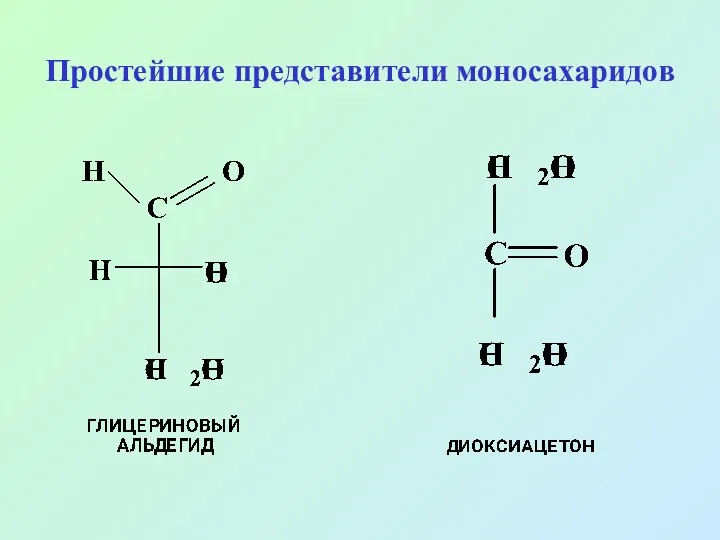
- 9. Простейшие представители моносахаридов
- 10. Стереоизомерия моносахаридов Все моносахариды, за исключением диоксиацетона, содержат хиральные центры, как правило их несколько. У альдогексоз
- 11. Многообразие форм молекул моносахаридов предполагает различные способы их изображения Для изображения ациклических форм моносахаридов приняты проекционные
- 12. Британский химик W.N.Haworth (лауреат Нобелевской премии в 1937) предложил удобный способ изображения циклической формы сахаров
- 13. Пяти- и шестичленные цепи имеют клешневидную конфигурацию и вследствие этого возможно сближение в пространстве двух функциональных
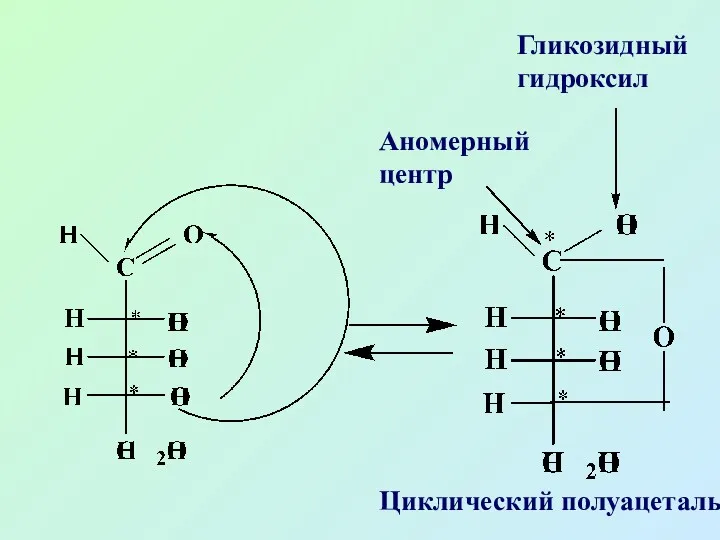
- 14. В циклической форме возникает дополнительный центр хиральности, т.е. асимметрическим становится карбонильный атом углерода. Этот новый хиральный
- 15. Аномерный центр Гликозидный гидроксил Циклический полуацеталь
- 16. У α-аномера конфигурация аномерного центра совпадает с конфигурацией концевого, наиболее удаленного асимметрического атома углерода, а у
- 17. Относительная конфигурация моносахаридов, т.е. принадлежность к D-и L-стереохимическим рядам определяется путем сравнения конфигурации хирального атома углерода,
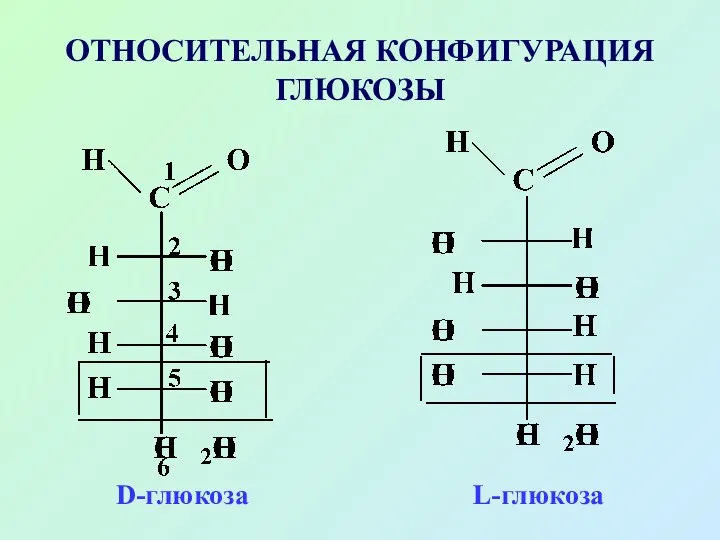
- 18. ОТНОСИТЕЛЬНАЯ КОНФИГУРАЦИЯ ГЛЮКОЗЫ D-глюкоза L-глюкоза
- 19. Знак вращения (+) или (–) определяется экспериментально Подавляющее большинство природных моносахаридов относится к D-ряду, но могут
- 20. Эпимеры – диастереомеры, различающиеся конфигурацией только одного хирального атома
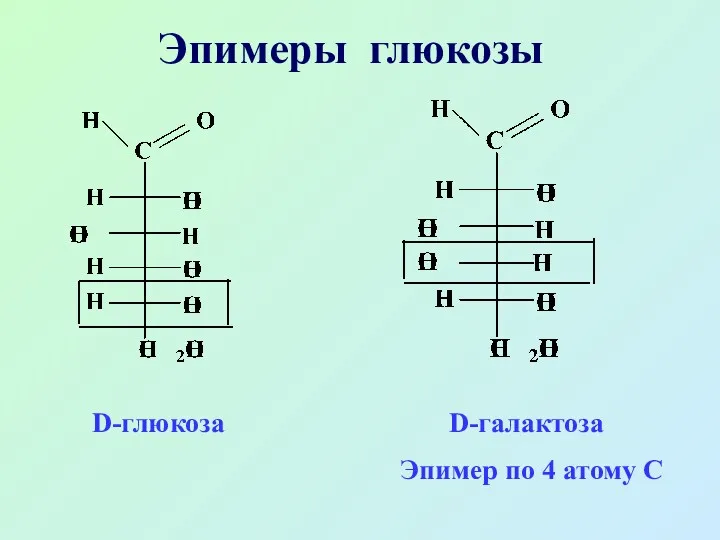
- 21. Эпимеры глюкозы D-глюкоза D-галактоза Эпимер по 4 атому С
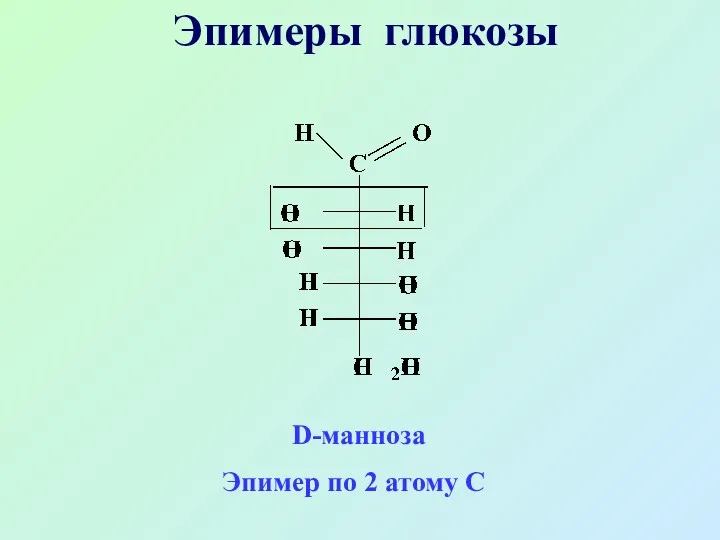
- 22. Эпимеры глюкозы D-манноза Эпимер по 2 атому С
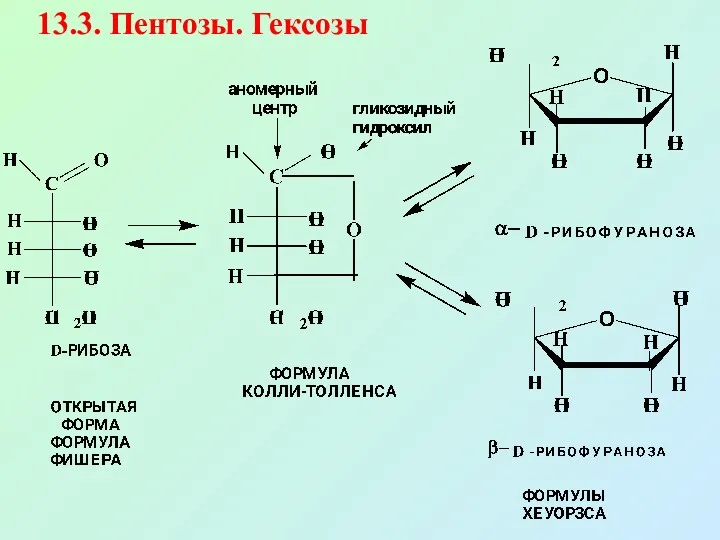
- 23. 13.3. Пентозы. Гексозы
- 24. Рибоза входит в состав нуклеиновых кислот, а в виде восстановленного спирта входит в состав биологически активных
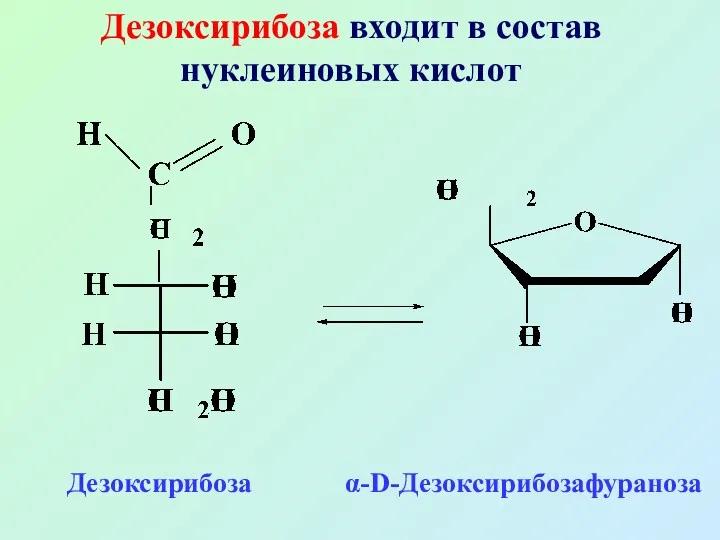
- 25. Дезоксирибоза входит в состав нуклеиновых кислот Дезоксирибоза α-D-Дезоксирибозафураноза
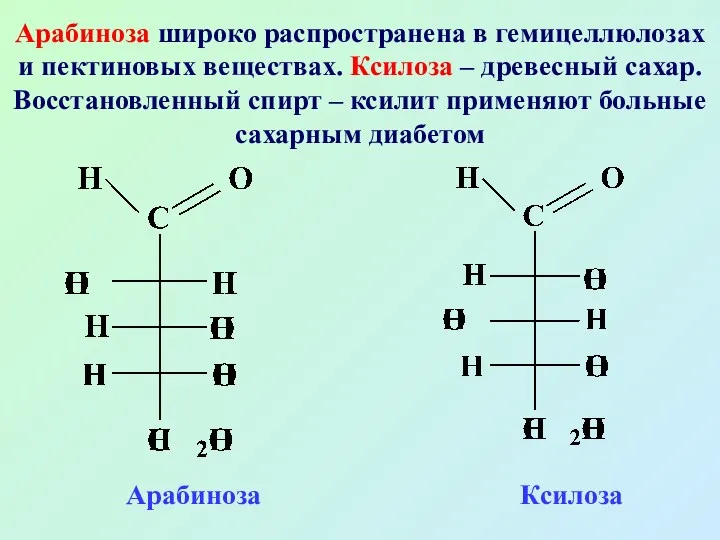
- 26. Арабиноза широко распространена в гемицеллюлозах и пектиновых веществах. Ксилоза – древесный сахар. Восстановленный спирт – ксилит
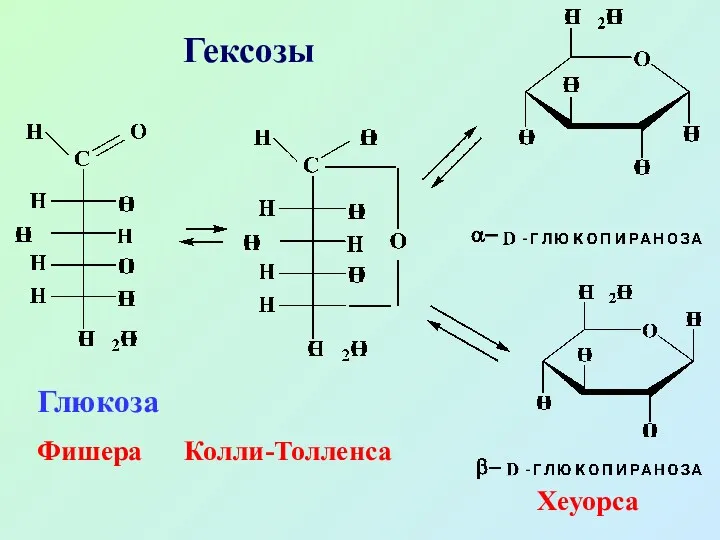
- 27. Гексозы Глюкоза Фишера Колли-Толленса Хеуорса
- 28. Глюкоза (виноградный сахар) содержится во всех фруктах, ягодах, меде В крови человека содержание глюкозы составляет 0,08
- 29. Фруктоза – плодовый сахар, встречается обычно вместе с глюкозой. В свободном виде находится в плодах, нектаре,
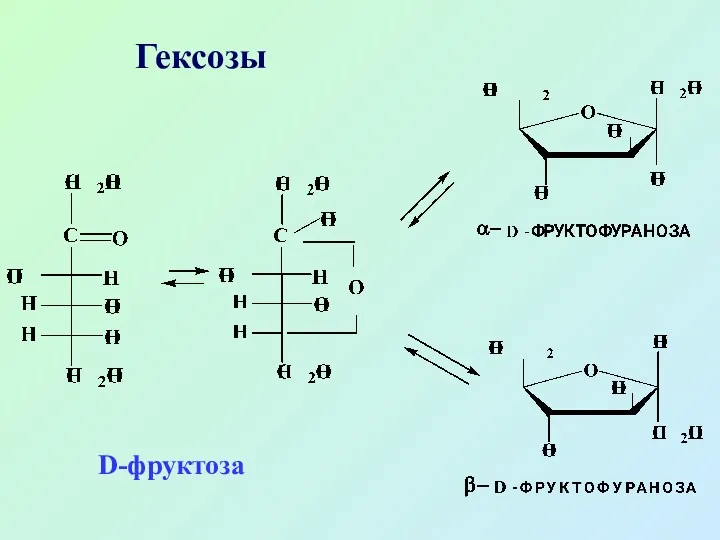
- 30. Гексозы D-фруктоза
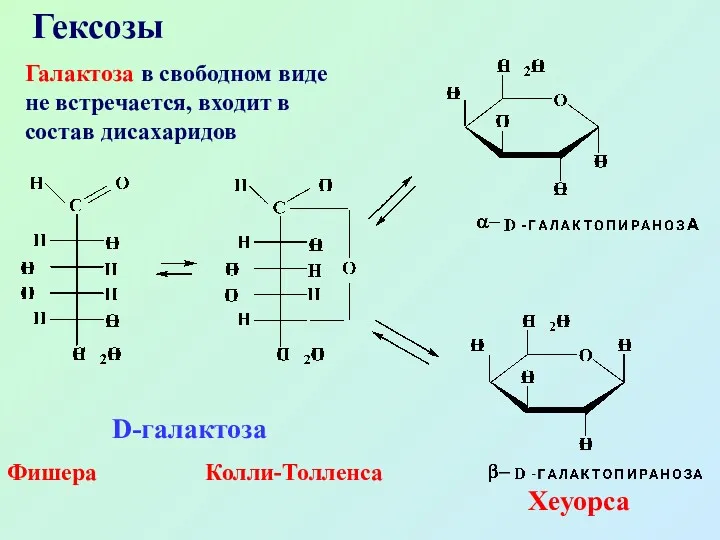
- 31. Гексозы Галактоза в свободном виде не встречается, входит в состав дисахаридов D-галактоза Фишера Колли-Толленса Хеуорса
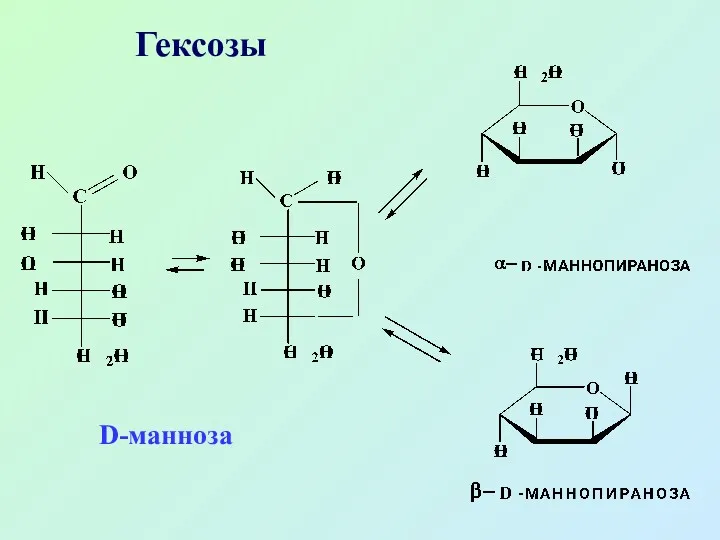
- 32. Гексозы D-манноза
- 33. Манноза образует сложные природные углеводы – маннаны, входит в состав гликопротеидов. Встречается в растениях, в составе
- 34. 13.4. Цикло-оксо таутомерия В кристаллическом состоянии все моносахариды находятся в циклической форме в виде α- или
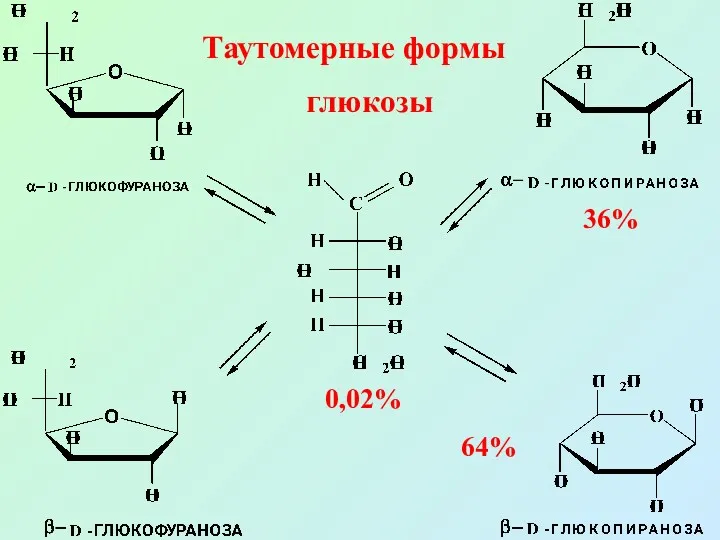
- 35. Таутомерные формы глюкозы 64% 36% 0,02%
- 36. Процесс растворения моносахаридов в воде сопровождается своеобразным оптическим эффектом, который получил название мутаротация – изменение удельного
- 37. Явление мутаротации связано с таутомерными превращениями глюкозы В смеси таутомеров глюкозы преобладают пиранозные формы, однако, хотя
- 38. Для пиранозной формы наиболее предпочтительна конформация кресла. Конформационное строение D-глюкопиранозы проливает свет на уникальность β-D-глюкопиранозы: единственный
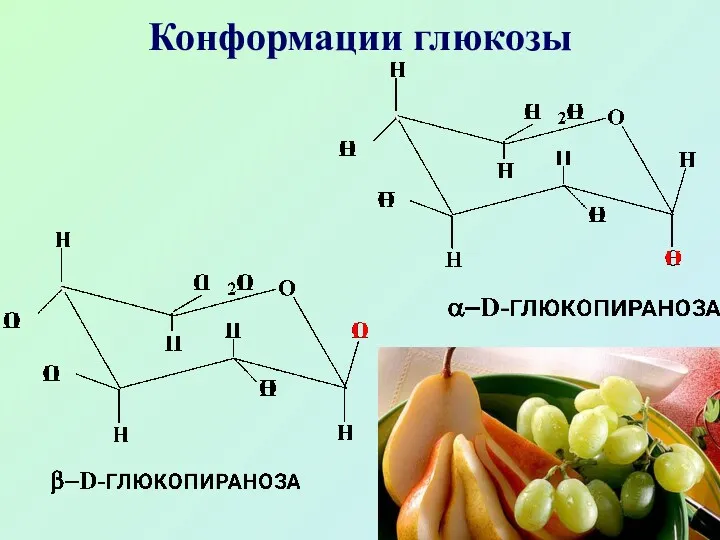
- 39. Конформации глюкозы
- 40. Благодаря строению (экваториальное расположение всех заместителей) β-глюкоза термодинамически устойчива, именно это и является причиной распространенности β-глюкозы
- 41. 13.5. Химические свойства моносахаридов
- 42. Для моносахаридов характерны как реакции, свойственные спиртам, так и альдегидам I.Реакции, обусловленные спирто-выми группами
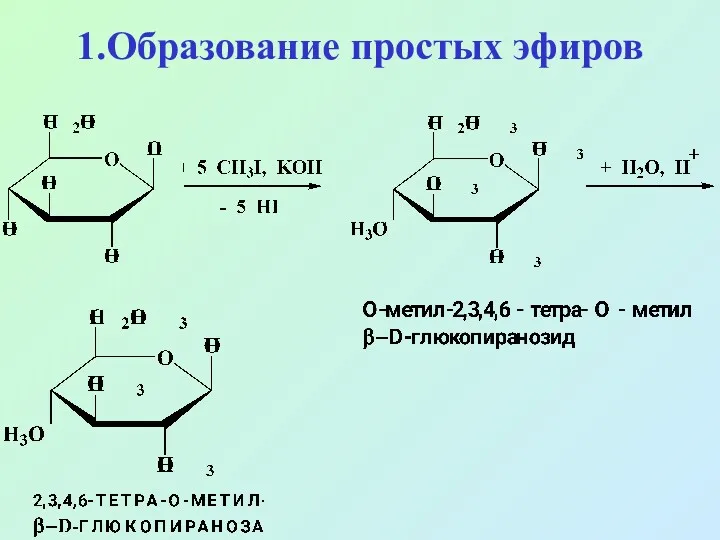
- 43. 1.Образование простых эфиров
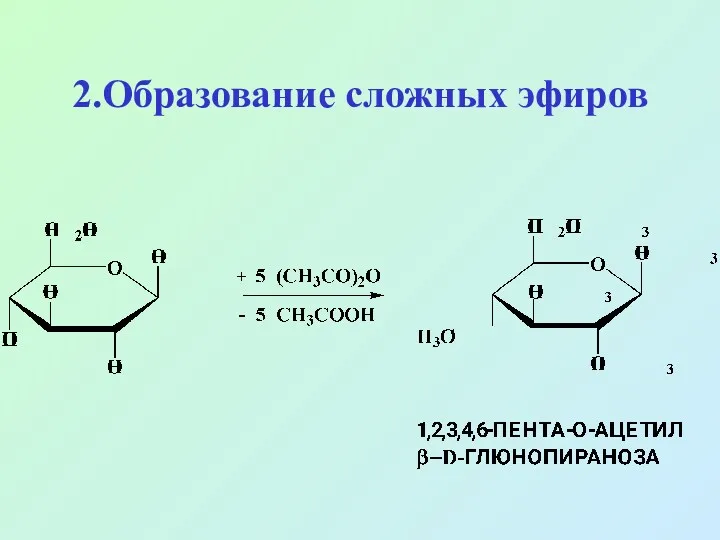
- 44. 2.Образование сложных эфиров
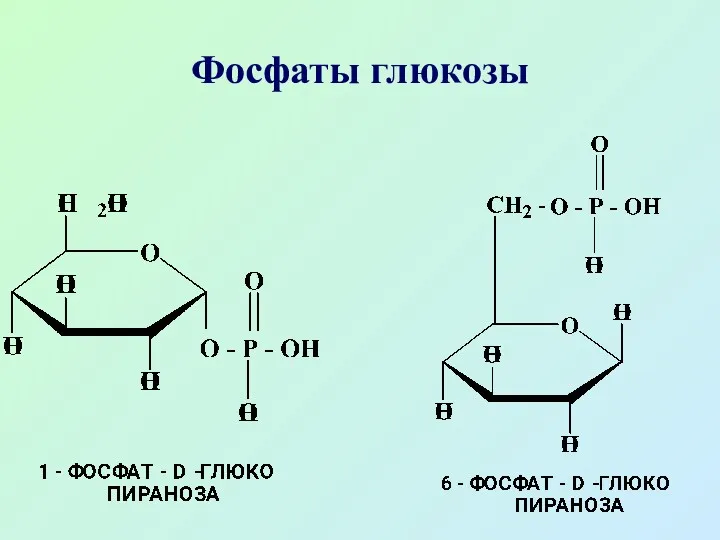
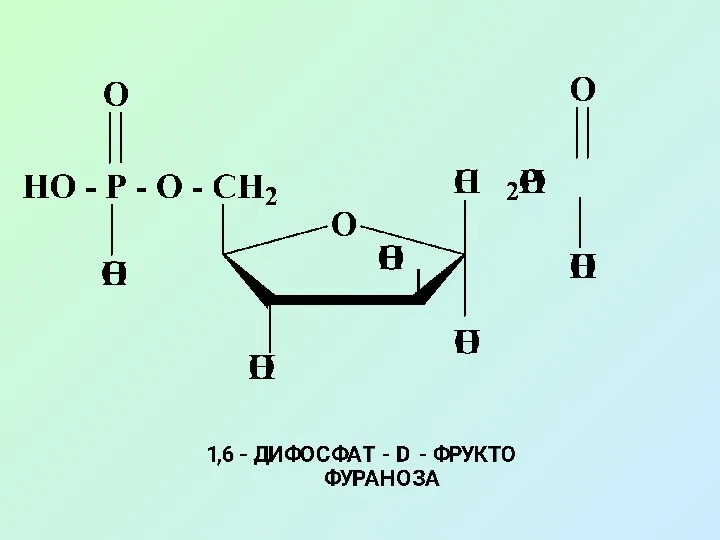
- 45. Из сложноэфирных производных наибольшее значение имеют эфиры фосфорной кислоты (фосфаты), они содержатся во всех растительных и
- 46. Фосфаты глюкозы
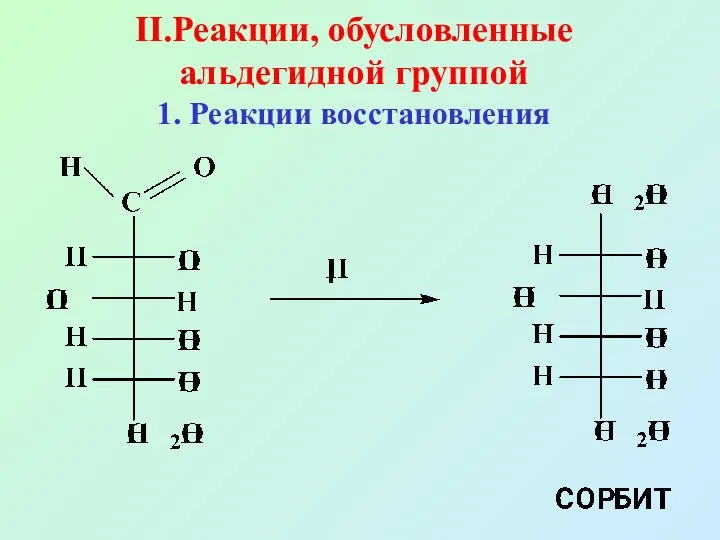
- 48. II.Реакции, обусловленные альдегидной группой 1. Реакции восстановления
- 49. При восстановлении ксилозы образуется ксилит, галактозы – дульцит, маннозы – маннит, рибозы – рибит
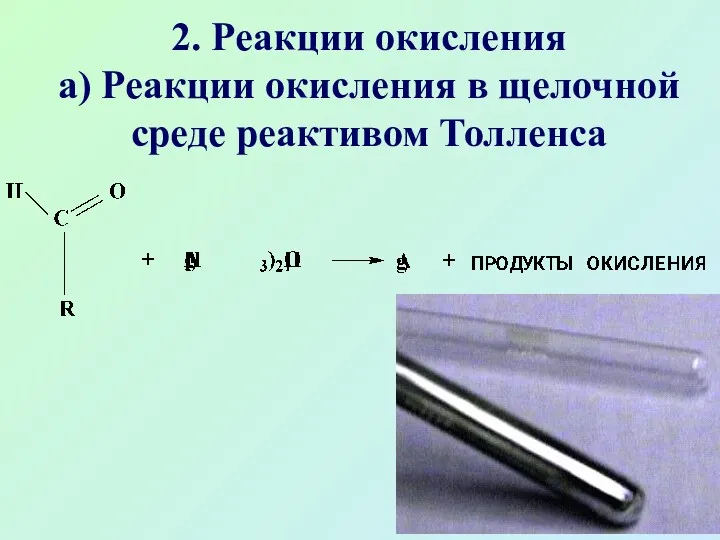
- 50. 2. Реакции окисления а) Реакции окисления в щелочной среде реактивом Толленса
- 51. б) Реакции окисления в щелочной среде реактивом Фелинга (реактивом Бенедикта)
- 52. Углеводы, дающие положительные реакции окисления в щелочной среде, называются восстанавливающими
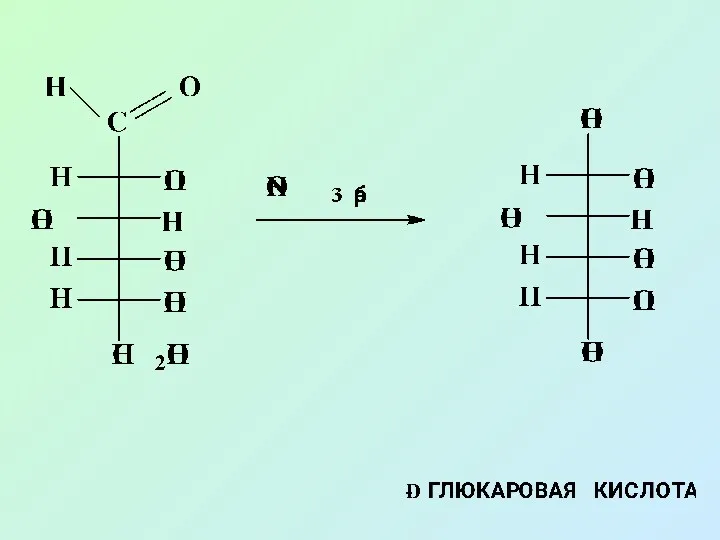
- 53. В) ОКИСЛЕНИЕ В КИСЛОЙ И НЕЙТРАЛЬНОЙ СРЕДЕ Окисление в нейтральной и кислой среде протекает без разрушения
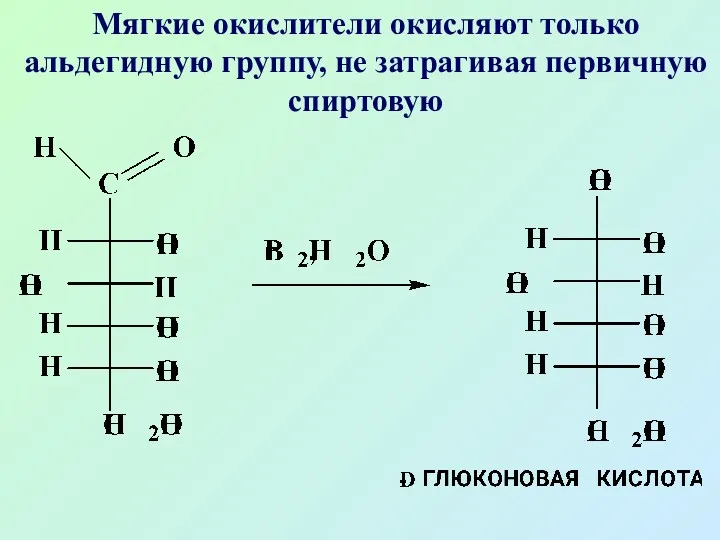
- 55. Мягкие окислители окисляют только альдегидную группу, не затрагивая первичную спиртовую
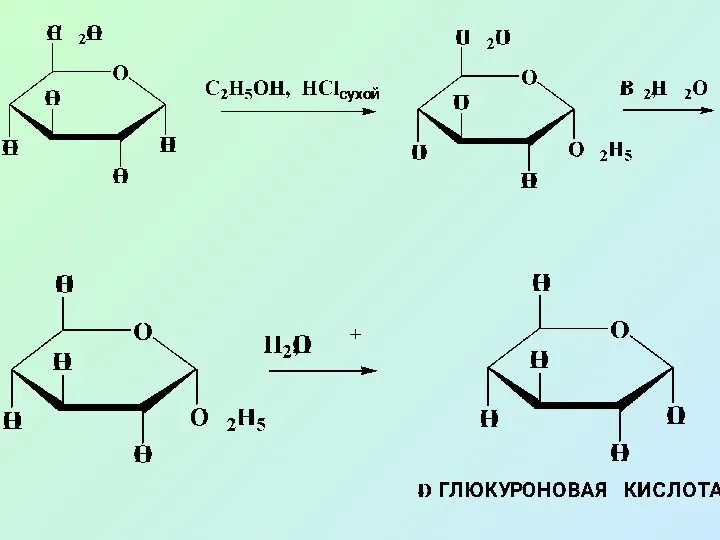
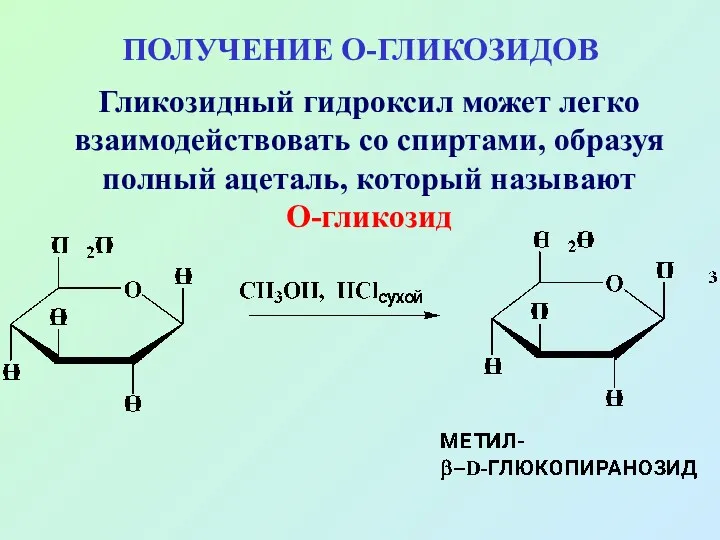
- 57. ПОЛУЧЕНИЕ О-ГЛИКОЗИДОВ Гликозидный гидроксил может легко взаимодействовать со спиртами, образуя полный ацеталь, который называют О-гликозид
- 58. О-гликозиды легко гидролизуются в кислой среде с образованием соответствующих моносахаридов, но устойчивы к гидролизу в щелочной
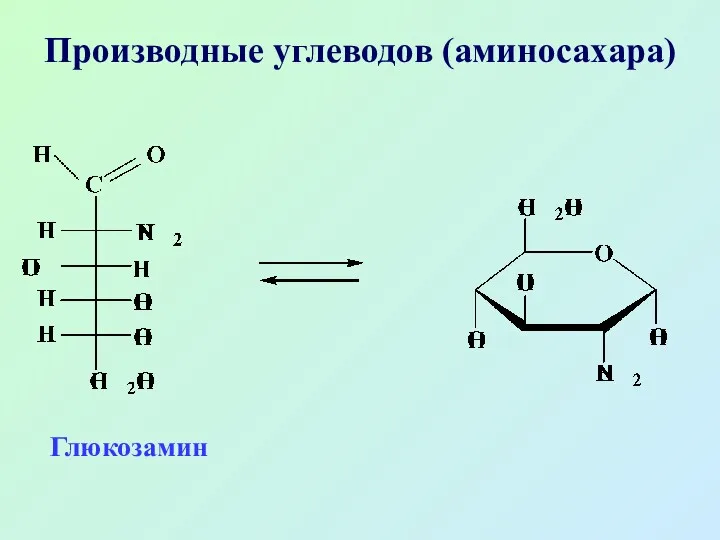
- 59. Аминопроизводные углеводов, аминосахара, входят в состав мукополисахаридов в организме человека и животных. Важнейшие из них глюкозамин,
- 60. Производные углеводов (аминосахара) Глюкозамин
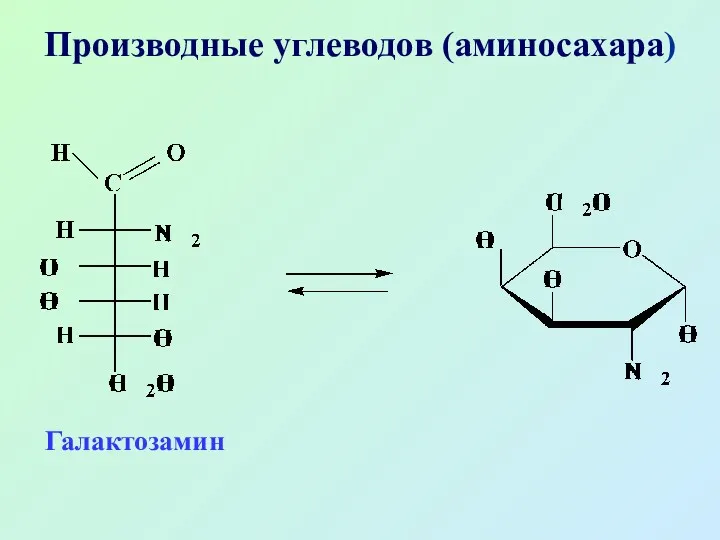
- 61. Производные углеводов (аминосахара) Галактозамин
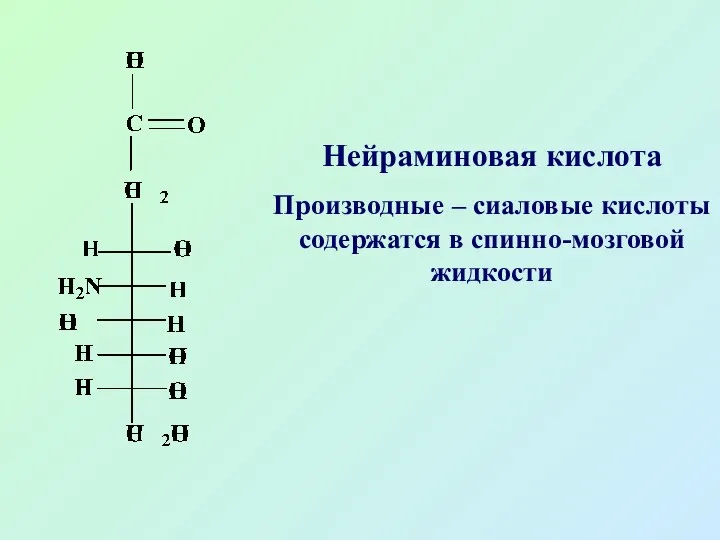
- 62. Нейраминовая кислота Производные – сиаловые кислоты содержатся в спинно-мозговой жидкости
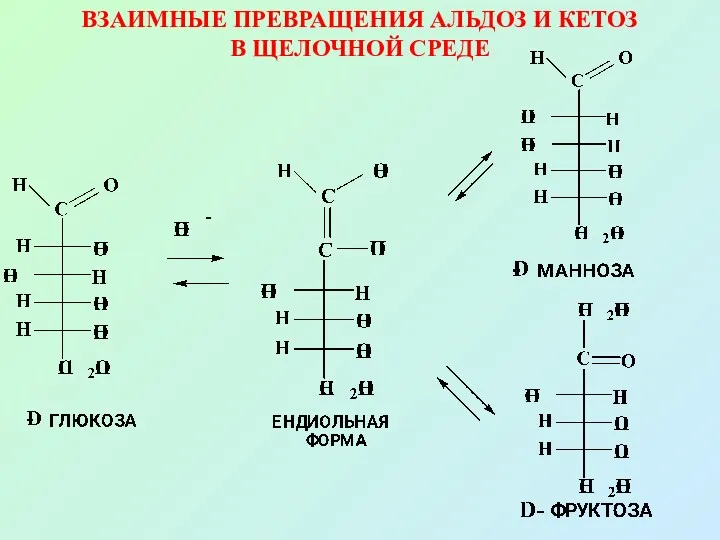
- 63. Взаимные превращения альдоз и кетоз в щелочной среде Вследствие наличия СН-кислотного центра у α-углеродного атома в
- 64. ВЗАИМНЫЕ ПРЕВРАЩЕНИЯ АЛЬДОЗ И КЕТОЗ В ЩЕЛОЧНОЙ СРЕДЕ
- 66. Скачать презентацию

































 Редкие виды растений в искусственных лесных насаждениях рядом с садоводческим товариществом Виктория
Редкие виды растений в искусственных лесных насаждениях рядом с садоводческим товариществом Виктория Методы изучения биологического круговорота веществ в фитоценозах
Методы изучения биологического круговорота веществ в фитоценозах Сахарозаменители. Натуральные сахарозаменители
Сахарозаменители. Натуральные сахарозаменители Қызынаққа зиян келтіретін бунақденелердің таралуы, биологиясы, зияндылығы және қолданатын күресу шаралар жүйесі
Қызынаққа зиян келтіретін бунақденелердің таралуы, биологиясы, зияндылығы және қолданатын күресу шаралар жүйесі Органы выделения у человека
Органы выделения у человека Животные. Простейшие
Животные. Простейшие Состав популяций
Состав популяций Итоговая контрольная работа. 6 класс
Итоговая контрольная работа. 6 класс Биотехнологическое производство сыра
Биотехнологическое производство сыра Слуховая сенсорная система
Слуховая сенсорная система Органы растений. Рост, развитие и размножение растений. Цветок
Органы растений. Рост, развитие и размножение растений. Цветок Адамның рефлекторлық реакциясын зерттеу
Адамның рефлекторлық реакциясын зерттеу Анатомия стебля растения
Анатомия стебля растения Животные холодных и жарких стран
Животные холодных и жарких стран Земледелие. Введение
Земледелие. Введение Хижі птахи
Хижі птахи Органеллы. Строение клеток эукариот
Органеллы. Строение клеток эукариот Презентация: Роль бактерий в природе и жизни человека.
Презентация: Роль бактерий в природе и жизни человека. Тест Полезные ископаемые (для 6 класса коррекционной школы 8 вида)
Тест Полезные ископаемые (для 6 класса коррекционной школы 8 вида) Движение крови по сосудам
Движение крови по сосудам Влажность воздуха
Влажность воздуха Бауырдың биохимиясы
Бауырдың биохимиясы Репликация ДНК
Репликация ДНК Митоздың биологиялық маңызы
Митоздың биологиялық маңызы Парнокопытные и непарнокопытные животные
Парнокопытные и непарнокопытные животные Гербициттер микология
Гербициттер микология Предмет и задачи цитологии
Предмет и задачи цитологии Тест. Поджелудочна железа
Тест. Поджелудочна железа