Взаимоотношение между структурой и функцией в клетках прокариотических и эукариотических микроорганизмов презентация
Содержание
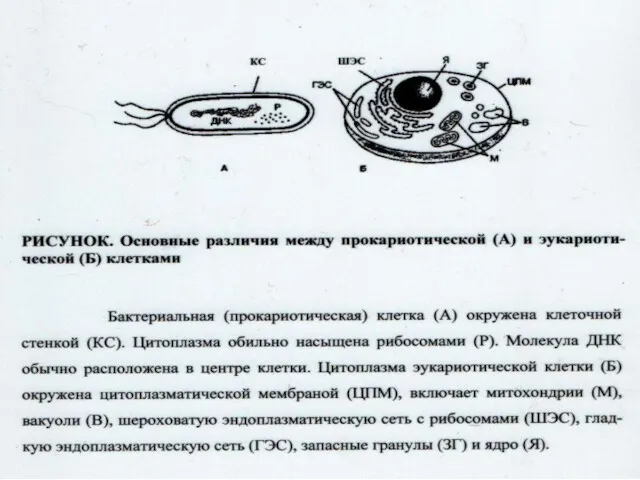
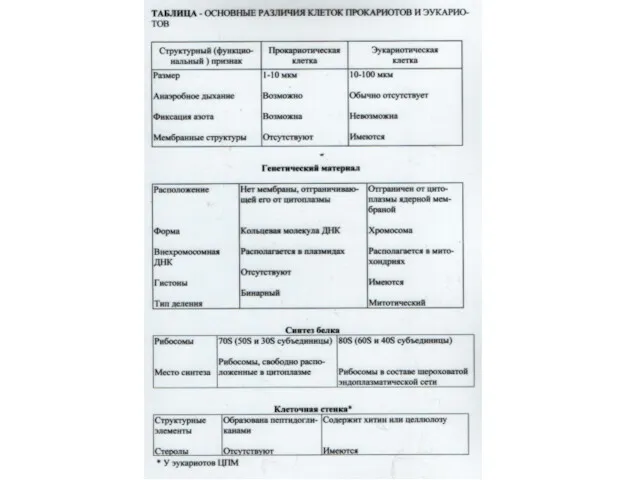
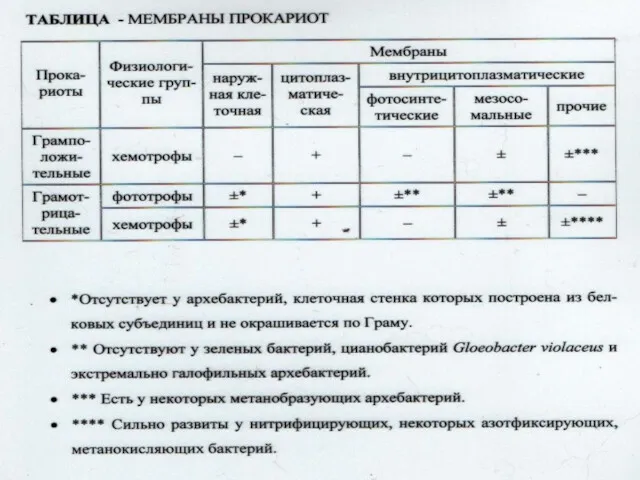
- 2. Вопросы: Общие представления о различиях в структурно-функциональной организации эукариотических и прокариотических микроорганизмов. Структурная организация и функционирование
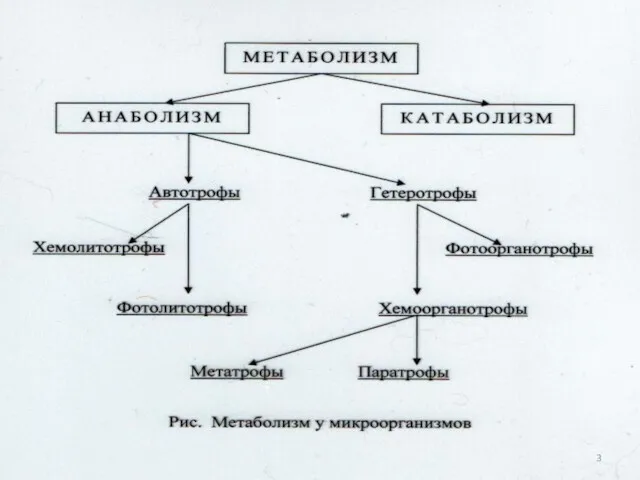
- 10. Лекция 1 Тема: «Общие представления об обмене веществ у микроорганизмов. Понятия анаболизма, катаболизма и метаболизма. Термодинамические
- 11. Вопросы: Общие представления об обмене веществ у микроорганизмов. Понятия анаболизма, катаболизма и метаболизма. Механизм метаболизма у
- 12. 3
- 13. 4
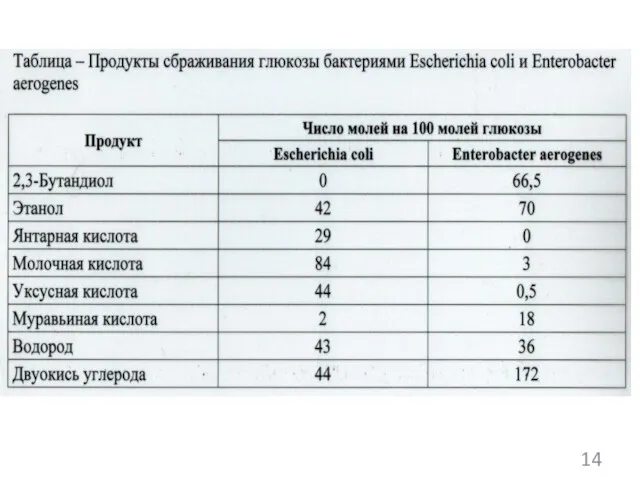
- 14. Расщепление глюкозы в аэробных условиях: С6H12O6+6O2 6CO2+6H2O ( G=-2872 кДЖ/моль) 5
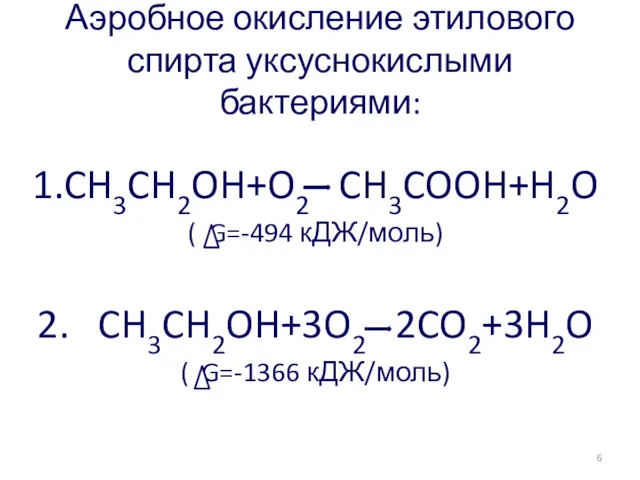
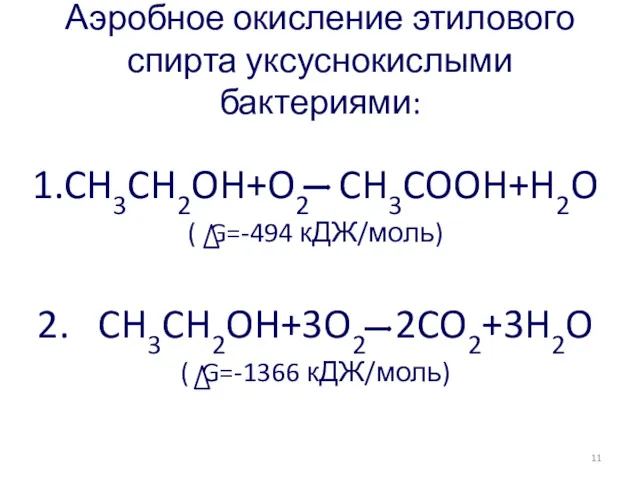
- 15. Аэробное окисление этилового спирта уксуснокислыми бактериями: 1.CH3CH2OH+O2 CH3COOH+H2O ( G=-494 кДЖ/моль) 2. CH3CH2OH+3O2 2CO2+3H2O ( G=-1366
- 16. Нитратное дыхание – восстановление нитратов до молекулярного азота: 5C6H12O6+24KNO3 24KHCO3+18H2O+12N2+6CO2 ( G=-1760 кДЖ/моль) Сульфатное дыхание –восстановление
- 17. Сбраживание глюкозы: C6H12O6 2C2H5OH+2CO2 ( G=-166 кДЖ/моль) 8
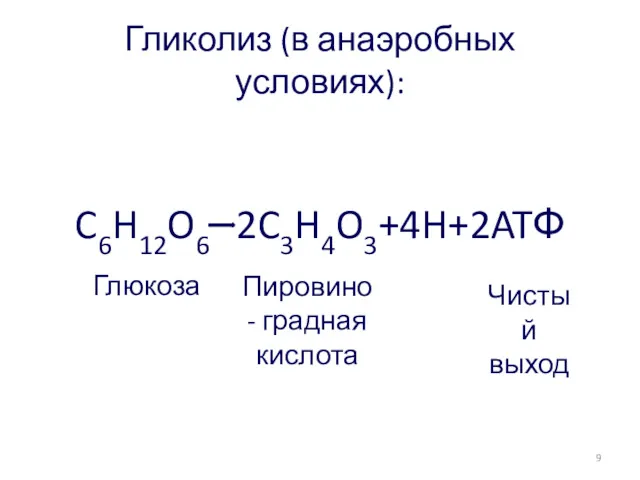
- 18. Гликолиз (в анаэробных условиях): C6H12O6 2C3H4O3+4H+2ATФ Глюкоза Пировино- градная кислота Чистый выход 9
- 19. Фотосинтез- процесс, при котором происходит превращение световой энергии в химическую. Фотосинтетический аппарат представлен тремя компонентами: антенна;
- 20. Свойства ферментов: специфичность действия термолабильность ферменты действуют при определенной pH Ферменты не изменяются к концу реакции,
- 21. Классификация ферментов: оксидоредуктазы; трансферазы; гидролазы; лиазы; изомеразы; лигазы (синтетазы). 12
- 22. Лекция 2 Тема: «Конструктивный метаболизм микробной клетки. Общие принципы биосинтеза макромолекул у микроорганизмов. Синтез аминокислот, нуклеотидов,
- 23. Вопросы: Общие принципы биосинтеза макромолекул у микроорганизмов; Синтез структурных компонентов микробной клетки; 2
- 24. 3
- 25. 4
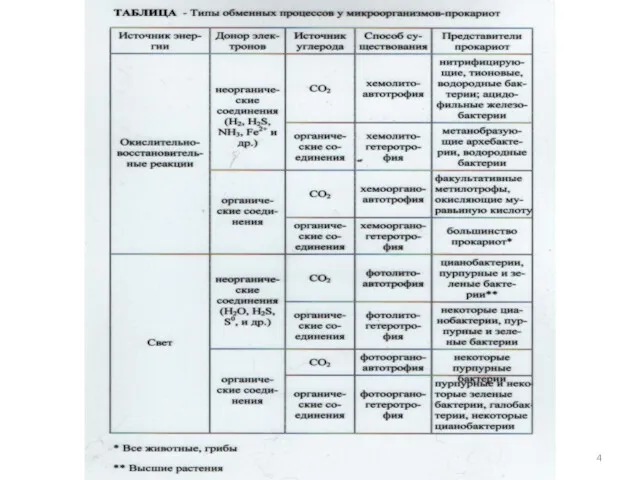
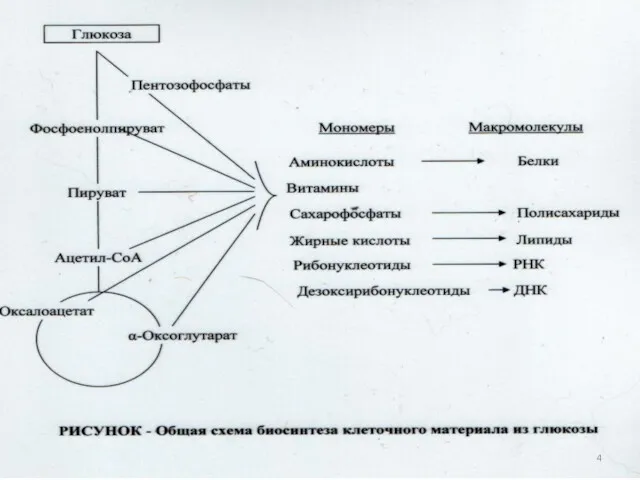
- 26. Группы прокариотов по способу использования углерода для конструктивного метаболизма: Автотрофы-микроорганизмы, способные синтезировать все компоненты клетки из
- 27. 6
- 28. 7
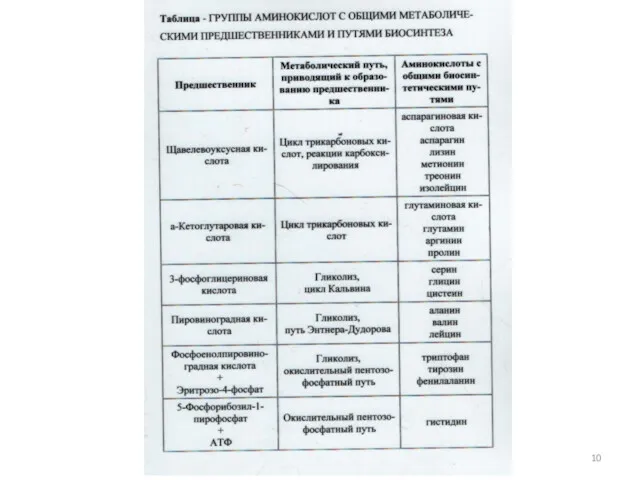
- 29. Синтез аминокислот посредством реакции переаминирования: Глутаминовая кислота + щавелевоуксусная кислота аспарагиновая кислота + α-кетоглутаровая кислота 8
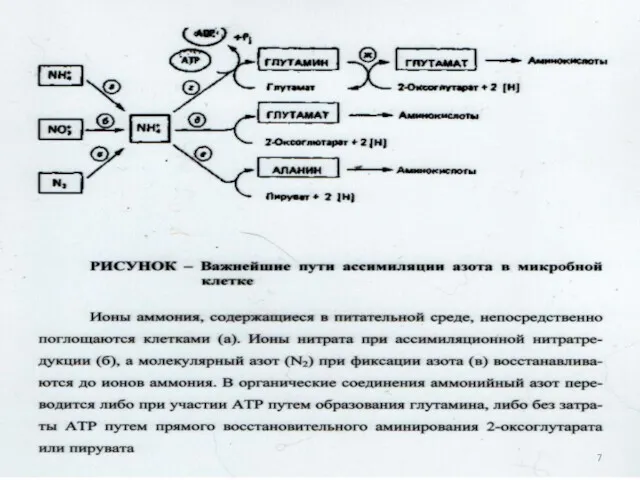
- 30. Включение азота аммиака в состав органических соединений: NH3 CO O NH3+CO2+2АТФ + 2АДФ+ФН PO3H2 карбамоилфосфат 9
- 31. 10
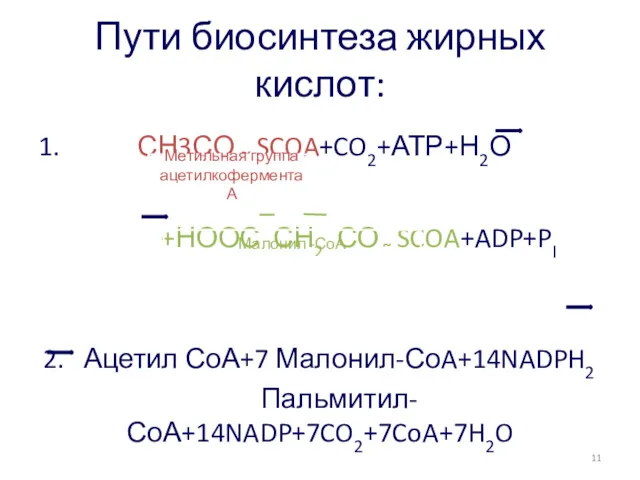
- 32. Пути биосинтеза жирных кислот: 1. СН3СО ῀ SCOA+CO2+АТР+Н2О +НООС СН2 СО ῀ SCOA+ADP+PI 2. Ацетил СоА+7
- 33. 12
- 34. Лекция 3 Тема: «Энергетический метаболизм микробной клетки. Пути метаболизма, приводящие к образованию макроэргов. Роль АТФ, пиридиновых
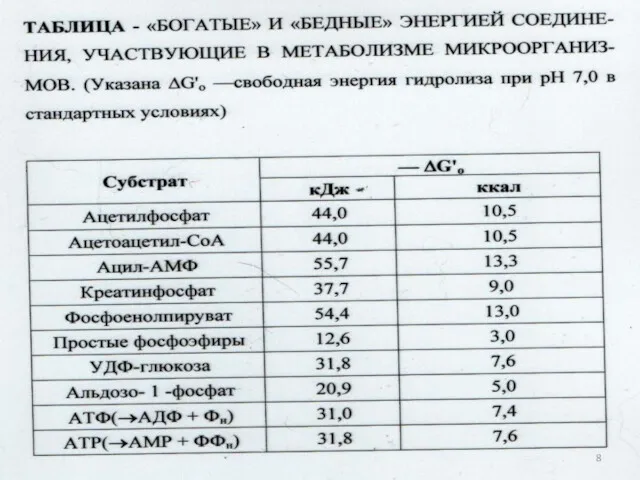
- 35. Вопросы: Пути метаболизма, приводящие к образованию макроэргов. Характеристика высокоэнергетических соединений. Роль высокоэнергетических соединений в клеточном метаболизме.
- 36. Общий вид процессов- источников энергии для прокариот А В+е- Например, (1) Fe2+ Fe3++e- (2) -CH2-CH2- -CH=CH-
- 37. Три способа получения энергии у прокариот: Дыхание Брожение Фотосинтез 4
- 38. 5
- 39. Три типа фотосинтеза у прокариот: Зависимый от бактерохлорофилла безкислородный фотосинтез (зеленые, пурпурные, гелеобактерии); Зависимый от хлорофилла
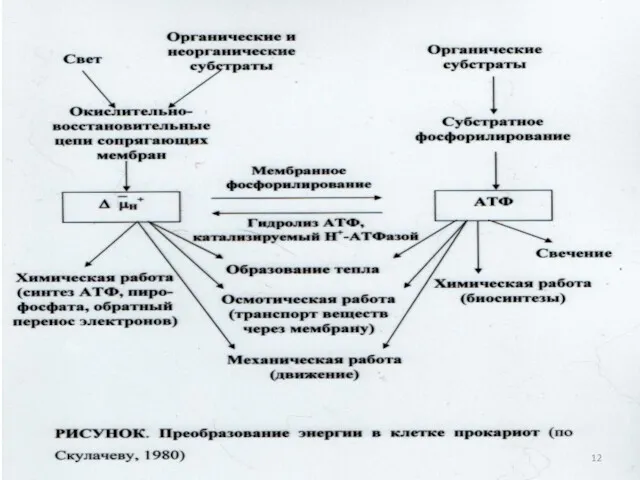
- 40. Две универсальные формы энергии у прокариотов: Энергия высокоэнергетических химических соединений (химическая); Энергия трансмембранного потенциала ионов водорода
- 41. 8
- 42. Выделение свободной энергии при гидролизе малекулы АТФ: АТФ+Н2 АДФ+ФН G0’=-31,8кДЖ/моль 2. АДФ+Н2 АМФ+ФН G0’=-31,8кДЖ/моль 3. АМФ+Н2
- 43. 10
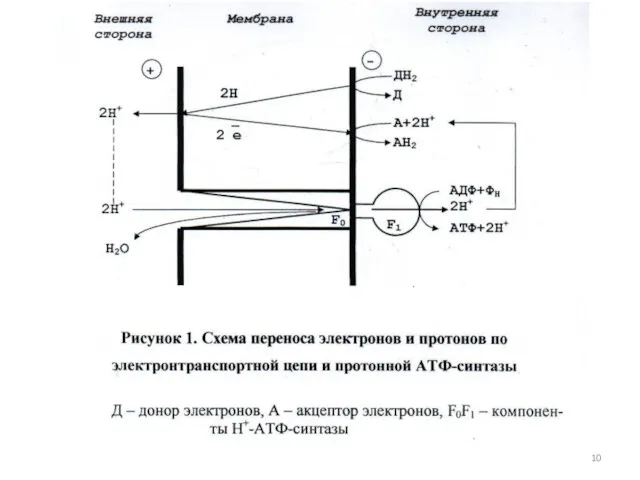
- 44. Уравнение реакции синтеза и гидролиза АТФ в клеточной мембране в присутствии Н+-АТФ синтазы АДФ+ ФН+nHHAP+ АТФ+H2O+nHвнутр+
- 45. 12
- 46. 13
- 47. Обратимые реакции окисления-восстановления НАД и НАДФ НАД++2Н НАД Н+Н+ НАДФ++2Н НАДФ Н+Н+ 14
- 48. 15
- 49. Лекция 4 Тема: «Дыхание. Аэробный и анаэробный типы дыхания у микроорганизмов. Внутриклеточная локализация, строение и физиологическая
- 50. Вопросы: Определение и природа дыхания, его типы Механизм дыхательного процесса. Внутриклеточная локализация, строение и физиологическая функция
- 51. Ферментативное поглощение молекулярного кислорода – дыхание – подразделяется на: Не связанное с запасанием энергии для клетки
- 52. 4
- 53. Дыхание бактерий представляет собой метаболический процесс ферментативного окисления различных органических соединений и некоторых минеральных веществ, идущий
- 54. Деление микроорганизмов по типу дыхания: Аэробы Анаэробы Факультативные анаэробы 6
- 55. 7
- 56. 8
- 57. Расщепление глюкозы в аэробных условиях: С6H12O6+6O2 6CO2+6H2O ( G=-2872 кДЖ/моль) 9
- 58. Дыхательная цепь –это система дыхательных ферментов, которые находятся в мембранах микробных клеток 10
- 59. Аэробное окисление этилового спирта уксуснокислыми бактериями: 1.CH3CH2OH+O2 CH3COOH+H2O ( G=-494 кДЖ/моль) 2. CH3CH2OH+3O2 2CO2+3H2O ( G=-1366
- 60. 12
- 61. 13
- 62. Нитратное дыхание – восстановление нитратов до молекулярного азота: 5C6H12O6+24KNO3 24KHCO3+18H2O+12N2+6CO2 ( G=-1760 кДЖ/моль) Сульфатное дыхание –восстановление
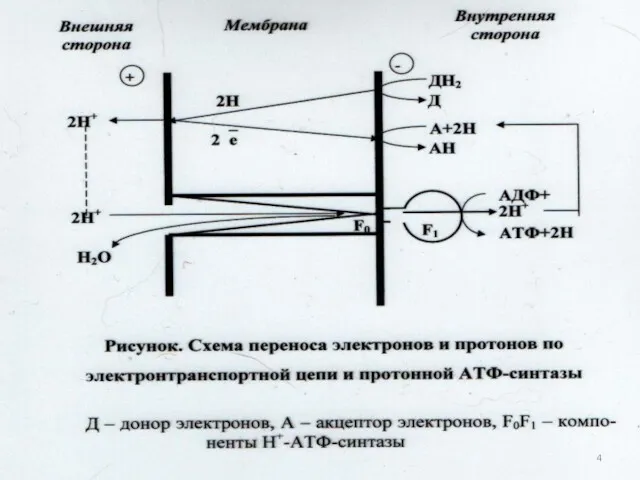
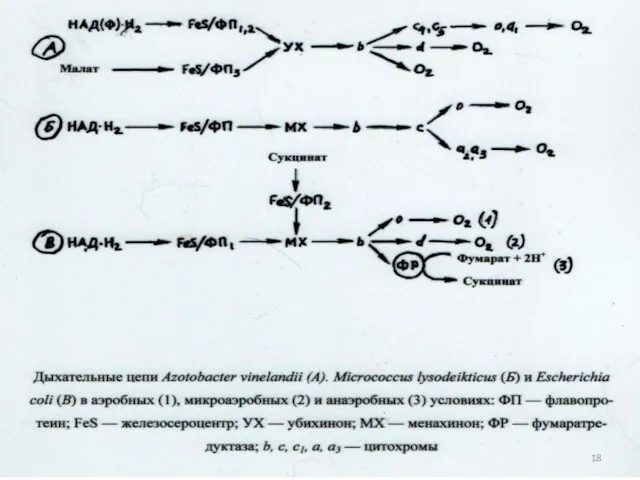
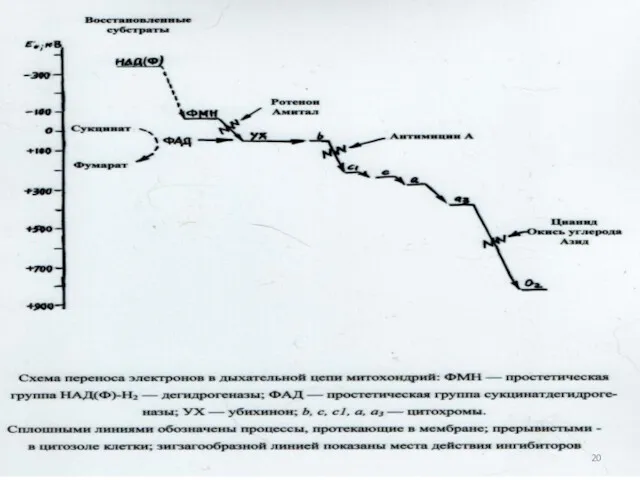
- 63. Три составляющих механизма дыхания микроорганизмов Клеточная локализация и компонентный состав переносчиков электронов и протонов в дыхательной
- 64. 16
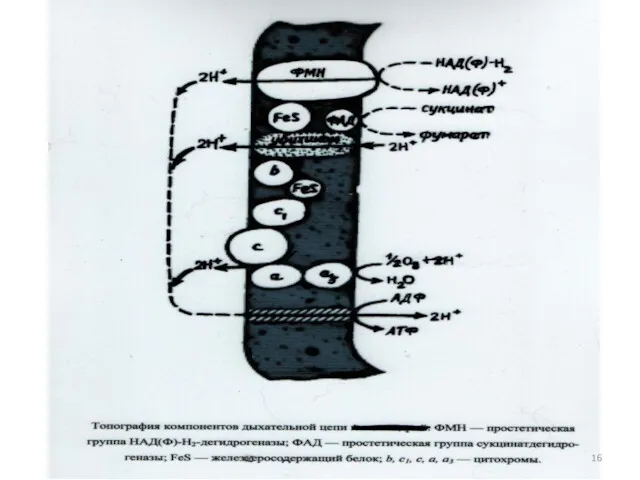
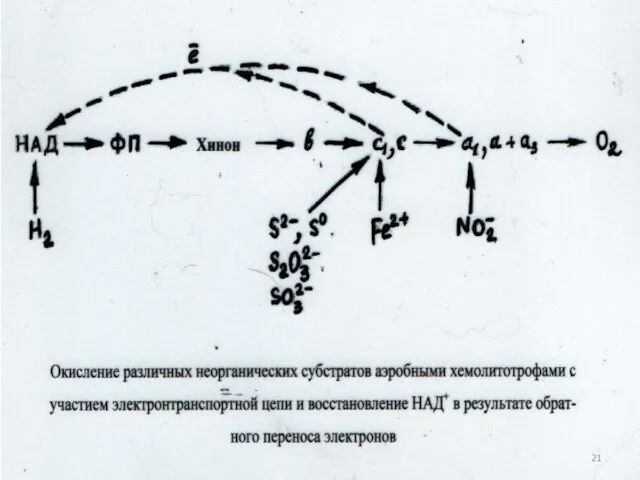
- 65. Компоненты электротранспортной цепи, участвующие в окислении водорода Флавопротеины- ферменты, содержащие в качестве простетических групп флавинмононуклеотид (ФМН)
- 66. 18
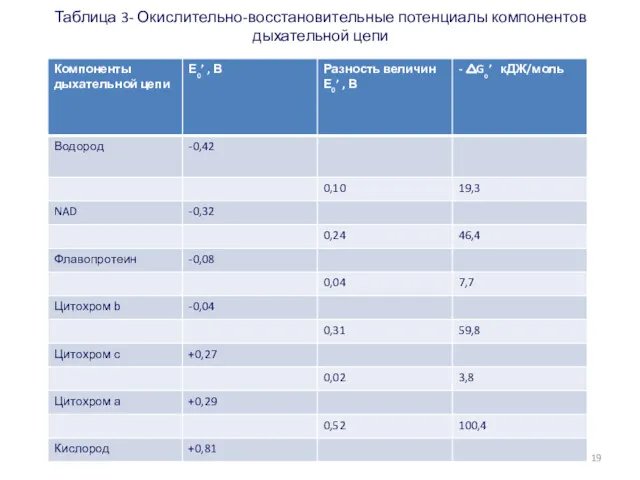
- 67. Таблица 3- Окислительно-восстановительные потенциалы компонентов дыхательной цепи 19
- 68. 20
- 69. 21
- 70. Лекция 4 Тема : «Брожение. Типы брожения у микроорганизмов. Сбраживаемые и несбраживаемые соединения. Спиртовое, молочнокислое, пропионовокислое
- 71. Вопросы: Определение и природа бражения Сбраживаемые и несбраживаемые соединения, их роль в природном балансе Типы бражения
- 72. Брожение- это процессы, посредством которых организмы получают химическую энергию из глюкозы и других субстратов в отсутствие
- 73. Сбраживание глюкозы дрожжевым соком (уравнение Гардена- Йонга): 2C6H12O6+2Pi 2CO2+2C2H5OH+2H2O+фруктозо-1, 6-бифосфат 4
- 74. Две фазы процесса брожения: Начальная(общая) фаза- проходит в анаэробных условиях, при этом сахар расщепляется до пировиноградной
- 75. Типы катаболических реакций субстратного фосфорилирования, приводящие к синтезу АТФ при брожении: Окислительно-восстановительные реакции в процессе брожения
- 76. Схема ферментативного синтеза ацилфосфатов (предшественников АТФ) из ангидридов фосфорной кислоты: ацил-КоА+Фн ацилфосфат+КоА-SH 7
- 77. Типы реакций, приводящих к синтезу АТФ при брожении: 1. 1,3-фосфоглицерат+АДФ 3-фосфоглицерат+АТФ (катализатор- фосфоглицераткиназа) 2. фосфоенолпируват+АДФ пируват+АТФ
- 78. Химическое вещество может быть подвергнуто сбраживанию, если оно содержит неполностью окисленные(или восстановленные) углеродные атомы. Процесс брожения
- 79. Соединения, сбраживаемые микроорганизмами: полисахариды, гексозы, пентозы, тетрозы, многоатомные спирты, органические кислоты, аминокислоты(за исключением ароматический), пурины и
- 80. Причины невозможности сбраживания некоторых органических соединений: Соединения содержат только атомы углерода и водорода; при расщеплении таких
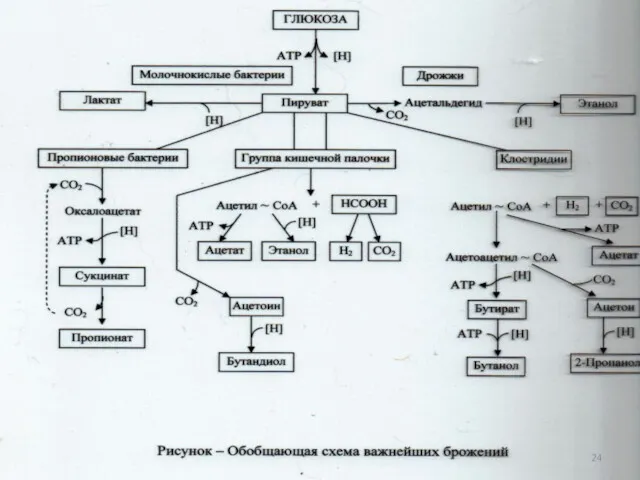
- 81. Типы брожения: Молочнокислое Спиртовое Маслянокислое Муравьинокислое Пропионовокислое Уксуснокислое и др. 12
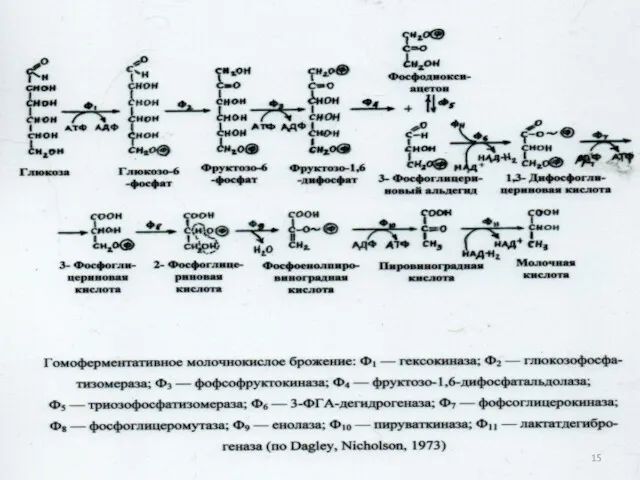
- 82. Последовательность биохимических реакций, лежащих в основе гомоферментативного молочнокислого брожения получила название гликолитического пути( гликолиза), фруктозодифосфатного пути.
- 83. Схема фосфоролитического отщепления глюкозного остатка при гликолизе полисахаридов (глюкоза)n+HPO42- (глюкоза)n-1+глюкозо-1-фосфат 14
- 84. 15
- 85. Окисление 3- фосфоглицеральдегида до 1,3- дифосфоглицериновой кислоты- важный этап гликолитического пути: 3-ФГА+НАД++Фн 1,3-ФГК+НАД-Н2 16
- 86. Схема процесса гомоферментативного молочнокислого брожения: Глюкоза+2Фн+2АДФ 2 молочная кислота+2АТФ+2Н2О 17
- 87. Для гетероферментативного молочнокислого брожения характерно отсутствие ключевого фермента гликолитического пути- фруктозодифосфатальдолазы, а также триозофосфатизомиразы 18
- 88. 19
- 89. 20
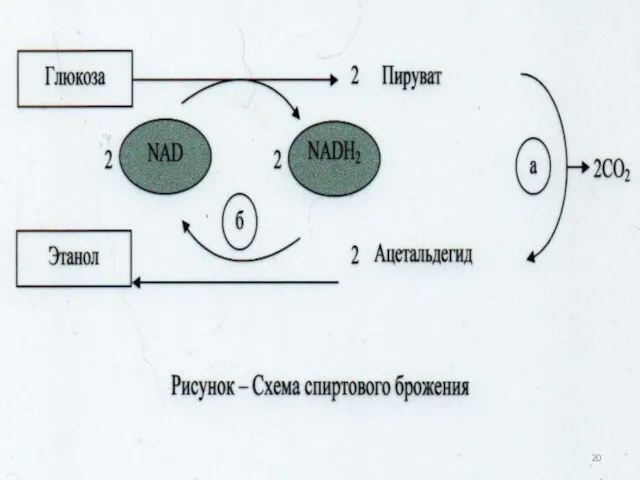
- 90. Уравнение процесса спиртового брожения: С6Н12О6+2Фн+2АДФ 2СН3-СН2ОН+2СО2+2АТФ+2Н2О 21
- 91. 22
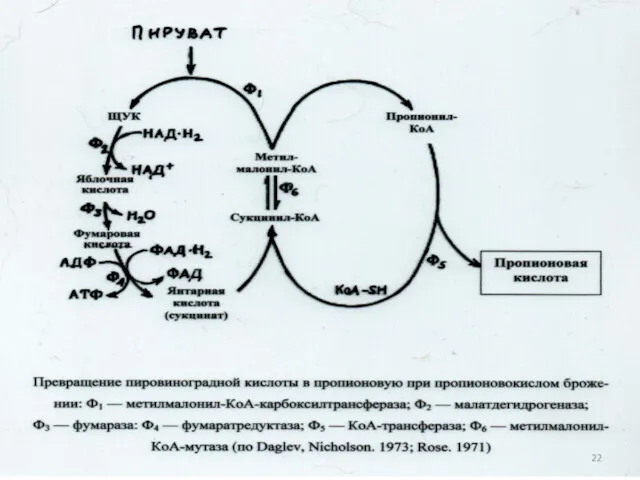
- 92. Реакция превращения сукцинил-КоА в метилмалонил-КоА, катализируемая мутазой, является ключевой в пропионовокислом брожении, так как в ней
- 93. 24
- 94. Лекция 5 Тема: «Фотосинтез. Спектральный состав солнечного света. Фотосинтезирующий аппарат микроорганизмов, различия между кислородным и бескислородным
- 95. Вопросы: Спектральный состав солнечного света Фотосинтез и фотосинтезирующие микроорганизмы Особенности конструктивного метаболизма у фотосинтезирующих бактерий( биосинтетические
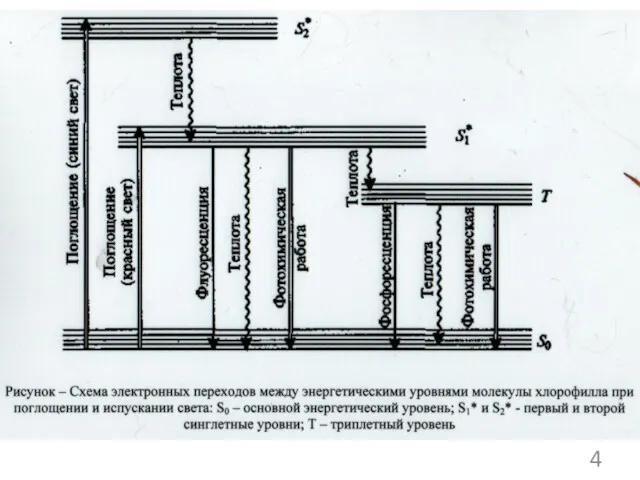
- 96. Фотон- это дискретная доза энергии, обратно пропорциональная длине волны электромагнитного излучения. Ультрафиолетовый, видимый и ближний инфракрасный
- 97. 4
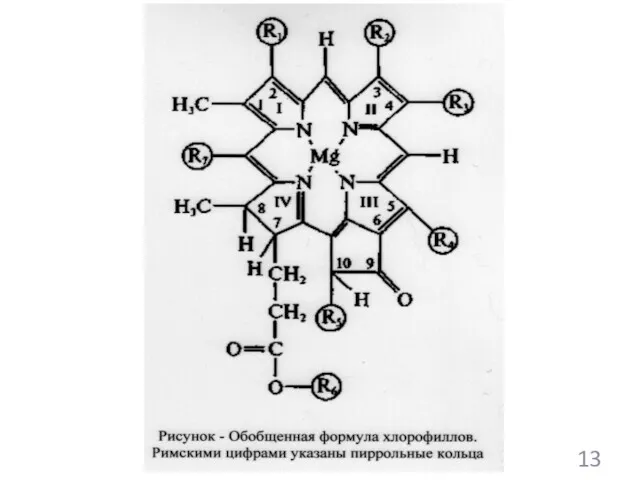
- 98. Фотосинтез- процесс, при котором происходит превращение световой энергии в химическую. Специальные пигменты микроорганизмов и растений с
- 99. Фотофосфорилирование- это процесс образования АТФ при переносе энергии света поглощённого фотосинтетической пигментной системой. 6
- 100. Кислородный (оксигенный) фотосинтез- это процесс превращения световой энергии в химическую при использовании в качестве единственного источника
- 101. Бескислородный (аноксигенный) фотосинтез-это процесс превращения световой энергии в химическую, при котором фотосинтезирующие микроорганизмы (пурпурные и зеленые
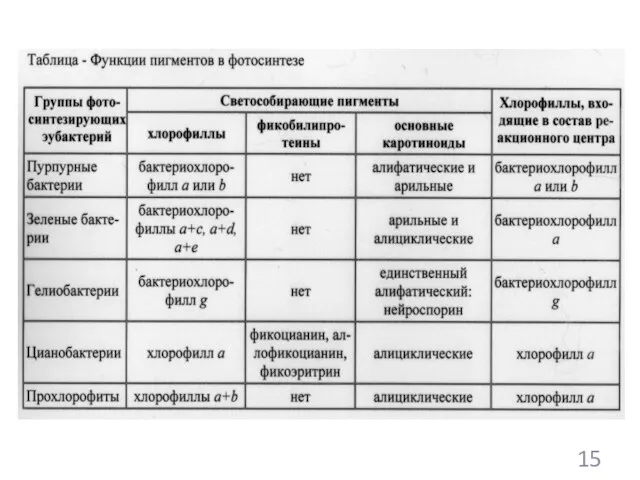
- 102. Три основные группы фотосинтезирующих грамотрицательных микроорганизмов: Цианобактерии Пурпурные бактерии Зеленые бактерии 9
- 103. 10
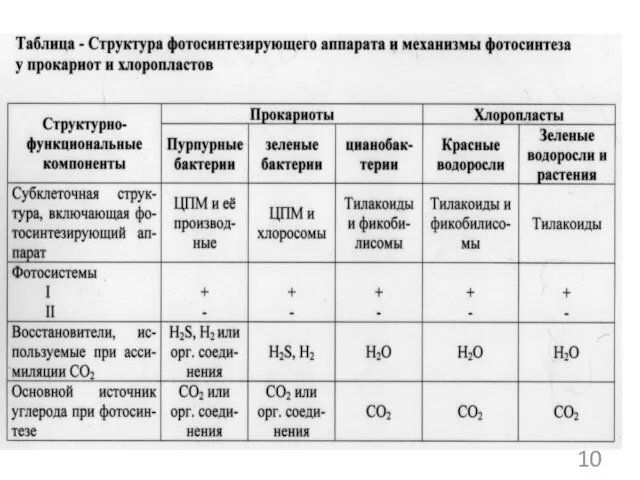
- 104. Фотосинтезирующий аппарат- это мембраносвязанная система пигментов, переносчиков электронов, липидов и белков, обеспечивающая превращение энергии при фотосинтезе.
- 105. Два класса химических соединений фотосинтетических пигментов: Пигменты, в основе которых лежит тетрапиррольная структура (хлорофилы, фикобилипротеины) Пигменты,
- 106. 13
- 107. Каратиноиды представляют собой продукт конденсации остатков изопрена: СН=С-СН=СН- Фикобилипротеины представляют собой водорастворимые хромопротеиды, содержащие линейные тетраперролы
- 108. 15
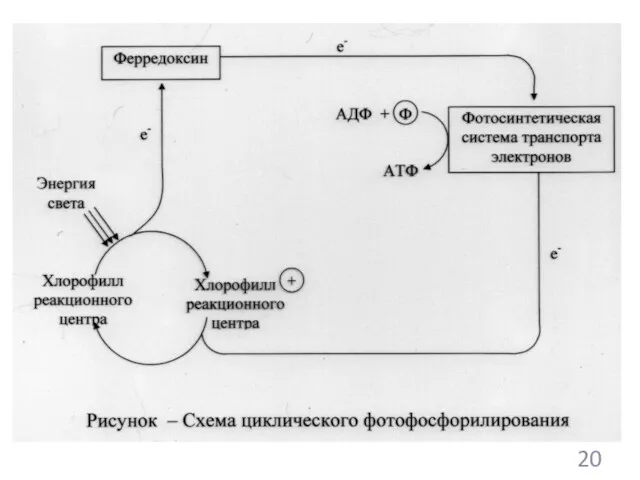
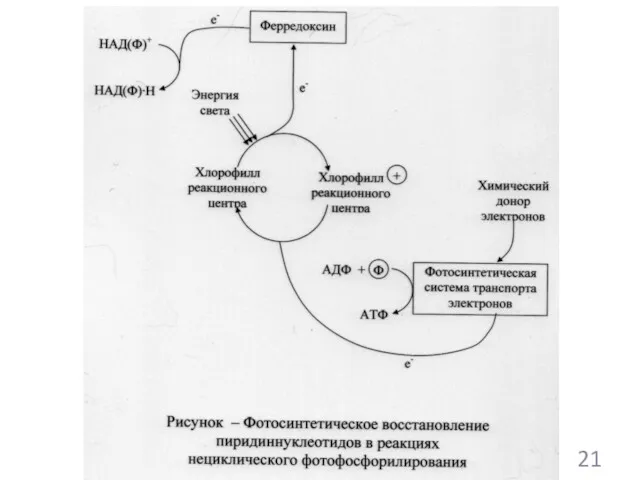
- 109. Процесс фотохимического превращения энергии: 1. Хлорофилл+энергия света хлорофилл++е- 2. Ферредоксин+е- восстановленный ферредоксин 16
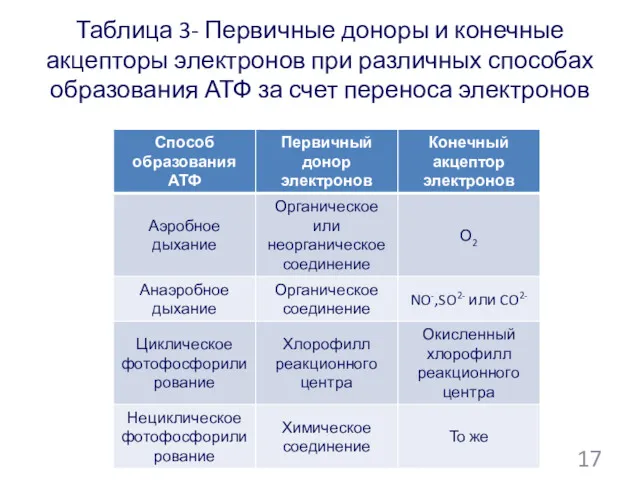
- 110. Таблица 3- Первичные доноры и конечные акцепторы электронов при различных способах образования АТФ за счет переноса
- 111. Общие свойства цепей переноса электронов в реакционных центрах: Компоненты цепи- это переносчики, способные легко вступать в
- 112. Типы процессов образования АТФ у фотосинтезирующих микроорганизмов: Циклическое фотофосфорилирование Нециклическое фотофосфорилирование Сопряженное фотофосфорилирование (комбинация циклического и
- 113. 20
- 114. 21
- 115. 22
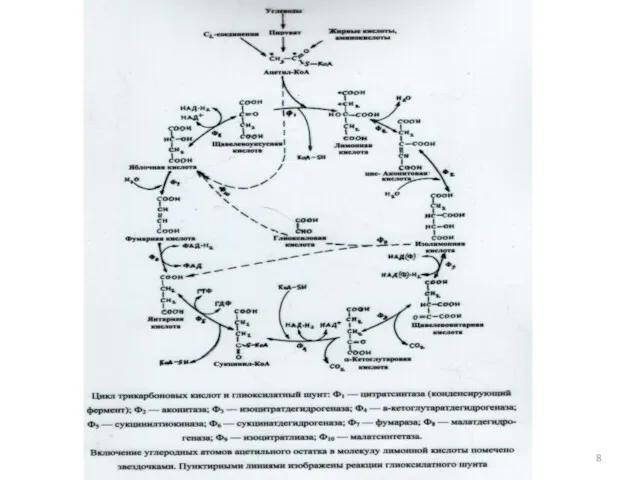
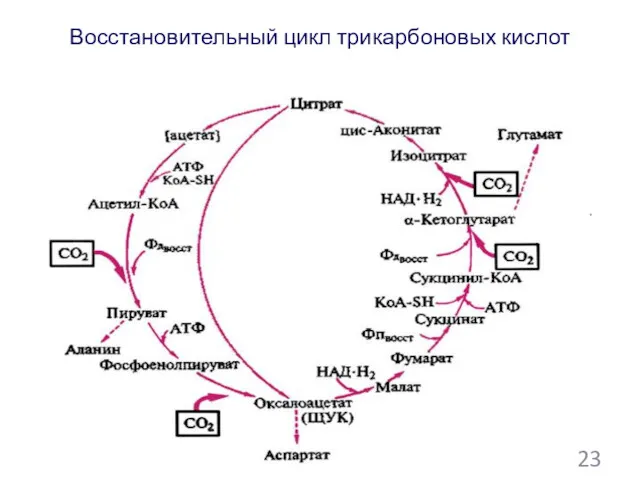
- 116. Восстановительный цикл трикарбоновых кислот 23
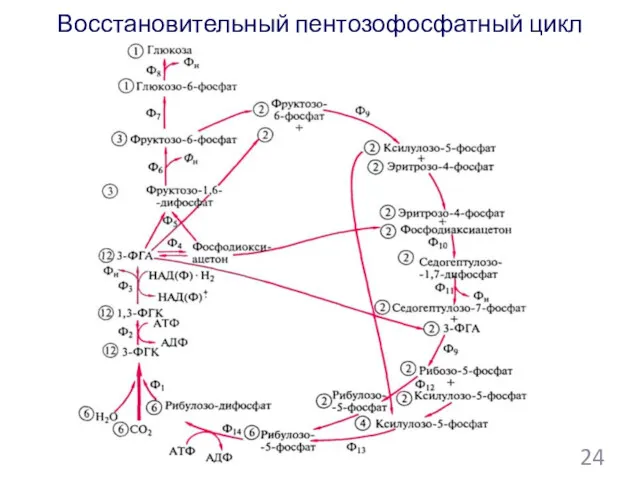
- 117. Восстановительный пентозофосфатный цикл 24
- 118. Лекция 6 Тема: «Методы исследования обмена веществ у микроорганизмов. Изучение ферментных систем, участвующих в превращении и
- 119. Вопросы: Стратегия обмена веществ у микроорганизмов. Методы исследования обмена веществ у микроорганизмов. Изучение ферментных систем, участвующих
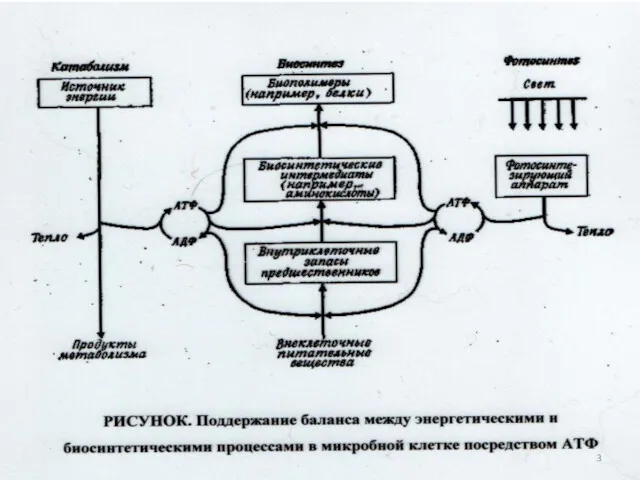
- 120. Две стратегические функции метаболических путей в микроорганизмах: Наработка и трансформация энергии в форме АТФ, электрохимического градиента
- 121. 4
- 122. Пути метаболизма – это последовательность скоординированных реакций, имеющих биосинтетическое или биоэнергетическое значение, например, цепь переносчиков электронов,
- 123. Основные методы исследования обмена веществ у микроорганизмов 1. Идентификация промежуточных продуктов Основным методом исследования обмена веществ
- 124. Основные методы исследования обмена веществ у микроорганизмов 2. Использование ингибиторов метаболизма При добавлении в растущую культуру
- 125. Основные методы исследования обмена веществ у микроорганизмов 3. Использование аналогов субстратов Ферменты определенного пути метаболизма могут
- 126. Основные методы исследования обмена веществ у микроорганизмов 4. Метод последовательной индукции. При сравнении продуктов метаболизма клеток,
- 127. Основные методы исследования обмена веществ у микроорганизмов 5. Одновременная адаптация. При выращивании бактерий на субстрате «А»
- 128. Основные методы исследования обмена веществ у микроорганизмов 6. Использование клеточных экстрактов. Все выше перечисленные методики осуществляются
- 129. 12
- 130. 13
- 131. 14
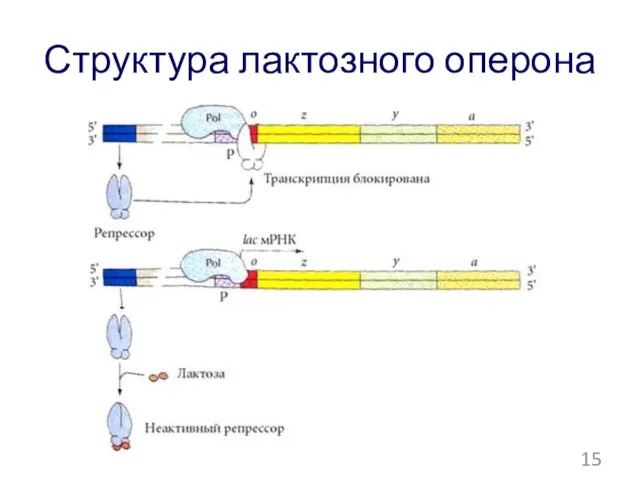
- 132. Структура лактозного оперона 15
- 133. Типы мутантов микроорганизмов с дефектами регуляции процесса биосинтеза ферментов Мутанты, не образующие функционально полноценного репрессорного белка
- 134. Некоторые методы получения мутантов с дефектами регуляции процесса биосинтеза ферментов 1. Мутанты, конститутивно образующие катаболические ферменты.
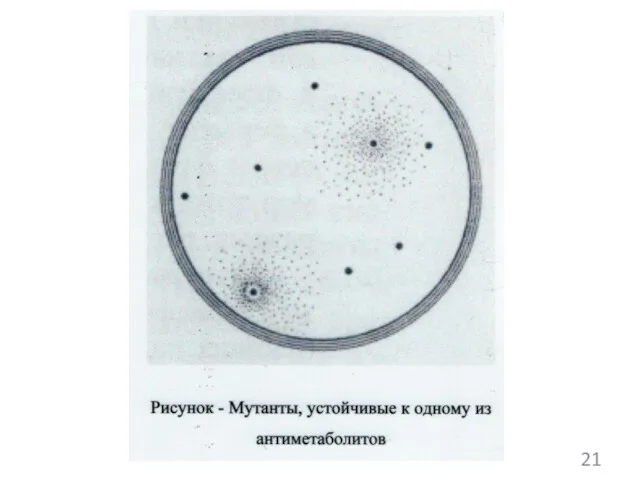
- 135. Типы мутаций, приводящих к устойчивости бактерий к антиметаболитам Мутации, приводящие к «аллостерической нечувствительности» (изменяется структура фермента
- 136. Типы мутаций, приводящих к устойчивости бактерий к антиметаболитам 3. Мутации, затрагивающие каталитические центры ферментов, активирующие метаболиты
- 137. Типы мутаций, приводящих к устойчивости бактерий к антиметаболитам 5. Мутации, обусловливающие конститутивное расщепление метаболитов (вырабатывается фермент,
- 138. 21
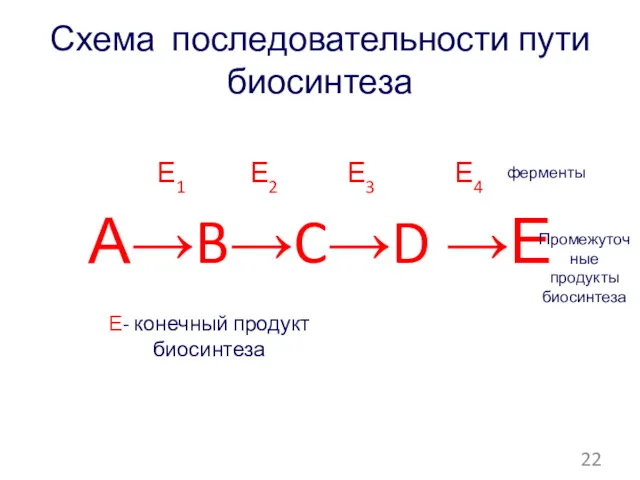
- 139. Схема последовательности пути биосинтеза Е1 Е2 Е3 Е4 А→B→C→D →Е ферменты Промежуточные продукты биосинтеза Е- конечный
- 140. 23
- 141. 24
- 143. Скачать презентацию























































































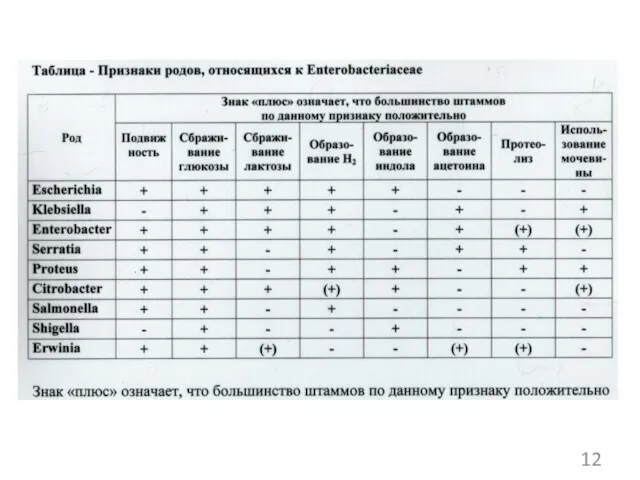







 Желілілер типінің белгілері
Желілілер типінің белгілері Природа и регуляция мышечного тонуса
Природа и регуляция мышечного тонуса Тұқымқуалаушылықтың молекулалық негіздері. Тұқым қуалайтын ақпараттың жүзеге асырылуы. Дәріс 1
Тұқымқуалаушылықтың молекулалық негіздері. Тұқым қуалайтын ақпараттың жүзеге асырылуы. Дәріс 1 Жабық тұқымды өсімдіктер бөлімі
Жабық тұқымды өсімдіктер бөлімі Видоизменённые побеги
Видоизменённые побеги Жизненные циклы голосеменных растений на примере сосны и покрытосеменных растений
Жизненные циклы голосеменных растений на примере сосны и покрытосеменных растений Бор в организме человека
Бор в организме человека Внешнее строение листа
Внешнее строение листа Физиология пищеварения
Физиология пищеварения Комнатные растения
Комнатные растения Удивительные грибы - 2
Удивительные грибы - 2 Аталық жыныс безі және. Сперматогенез
Аталық жыныс безі және. Сперматогенез Кишечник
Кишечник Высшие споровые растения. Отдел Моховидные
Высшие споровые растения. Отдел Моховидные Бионика органов чувств человека (9 класс)
Бионика органов чувств человека (9 класс) Введение в анатомию человека. Опорно-двигательный аппарат
Введение в анатомию человека. Опорно-двигательный аппарат Строение растительной и животной клеток
Строение растительной и животной клеток Сходства и различия в строении прокариотических и эукариотических клеток
Сходства и различия в строении прокариотических и эукариотических клеток Звук. Звуковая волна. Уши и слух
Звук. Звуковая волна. Уши и слух Бесплодие сельскохозяйственных животных
Бесплодие сельскохозяйственных животных Особенности строения клетки
Особенности строения клетки Палеоботаника. Прокариоты. Царство дробянки
Палеоботаника. Прокариоты. Царство дробянки Типы развития насекомых
Типы развития насекомых Индивидуальные параметры тела
Индивидуальные параметры тела Метаболизм углеводов
Метаболизм углеводов Мышцы головы. Лекция № 8
Мышцы головы. Лекция № 8 Анализаторлар. Рецепторлар
Анализаторлар. Рецепторлар Животные Пермского периода
Животные Пермского периода