Слайд 2
Слайд 3

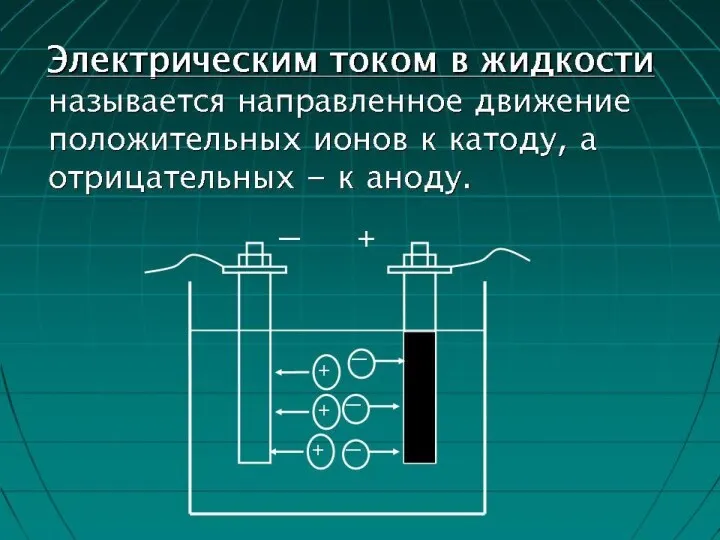
Жидкости, как и твердые тела, могут быть проводниками, полупроводниками и диэлектриками. Речь
пойдет о жидкостях-проводниках. Причем не о жидкостях с электронной проводимостью (расплавленные металлы), а о жидкостях-проводниках второго рода (растворы и расплавы солей, кислот, оснований). Тип проводимости таких проводников – ионный.
Проводники второго рода – такие проводники, в которых при протекании тока происходят химические процессы.
Слайд 4

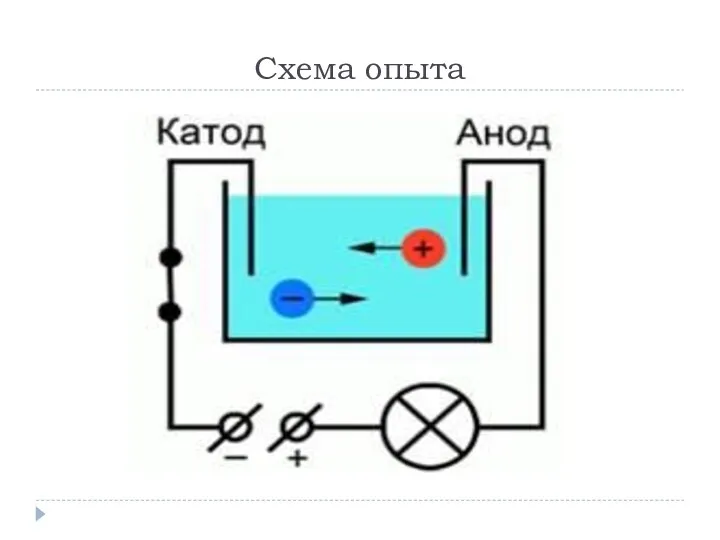
Для лучшего понимания процесса проводимоcти тока в жидкостях, можно представить следующий
опыт: В ванну с водой поместили два электрода, подключенные к источнику тока, в цепи в качестве индикатора тока можно взять лампочку. Если замкнуть такую цепь, лампа гореть не будет, что означает отсутствие тока, а это значит, что в цепи есть разрыв, и вода сама по себе ток не проводит. Но если в ванную поместить некоторое количество NaCl – поваренной соли – и повторить замыкание, то лампочка загорится. Это значит, что в ванной между катодом и анодом начали двигаться свободные носители заряда, в данном случае ионы
Слайд 5
Слайд 6
Проводимость электролитов
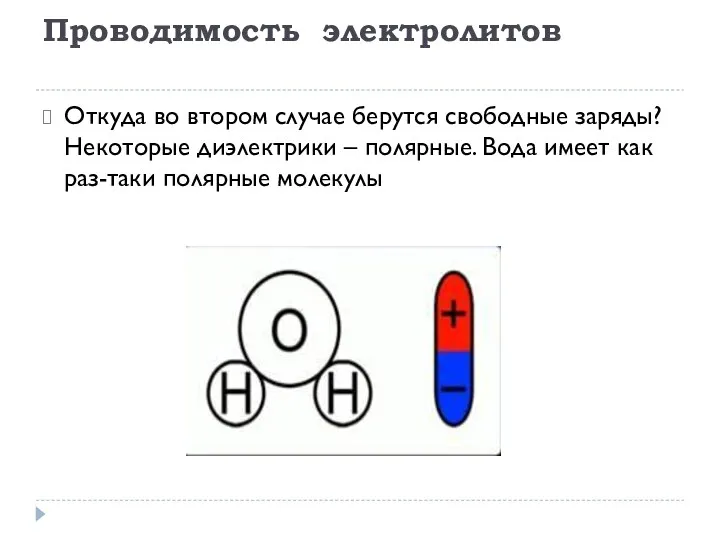
Откуда во втором случае берутся свободные заряды? Некоторые диэлектрики –
полярные. Вода имеет как раз-таки полярные молекулы
Слайд 7

При внесении в воду соли молекулы воды ориентируются таким образом, что
их отрицательные полюса находятся возле натрия, положительные – возле хлора. В результате взаимодействий между зарядами молекулы воды разрывают молекулы соли на пары разноименных ионов. Ион натрия имеет положительный заряд, ион хлора – отрицательный Именно эти ионы и будут двигаться между электродами под действием электрического поля.
Слайд 8
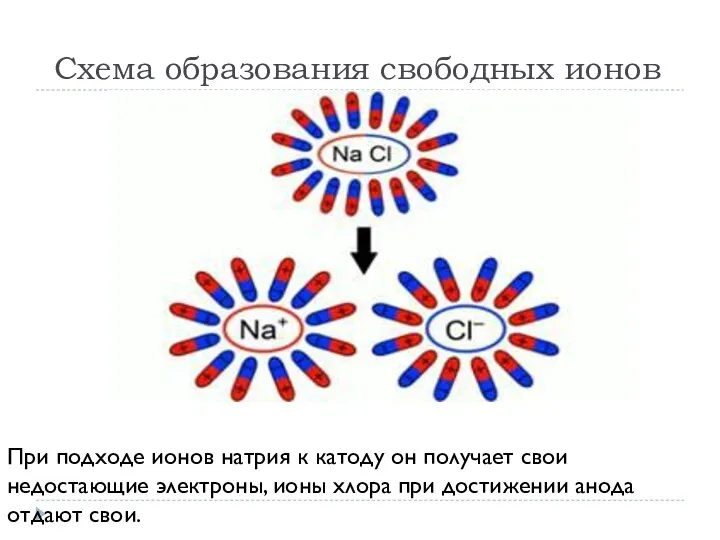
Схема образования свободных ионов
При подходе ионов натрия к катоду он получает
свои недостающие электроны, ионы хлора при достижении анода отдают свои.
Слайд 9

Электролиз
Так как протекание тока в жидкостях связано с переносом вещества, при
таком токе имеет место процесс электролиза.
Электролиз – процесс, связанный с окислительно-восстановительными реакциями, при которых на электродах выделяется вещество.
Вещества, которые в результате подобных расщеплений обеспечивают ионную проводимость, называются электролитами. Такое название предложил английский физик Майкл Фарадей
Слайд 10

Электролиз позволяет получать из растворов вещества в достаточно чистом виде, поэтому
его применяют для получения редких материалов, как натрий, кальций… в чистом виде. Этим занимается так называемая электролитическая металлугия.









 Основы технологии двигателя
Основы технологии двигателя Тепловые двигатели. Простейший тепловой двигатель
Тепловые двигатели. Простейший тепловой двигатель Техническая механика. Введение, основные понятия
Техническая механика. Введение, основные понятия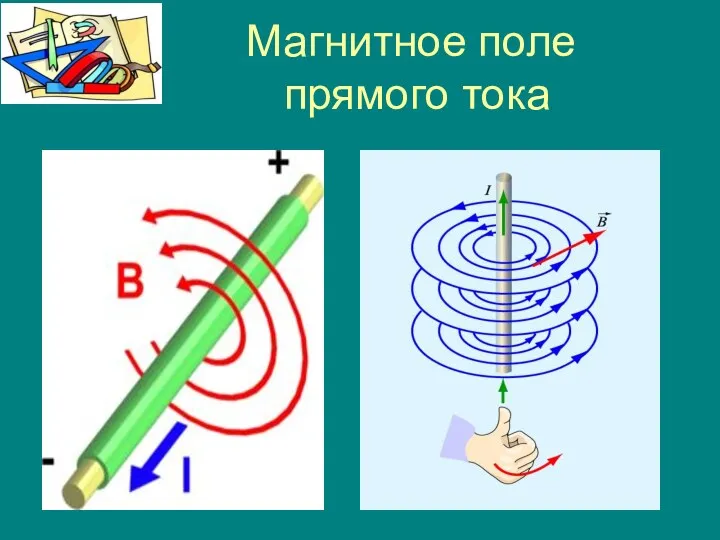 Магнитное поле прямого тока
Магнитное поле прямого тока Магистральный двухсекционный тепловоз 2ТЭ116
Магистральный двухсекционный тепловоз 2ТЭ116 Магнитные цепи. Лекция 9
Магнитные цепи. Лекция 9 Соотношение неопределённостей Гейзенберга. Волновая функция и её статистический смысл
Соотношение неопределённостей Гейзенберга. Волновая функция и её статистический смысл Проектирование виража на дорогах
Проектирование виража на дорогах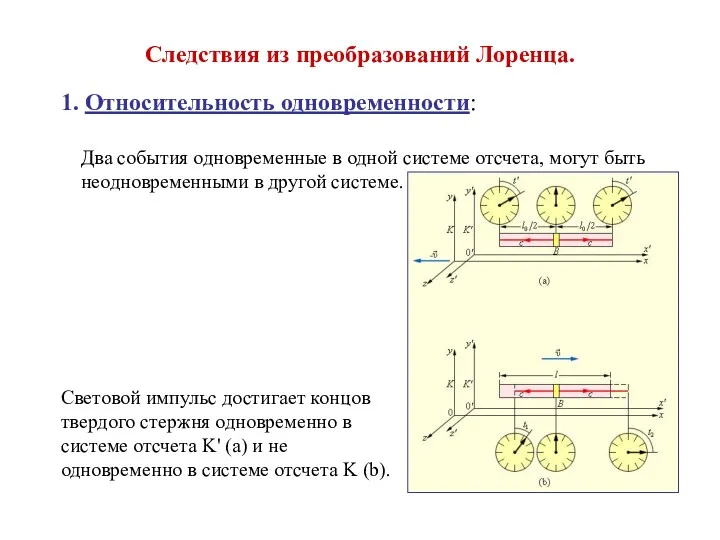 Следствия из преобразований Лоренца
Следствия из преобразований Лоренца КПД теплового двигателя
КПД теплового двигателя Содержание авиационной техники, ее получение, учет и списание
Содержание авиационной техники, ее получение, учет и списание Организация учебных занятий по физике с элементами системно-деятельностного подхода
Организация учебных занятий по физике с элементами системно-деятельностного подхода Исходные данные. Техническая характеристика
Исходные данные. Техническая характеристика Простые механизмы. Рычаг. Условие равновесия рычага
Простые механизмы. Рычаг. Условие равновесия рычага Тепловые двигатели и охрана окружающей среды
Тепловые двигатели и охрана окружающей среды Внутрицентровое поглощение света на примесных уровнях в ИК-диапазоне
Внутрицентровое поглощение света на примесных уровнях в ИК-диапазоне Детали машин и основы конструирования. Основы проектирования, критерии работоспособности и расчета деталей машин. (Лекция 1)
Детали машин и основы конструирования. Основы проектирования, критерии работоспособности и расчета деталей машин. (Лекция 1) Вес тела. Невесомость. Перегрузки
Вес тела. Невесомость. Перегрузки Производительность агрегатов. Основные понятия, определения и расчеты
Производительность агрегатов. Основные понятия, определения и расчеты Влажность воздуха
Влажность воздуха Колебания и волны. Лекция 14
Колебания и волны. Лекция 14 Применение изотопов человеком
Применение изотопов человеком Лазеры. Свойства лазерного излучения. Виды лазеров
Лазеры. Свойства лазерного излучения. Виды лазеров Электростатика. Потенциал. Работа электрического поля. Электроемкость. Постоянный и переменный ток
Электростатика. Потенциал. Работа электрического поля. Электроемкость. Постоянный и переменный ток Решение задач по теме: Характеристики тока. Последовательное и параллельное соединение проводников
Решение задач по теме: Характеристики тока. Последовательное и параллельное соединение проводников Визначення середньої швидкості нерівномірного руху
Визначення середньої швидкості нерівномірного руху Sources of the мagnetic field/
Sources of the мagnetic field/ Виртуальный музей радиосвязи
Виртуальный музей радиосвязи