Содержание
- 2. Демокрит 460–370 гг. до н.э. Демокрит считал, что существуют только атомы и пустота. Атомы — неделимые
- 3. Лукреций Кар 99–55 гг. до н.э. Эпикур 342–271 гг. до н.э. Учения Демокрита поддерживали Лукреций Кар
- 4. Причины зарождения молекулярно-кинетической теории В классической механике изучалось механическое движение.
- 5. Изменение температуры тел способно изменить его до неузнаваемости. Данные изменения связаны с движением и взаимодействием частиц,
- 6. Молекулярно-кинетическая теория (МКТ) занимается изучением свойств веществ, основываясь при этом на представлениях о частицах вещества.
- 7. Цель молекулярно-кинетической теории — объяснение свойств макроскопических тел и тепловых процессов, протекающих в них.
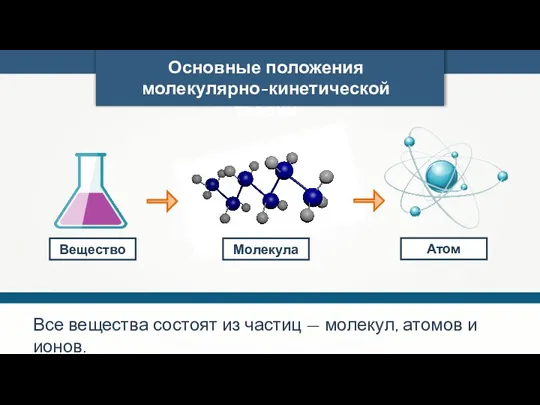
- 8. Основные положения молекулярно-кинетической теории Все вещества состоят из частиц — молекул, атомов и ионов. Вещество Молекула
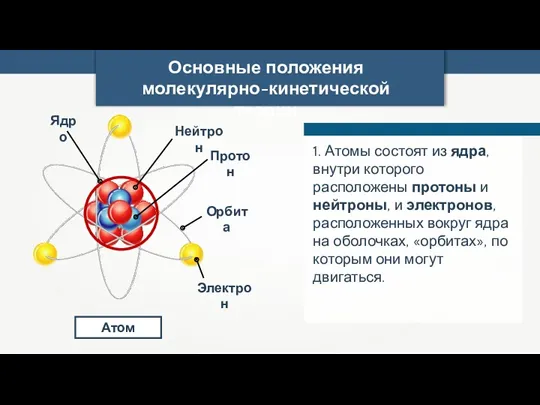
- 9. Основные положения молекулярно-кинетической теории Атом 1. Атомы состоят из ядра, внутри которого расположены протоны и нейтроны,
- 10. Основные положения молекулярно-кинетической теории 2. Частицы вещества беспрерывно и беспорядочно движутся.
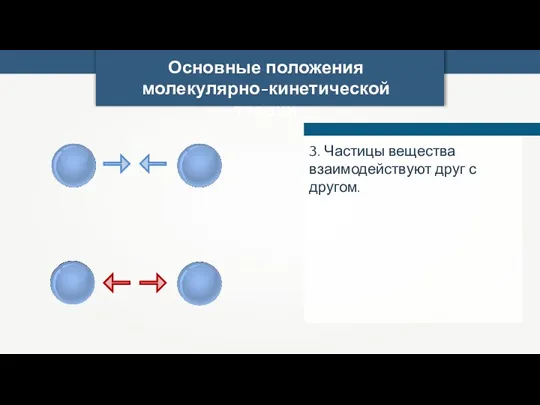
- 11. Основные положения молекулярно-кинетической теории 3. Частицы вещества взаимодействуют друг с другом.
- 12. Беспорядочное (хаотичное) движение атомов и молекул в веществе называют тепловым движением, потому что скорость движения частиц
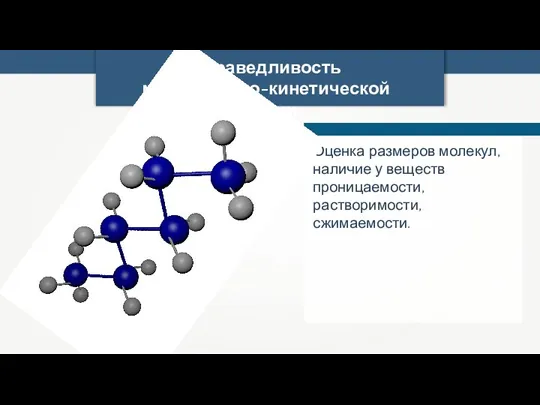
- 13. Справедливость молекулярно-кинетической теории Оценка размеров молекул, наличие у веществ проницаемости, растворимости, сжимаемости.
- 14. Справедливость молекулярно-кинетической теории Наличие прочности, упругости, смачивания, прилипания.
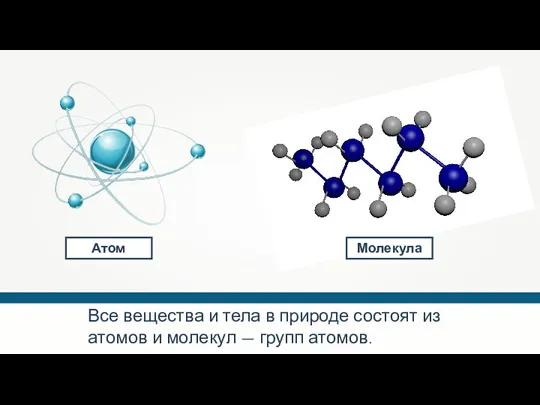
- 15. Все вещества и тела в природе состоят из атомов и молекул — групп атомов. Атом Молекула
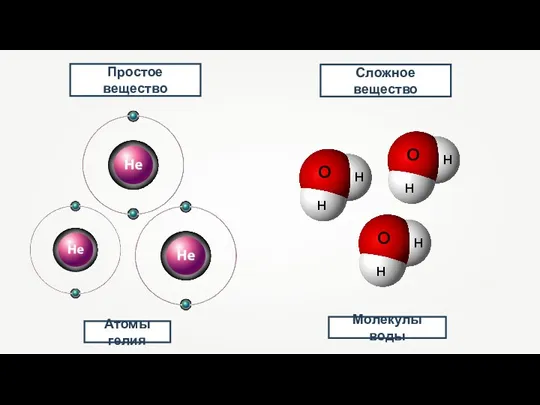
- 18. Атомы гелия Простое вещество Молекулы воды Сложное вещество
- 19. Ионы соли NaCl Что такое ионы?
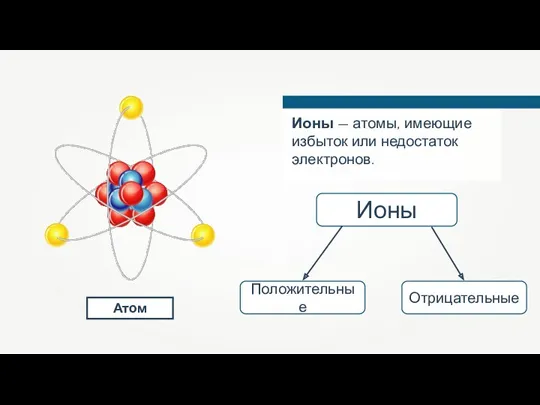
- 20. Атом Ионы — атомы, имеющие избыток или недостаток электронов. Ионы Положительные Отрицательные
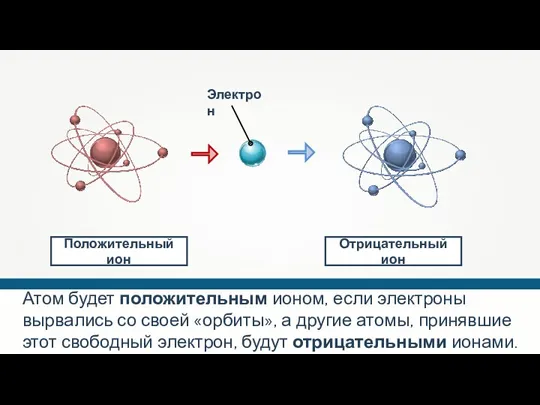
- 21. Атом будет положительным ионом, если электроны вырвались со своей «орбиты», а другие атомы, принявшие этот свободный
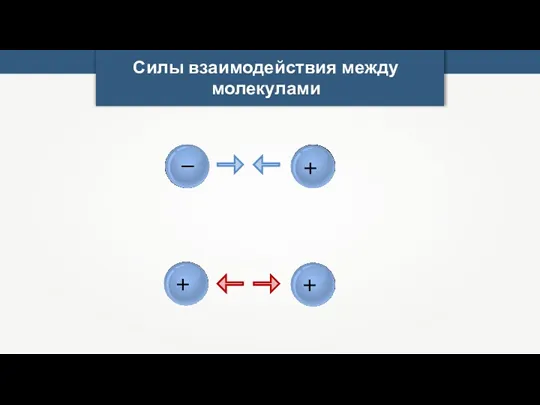
- 22. Greg L Силы взаимодействия между молекулами Частицы вещества беспрерывно и беспорядочно движутся и взаимодействуют друг с
- 23. Силы взаимодействия между молекулами – + + +
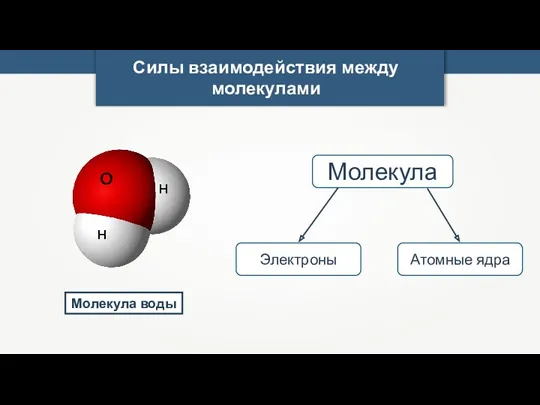
- 24. Молекула воды Силы взаимодействия между молекулами Молекула Электроны Атомные ядра
- 25. Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия практически не
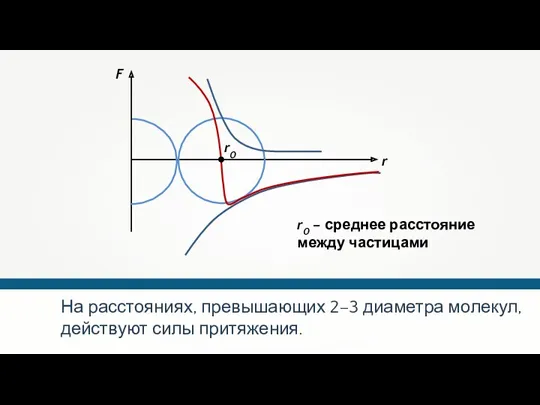
- 26. На расстояниях, превышающих 2–3 диаметра молекул, действуют силы притяжения. r0 r0 – среднее расстояние между частицами
- 27. Тепловое движение молекул Greg L В газах расстояние между атомами или молекулами в среднем во много
- 28. Тепловое движение молекул При больших расстояниях между молекулами силы притяжения малы и не способны удержать молекулы
- 29. Тепловое движение молекул Газы не сохраняют ни формы, ни объёма, их объём и форма совпадают с
- 30. Тепловое движение молекул Молекулы жидкости расположены почти вплотную друг к другу. Поэтому жидкости очень плохо сжимаются
- 31. Тепловое движение молекул Время от времени молекула совершает переходы из одного оседлого состояния в другое, как
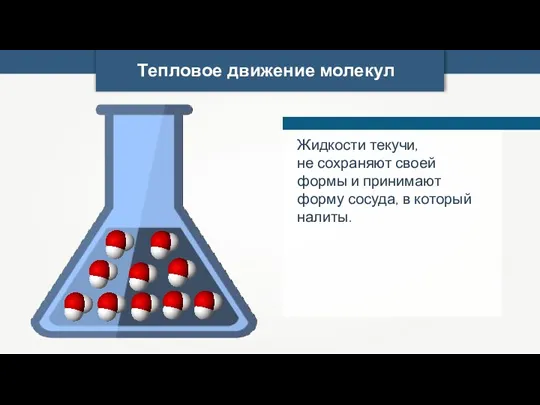
- 32. Тепловое движение молекул Жидкости текучи, не сохраняют своей формы и принимают форму сосуда, в который налиты.
- 33. Тепловое движение молекул Теория жидкого состояния вещества впервые была разработана крупным советским физиком-теоретиком Яковом Ильичом Френкелем.
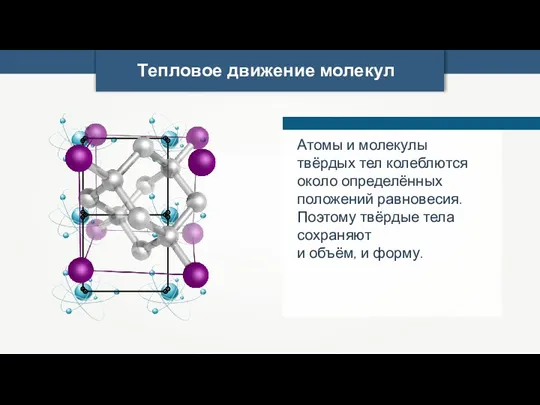
- 34. Тепловое движение молекул Атомы и молекулы твёрдых тел колеблются около определённых положений равновесия. Поэтому твёрдые тела
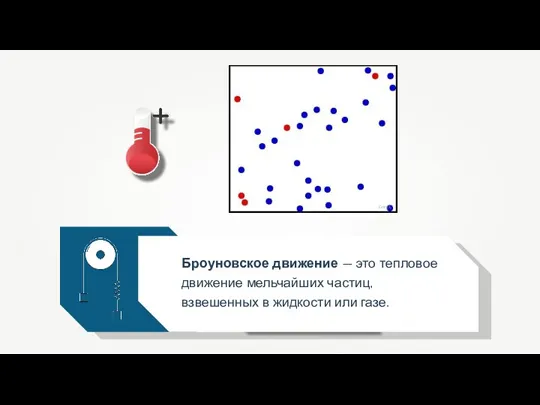
- 35. Броуновское движение — это тепловое движение мельчайших частиц, взвешенных в жидкости или газе. Greg L
- 36. Роберт Броун 1773–1858 гг. Броуновское движение частиц было открыто английским ботаником Броуном в 1827 г. и
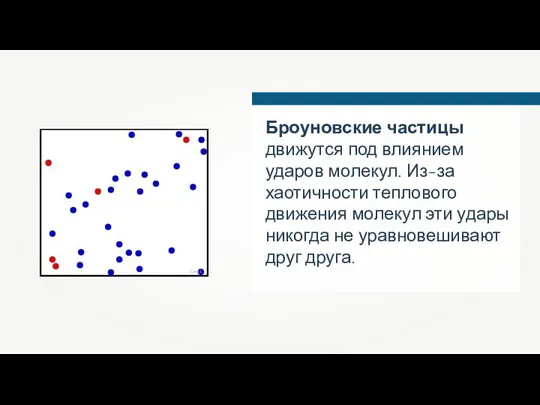
- 37. Броуновские частицы движутся под влиянием ударов молекул. Из-за хаотичности теплового движения молекул эти удары никогда не
- 38. Молекулярно-кинетическая теория броуновского движения была создана Альбертом Эйнштейном в 1905 году. Альберт Эйнштейн 1879–1955 гг.
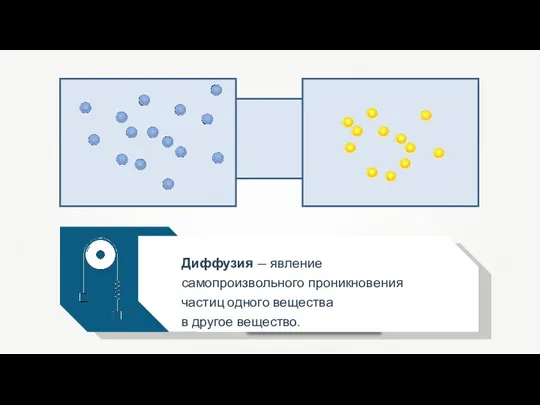
- 39. Диффузия — явление самопроизвольного проникновения частиц одного вещества в другое вещество.
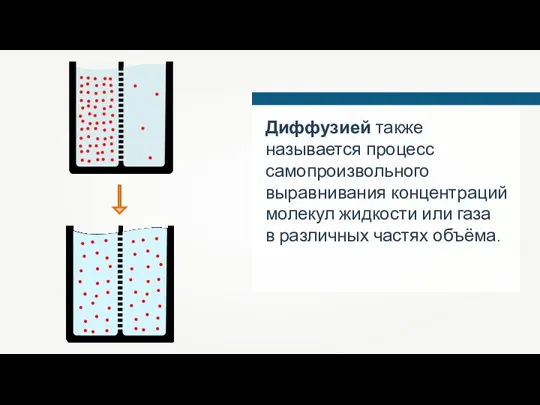
- 40. Диффузией также называется процесс самопроизвольного выравнивания концентраций молекул жидкости или газа в различных частях объёма.
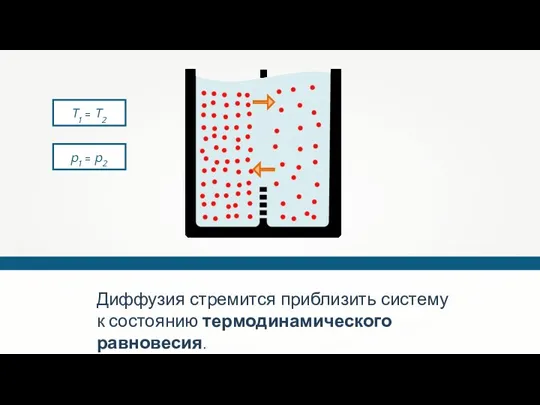
- 41. Диффузия стремится приблизить систему к состоянию термодинамического равновесия. T1 = T2 p1 = p2
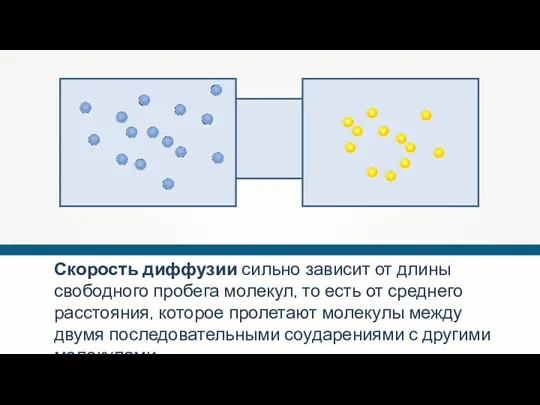
- 42. Скорость диффузии сильно зависит от длины свободного пробега молекул, то есть от среднего расстояния, которое пролетают
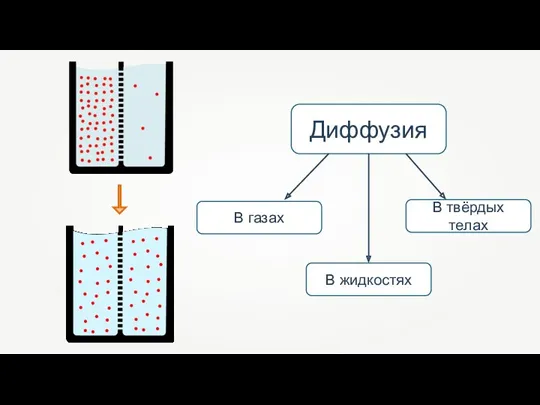
- 43. Диффузия В твёрдых телах В жидкостях В газах
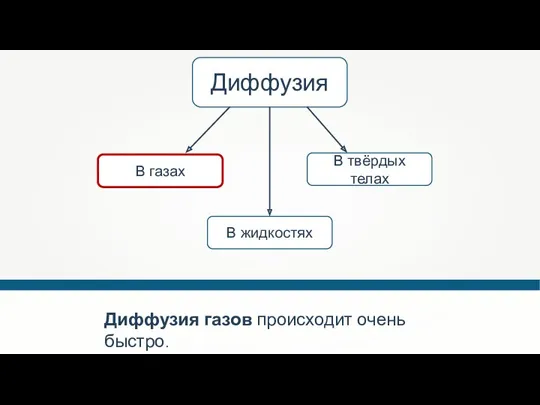
- 44. Диффузия В твёрдых телах В жидкостях В газах Диффузия газов происходит очень быстро.
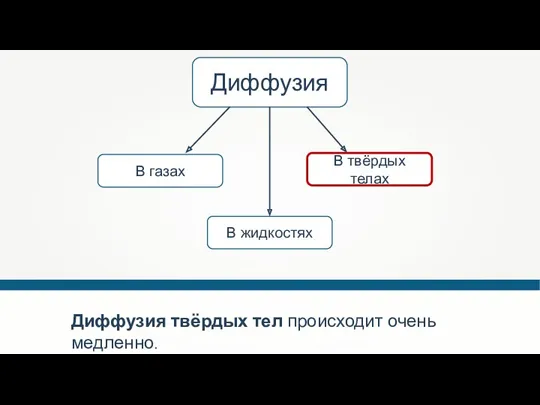
- 45. Диффузия В твёрдых телах В жидкостях В газах Диффузия твёрдых тел происходит очень медленно.
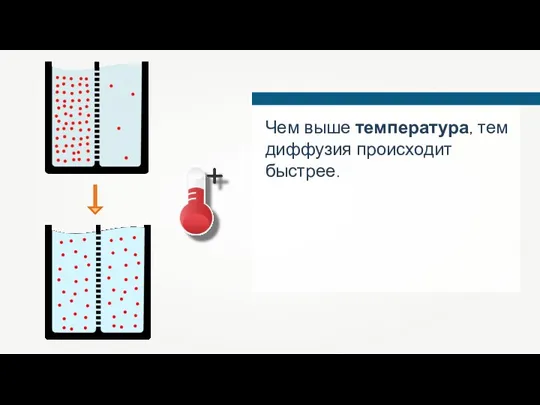
- 46. Чем выше температура, тем диффузия происходит быстрее.
- 53. Скачать презентацию





















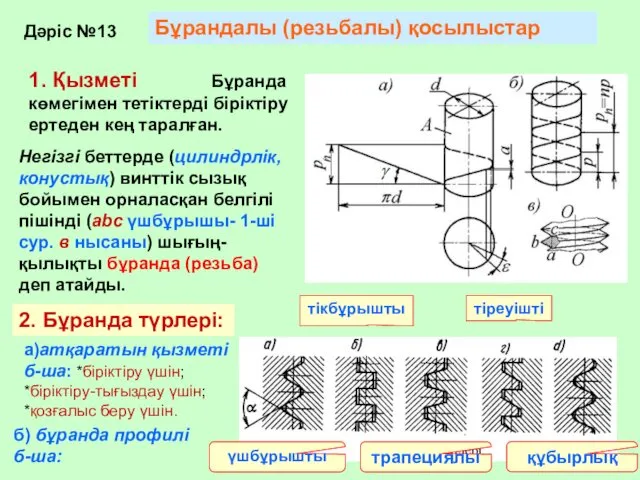 Бұрандалы қосылыстар
Бұрандалы қосылыстар Допуски и посадки подшипников качения
Допуски и посадки подшипников качения Маятники. Види маятників
Маятники. Види маятників Термодинамика и статистическая физика
Термодинамика и статистическая физика Механическое движение
Механическое движение Электрический ток. Закон Ома для участка цепи
Электрический ток. Закон Ома для участка цепи Теплообменные аппараты
Теплообменные аппараты Закон Архимеда
Закон Архимеда Солнечные батареи
Солнечные батареи Применение аккумуляторов
Применение аккумуляторов Механические колебания. 11 класс
Механические колебания. 11 класс Автоматтық жүйелер: негізгі анықтамалар, функционалдық схемалар. Ақпарат ұғымы, саны. Хабарлама
Автоматтық жүйелер: негізгі анықтамалар, функционалдық схемалар. Ақпарат ұғымы, саны. Хабарлама Элементы оптоэлектроники. Приборы с зарядовой связью. Светодиоды. (Лекция 14.2)
Элементы оптоэлектроники. Приборы с зарядовой связью. Светодиоды. (Лекция 14.2) Деформация и механические свойства материалов
Деформация и механические свойства материалов Элементы квантовой механики. Лекция 12
Элементы квантовой механики. Лекция 12 Техническое обслуживание и ремонт систем зажигания
Техническое обслуживание и ремонт систем зажигания Теплотехнические схемы парогенераторов АЭС
Теплотехнические схемы парогенераторов АЭС Эксплуатация, диагностика и организация ремонта прокатного оборудования
Эксплуатация, диагностика и организация ремонта прокатного оборудования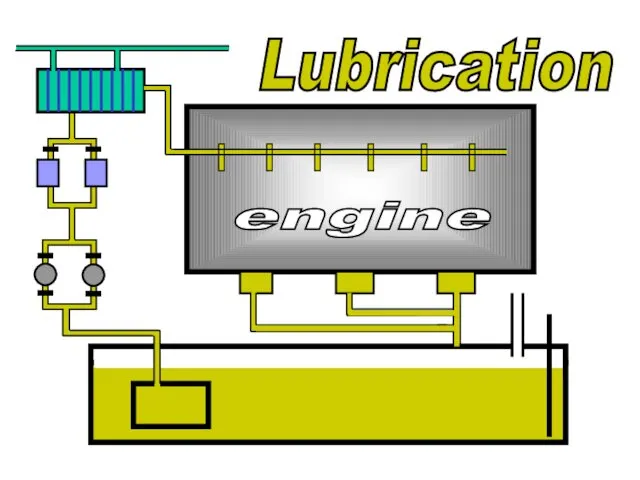 Lubrication
Lubrication Строение атома и атомного ядра. Использование энергии атомных ядер
Строение атома и атомного ядра. Использование энергии атомных ядер Нагрев материалов лазерным излучением
Нагрев материалов лазерным излучением Опорно поворотные устройства специального назначения
Опорно поворотные устройства специального назначения Элементы машиноведения. Бытовая швейная машина
Элементы машиноведения. Бытовая швейная машина Физика и методы научного познания (урок № 1)
Физика и методы научного познания (урок № 1) Источник тока. Закон Ома длоя замкнутой цепи
Источник тока. Закон Ома длоя замкнутой цепи Оптические приборы
Оптические приборы Парообразование и конденсация. Удельная теплота парообразования и конденсации
Парообразование и конденсация. Удельная теплота парообразования и конденсации Защита от шума
Защита от шума