Содержание
- 2. Давайте вспомним!
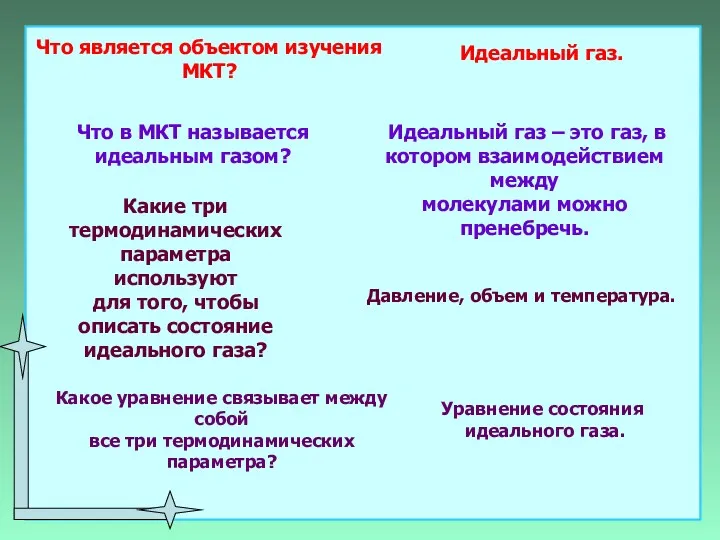
- 3. Что является объектом изучения МКТ? Идеальный газ. Что в МКТ называется идеальным газом? Идеальный газ –
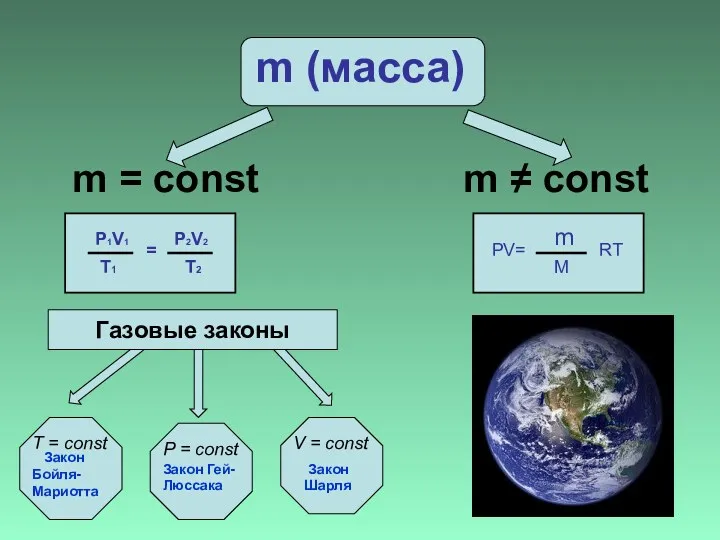
- 4. m (масса) m = const m ≠ const P1V1 T1 = P2V2 T2 PV= m M
- 5. Изопроцессы – процессы, протекающие при неизменном значении одного из параметров. “изо” - постоянство 1.Изотермический 2.Изобарный 3.Изохорный
- 6. Изотермический процесс Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называют изотермическим. «термо» -
- 8. Закон Бойля-Мариотта в 1662 г. в 1676 г.
- 9. Изотермический процесс
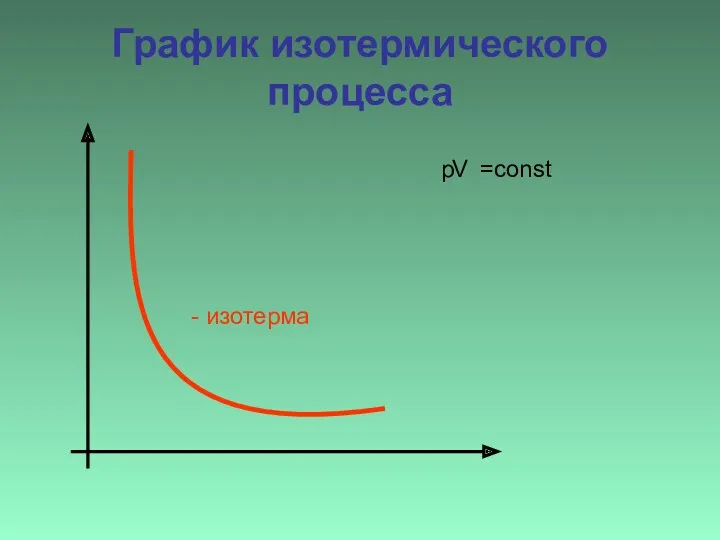
- 10. График изотермического процесса - изотерма p V =const
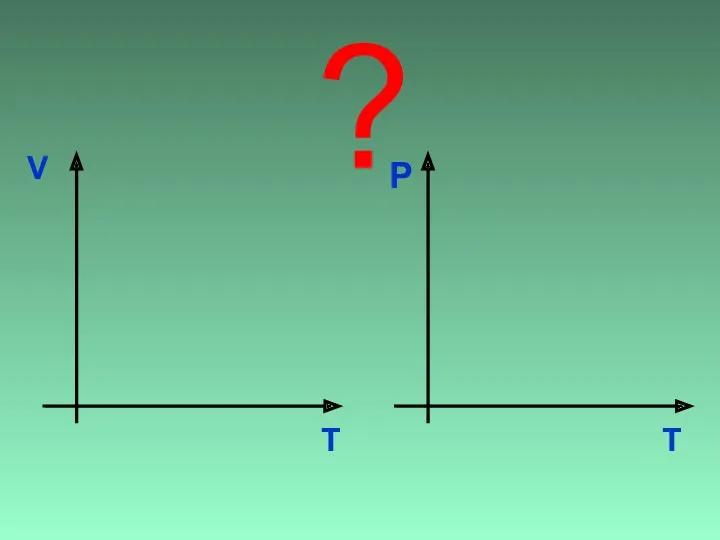
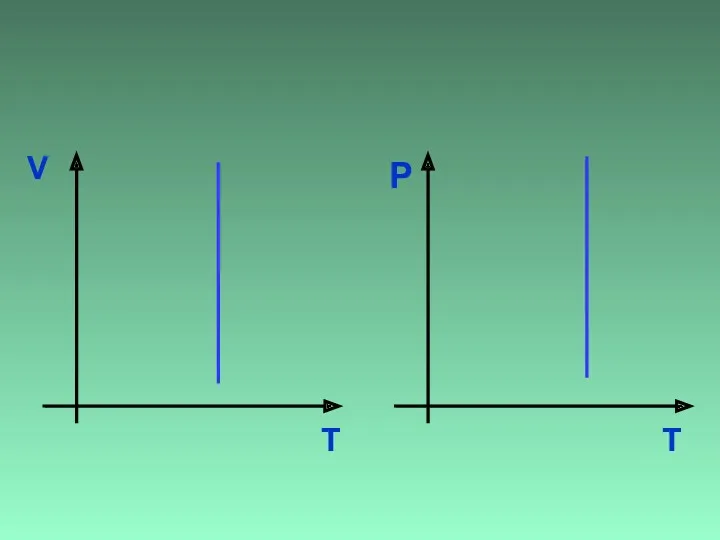
- 11. V T ? T P
- 12. V T T P
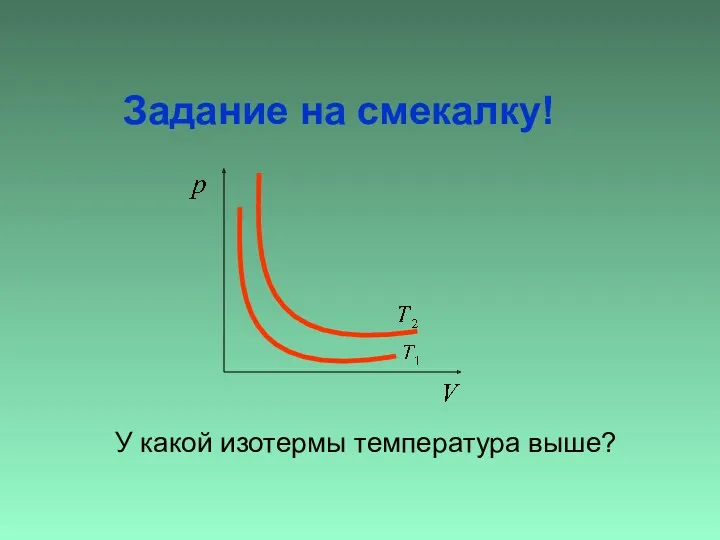
- 13. У какой изотермы температура выше? Задание на смекалку!
- 14. Изобарный процесс Изобарный процесс – процесс изменения состояния определенной массы газа при постоянном давлении. “барос”(греч.) -
- 15. Закон Гей-Люсаака
- 16. Изобарный процесс
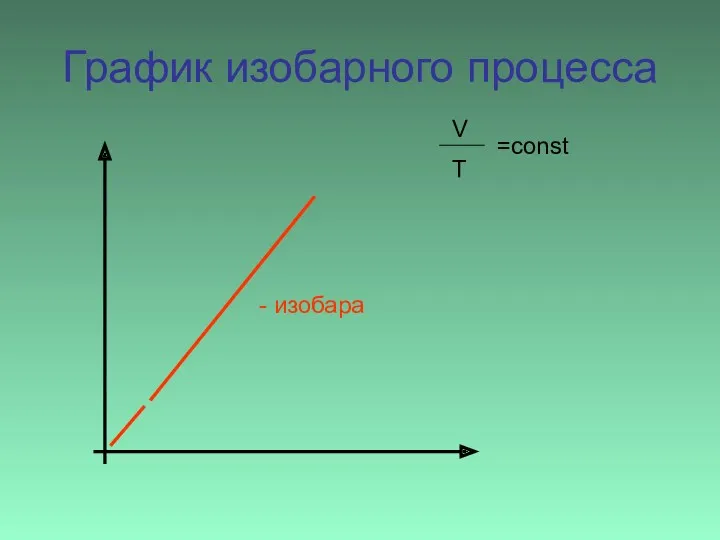
- 17. График изобарного процесса - изобара V T =const
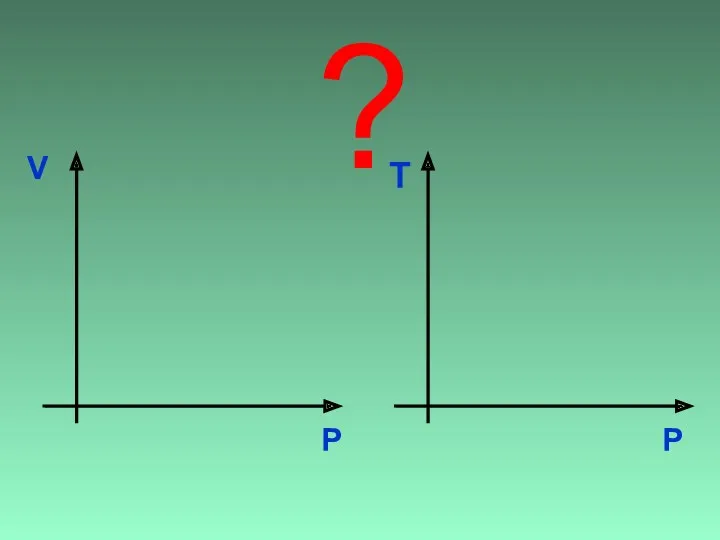
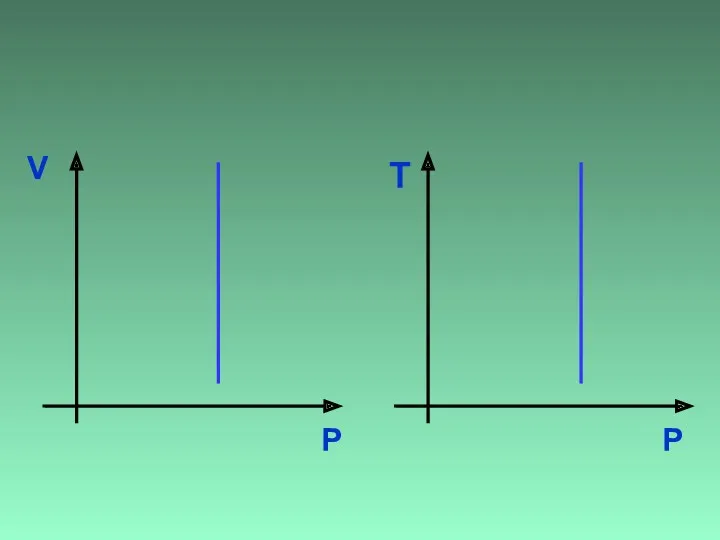
- 18. V Р ? Р Т
- 19. V Р Р Т
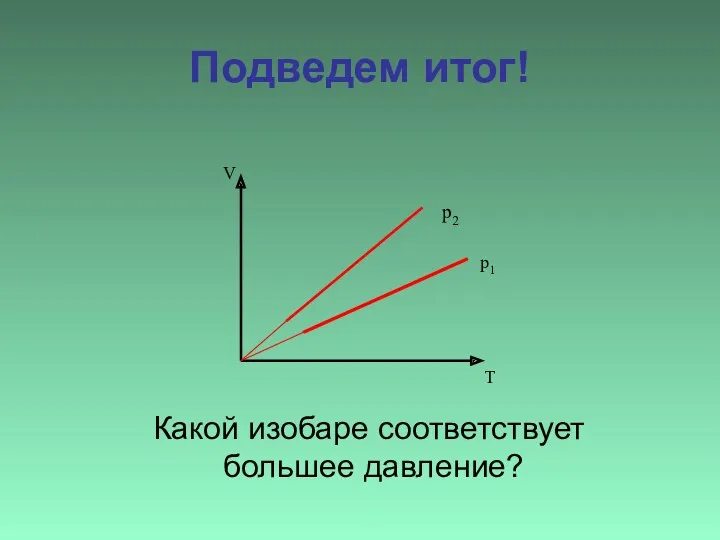
- 20. Подведем итог! Какой изобаре соответствует большее давление? V T p1 p2
- 21. Изохорный процесс Процесс изменения состояния термодинамической системы макроскопических тел при постоянном объеме называют изохорным. “хорос”(греч.) -
- 22. Закон Шарля
- 23. Изохорный процесс Давление данной массы газа при постоянном объёме прямопропорционально температуре. V=const
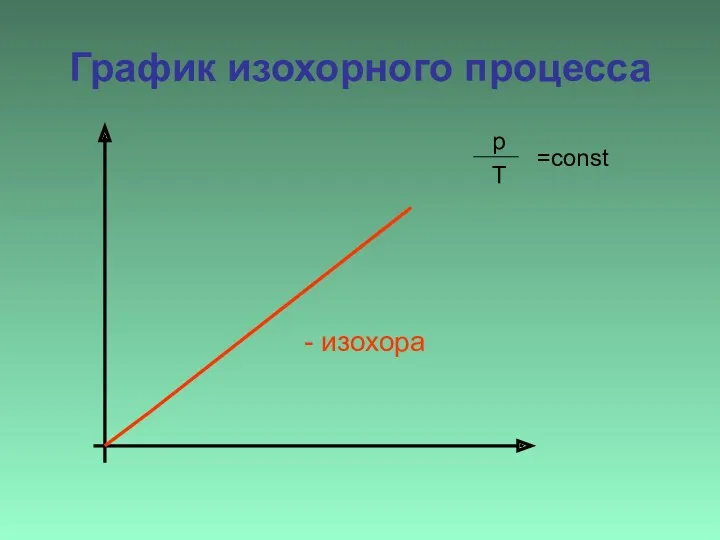
- 24. График изохорного процесса - изохора p Т =const
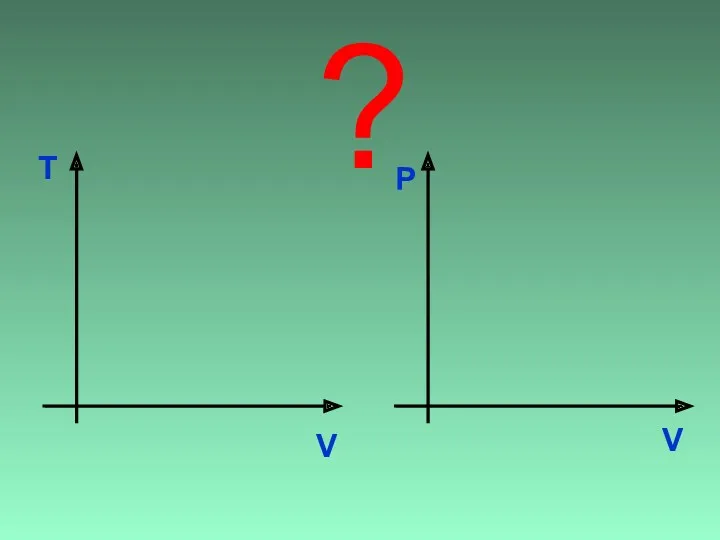
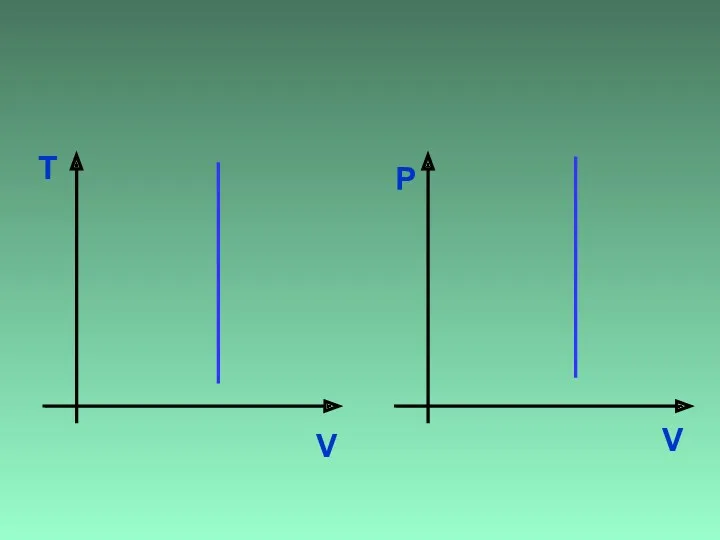
- 25. V T ? V Р
- 26. V T V Р
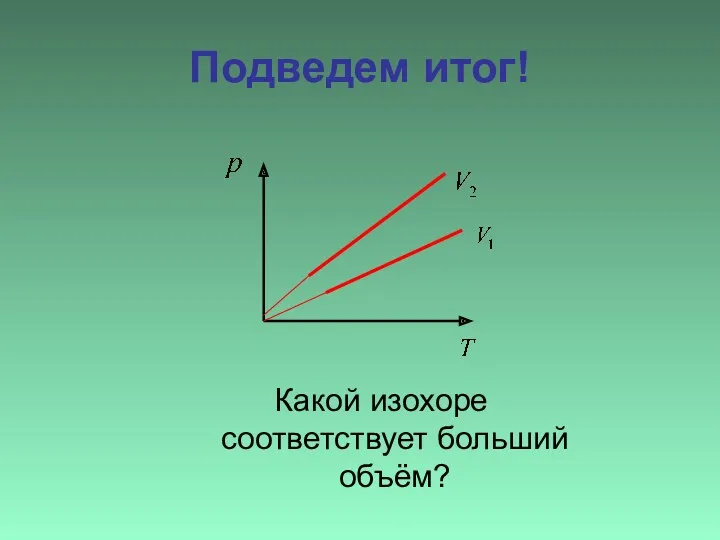
- 27. Подведем итог! Какой изохоре соответствует больший объём?
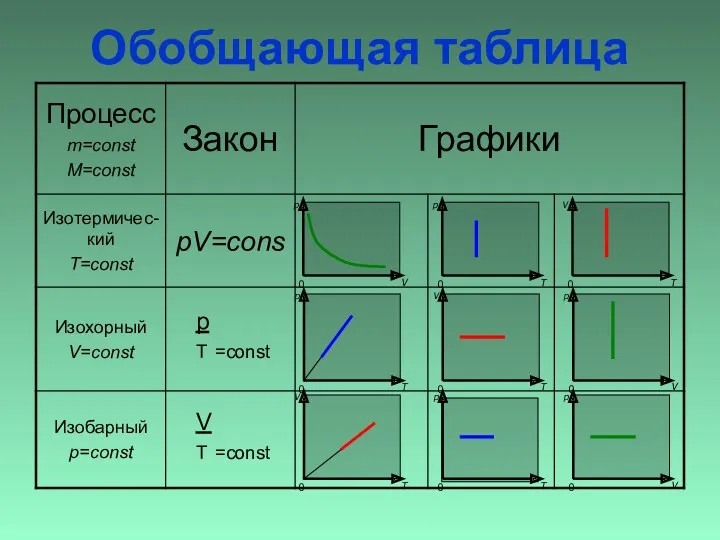
- 28. Обобщающая таблица
- 29. Проверь себя!
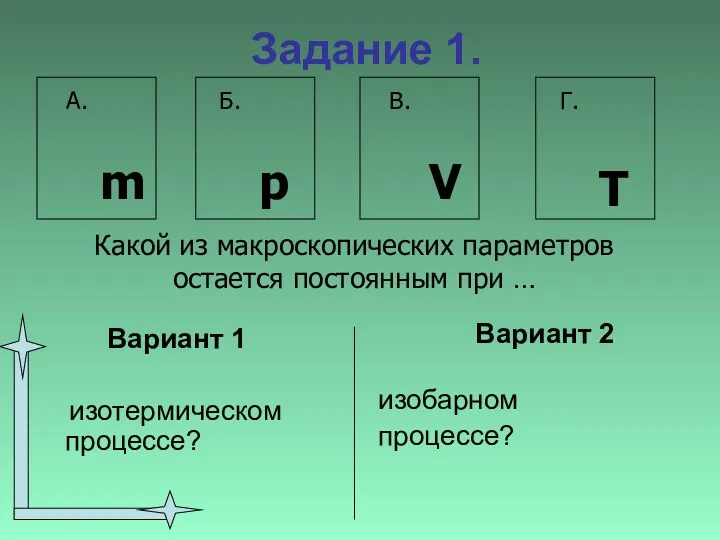
- 30. Задание 1. Вариант 1 изотермическом процессе? Вариант 2 изобарном процессе? Какой из макроскопических параметров остается постоянным
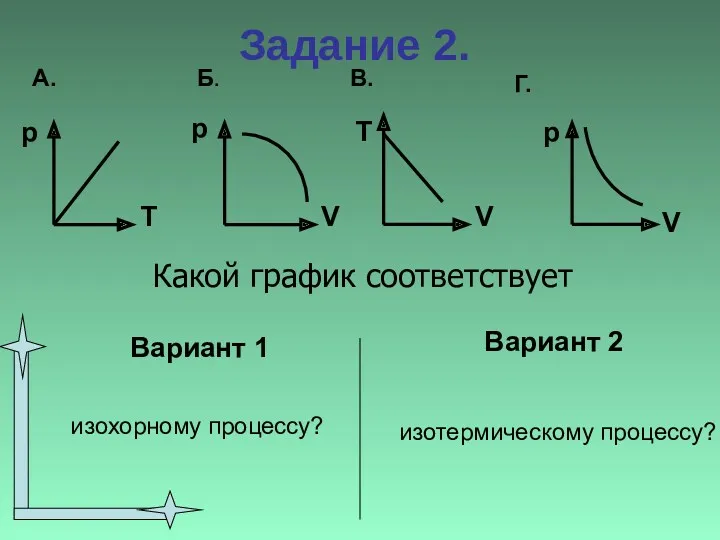
- 31. Вариант 1 изохорному процессу? Вариант 2 изотермическому процессу? Задание 2. Какой график соответствует
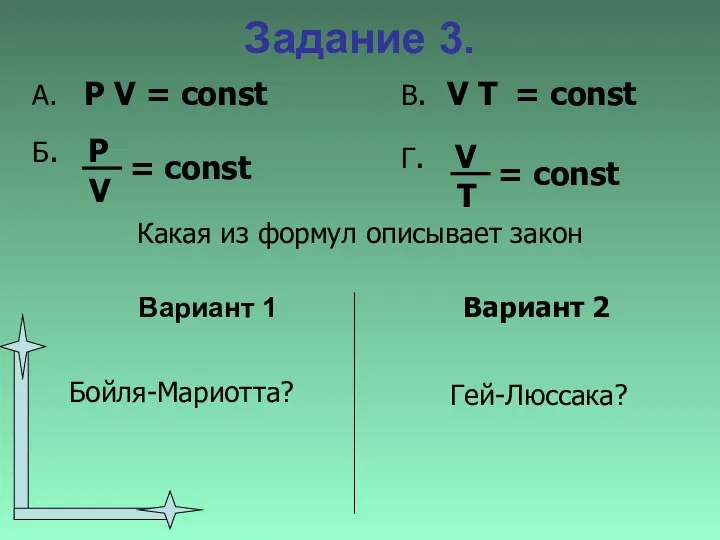
- 32. Задание 3. Вариант 1 Какая из формул описывает закон Вариант 2 Бойля-Мариотта? Гей-Люссака?
- 33. Задание 4. Догадайтесь, о каком изопроцессе идет речь в каждом случае? Вариант 1. Сосуд с газом
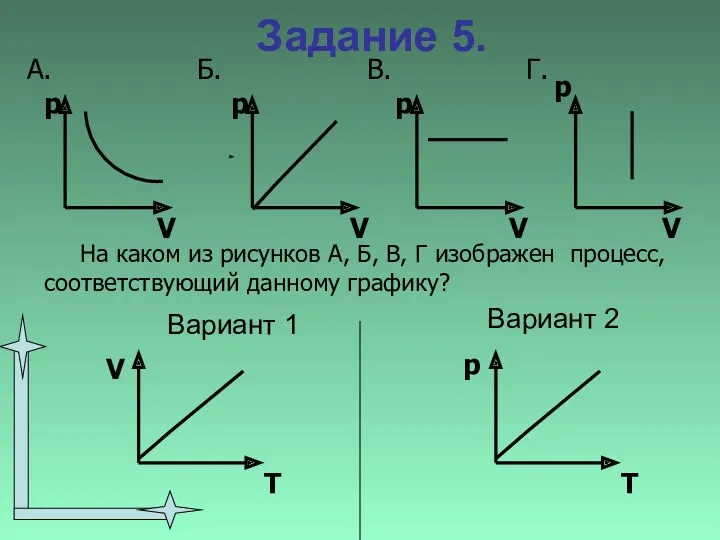
- 34. Задание 5. Вариант 1 Вариант 2 В. p На каком из рисунков А, Б, В, Г
- 35. Проверь правильность своих ответов
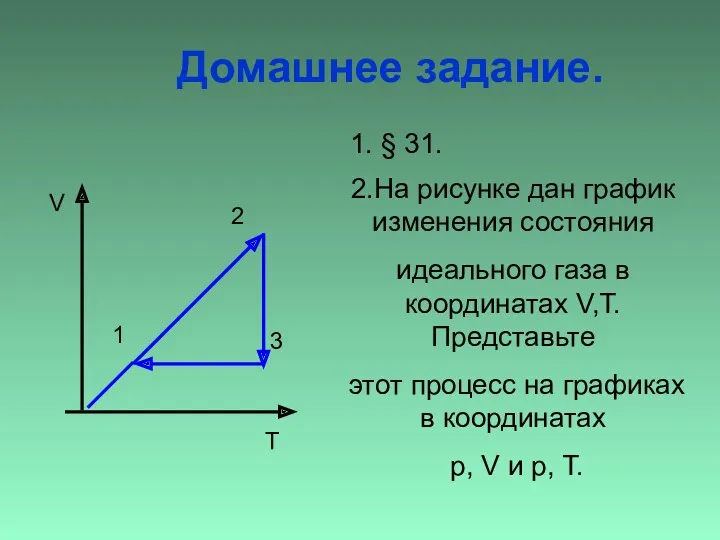
- 36. Домашнее задание. 2.На рисунке дан график изменения состояния идеального газа в координатах V,T.Представьте этот процесс на
- 38. Скачать презентацию















 Основные понятия и аксиомы статики
Основные понятия и аксиомы статики Основные законы идеального газа
Основные законы идеального газа Первое начало термодинамики
Первое начало термодинамики Электрический ток, сила тока. Закон Ома для участка цепи
Электрический ток, сила тока. Закон Ома для участка цепи презентация к внеклассному мероприятию Что? Где? Когда?
презентация к внеклассному мероприятию Что? Где? Когда? Ядерная геофизика
Ядерная геофизика Электромагнитная картина мира
Электромагнитная картина мира Основы гидравлики
Основы гидравлики Закон Ома для участка цепи. Урок 35
Закон Ома для участка цепи. Урок 35 Прямолинейное равноускоренное движение
Прямолинейное равноускоренное движение Давление. Единицы давления. Способы уменьшения и увеличения давления
Давление. Единицы давления. Способы уменьшения и увеличения давления Управление и характеристики машин
Управление и характеристики машин Урок физики в 8 классе по теме Плотность
Урок физики в 8 классе по теме Плотность Прибор для демонстрации графиков электромагнитных колебаний
Прибор для демонстрации графиков электромагнитных колебаний Машины постоянного тока. Устройство, материалы и принцип действия. Карточка 16
Машины постоянного тока. Устройство, материалы и принцип действия. Карточка 16 Необычные виды транспорта в разных странах мира
Необычные виды транспорта в разных странах мира Lubrication engine
Lubrication engine Своя Игра на тему: Давление
Своя Игра на тему: Давление Реакторы на быстрых нейтронах
Реакторы на быстрых нейтронах Свет в нашей жизни.
Свет в нашей жизни. Кручение стержней круглого сечения
Кручение стержней круглого сечения Способы постановки проблемы на уроках физики
Способы постановки проблемы на уроках физики Презентация Линзы
Презентация Линзы Форма и ширина спектральной линии
Форма и ширина спектральной линии свободное падение тел
свободное падение тел Расчет давления жидкости на дно и стенки сосуда урок физики в 7 классе с применением интерактивной доски
Расчет давления жидкости на дно и стенки сосуда урок физики в 7 классе с применением интерактивной доски Тема 1. Електромобілі та основні етапи їх розвитку. Частина 1
Тема 1. Електромобілі та основні етапи їх розвитку. Частина 1 Движение абсолютно твёрдого тела
Движение абсолютно твёрдого тела