Содержание
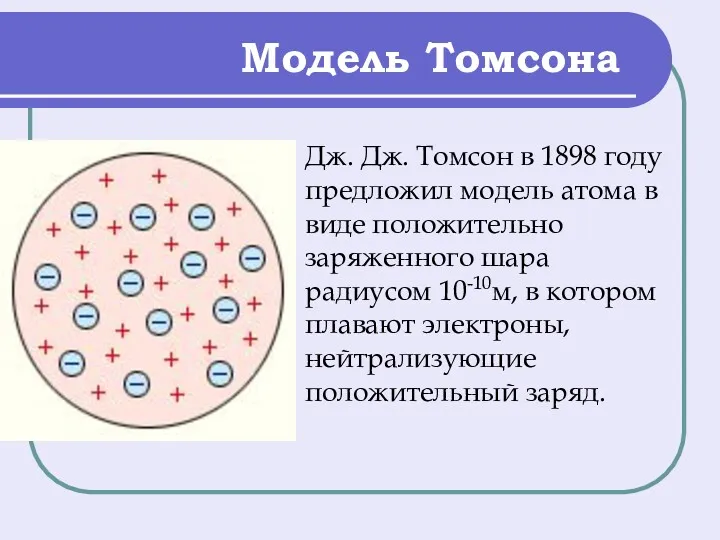
- 2. Модель Томсона Дж. Дж. Томсон в 1898 году предложил модель атома в виде положительно заряженного шара
- 3. Атомное ядро Результаты опытов по проверке правильности «пудинговой» модели атома, проведённые в 1911 году английским физиком
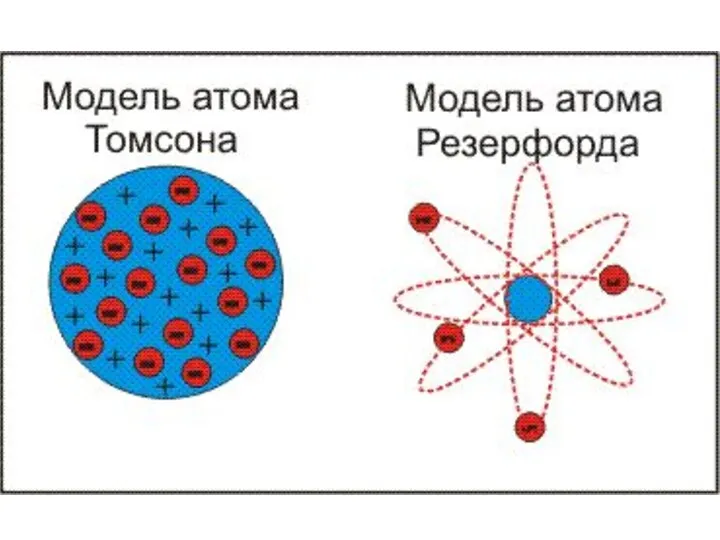
- 5. Модель Резерфорда (1911 г.)
- 6. Атомное ядро Выяснилось, что диаметр атома оценивается как 10-10 м В ходе этих экспериментов выяснилось, что
- 7. После открытия атомного ядра возник вопрос: не является ли и оно составным? Может быть, и ядро
- 8. Кислород Азот
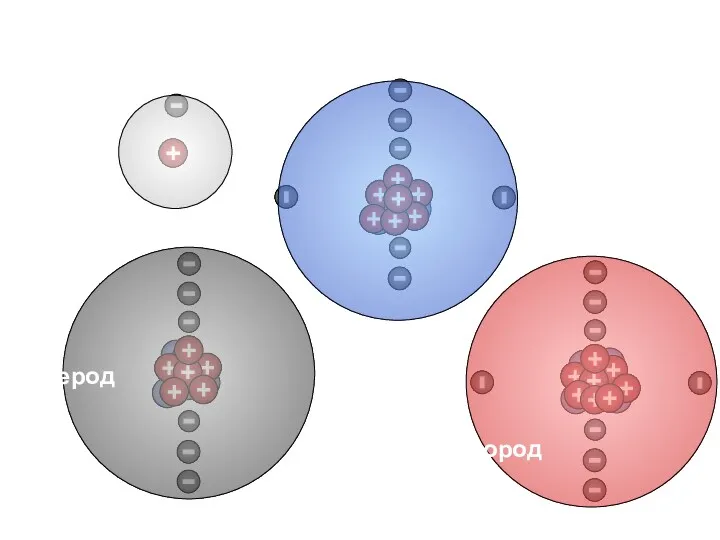
- 9. Водород Азот Кислород Углерод
- 10. Протоны В 1911 году Эрнест Резерфорд высказал предположение, что ядра состоят из частиц, которые были названы
- 11. ПОЛУЧЕНИЕ ПРОТОНА
- 12. Нейтроны В 1919 году Эрнест Резерфорд высказал предположение, что ядра в состав ядра помимо протонов, входят
- 13. ПОЛУЧЕНИЕ НЕЙТРОНА
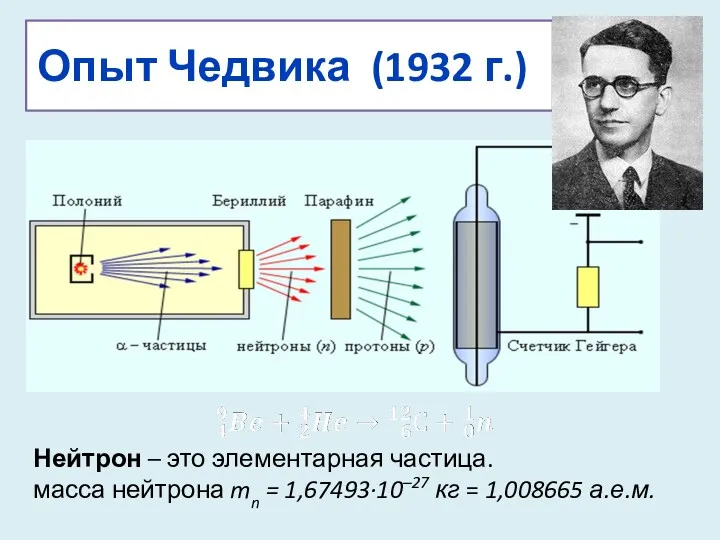
- 14. Опыт Чедвика (1932 г.) Нейтрон – это элементарная частица. масса нейтрона mn = 1,67493·10–27 кг =
- 15. Нуклоны Протоны и нейтроны имеют общее название – нуклоны. По современным данным протоны и нейтроны считаются
- 16. НУКЛОНЫ: ПРОТОНЫ И НЕЙТРОНЫ
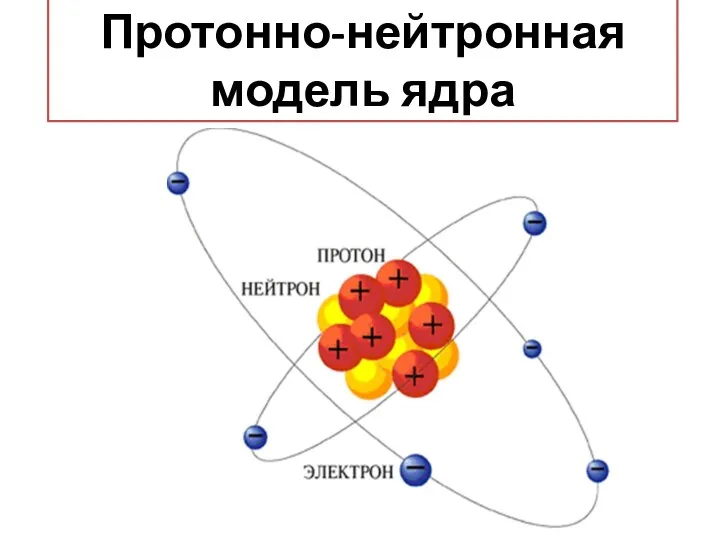
- 17. ПРОТОННО – НЕЙТРОННАЯ МОДЕЛЬ ЯДРА
- 18. Протонно-нейтронная модель ядра (1932 г.) Иваненко Д.Д. (1904 – 1994) Гейзенберг Ф.К. (1901 – 1976)
- 19. Протонно-нейтронная модель ядра
- 20. Z – зарядовое число А – массовое число ЗАРЯДОВОЕ И МАССОВОЕ ЧИСЛА
- 21. Количество протонов в ядре называют зарядовым числом Z
- 22. Зарядовое число равно номеру химического элемента в периодической системе элементов Менделеева. Химические свойства элемента определяются зарядовым
- 23. Число нейтронов в ядре обозначают
- 24. Количество протонов в ядре называют зарядовым числом Z
- 25. Зарядовое число равно номеру химического элемента в периодической системе элементов Менделеева. Химические свойства элемента определяются зарядовым
- 26. Число нейтронов в ядре обозначают
- 27. Массовое число НУКЛОНОВ В ЯДРЕ АТОМА A = Z + N
- 28. Массовое число определяет относительную атомную массу химического элемента. Она равна произведению массового числа на атомную единицу
- 29. Ядро атома обозначают так же, как и соответствующий химический элемент, ставя перед ним вверху – массовое
- 30. Изотопы Выяснилось, что существуют ядра с одинаковым зарядом, но разными массами. Такие ядра назвали изотопами
- 31. ИЗОТОПЫ РАЗНОВИДНОСТИ ХИМИЧЕСКОГО ЭЛЕМЕНТА, ОТЛИЧАЮЩИЕСЯ КОЛИЧЕСТВОМ НЕЙТРОНОВ
- 32. ИЗОТОПЫ РАЗНОВИДНОСТИ ХИМИЧЕСКОГО ЭЛЕМЕНТА, ОТЛИЧАЮЩИЕСЯ КОЛИЧЕСТВОМ НЕЙТРОНОВ
- 33. ИЗОТОПЫ ВОДОРОДА
- 34. Задание: 1. Ответьте на вопросы теста 2. Алюминий занимает в таблице Менделеева тринадцатую клетку, его масса
- 35. Два ядра имеют одинаковое массовое число. Могут ли заряды этих ядер быть различными? Обоснуйте ваш ответ.
- 36. Два ядра имеют одинаковые заряды, но разные массовые числа. Являются ли эти ядра изотопами одного и
- 37. 3. Выберите правильный ответ: число нейтронов в ядре всегда равно числу протонов число электронов в атоме
- 38. А) 10 -8 м 1) 10 -8 см 2) 10 -10см 3) 10 -9см 4. Результаты
- 40. Скачать презентацию




























 Презентация. Гости из космоса
Презентация. Гости из космоса Люди нашего края Голобоков
Люди нашего края Голобоков Электроосветительные приборы
Электроосветительные приборы Электроемкость. Конденсаторы. Урок физики в 10 классе
Электроемкость. Конденсаторы. Урок физики в 10 классе Фрикционные передачи
Фрикционные передачи Поляризация света
Поляризация света Презентация Электронно-дырочный переход. Транзистор
Презентация Электронно-дырочный переход. Транзистор Инерция
Инерция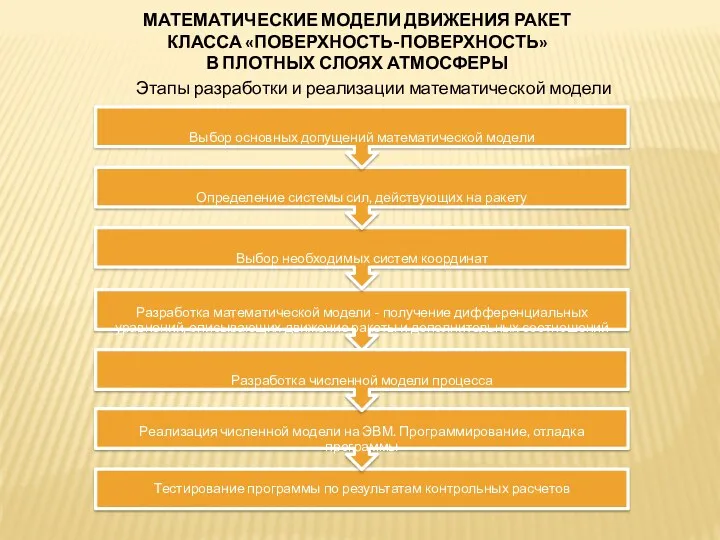 Математические модели движения ракет класса поверхность-поверхность в плотных слоях атмосферы
Математические модели движения ракет класса поверхность-поверхность в плотных слоях атмосферы Сдвиг и кручение. Закон Гука при сдвиге. Условие прочности при чистом сдвиге
Сдвиг и кручение. Закон Гука при сдвиге. Условие прочности при чистом сдвиге Многодисковая муфта с фрикционными дисками
Многодисковая муфта с фрикционными дисками Презентация к уроку по физике для 8 класса по теме Влажность воздуха
Презентация к уроку по физике для 8 класса по теме Влажность воздуха Тұтас орталар механикасының элементтері
Тұтас орталар механикасының элементтері Масса и размеры молекул. Количество вещества
Масса и размеры молекул. Количество вещества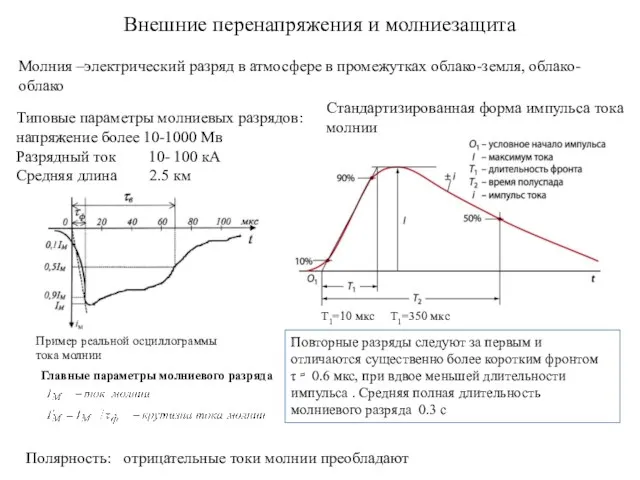 Внешние перенапряжения и молниезащита. (Лекция 2.4)
Внешние перенапряжения и молниезащита. (Лекция 2.4) Структурные уровни организации материи. Микро-, макро-, мегамиры
Структурные уровни организации материи. Микро-, макро-, мегамиры урок по физике Магнитное поле
урок по физике Магнитное поле Тормозная система
Тормозная система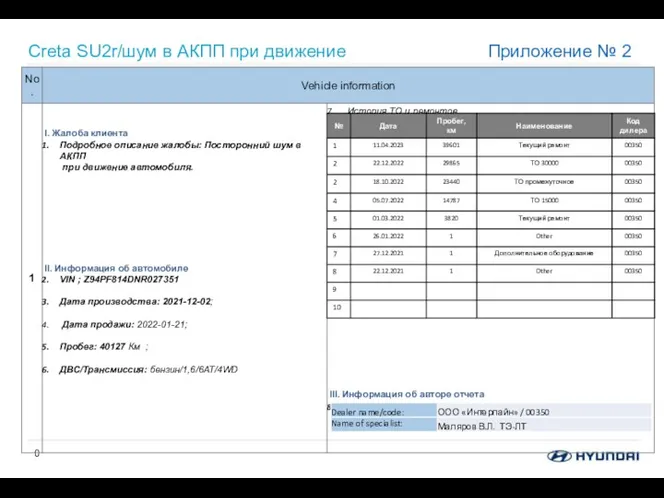 Creta SU2r/шум в АКПП при движение
Creta SU2r/шум в АКПП при движение Состав ядра. Ядерные силы
Состав ядра. Ядерные силы Элементарные частицы. Античастицы
Элементарные частицы. Античастицы Презентация.Реактивное движение
Презентация.Реактивное движение Архимедова сила
Архимедова сила М.В.Ломоносов
М.В.Ломоносов Испарение и конденсация. Кипение жидкости. Подготовка к ГИА
Испарение и конденсация. Кипение жидкости. Подготовка к ГИА Заземляющие устройства в установках высокого напряжение. (Лекция 17)
Заземляющие устройства в установках высокого напряжение. (Лекция 17) виды излучений. физика 11 класс
виды излучений. физика 11 класс Электрический ток в различных средах. Вещества
Электрический ток в различных средах. Вещества