Термодинамиканың бірінші бастамасы. Термодинамиканың бірінші бастамасын түрлі жылулық процестерге қолдану презентация
- Главная
- Физика
- Термодинамиканың бірінші бастамасы. Термодинамиканың бірінші бастамасын түрлі жылулық процестерге қолдану

Содержание
- 2. Энергияның сақталу заңы бойынша; Табиғатта энергия жоқтан пайда болмайды және жоғалмайды; ол тек бір түрден басқа
- 3. Изохоралық процесс. Бұл процесте газ көлемi өзгермейдi: V = const. Газдың iшкi энергиясының өзгерiсi оған берiлген
- 4. Изобаралық процесс. Изобаралық процесс кезiндегi газға берiлген жылу мөлшерi оның iшкi энергиясының бiрге өзгеруiне және қысым
- 5. Жаңа сабақты бекітуге арналған сұрақтар: 1. Егер сыртқы күштер идеал газбен, уақыттың кез келген мезетінде атқарылған
- 6. Тест сұрақтары: Газ заңдары дегеніміз не? Параметрлерінің біреуінің мәні өзгермей қалған кездегі процестер Газдың бір параметрінің
- 7. 6. Менделеев-Клапейрон теңдеуі: a. P=nKT b. P1V1=P2V2 c. 7. Молекула жылдамдығын алғаш өлшеген ғалым a. Штерн
- 8. Үй тапсырмасы: Есеп шығару: А.П.Рымкевичтің «Физика есептерінің жинағы» № 626. Массасы m газ T –ға изобаралық
- 10. Скачать презентацию
Слайд 2
Энергияның сақталу заңы бойынша; Табиғатта энергия жоқтан пайда болмайды және жоғалмайды;
Энергияның сақталу заңы бойынша; Табиғатта энергия жоқтан пайда болмайды және жоғалмайды;
ол тек бір түрден басқа түрге, бір денеден басқа денеге ауысады, ал денелердің тұйық жүйесіндегі толық энергия өзгеріссіз қалады.
Термодинамиканың бірінші заңының формуласы: ∆U=A+Q
(мұнда ∆U – жүйенің ішкі энергиясының өзгеруі, A – сыртқы күштер жұмысы, Q – жүйеге берілген жылу мөлшері) тура термодинамикалық процесс нәтижесіндегі жүйенің ішкі энергиясының өзгеруін көрсетеді.
Термодинамиканың бірінші заңының формуласы: ∆U=A+Q
(мұнда ∆U – жүйенің ішкі энергиясының өзгеруі, A – сыртқы күштер жұмысы, Q – жүйеге берілген жылу мөлшері) тура термодинамикалық процесс нәтижесіндегі жүйенің ішкі энергиясының өзгеруін көрсетеді.
Слайд 3
Изохоралық процесс. Бұл процесте газ көлемi өзгермейдi: V = const. Газдың
Изохоралық процесс. Бұл процесте газ көлемi өзгермейдi: V = const. Газдың
iшкi энергиясының өзгерiсi оған берiлген жылу мөлшерiне тең: ΔU = Q. Егер газ қыздырылса , онда Q > 0 және ΔU > 0 – iшкi энергия ұлғаяды. Газды суытқан кезде: Q < 0 және ΔU < 0, оның iшкi энергиясы азаяды. Изохоралық процесс кезiнде газ көлемi өзгермейдi, демек, газдың жұмысы нөлге тең болады. Газдың iшкi энергиясының өзгерiсi оған берiлген жылу мөлшерiне тең болады.
Изотермалық процесс. Изотермалық процесс кезiнде газдың температурасы тұрақты болады (Т = const) және оның iшкi энергиясы өзгермейдi. Газға берiлген барлық жылу мөлшерi пайдалы жұмыс атқаруға жұмсалады: Q = А′. Газ белгiлi жылу мөлшерiн (Q > 0) алған кезде, ол оң жұмыс атқарады (А′ > 0). Керiсiнше, егер газ қоршаған ортаға жылу берсе, онда оның атқарған жұмысы терiс болып саналады. Изотермалық процесс кезiнде газдың температурасы тұрақты және iшкi энергиясы өзгермейдi. Газға берiлген барлық жылу мөлшерi пайдалы жұмыс жасауға жұмсалады.
Изотермалық процесс. Изотермалық процесс кезiнде газдың температурасы тұрақты болады (Т = const) және оның iшкi энергиясы өзгермейдi. Газға берiлген барлық жылу мөлшерi пайдалы жұмыс атқаруға жұмсалады: Q = А′. Газ белгiлi жылу мөлшерiн (Q > 0) алған кезде, ол оң жұмыс атқарады (А′ > 0). Керiсiнше, егер газ қоршаған ортаға жылу берсе, онда оның атқарған жұмысы терiс болып саналады. Изотермалық процесс кезiнде газдың температурасы тұрақты және iшкi энергиясы өзгермейдi. Газға берiлген барлық жылу мөлшерi пайдалы жұмыс жасауға жұмсалады.
Слайд 4
Изобаралық процесс. Изобаралық процесс кезiндегi газға берiлген жылу мөлшерi оның iшкi
Изобаралық процесс. Изобаралық процесс кезiндегi газға берiлген жылу мөлшерi оның iшкi
энергиясының бiрге өзгеруiне және қысым тұрақты болған кезде P = const жұмысты атқаруға шығындалады. Изобаралық процесс кезiнде газға берiлетiн жылу мөлшерi, онымен бiрге оның iшкi энергиясының өзгеруiне және қысым тұрақты болған кезде жасалынатын жұмысқа шығындалады.
Адиабаталық процесс. Қоршаған ортамен жылу алмасуы болмайтын жағдайда өтетiн жүйедегi изопроцесс адиабаталық процесс деп аталады. Адиабаталық процесс кезiнде жылу алмасу болмайды. Сонда жүйенiң iшкi энергиясы тек қана онымен жасалған жұмыстың есебiнен өзгередi.
Адиабаталық процесс кезiнде Q = 0 және жүйенiң iшкi энергиясының өзгеруi жұмыс атқару арқылы ғана жүредi: ΔU= А.
Адиабаталық процесс. Қоршаған ортамен жылу алмасуы болмайтын жағдайда өтетiн жүйедегi изопроцесс адиабаталық процесс деп аталады. Адиабаталық процесс кезiнде жылу алмасу болмайды. Сонда жүйенiң iшкi энергиясы тек қана онымен жасалған жұмыстың есебiнен өзгередi.
Адиабаталық процесс кезiнде Q = 0 және жүйенiң iшкi энергиясының өзгеруi жұмыс атқару арқылы ғана жүредi: ΔU= А.
Слайд 5
Жаңа сабақты бекітуге арналған сұрақтар:
1. Егер сыртқы күштер идеал газбен, уақыттың
Жаңа сабақты бекітуге арналған сұрақтар:
1. Егер сыртқы күштер идеал газбен, уақыттың
кез келген мезетінде атқарылған жұмыс газдың қоршаған денелерге беретін ΔQ жылу мөлшерінде тең болатындай етіп, жұмыс істесе, онда бұл процесс …………. деп аталады?
2. Егер идеал газ қоршаған денелерге жылу мөлшерін бергенде уақыттың кез келген мезетінде берілген жылу мөлшері газдың ішкі энергиясының ΔU өзгеруіне тең болса, онда процесс ………. деп аталады.
3. Идеал газдың жұмысы қай процессте нөлге тең?
4. Уақыттың кез келген мезетінде берілген жылу мөлшері газдың атқарған жұмысына тең болатындай етіп, идеал газға жылу берілу қай процесте жүзеге асырылады?
5. Термодинамиканың бірінші заңында қандай заң жатыр?
6. Изотермиялық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңдер.
7. Изохоралық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңдер.
8. Изобаралық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңіз.
9. Газдың сығылу жұмысы оның ішкі энергиясының өзгерісіне тең болып шықты. Бұл қандай процеске сәйкес келеді?
10. Қандай процесс кезінде ең көп жұмыс атқарылады?
2. Егер идеал газ қоршаған денелерге жылу мөлшерін бергенде уақыттың кез келген мезетінде берілген жылу мөлшері газдың ішкі энергиясының ΔU өзгеруіне тең болса, онда процесс ………. деп аталады.
3. Идеал газдың жұмысы қай процессте нөлге тең?
4. Уақыттың кез келген мезетінде берілген жылу мөлшері газдың атқарған жұмысына тең болатындай етіп, идеал газға жылу берілу қай процесте жүзеге асырылады?
5. Термодинамиканың бірінші заңында қандай заң жатыр?
6. Изотермиялық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңдер.
7. Изохоралық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңдер.
8. Изобаралық процесс үшін термодинамиканың бірінші заңының математикалық өрнегін көрсетіңіз.
9. Газдың сығылу жұмысы оның ішкі энергиясының өзгерісіне тең болып шықты. Бұл қандай процеске сәйкес келеді?
10. Қандай процесс кезінде ең көп жұмыс атқарылады?
Слайд 6
Тест сұрақтары:
Газ заңдары дегеніміз не?
Параметрлерінің біреуінің мәні өзгермей қалған кездегі процестер
Газдың
Тест сұрақтары:
Газ заңдары дегеніміз не?
Параметрлерінің біреуінің мәні өзгермей қалған кездегі процестер
Газдың
бір параметрінің мәні тағайындалып қалған екі мәндер арасындағы сандық тәуелділік
Газдың екі параметрлерінің мәні тұрақты болған кездегі процестер
2. Бір атомды идеал газдың ішкі энергиясын анықтайтын формула
ΔU=A+Q
U=RT
U=3m/2M RT
3. Адиабаталық процесс
Параметрінің біреуінің мәні өзгермей қалған кезде өтетін процесс
Қысым тұрақты болған кезде термодинамика жүйе күйінің өзгеру процессі
Жылу алмайтын, жылу бермейтін процесс
4. Термодинамика ғылымы нені зерттейді?
Жұмыс атқармай энергияның бір денеден екінші денеге берілу процессі
Жылу құбылыстарына арналған энергияның сақталу заңы
Денелердің молекулалық құрылымы ескерілмейтін жылулық процестер теориясы
5. Ішкі энергия дегеніміз не?
Барлық молекулалардың кинетикалық энергиясымен осы бөлшектердің өзара әсерлесуін потенциялдық энергиясының қосындысына тең
Жылу алмасу (жылу беру) кезінде дене алатын не жоғалтатын энергия
Механикалық жұмыс жасау кезінде дененің энергия бөлуі
Газдың екі параметрлерінің мәні тұрақты болған кездегі процестер
2. Бір атомды идеал газдың ішкі энергиясын анықтайтын формула
ΔU=A+Q
U=RT
U=3m/2M RT
3. Адиабаталық процесс
Параметрінің біреуінің мәні өзгермей қалған кезде өтетін процесс
Қысым тұрақты болған кезде термодинамика жүйе күйінің өзгеру процессі
Жылу алмайтын, жылу бермейтін процесс
4. Термодинамика ғылымы нені зерттейді?
Жұмыс атқармай энергияның бір денеден екінші денеге берілу процессі
Жылу құбылыстарына арналған энергияның сақталу заңы
Денелердің молекулалық құрылымы ескерілмейтін жылулық процестер теориясы
5. Ішкі энергия дегеніміз не?
Барлық молекулалардың кинетикалық энергиясымен осы бөлшектердің өзара әсерлесуін потенциялдық энергиясының қосындысына тең
Жылу алмасу (жылу беру) кезінде дене алатын не жоғалтатын энергия
Механикалық жұмыс жасау кезінде дененің энергия бөлуі
Слайд 7
6. Менделеев-Клапейрон теңдеуі:
a. P=nKT
b. P1V1=P2V2
c.
7. Молекула жылдамдығын алғаш өлшеген ғалым
a. Штерн
b. Шарль
Гей-Люссак
8. Термодинамиканың бірінші заңы
a. Денелердің
6. Менделеев-Клапейрон теңдеуі:
a. P=nKT
b. P1V1=P2V2
c.
7. Молекула жылдамдығын алғаш өлшеген ғалым
a. Штерн
b. Шарль
Гей-Люссак
8. Термодинамиканың бірінші заңы
a. Денелердің
молекулалық құрылымы ескерілмейтін жылулық процестер теориясы
b. Жылу құбылыстарына арналған энергияның сақталу заңы*
c. Ішкі энергияның механикалық түрге айналу процесін көрсететін заң
b. Жылу құбылыстарына арналған энергияның сақталу заңы*
c. Ішкі энергияның механикалық түрге айналу процесін көрсететін заң
Слайд 8
Үй тапсырмасы:
Есеп шығару: А.П.Рымкевичтің «Физика есептерінің жинағы»
№ 626.
Үй тапсырмасы:
Есеп шығару: А.П.Рымкевичтің «Физика есептерінің жинағы»
№ 626.
Массасы m газ T –ға изобаралық түрде қыздырылды. 1) Газдың істеген А жұмысын; 2) газға берілген Q жылу мөлшерін; 3) ішкі энергияның өзгерісін анықтаңдар.
№ 627. 800 моль газды 500 К-ге изобаралық қыздыру үшін 9,4 МДж жылу мөлшері берілді. Газдың жұмысын және ішкі энергиясының өсімшесін табыңдар.
№ 627. 800 моль газды 500 К-ге изобаралық қыздыру үшін 9,4 МДж жылу мөлшері берілді. Газдың жұмысын және ішкі энергиясының өсімшесін табыңдар.







 Cәләтле балаларны үстерү
Cәләтле балаларны үстерү Организация участка по ремонту и настройке топливной аппаратуры дизельных двигателей
Организация участка по ремонту и настройке топливной аппаратуры дизельных двигателей Физическая викторина 7-8 классы.
Физическая викторина 7-8 классы. Основні уявлення про силу, момент сили
Основні уявлення про силу, момент сили Физические основы магнитного метода контроля
Физические основы магнитного метода контроля Электротехническое материаловедение
Электротехническое материаловедение Электромагнитные колебания и волны. Разбор задач ЕГЭ
Электромагнитные колебания и волны. Разбор задач ЕГЭ Улаштування та технічне обслуговування гальм з гідроприводом. Влаштування та ТО гальм з пневмоприводом (8)
Улаштування та технічне обслуговування гальм з гідроприводом. Влаштування та ТО гальм з пневмоприводом (8) Физическая игра Счастливый случай. 8 класс
Физическая игра Счастливый случай. 8 класс Виды электрических схем и их компонентов
Виды электрических схем и их компонентов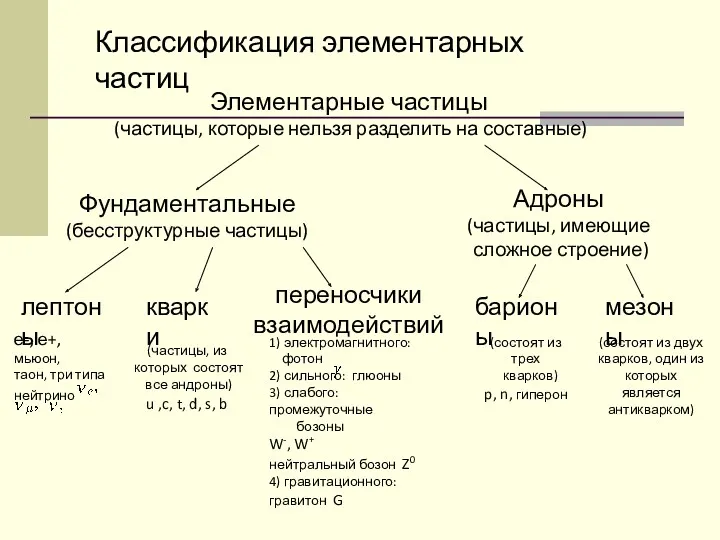 конспект урока по теме Мир элементарных частиц
конспект урока по теме Мир элементарных частиц Испарение и конденсация
Испарение и конденсация Тема: Взаємодія тіл. Виштовхувальна сила. Закон Архімеда
Тема: Взаємодія тіл. Виштовхувальна сила. Закон Архімеда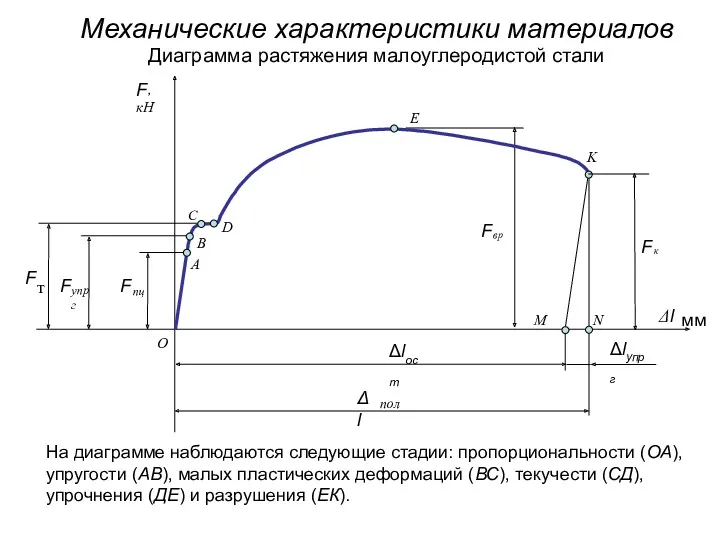 Механические характеристики материалов
Механические характеристики материалов Экспериментальное исследование явления поляризации света
Экспериментальное исследование явления поляризации света Основное уравнение молекулярно-кинетической теории
Основное уравнение молекулярно-кинетической теории Зависимость ускорения свободного падения от длины нити маятника
Зависимость ускорения свободного падения от длины нити маятника Износостойкие материалы
Износостойкие материалы Проводниковые материалы
Проводниковые материалы 20230930_sila_treniya
20230930_sila_treniya Сила трения. Трение в природе и технике. 9 класс
Сила трения. Трение в природе и технике. 9 класс Көч – җисемнәрнең үзара тәэсир итешү үлчәме ул
Көч – җисемнәрнең үзара тәэсир итешү үлчәме ул Грузозахватные устройства и приспособления
Грузозахватные устройства и приспособления Инфракрасное излучение
Инфракрасное излучение O’zbekiston Respublikasi Oliy va o’rta maxsus ta’lim vazirligi
O’zbekiston Respublikasi Oliy va o’rta maxsus ta’lim vazirligi Ядерные реакии
Ядерные реакии Тепловые явления. 8 класс
Тепловые явления. 8 класс Проект дільниці механічної обробки пуансонотримача
Проект дільниці механічної обробки пуансонотримача