Содержание
- 2. На рис. изображены экспериментальные кривые зависимости произведения pV от p при Т = const для водорода
- 3. МКТ идеального газа не объясняет этой закономерности. Самым простым из них и вместе с тем дающим
- 4. Атомы и молекулы вещества – сложные системы движущихся заряженных частиц, между которыми действуют силы притяжения и
- 5. Поправка на собственный объем молекул (учет сил отталкивания). В уравнении состояния идеального газа для моля Vμ
- 6. В расчете на одну молекулу, недоступным оказывается объем, равный учетверенному объему одной молекулы. Для всех молекул,
- 7. Можно получить, что внутренне давление обратно пропорционально квадрату молярного объема: Таким образом, уравнение состояния реального газа
- 8. Теоретические и экспериментальные изотермы реального газа. Фазовые превращения Рассмотрим теоретические изотермы реального газа, описываемые уравнением Ван-дер-Ваальса.
- 9. Семейство теоретических изотерм Ван-дер-Ваальса для некоторых значений температур. При высоких температурах эти изотермы мало отличаются от
- 10. При повышении температуры максимум и минимум на завитке сближаются и при некоторой температуре сливаются в одну
- 11. ВС – конденсация пара. Как видно из диаграммы, конденсация происходит при неизменном давлении рн, равном давлению
- 12. Если через крайние точки горизонтальных участков изотерм провести линию (рис. пунктир), получится колокообразная кривая. Эта кривая
- 13. Критическое состояние вещества – состояние, при котором исчезает различие между жидкостью и ее насыщенным паром (пар,
- 14. Внутренняя энергия реального газа Внутренняя энергия реального газа складывается из кинетической энергии хаотического движения молекул и
- 15. Работа консервативных сил притяжения равна убыли потенциальной энергии газа Проинтегрируем выражение Константу С выберем так, чтобы
- 16. Таким образом, внутренняя энергия одного моля газа равна При расширении реального газа в пустоту в адиабатических
- 18. Скачать презентацию
 Плоские электромагнитные волны. Устройство и параметры однородных линий передач
Плоские электромагнитные волны. Устройство и параметры однородных линий передач Основные операции при склеивании
Основные операции при склеивании Правило левой руки
Правило левой руки Свободные и вынужденные электромагнитные колебания. Колебательный контур
Свободные и вынужденные электромагнитные колебания. Колебательный контур Типы волоконной оптики, способы изготовления и применения
Типы волоконной оптики, способы изготовления и применения Давление. Сила давления
Давление. Сила давления Кинетика химических превращений. (Тема 4.3)
Кинетика химических превращений. (Тема 4.3) Образование плоских стержневых систем. Их элементы и связи. Лекция 2
Образование плоских стержневых систем. Их элементы и связи. Лекция 2 Дисциплина: Инженерная механика. Введение
Дисциплина: Инженерная механика. Введение Презентация по теме Закон всемирного тяготения
Презентация по теме Закон всемирного тяготения Молекулярно-кинетические представления о строении тел (лекция № 10)
Молекулярно-кинетические представления о строении тел (лекция № 10) Батарейка своими руками
Батарейка своими руками Многоэлектронные атомы. Взаимодействие атомов с излучением
Многоэлектронные атомы. Взаимодействие атомов с излучением Соединения деталей машин
Соединения деталей машин Жалпы физика курсы, жоғарғы оқу орындарындағы физикалық білімнің іргетасы бола отырып
Жалпы физика курсы, жоғарғы оқу орындарындағы физикалық білімнің іргетасы бола отырып Конспект и презентация урока по темеПервоначальные сведения о строении вещества
Конспект и презентация урока по темеПервоначальные сведения о строении вещества Магнитное поле. Лекция 3а
Магнитное поле. Лекция 3а Плотность вещества
Плотность вещества Гибридные двигатели
Гибридные двигатели Основные параметры метода контроля
Основные параметры метода контроля Молекулярная физика и термодинамика. Молекулярная физика
Молекулярная физика и термодинамика. Молекулярная физика Динамика идеальной жидкости
Динамика идеальной жидкости Викторина Что, Где, Когда, Почему?
Викторина Что, Где, Когда, Почему? Допустимі навантаження на грунт. Методи кількісної оцінки ступеня стійкості укосів і схилів. (Лекція 8)
Допустимі навантаження на грунт. Методи кількісної оцінки ступеня стійкості укосів і схилів. (Лекція 8) Планетарные передачи
Планетарные передачи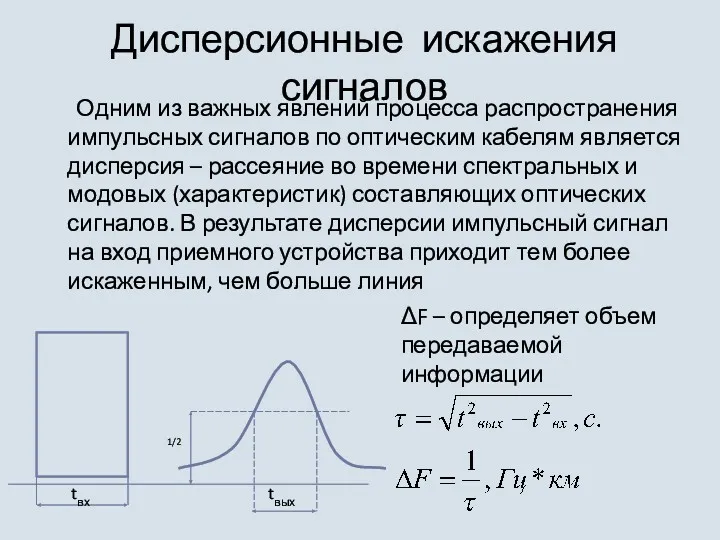 Дисперсионные искажения сигналов
Дисперсионные искажения сигналов Two types of transformers
Two types of transformers Интерференция. Подготовка к ЕГЭ
Интерференция. Подготовка к ЕГЭ