Содержание
- 2. МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ ПРИКАЗ 25 ноября 2002 г N 363 ОБ УТВЕРЖДЕНИИ ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
- 3. Определить показание к гемотрансфузии
- 4. ЭРИТРОЦИТЫ Потеря 25 - 30% объема циркулирующей крови; Снижением уровня гемоглобина ниже 70 - 80 г/л
- 5. ПЛАЗМА а) острый ДВС-синдром, осложняющий течение шоков различного генеза (септического, геморрагического, гемолитического) или вызванный другими причинами
- 6. г) передозировка антикоагулянтов непрямого действия (дикумарин и другие); д) терапевтический плазмаферез у пациентов с тромботической тромбоцитопенической
- 7. Показания к трансфузии тромбоцитов определяет лечащий врач на основании анализа клинической картины и причин тромбоцитопении, степени
- 8. 2. Собрать гемотрансфузионный анамнез Трансфузии были/не были Трансфузии по индивидуальному подбору в прошлом: были/не были Реакции
- 9. 3. Получить согласие больного на гемотрансфузию Врач, производящий трансфузию компонентов крови, обязан, независимо от произведенных ранее
- 10. 4. Первичное определение групповой принадлежности Определить группу крови система АВО реципиента простой методикой (цоликлоны) п.18 приказа
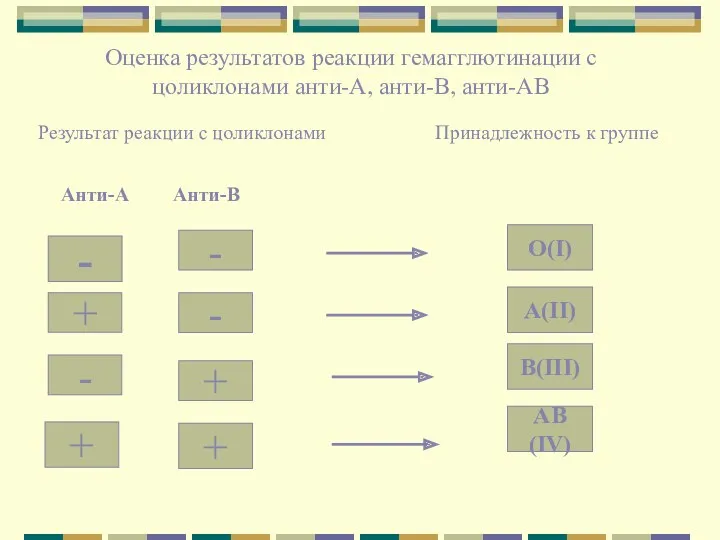
- 11. Оценка результатов реакции гемагглютинации с цоликлонами анти-А, анти-В, анти-АВ Результат реакции с цоликлонами Принадлежность к группе
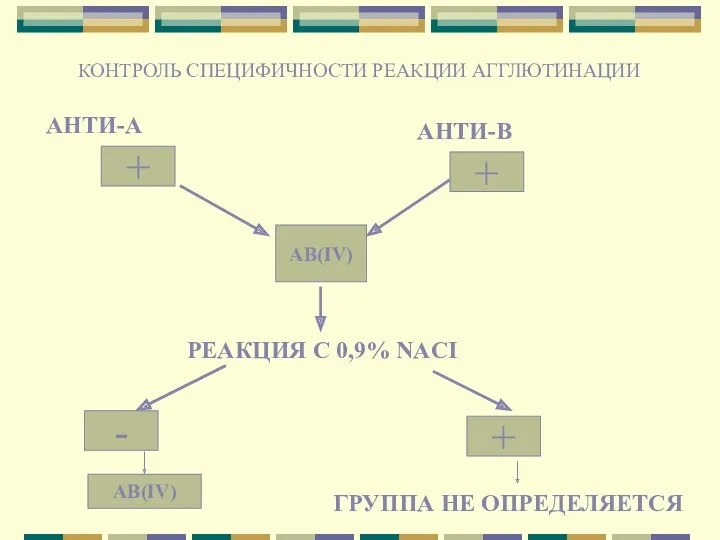
- 12. КОНТРОЛЬ СПЕЦИФИЧНОСТИ РЕАКЦИИ АГГЛЮТИНАЦИИ АНТИ-А АНТИ-В + + АB(IV) РЕАКЦИЯ С 0,9% NACI АВ(IV) ГРУППА НЕ
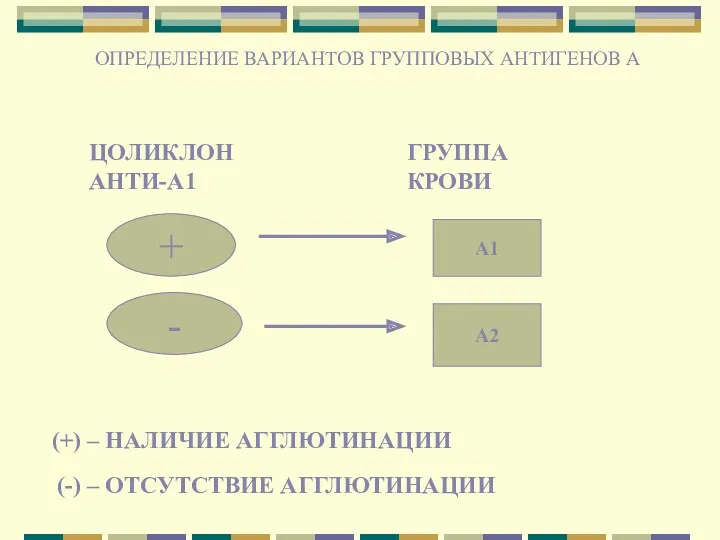
- 13. ОПРЕДЕЛЕНИЕ ВАРИАНТОВ ГРУППОВЫХ АНТИГЕНОВ А ЦОЛИКЛОН АНТИ-А1 ГРУППА КРОВИ А1 A2 + - (+) – НАЛИЧИЕ
- 14. 5. Определить резус - принадлежность реципиента (цоликлон анти – D - СУПЕР)
- 15. 6. Получить лабораторное подтверждение групповой и резус – принадлежности Первичный экстренный пациент: Подтверждение группы крови АВО
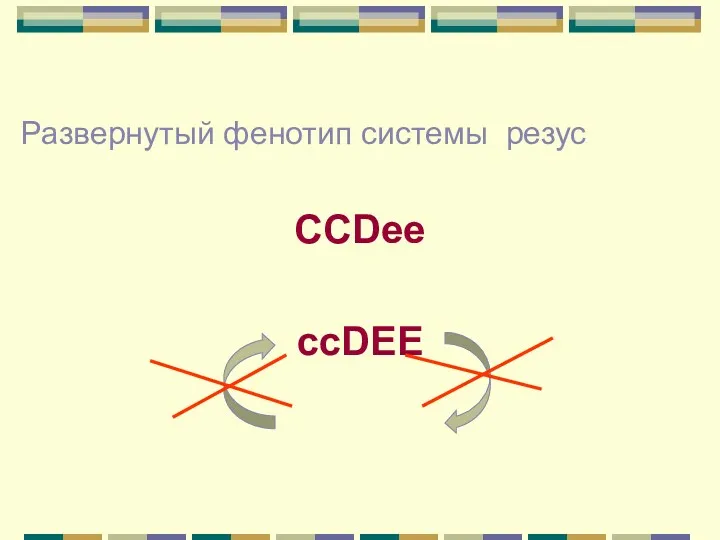
- 16. Развернутый фенотип системы резус ССDee ccDEE
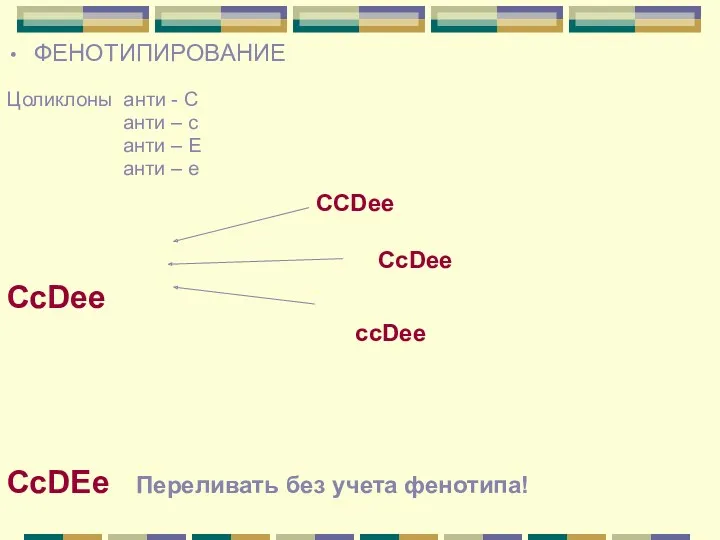
- 17. ФЕНОТИПИРОВАНИЕ Цоликлоны анти - С анти – с анти – Е анти – е СсDee СсDEe
- 18. После получения лабораторного подтверждения, информация о групповой и резус принадлежности больного выносится на титульный лист истории
- 19. 7. Переопределить группу крови из контейнера
- 20. 8. Провести пробы на совместимость (in vitra) - на плоскости (холодовая) 2-3 капли сыворотки реципиента 1
- 21. - в пробирке (тепловая) В пробирку вносят 1 небольшую каплю (0,02-0,03 мл) эритроцитов донора и касаются
- 22. 9. Провести пробу на индивидуальную совместимость (биологическая проба) in viva Биологическая проба проводится посредством однократного переливания
- 23. При индивидуальном подборе определяются фенотип донора и реципиента, устанавливается наличие и специфичность антител в крови реципиента
- 24. 10. Фиксировать время начала и окончания трансфузии 11. После окончания гемотрансфузии наблюдать за больным в течение
- 25. 12. Общий анализ крови через 12 часов. 13.Пробирка с кровью реципиента, взятая до трансфузии и гемакон
- 26. Благодарю за внимание!
- 27. Национальный стандарт Российской федерации Кровь донорская и ее компоненты. Контейнеры с консервированной кровью и ее компонентами.
- 28. Виды маркировки: технологическая (промежуточная); маркировка готовой продукции; маркировка несоответствующей продукции (непригодной к переливанию реципиенту); - клиническая
- 29. Клиническая маркировка Применяется в лечебных учреждениях для информирования медицинского персонала о подборе компонента крови для конкретного
- 30. ТРЕБОВАНИЯ К КЛИНИЧЕСКОЙ МАРКИРОВКЕ: нанесена разборчивым почерком или с помощью печатного устройства; сохраняться до окончания проведения
- 31. ТРЕБОВАНИЯ К КЛИНИЧЕСКОЙ МАРКЕРОВКЕ: обеспечивать точную идентификацию пациента, к которому относятся информационные или разрешительные надписи (полностью
- 32. Этикетка, предназначенная для клинической маркировки, может быть предварительно наклеена или прикреплена другим способом к контейнеру с
- 33. Клиническая этикетка должна содержать следующую информацию: Описание компонента крови: номер контейнера, наименование компонента крови, - группа
- 34. 2. Описание реципиента: фамилия, имя, отчество реципиента, наименование отделения, в котором пациент получает лечение, номер палаты
- 35. 3. Описание процедуры индивидуального подбора: наименование процедуры, ее результат, фамилия, инициалы и подпись лица, проводившего индивидуальный
- 37. Скачать презентацию





























 Постепенная потеря зрения
Постепенная потеря зрения Лечение огнестрельных ранений живота
Лечение огнестрельных ранений живота Офтальмология. Заболевание иридоциклит
Офтальмология. Заболевание иридоциклит Синдром Внезапной Смерти Младенцев
Синдром Внезапной Смерти Младенцев Заболевания толстой кишки
Заболевания толстой кишки Общественное здоровье. Лекция 3. Планирование в здравоохранении
Общественное здоровье. Лекция 3. Планирование в здравоохранении Острая почечная недостаточность (ОПН)
Острая почечная недостаточность (ОПН) Санаторно-курортное обслуживание населения в СССР
Санаторно-курортное обслуживание населения в СССР Инструментальные методы диагностики в гастроэнтерологии. Фиброгастродуоденоскопия
Инструментальные методы диагностики в гастроэнтерологии. Фиброгастродуоденоскопия Жатыр мойнының қатерлі ісігі жүктілік кезінде
Жатыр мойнының қатерлі ісігі жүктілік кезінде Консервированные корма для кошек и собак
Консервированные корма для кошек и собак Роль ультразвукового исследования в дифференциальной диагностики синдрома острой мошонки у детей
Роль ультразвукового исследования в дифференциальной диагностики синдрома острой мошонки у детей Жүректің ишемиялық аурулары кезіндегі ультрадыбыстық зерттеулер
Жүректің ишемиялық аурулары кезіндегі ультрадыбыстық зерттеулер Организация медицинской помощи взрослым пациентам с гемофилией
Организация медицинской помощи взрослым пациентам с гемофилией Ботулизм
Ботулизм Логопедия. Дизартрия
Логопедия. Дизартрия Регенерация тканей и органов (стволовые клетки)
Регенерация тканей и органов (стволовые клетки) Роль акушерки в профилактике геморрагического шока в послеродовом периоде
Роль акушерки в профилактике геморрагического шока в послеродовом периоде Restauration d'une dent pulpée
Restauration d'une dent pulpée Ювенильді идиопатиялық артрит емінде адам иммуноглобулинін тағайындау
Ювенильді идиопатиялық артрит емінде адам иммуноглобулинін тағайындау Строение кожи
Строение кожи Регенерация костной ткани
Регенерация костной ткани Медикалық-генетикалық кеңес. Пренатальдық диогностика әдістері
Медикалық-генетикалық кеңес. Пренатальдық диогностика әдістері Острая сердечная недостаточность (ОСН)
Острая сердечная недостаточность (ОСН) Вспомогательные вещества. Значение в фармацевтической технологии
Вспомогательные вещества. Значение в фармацевтической технологии Рентгенография. Показания к рентгенографии
Рентгенография. Показания к рентгенографии Инфекции дыхательных путей
Инфекции дыхательных путей Тики (тикозные гиперкинезы)
Тики (тикозные гиперкинезы)