Содержание
- 2. Введение В пособии рассматриваются основные понятия, связанные с химиотерапией, основные группы антибиотиков. Особое внимание уделено механизмам
- 3. Место антибиотиков в фармакотерапии инфекционных заболеваний Противомикробное средство – лекарственное средство, губительно действующее на микроорганизмы В
- 4. Избирательность противомикробного действия Избирательность противомикробного действия химиотерапевтических средств подразумевает: возможность подбора такой дозы препарата, которая, оказывая
- 5. Химиотерапевтическое средство, химиотерапия Противомикробное* химиотерапевтическое средство – лекарственное средство, избирательно подавляющее жизнедеятельность микроорганизмов химиотерапия – лечение
- 6. Классификация химиотерапевтических средств Химиотерапевтические средства в зависимости от происхождения делятся на: химиотерапевтические средства природного происхождения (антибиотики)
- 7. Антибиотики Антибиотики – химиотерапевтические средства естественного происхождения, а также их производные или синтетические аналоги.
- 8. Памятные даты в истории антибиотиков На возможность применения продуктов жизнедеятельности микроорганизмов в лечебных целях одними из
- 9. Памятные даты в истории антибиотиков (продолжение) В 1942 г. З.В. Ермольева получила крустозин (советский пенициллин) В
- 10. История антибиотиков после 1963г. Процесс открытия новых антибиотических структур продолжается и в настоящее время. Так, за
- 11. А.Флеминг (1881-1955). В 1929 г. открыл пенициллин
- 12. Зинаида Виссарионовна Ермольева (1898-1974) Автор первого отечественного пенициллина (1942)
- 13. Принципы химиотерапии (антибиотикотерапии) выбор антибиотика должен осуществляться в соответствии с клинико-бактериологическим диагнозом и имеющимися у больного
- 14. Резистентность микроорганизма Первичная антибиотикорезистентность – устойчивость микроорганизма к химиотерапевтическому средству, существующая до начала лечения, т.е. связанная
- 15. Способы классификации антибиотиков По химической структуре По происхождению По спектру антимикробной активности По виду антимикробного действия
- 16. Происхождение антибиотиков Биосинтетические (природные) антибиотики – антибиотики, синтезирующиеся биологическим объектом. Чаще всего природные антибиотики выделяются из
- 17. Источники получения биосинтетических антибиотиков грибы (кроме актиномицетов) Penicillium – пенициллины Cephalosporium – цефалоспорины актиномицеты Streptomyces –
- 18. Спектр антимикробной активности Спектр антимикробной активности – перечень микроорганизмов, не имеющих первичной устойчивости к данному химиотерапевтическому
- 19. Виды химиотерапевтического действия Бактерицидное* действие – гибель возбудителей заболевания, обусловленная нарушением структурной целостности организма-мишени (нарушение синтеза
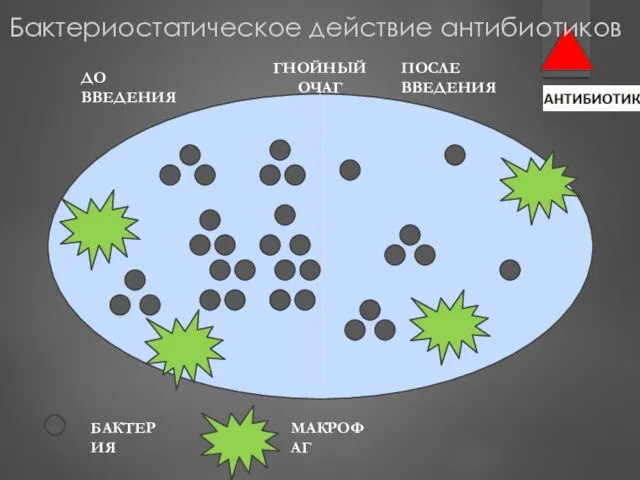
- 20. ГНОЙНЫЙ ОЧАГ БАКТЕРИЯ МАКРОФАГ ДО ВВЕДЕНИЯ ПОСЛЕ ВВЕДЕНИЯ Бактериостатическое действие антибиотиков
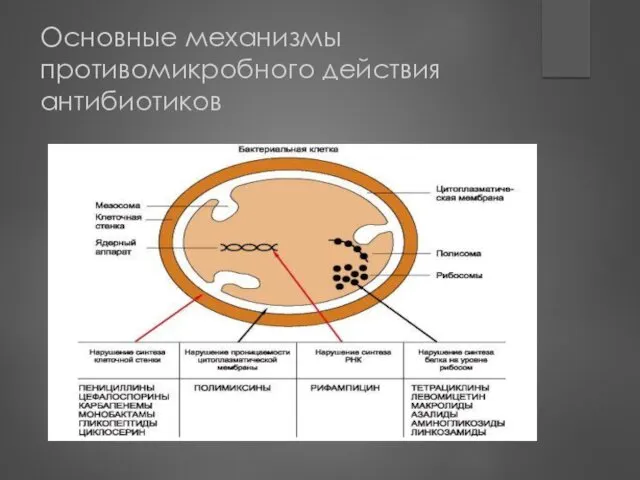
- 21. Возможные механизмы химиотерапевтического действия нарушение синтеза клеточной стенки нарушение проницаемости цитоплазматической мембраны нарушение трансляции белка на
- 22. Основные механизмы противомикробного действия антибиотиков
- 23. Поколения (генерации) антибиотиков Поколение – совокупность препаратов, принадлежащих к одной фармакотерапевтической группе, имеющих сходную химическую структуру
- 24. Препараты выбора и резерва Препарат выбора (антибиотик I ряда) – препарат, использующийся при данной патологии в
- 25. Классификация антибиотиков по химической структуре β-лактамные антибиотики Гликопептиды Макролиды Линкозамиды Амфениколы Тетрациклины Аминогликозиды Рифамицины Полимиксины Полиены
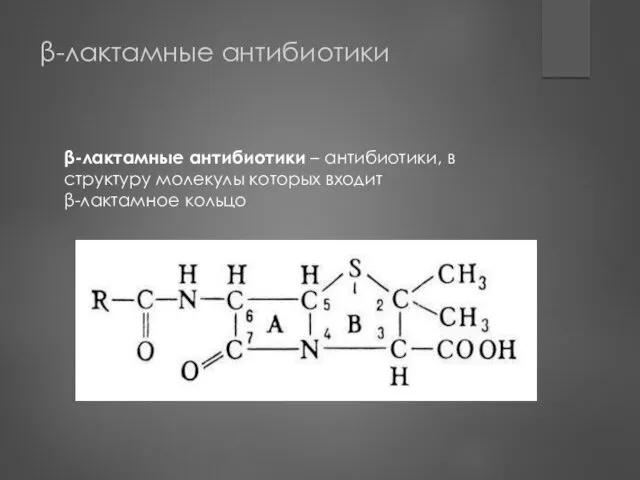
- 26. β-лактамные антибиотики β-лактамные антибиотики – антибиотики, в структуру молекулы которых входит β-лактамное кольцо
- 27. Классификация β-лактамных антибиотиков по химической структуре Пенициллины Цефалоспорины Карбапенемы* Монобактамы * Наряду с карбапенемами к этой
- 28. Первичная фармакологическая реакция (ПФР) бактерицидного эффекта β‑лактамных антибиотиков β‑лактамное кольцо является аналогом дипептида D-аланил-D-аланин, участвующего в
- 29. Пенициллинсвязывающие белки Пенициллинсвязывающие белки – структурные белки и белки-ферменты прокариотических клеток, способные специфически взаимодействовать с веществами,
- 30. Механизмы бактерицидного действия β‑лактамных антибиотиков Функции пенициллинсвязывающих белков, которые могут нарушаться β‑лактамными антибиотиками: синтез предшественников муреина
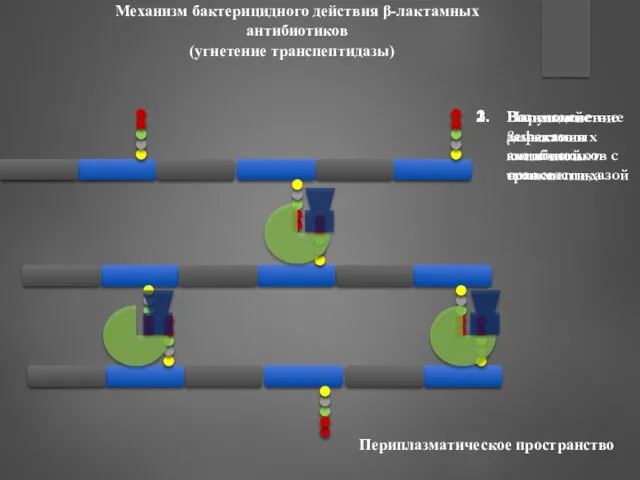
- 31. Механизм бактерицидного действия β‑лактамных антибиотиков – блокада транспептидазы Данный механизм для β‑лактамных антибиотиков является основным ПФР
- 32. Механизм бактерицидного действия β‑лактамных антибиотиков – включение в состав муреина ПФР – взаимодействие с ферментами, встраивающими
- 33. Механизм бактерицидного действия β‑лактамных антибиотиков – активация муреингидролазы ПФР – взаимодействие с ингибитором муреингидролазы на клеточной
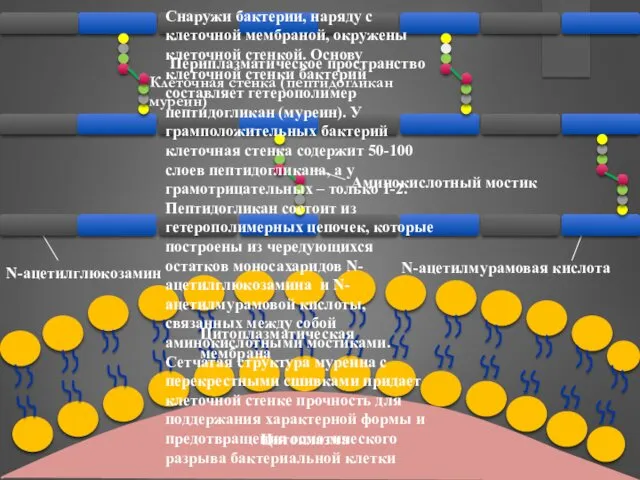
- 34. Цитоплазма Периплазматическое пространство Цитоплазматическая мембрана Снаружи бактерии, наряду с клеточной мембраной, окружены клеточной стенкой. Основу клеточной
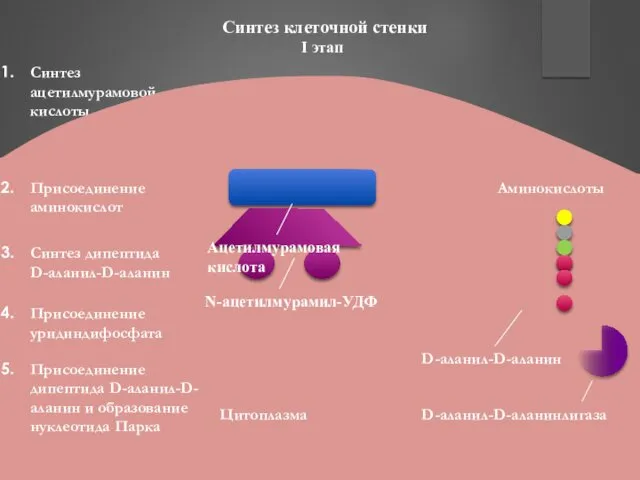
- 35. Аминокислоты Синтез клеточной стенки I этап Синтез ацетилмурамовой кислоты Присоединение аминокислот Синтез дипептида D-аланил-D-аланин Присоединение уридиндифосфата
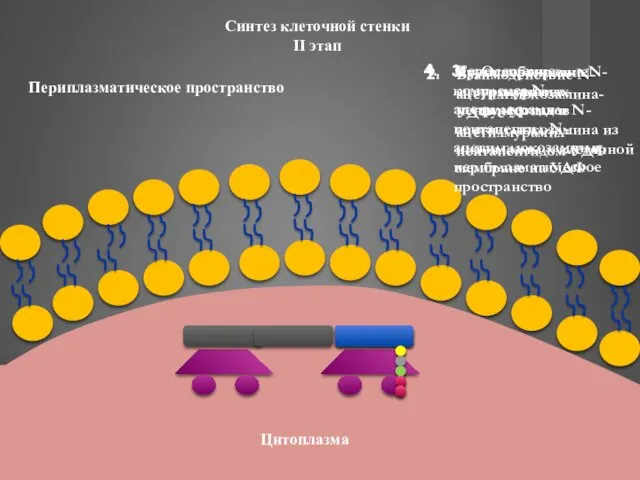
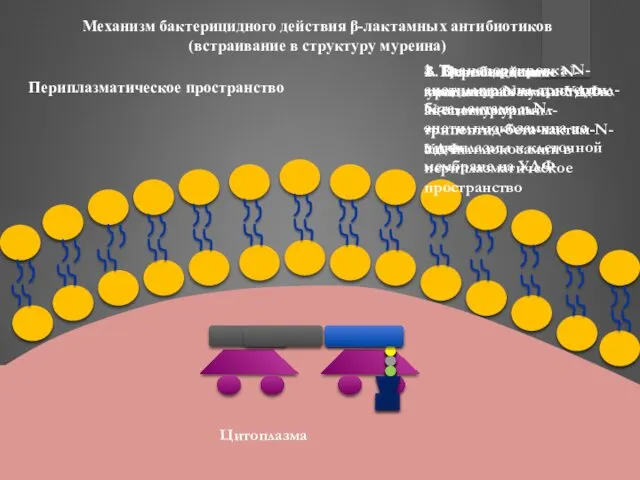
- 36. Синтез клеточной стенки II этап Транспортировка N-ацетилмурамил-пентапептида и N-ацетилглюкозамина из цитоплазмы к клеточной мембране на УДФ
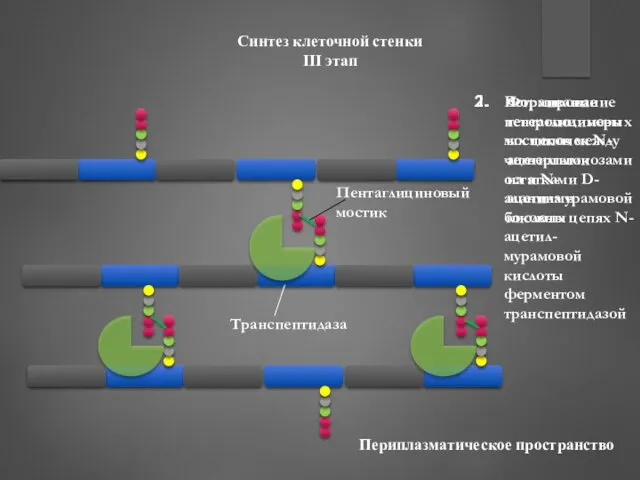
- 37. Синтез клеточной стенки III этап Формирование гетерополимерных цепочек N-ацетилглюкозамина и N- ацетилмурамовой кислоты Встраивание пентаглициновых мостиков
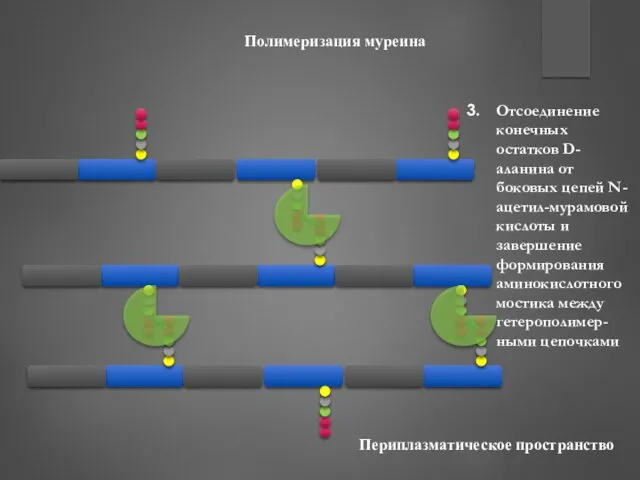
- 38. Полимеризация муреина Отсоединение конечных остатков D-аланина от боковых цепей N-ацетил-мурамовой кислоты и завершение формирования аминокислотного мостика
- 39. Механизм бактерицидного действия β-лактамных антибиотиков Взаимодействие β-лактамных антибиотиков с транспептидазой Нарушение замыкания аминокислот-ного мостика Возникновение дефектов
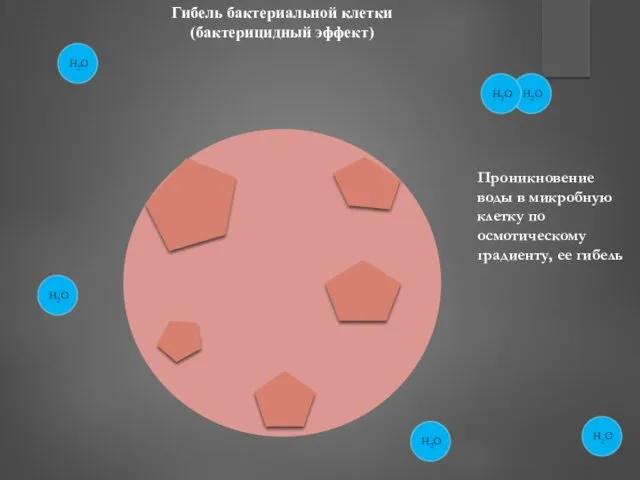
- 40. Гибель бактериальной клетки (бактерицидный эффект) Проникновение воды в микробную клетку по осмотическому градиенту, ее гибель
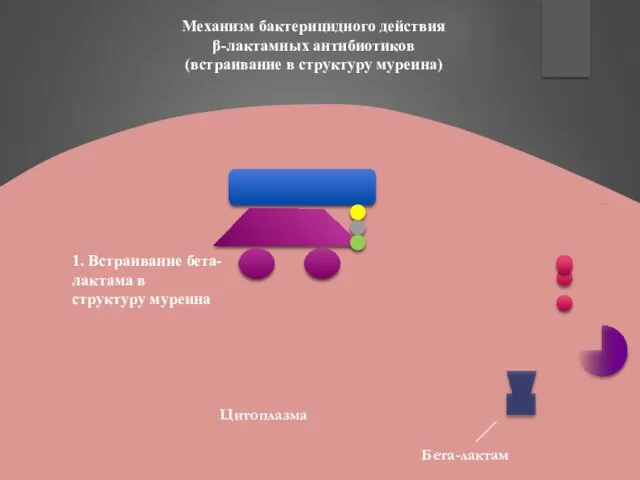
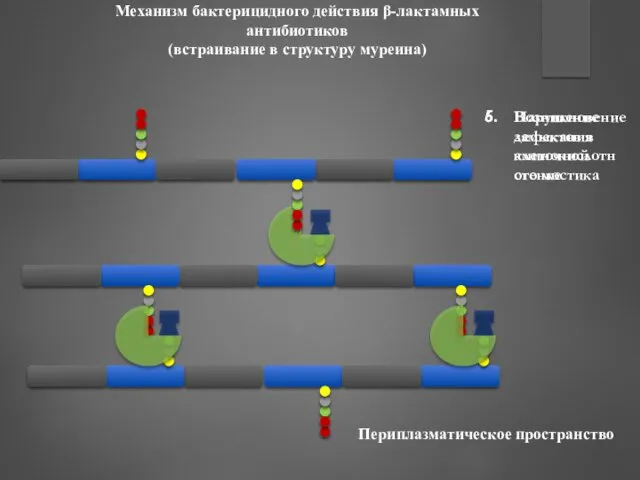
- 41. Механизм бактерицидного действия β-лактамных антибиотиков (встраивание в структуру муреина) 1. Встраивание бета-лактама в структуру муреина Цитоплазма
- 42. Механизм бактерицидного действия β-лактамных антибиотиков (встраивание в структуру муреина) 4. Перемещение комплекса N-ацетилмурамил-трипептид-бета-лактам-N-ацетилглюкозамин в периплазматическое пространство
- 43. Механизм бактерицидного действия β-лактамных антибиотиков (встраивание в структуру муреина) Нарушение замыкания аминокислотного мостика Возникновение дефектов в
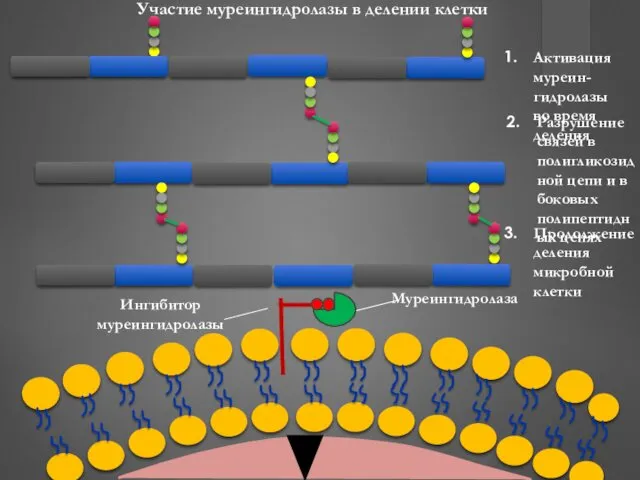
- 44. Участие муреингидролазы в делении клетки Активация муреин-гидролазы во время деления Разрушение связей в полигликозидной цепи и
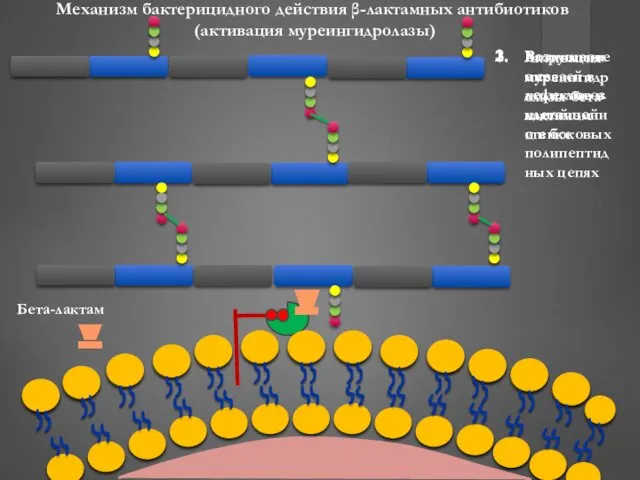
- 45. Механизм бактерицидного действия β-лактамных антибиотиков (активация муреингидролазы) Активация муреингидролазы бета-лактамом Разрушение связей в полигликозидной цепи и
- 46. Избирательность противомикробного действия β‑лактамных антибиотиков клеточная стенка у животных и человека отсутствует, ацетилмурамовая кислота не является
- 47. Нежелательные эффекты β-лактамных антибиотиков аллергические реакции – крапивница, лихорадка, бронхоспазм, васкулит, сывороточная болезнь, отек Квинке, эритродермия,
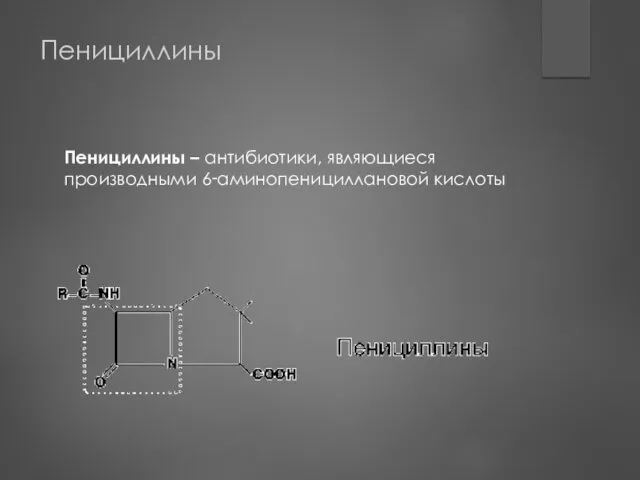
- 48. Пенициллины Пенициллины – антибиотики, являющиеся производными 6‑аминопенициллановой кислоты
- 49. Классификация пенициллинов по происхождению Биосинтетические Полусинтетические
- 50. Классификации биосинтетических пенициллинов по пути введения и продолжительности действия Кислотоустойчивые (вводятся внутрь) – феноксиметилпенициллин Кислотонеустойчивые (вводятся
- 51. Фармакокинетика биосинтетических пенициллинов разрушаются пенициллиназами разрушаются соляной кислотой, поэтому внутрь не применяются феноксиметилпенициллин не разрушается соляной
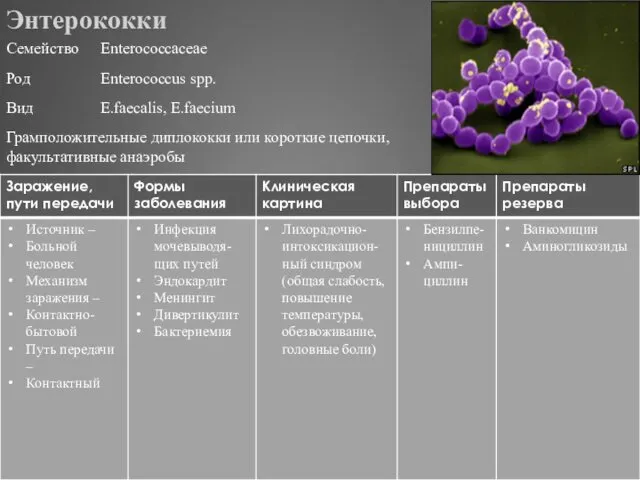
- 52. Спектр антимикробного действия биосинтетических пенициллинов Грамположительные кокки: стрептококки, пневмококки, энтерококки (устойчивы к низким концентрациям), стафилококки (большинство
- 53. Показания к назначению биосинтетических пенициллинов стрептококковые и пневмококковые инфекции – тонзиллофарингит, рожа, скарлатина, пневмококковая пневмония лептоспироз,
- 54. β-лактамазы β-лактамаза – бактериальный фермент расщепляющий β-лактамное кольцо и инактивирующий содержащий такое кольцо антибиотик β-лактамазы в
- 55. Классификация полусинтетических пенициллинов по химической структуре Изоксазолпенициллины – оксациллин, клоксациллин, флуклоксациллин Аминопенициллины – ампициллин, амоксициллин Амидинопенициллины
- 56. Изоксазолпенициллины Уступают биосинтетическим пенициллинам и аминопенициллинам в антимикробной активности Не разрушаются стафилококковыми β-лактамазами и способны блокировать
- 57. Аминопенициллины Действуют на грамположительные микроорганизмы: S.pyogenes, S.Pneumoniae, B.pertussis, C.diphtheria, L. monocytogenes, H.pylori, M.catarrhalis, S.aureus и некоторых
- 58. Особенности отдельных аминопенициллинов амоксициллин при приеме внутрь имеет биодоступность 80-90 %, в крови и тканях создает
- 59. Амидинопенициллины в спектр действия входят только грамотрицательные энтеробактерии – эшерихии, шигеллы, сальмонеллы, клебсиеллы, протей при энтеральном
- 60. Карбоксипенициллины и уреидопенициллины Спектр действия широкий, наибольшее значение имеет активность в отношении P.аeruginosa, но сейчас многие
- 61. «Защищенные» пенициллины «защищенные» пенициллины – комбинированные препараты, содержащие β-лактамы и ингибиторы β-лактамаз. Примеры препаратов амоксициллин/клавулановая кислота
- 62. Ингибиторы β-лактамаз ингибиторы β-лактамаз – вещества β-лактамной природы, обладающие минимальной антибактериальной активностью, но способные необратимо связываться
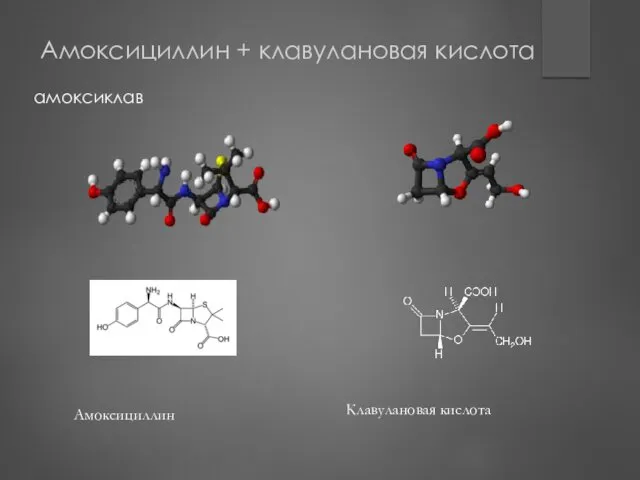
- 63. Амоксициллин + клавулановая кислота амоксиклав Клавулановая кислота Амоксициллин
- 64. Спектр антимикробного действия «защищенных» пенициллинов Грамположительные кокки: стафилококки (включая пенициллиноустойчивые штаммы S.aureus и S.epidermidis), стрептококки, энтерококки
- 65. Показания к назначению «защищенных» пенициллинов Бактериальные инфекции верхних и нижних дыхательных путей Инфекции желчевыводящих путей (острый
- 66. Нежелательные эффекты пенициллинов Общие для всех β-лактамных антибиотиков нежелательные эффекты гиперкалиемия при использовании бензилпенициллина калиевой соли
- 67. Противопоказания аллергическая реакция на пенициллины или другие β-лактамные антибиотики в анамнезе аллергическая реакция на прокаин или
- 68. Цефалоспорины Цефалоспорины – антибиотики, являющиеся производными 7‑аминоцефалоспорановой кислоты
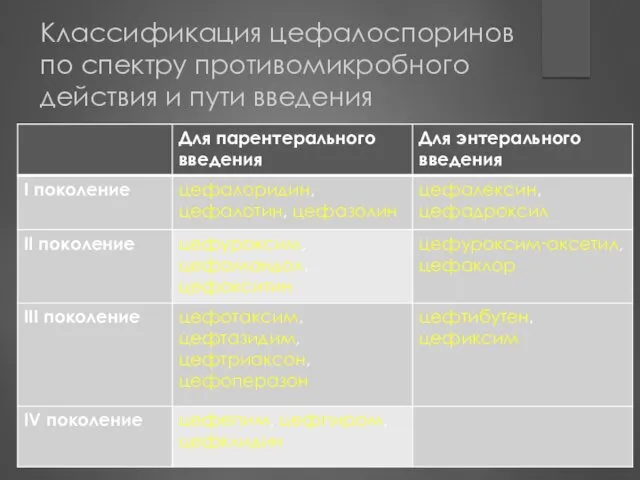
- 69. Классификация цефалоспоринов по спектру противомикробного действия и пути введения
- 70. Цефалоспорины I-го поколения Спектр антимикробного действия включает грамположительные бактерии и кокки кроме энтерококков и MRSA У
- 71. Цефалоспорины II-го поколения сохраняется активность против грамположительных микробов дополнительно в спектр включаются грамотрицательные бактерии Н.influenzae, М.catarrhalis,
- 72. Цефалоспорины III - поколения высокоактивны относительно грамотрицательной флоры, включая проблемные микроорганизмы: серрации, цитробактерии, индолполпожительные протеи, что
- 73. Цефалоспорины IV - поколения Спектр действия максимально широк. Одинаково активны относительно и грамотрицательной, и грамположительной флоры.
- 74. Нежелательные эффекты цефалоспоринов Общие для всех β-лактамных антибиотиков нежелательные эффекты нефротоксичность – у цефалоспоринов I-II поколений.
- 75. Противопоказания аллергическая реакция на цефалоспорины или другие β-лактамные антибиотики в анамнезе аллергическая реакция на прокаин или
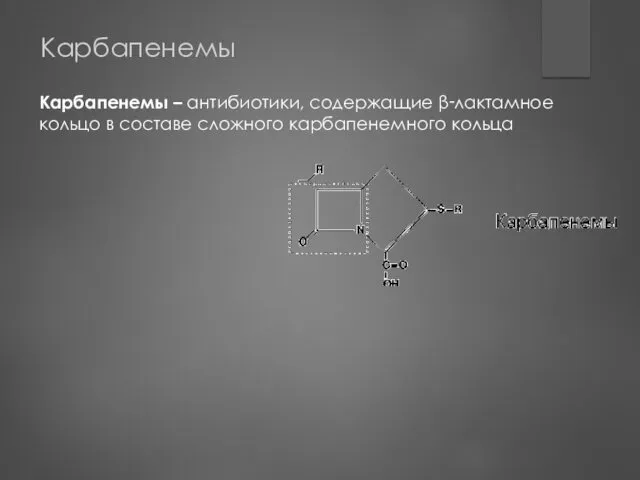
- 76. Карбапенемы Карбапенемы – антибиотики, содержащие β‑лактамное кольцо в составе сложного карбапенемного кольца
- 77. Классификация карбапенемов Долгое время использовался лишь имипенем, затем появились весьма сходные с ним меропенем и дорипенем.
- 78. Карбапенемы I-го поколения Спектр действия максимально широк, в т.ч. включает P.aeruginosa, но не включает MRSA и
- 79. Кратность введения – 1 раз в сутки Спектр антимикробного действия уже, чем у препаратов I поколения
- 80. Нежелательные эффекты карбапенемов Общие для всех β-лактамных антибиотиков нежелательные эффекты При применении более 2 недель имипенем
- 81. Монобактамы В настоящее время группа представлена одним синтетическим препаратом азтреонамом Монобактамы – антибиотики, содержащие в свей
- 82. Спектр антимикробного действия азтреонама Устойчив ко многим β-лактамазам, продуцируемым аэробной грамотрицательной флорой, но разрушается β-лактамазами стафилококков
- 83. Показания к назначению азтреонама Препарат резерва при инфекциях, вызванных аэробными грамотрицательными бактериями: инфекции мочевыделительной системы (пиелонефриты,
- 84. Противопоказания аллергическая реакция на азтреонам или другие β-лактамные антибиотики в анамнезе Нежелательные эффекты азтреонама Общие для
- 85. Эндотоксический шок эндотоксический шок – осложнение химиотерапии, проявляющееся критическим снижением артериального давления и возникающее при первом
- 86. Гликопептиды Гликопептиды - антибиотики, имеющие структуру гликопептидов (пептидогликанов), т.е. пептидов, содержащих аминокислотные остатки, к боковым цепям
- 87. Точки приложения гликопептидов Синтез клеточной стенки Проницаемость цитоплазматической мембраны Синтез РНК Последние два механизма практически не
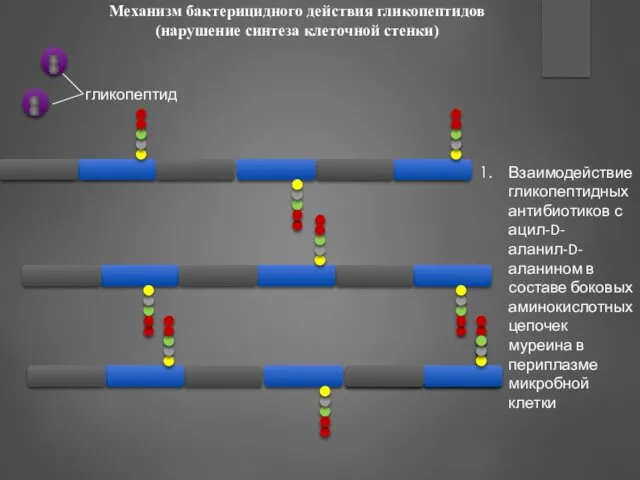
- 88. Механизм бактерицидного действия гликопептидов – нарушение синтеза клеточной стенки ПФР – взаимодействие с ацил-D-аланил-D-аланином в составе
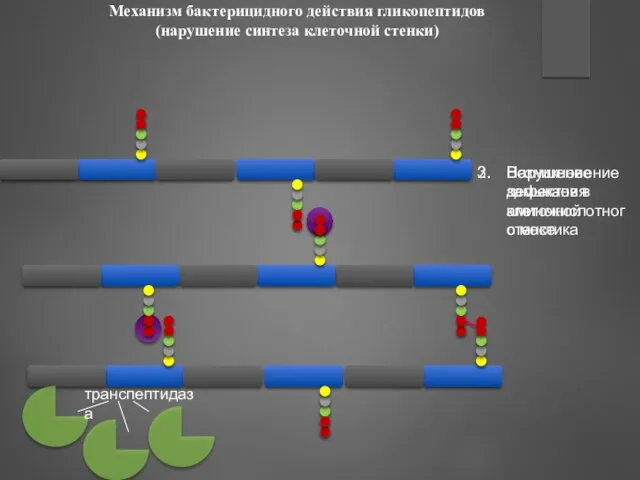
- 89. Механизм бактерицидного действия гликопептидов (нарушение синтеза клеточной стенки) Взаимодействие гликопептидных антибиотиков с ацил-D-аланил-D-аланином в составе боковых
- 90. Механизм бактерицидного действия гликопептидов (нарушение синтеза клеточной стенки) Нарушение замыкания аминокислотного мостика Возникновение дефектов в клеточной
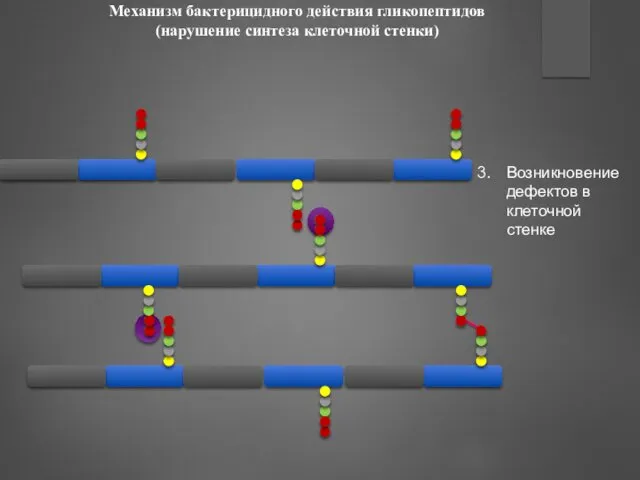
- 91. Механизм бактерицидного действия гликопептидов (нарушение синтеза клеточной стенки) Возникновение дефектов в клеточной стенке
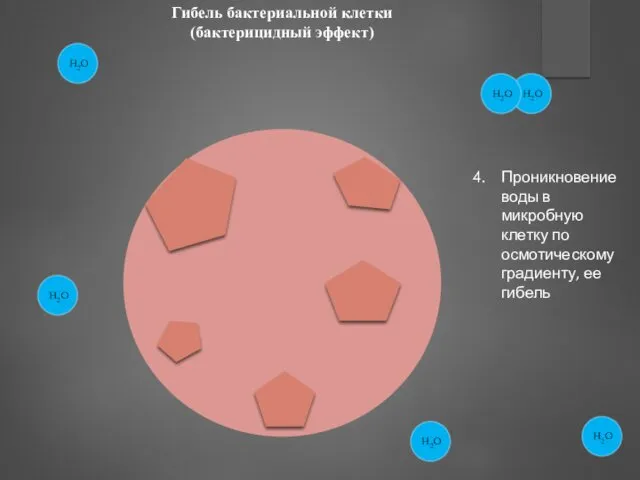
- 92. Гибель бактериальной клетки (бактерицидный эффект) Проникновение воды в микробную клетку по осмотическому градиенту, ее гибель
- 93. Избирательность противомикробного действия гликопептидов клеточная стенка у животных и человека отсутствует, D-аланин в обмене веществ не
- 94. Спектр антимикробного действия гликопептидов грамположительные аэробные и анаэробные микроорганизмы: стафилококки (включая MRSA), стрептококки, пневмококки, энтерококки, пептострептококки,
- 95. Показания к назначению гликопептидов Полирезистентные штаммы стафилококков и стрептококков Псевдомембранозный колит, вызванный C.difficile, в т.ч. на
- 96. Нежелательные эффекты гликопептидов Синдром «красной шеи» Нефротоксичность Ототоксичность Гематотоксичность Противопоказания Аллергическая реакция на гликопептиды I триместр
- 97. Условия назначения гликопептидов строгий расчет дозы на массу тела и соблюдение режима дозирования проведение терапевтического мониторинга
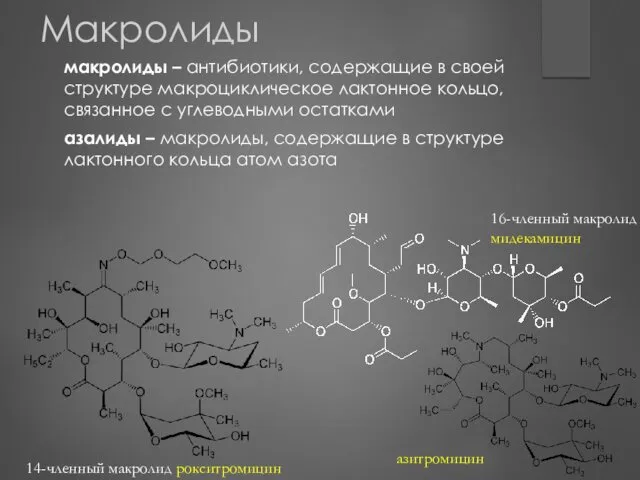
- 98. Макролиды макролиды – антибиотики, содержащие в своей структуре макроциклическое лактонное кольцо, связанное с углеводными остатками 14-членный
- 99. Механизм бактериостатического действия макролидов – нарушение синтеза белка ПФР – взаимодействие с ферментом пептидтранслоказа на большой
- 100. Избирательность противомикробного действия макролидов большая субъединица рибосомы человека отличается от микробной макролиды обладают высокой избирательностью противомикробного
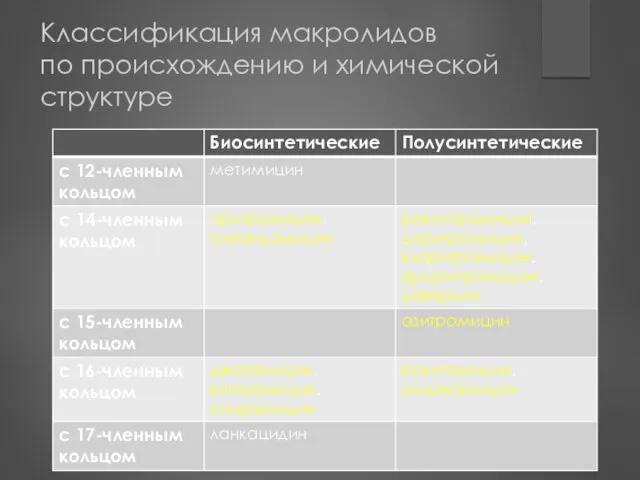
- 101. Классификация макролидов по химической структуре, в зависимости от числа атомов в кольце с 12-членным кольцом –
- 102. Классификация макролидов по происхождению Природные – эритромицин, олеандомицин, джозамицин, китазамицин, спирамицин Полусинтетические – рокситромицин, диритромицин, кларитромицин,
- 103. Классификация макролидов по происхождению и химической структуре
- 104. Классификация макролидов по спектру химиотерапевтического действия продолжительности противомикробного эффекта I поколение – эритромицин, олеандомицин II поколение
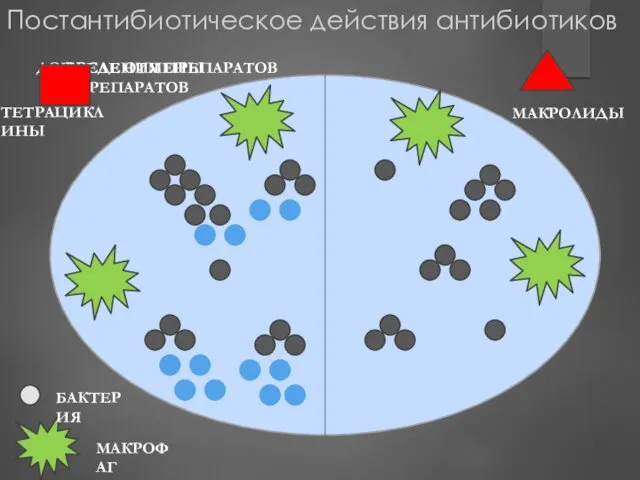
- 105. ДО ВВЕДЕНИЯ ПРЕПАРАТОВ ТЕТРАЦИКЛИНЫ МАКРОЛИДЫ ПОСЛЕ ОТМЕНЫ ПРЕПАРАТОВ БАКТЕРИЯ МАКРОФАГ Постантибиотическое действия антибиотиков
- 106. Макролиды I поколения Спектр антимикробного действия включает стафилококки, кроме МRSA, стрептококки, пневмококки, С.diphtheriae, листерии, М.catarrhalis, В.pertussis,
- 107. Макролиды II поколения У кларитромицина спектр антимикробного действия дополнительно к макролидам I поколения включает H.pylori, атипичные
- 108. Макролиды III поколения Под макролидами III поколения в настоящее время обычно понимают азалиды Азитромицин превосходит макролиды
- 109. Фармакокинетика макролидов Эритромицин всасывается в ЖКТ не полностью, причем биодоступность значительно снижается в присутствии пищи. На
- 110. Нежелательные эффекты макролидов Макролиды являются одной из самых безопасных групп антибиотиков. Нежелательные реакции в целом встречаются
- 111. Противопоказания аллергическая реакция на макролиды беременность (кларитромицин, мидекамицин, рокситромицин) кормление грудью (джозамицин, кларитромицин, мидекамицин, рокситромицин, спирамицин)
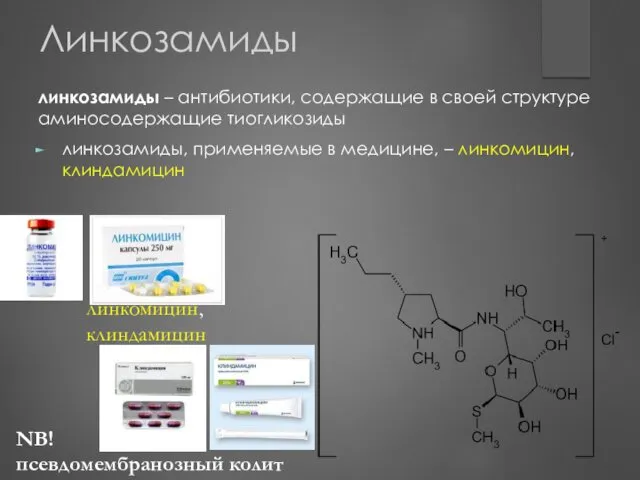
- 112. Линкозамиды линкозамиды – антибиотики, содержащие в своей структуре аминосодержащие тиогликозиды линкозамиды, применяемые в медицине, – линкомицин,
- 113. Механизм бактериостатического действия линкозамидов – нарушение синтеза белка ПФР – взаимодействие с пептидтранслоказным центром 50S субъединицы
- 114. Избирательность противомикробного действия линкозамидов большая субъединица рибосомы человека отличается от микробной линкозамиды обладают высокой избирательностью противомикробного
- 115. Спектр антимикробной активности линкозамидов аэробные грамположительные кокки (стрептококки, стафилококки) анаэробные неспорообразующие грамположительные бактерии (Actinomyces spp., Propionibacterium
- 116. Показания к назначению линкозамидов стрептококковый тонзиллофарингит, аспирационная пневмония, абсцесс легкого, эмпиема плевры инфекции кожи и мягких
- 117. Фармакокинетика линкозамидов Линкомицин в ЖКТ всасывается плохо – на 30% при приеме натощак, и на 5%
- 118. Нежелательные эффекты линкозамидов псевдомембранозный колит аллергические реакции – сыпь, покраснение кожи, зуд. Описано возникновение полиморфной экссудативной
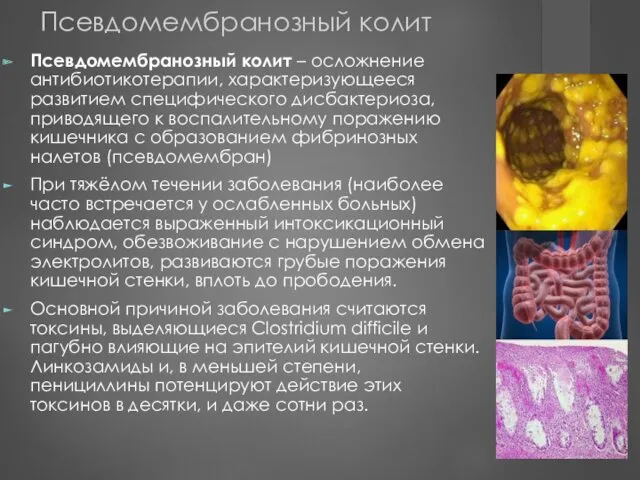
- 119. Псевдомембранозный колит Псевдомембранозный колит – осложнение антибиотикотерапии, характеризующееся развитием специфического дисбактериоза, приводящего к воспалительному поражению кишечника
- 120. Противопоказания заболевания желудочно-кишечного тракта в анамнезе: неспецифический язвенный колит, болезнь Крона, энтерит или колит, связанные с
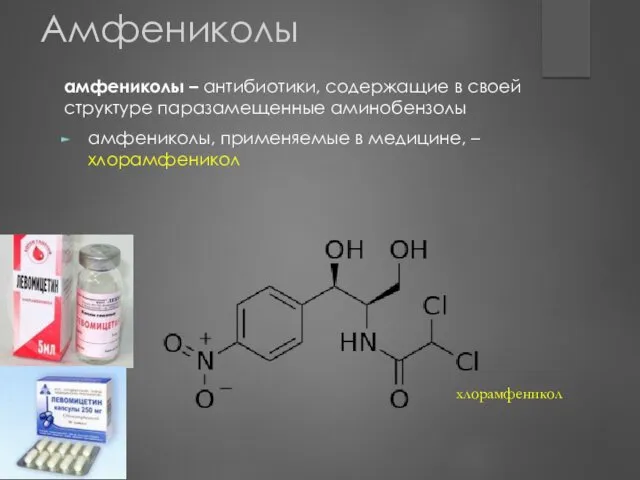
- 121. Амфениколы амфениколы – антибиотики, содержащие в своей структуре паразамещенные аминобензолы амфениколы, применяемые в медицине, – хлорамфеникол
- 122. Механизм бактериостатического действия амфениколов – нарушение синтеза белка ПФР – взаимодействие с участком большой субъединицы рибосомы
- 123. Механизм бактерицидного действия хлорамфеникола – нарушение проницаемости цитоплазматической мембраны ПФР – взаимодействие с участком большой субъединицы
- 124. Избирательность противомикробного действия амфениколов большая субъединица рибосомы человека отличается от микробной амфениколы обладают умеренной избирательностью противомикробного
- 125. Спектр химиотерапевтического действия хлорамфеникола действует бактериостатически на стрептококки, кишечную палочку, сальмонеллы, шигеллы, возбудители дифтерии, коклюша, сибирской
- 126. Фармакокинетика хлорамфеникола Хорошо проходит через барьеры, в т.ч. кишечный, гематоэнцефалический, гематоплацентарный Высокие концентрации создаются в ткани
- 127. Показания к назначению хлорамфеникола в связи с опасностью осложнений хлорамфеникол должен использоваться только в качестве препарата
- 128. Нежелательные эффекты хлорамфеникола Гематотоксическое действие «Серый коллапс» Нейротоксичность, неврит зрительного нерва Эндотоксический шок описан при использовании
- 129. Гематотоксическое действие хлорамфеникола Через 3-5 дней после приема хлорамфеникола угнетается эритроцитарный росток кроветворения, что проявляется анемией
- 130. Генетически обусловленные гематотоксические эффекты хлорамфеникола С частотой 1:24000 -1:40000 встречаются генетически предрасположенные люди, у которых продукты
- 131. Серый коллапс Серый коллапс (серый синдром новорожденных) – специфическое осложнение, возникающее у новорождённых в результате накопления
- 132. Противопоказания патология органов кроветворения аллергическая реакция на хлорамфеникол в анамнезе заболевание почек, печени беременность, лактация новорождённые
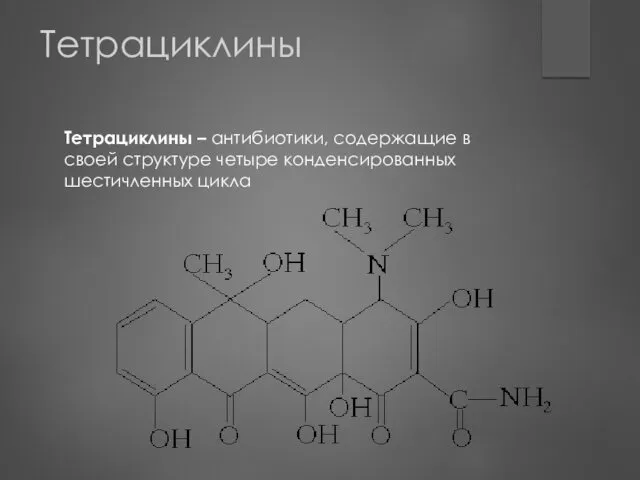
- 133. Тетрациклины Тетрациклины – антибиотики, содержащие в своей структуре четыре конденсированных шестичленных цикла
- 134. Механизм бактериостатического действия тетрациклинов – нарушение синтеза белка на рибосоме ПФР – взаимодействие с участком малой
- 135. Механизм бактериостатического действия тетрациклинов – нарушение образования металлопротеидов ПФР – взаимодействие с ионами двухвалентных металлов в
- 136. Избирательность противомикробного действия тетрациклинов в мембране микробной клетки имеются механизмы активного транспорта тетрациклинов внутрь клетки, поэтому
- 137. Классификация тетрациклинов по происхождению биосинтетические – хлортетрациклин, тетрациклин, окситетрациклин полусинтетические – морфоциклин, доксициклин, вибрамицин
- 138. Спектр антимикробной активности тетрациклинов пневмококки, менингококки листерии, H.influenzae, H.ducreyi, иерсинии, моракселлы, кампилобактеры (включая H.pylori), бруцеллы, бартонеллы,
- 139. При приеме внутрь тетрациклины хорошо всасываются, причем доксициклин лучше, чем тетрациклин. Биодоступность доксициклина не изменяется, а
- 140. Показания к назначению тетрациклинов особо опасные инфекции – бруцеллёз, туляремия, холера, чума, сибирская язва риккетсиозы –
- 141. Нежелательные эффекты тетрациклинов катаболическое действие гепатотоксичность вплоть до развития жировой дистрофии или некроза печени геморрагии тератогенное
- 142. Нежелательные эффекты тетрациклинов, зависящие от связывания с кальцием Образование хелатных комплексов тетрациклинов с ионами двухвалентных металлов,
- 143. Противопоказания детский возраст до 12 лет беременность, грудное вскармливание недостаточность функции печени анемия, лейкопения
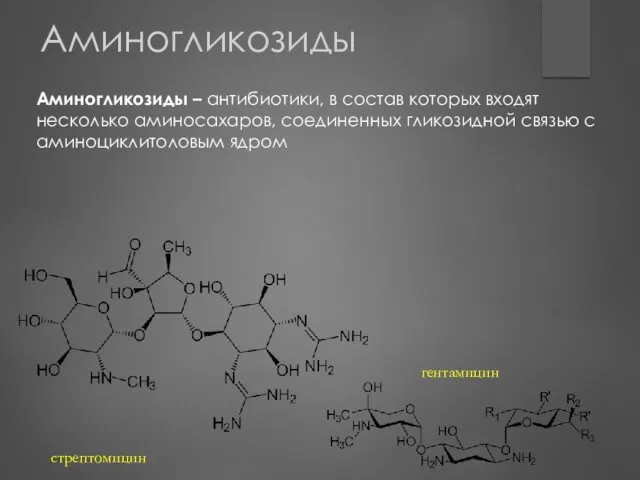
- 144. Аминогликозиды Аминогликозиды – антибиотики, в состав которых входят несколько аминосахаров, соединенных гликозидной связью с аминоциклитоловым ядром
- 145. Механизм бактериостатического действия аминогликозидов – нарушение инициализации синтеза белка в микробной клетке ПФР – взаимодействие с
- 146. Механизм вторичного бактерицидного действия аминогликозидов – искажение синтеза белка в микробной клетке ПФР – взаимодействие с
- 147. Классификация аминогликозидов по спектру антимикробного действия и устойчивости к аминогликозидазам I поколение – стрептомицин, канамицин, мономицин,
- 148. Аминогликозиды I поколения Спектр антимикробного действия включает стафилококки, энтерококки и энтеробактерии, включая E.coli, Klebsiella spp., Salmonella
- 149. Аминогликозиды II поколения Отличаются от препаратов I поколения активностью в отношении P.aeruginosa В отношении микобактерий туберкулёза
- 150. Аминогликозиды III поколения По сравлении с аминогликозидами II поколения в отношении P.aeruginosa оказывают еще более сильное
- 151. Аминогликозиды IV поколения В спектр антимикробного действия дополнительно к спектру препаратов III поколения включаются Aëromonas spp.,
- 152. Фармакокинетика аминогликозидов Молекулы аминогликозидов являются высокополярными соединениями, в связи с чем плохо растворяются в липидах и,
- 153. Показания к назначению аминогликозидов Неомицин
- 154. Нежелательные эффекты аминогликозидов ототоксическое действие ототоксическое действие аминогликозидов обратимо лишь в самом начале, часто приводит к
- 155. Противопоказания Аллергические реакции на аминогликозиды Беременность, грудное вскармливание Недостаточность функции печени и почек Заболевания органов слуха
- 156. Условия назначения аминогликозидов строгий расчет дозы на массу тела и соблюдение режима дозирования, а также проведение
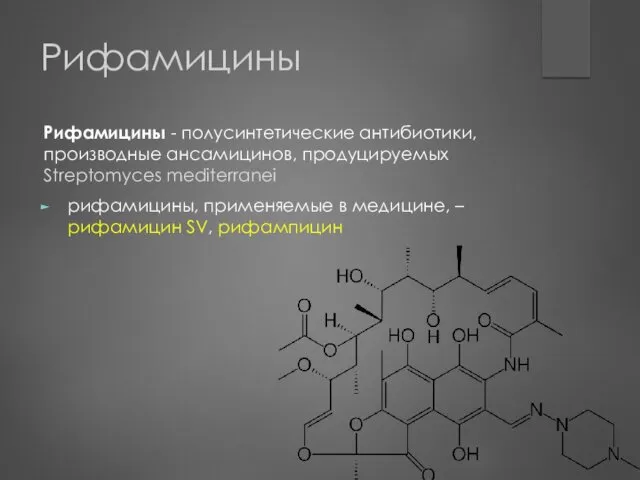
- 157. Рифамицины Рифамицины - полусинтетические антибиотики, производные ансамицинов, продуцируемых Streptomyces mediterranei рифамицины, применяемые в медицине, – рифамицин
- 158. Механизм бактериостатического действия рифамицинов – блокада ДНК-зависимой РНК-полимеразы ПФР – взаимодействие с ДНК-зависимой РНК-полимеразой микроорганизма блокируется
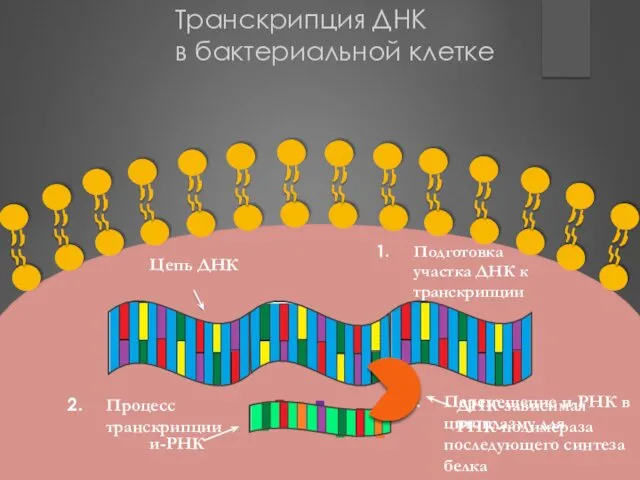
- 159. Транскрипция ДНК в бактериальной клетке Цепь ДНК Подготовка участка ДНК к транскрипции Процесс транскрипции Перемещение и-РНК
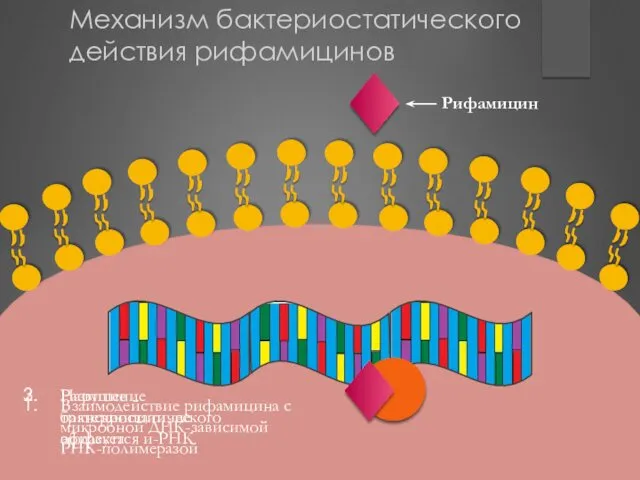
- 160. Взаимодействие рифамицина с микробной ДНК-зависимой РНК-полимеразой Развитие бактериостатического эффекта Нарушение транскрипции, не образуется и-РНК Механизм бактериостатического
- 161. Механизм бактериостатического действия рифамицинов – нарушение инициализации синтеза белка в микробной клетке ПФР – взаимодействие с
- 162. Избирательность противомикробного действия рифамицинов строение ДНК-зависимой РНК-полимеразы у прокариотов и у эукариотов различно рифамицины обладают умеренной
- 163. Спектр противомикробного действия рифамицинов в низких концентрациях активны в отношении M.tuberculosis, Staphylococcus spp., Streptococcus spp. (в
- 164. Фармакокинетика рифамицинов при внутримышечном введении максимальная концентрация в крови достигается через 30 мин, терапевтическая концентрация сохраняется
- 165. Показания к назначению рифамицинов туберкулёз, лепра пневмонии, вызванные полирезистентными штаммами стафилококков лечение заболеваний, вызванных гемофильной палочкой,
- 166. Нежелательные эффекты рифамицинов гепатотоксическое действие (гепатит, гипербилирубинемия, повышение активности печеночных трансаминаз) нейротоксическое действие (головная боль, нарушение
- 167. Противопоказания желтуха, недавно перенесенный (менее 1 года) инфекционный гепатит выраженные нарушения функции почек беременность, лактация аллергическая
- 168. Полимиксины Полимиксины – антибиотики, имеющие структуру циклических пептидов и узкий спектр противомикробного действия, влияя только на
- 169. Механизм бактерицидного действия полимиксинов – повышение проницаемости клеточной мембраны ПФР – взаимодействие с анионными участками клеточной
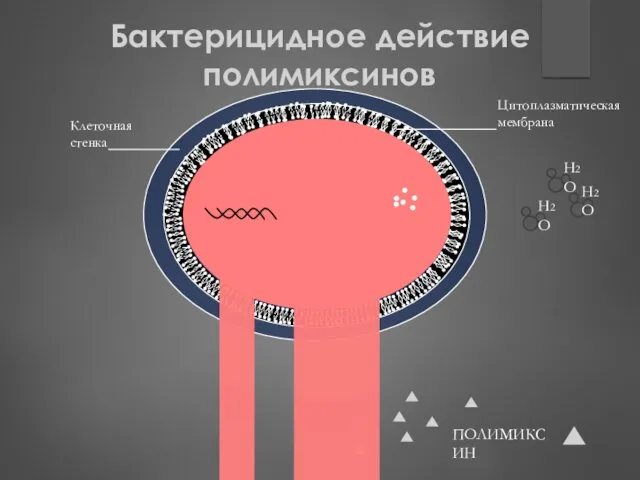
- 170. Клеточная стенка Цитоплазматическая мембрана ПОЛИМИКСИН H2O H2O H2O Бактерицидное действие полимиксинов
- 171. Избирательность противомикробного действия полимиксинов клетки кожи и слизистых оболочек животных и человека имеют лучшую, по сравнению
- 172. Спектр противомикробного действия полимиксинов грамотрицательные бактерии (кишечные палочки, сальмонеллы, шигеллы, клебсиеллы, иерсинии, энтеробактерии, H.influenzae) синегнойная палочка
- 173. Фармакокинетика полимиксинов не всасываются с поверхности кожи и слизистых оболочек, в т.ч. и из ЖКТ при
- 174. Показания к назначению полимиксинов инфекции, вызванные полирезистентными грамотрицательными бактериями, в т.ч. P.aeruginosa инфекционные заболевания глаз полимиксин
- 175. Нежелательные эффекты полимиксинов выраженная нефротоксичность, проявляющаяся повышением уровня креатинина и мочевины в крови, протеинурией и гематурией,
- 176. Противопоказания аллергические реакции на полимиксины беременность, лактация почечная недостаточность, миастения, ботулизм применение миорелаксантов и общих анестетиков
- 177. Фузафунгин Фузафунги́н – полипептидный антибиотик, продуцируемый Fusarium lateritium Спектр антимикробного действия включает стрептококки группы A, S.pneumoniae,
- 178. Полиены Полиеновые антибиотики – антибиотики содержащие не менее трех изолированных или сопряженных двойных связей атомов углерода.
- 179. Механизм фунгицидного действия полиеновых антибиотиков ПФР – взаимодействие с эргостеролом в клеточной мембране грибковой клетки нарушается
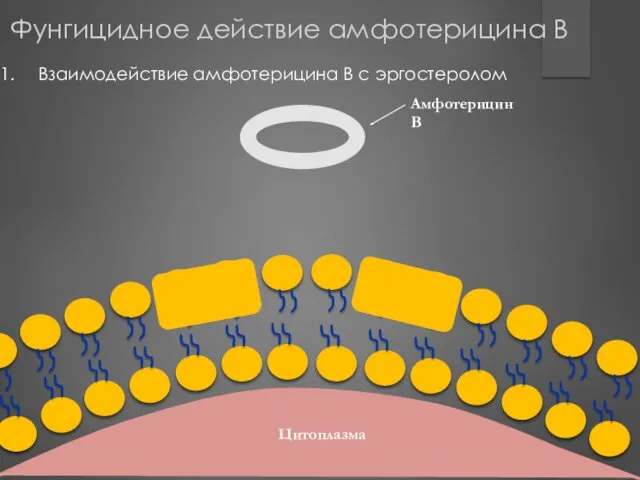
- 180. Механизм фунгицидного действия амфотерицина B ПФР – взаимодействие с эргостеролом в клеточной мембране грибковой клетки комплекс
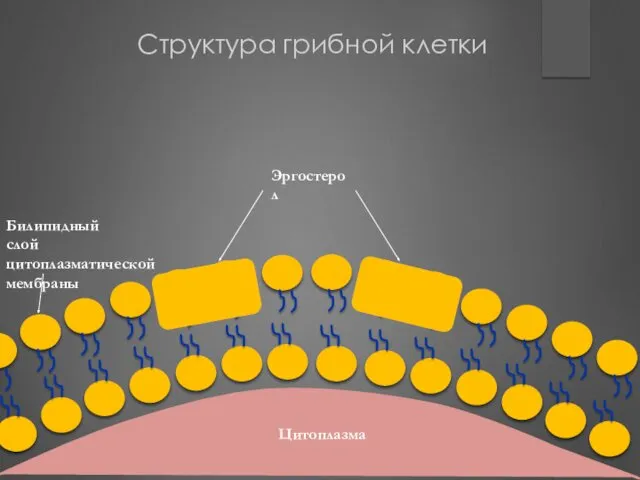
- 181. Структура грибной клетки Эргостерол Билипидный слой цитоплазматической мембраны Цитоплазма
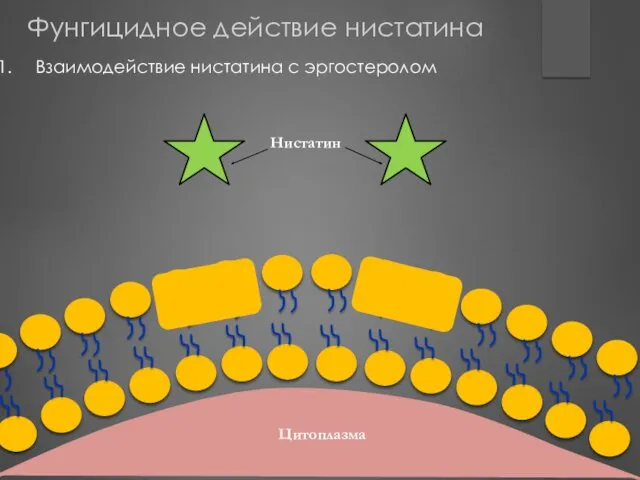
- 182. Цитоплазма Цитоплазма Фунгицидное действие нистатина Взаимодействие нистатина с эргостеролом Нистатин
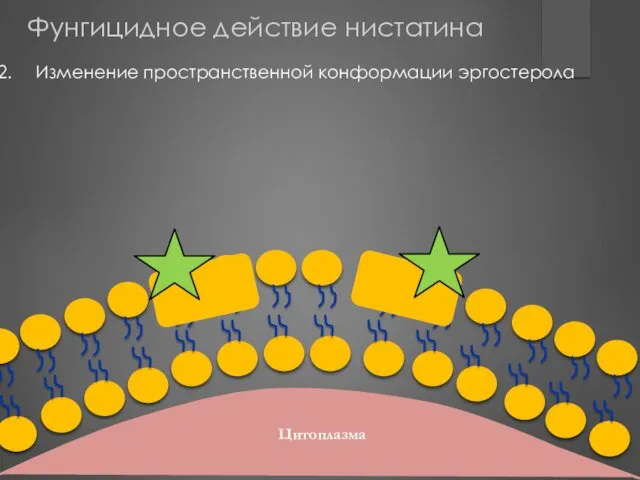
- 183. Изменение пространственной конформации эргостерола Цитоплазма Фунгицидное действие нистатина
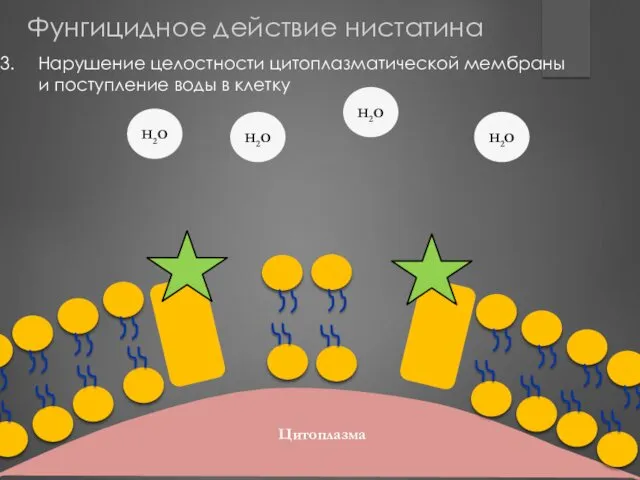
- 184. Цитоплазма Цитоплазма H2O H2O H2O H2O Нарушение целостности цитоплазматической мембраны и поступление воды в клетку Фунгицидное
- 185. Гибель грибковой клетки (фунгицидный эффект) Фунгицидное действие нистатина
- 186. Амфотерицин В Взаимодействие амфотерицина В с эргостеролом Цитоплазма Цитоплазма Фунгицидное действие амфотерицина В
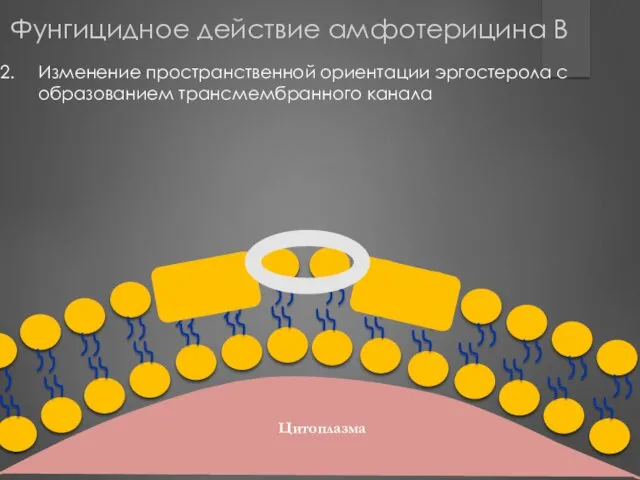
- 187. Цитоплазма Изменение пространственной ориентации эргостерола с образованием трансмембранного канала Фунгицидное действие амфотерицина В
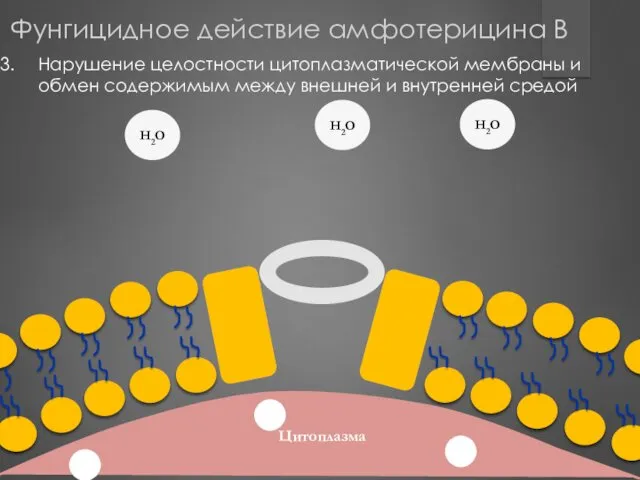
- 188. Цитоплазма Нарушение целостности цитоплазматической мембраны и обмен содержимым между внешней и внутренней средой H2O H2O H2O
- 189. Избирательность противомикробного действия полиеновых антибиотиков У человека и животных эргостерол в мембранах клеток отсутствует, а его
- 190. Классификация полиенов по способу применения препараты, назачаемые только для местного действия – нистатин, леворин препараты, применение
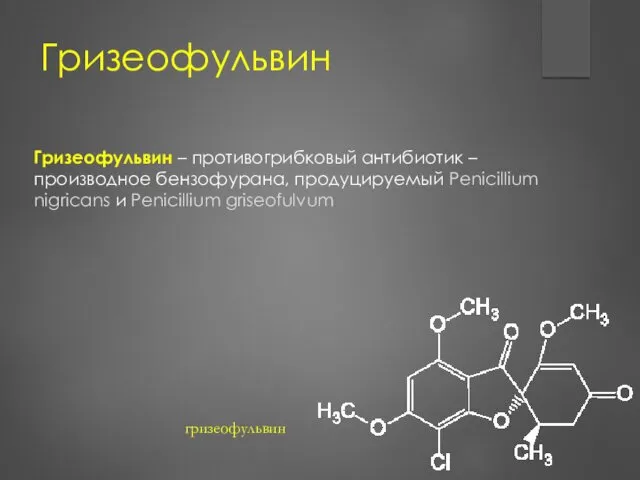
- 191. Гризеофульвин Гризеофульвин – противогрибковый антибиотик – производное бензофурана, продуцируемый Penicillium nigricans и Penicillium griseofulvum гризеофульвин
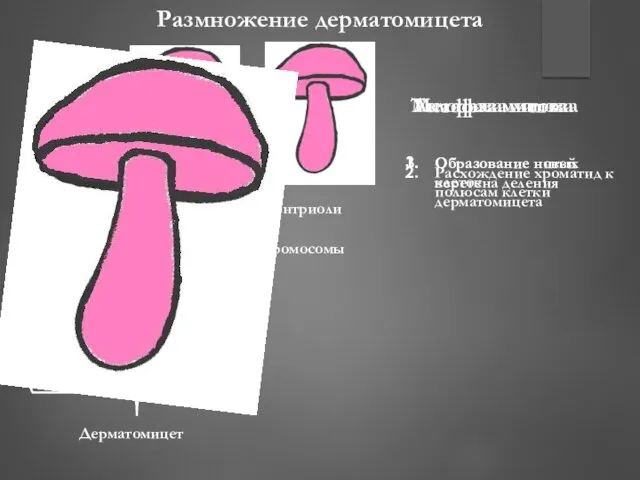
- 192. Механизм фунгистатического действия гризеофульвина ПФР – взаимодействие белками микротрубочек веретена деления дерматомицетов нарушается расхождение хромосом при
- 193. Эпидермис Дерма Кератиноцит со зрелым кератином Дерматомицет Предшественник кератиноцита с незрелым кератином Размножение дерматомицетов в эпидермисе
- 194. Метафаза митоза Анафаза митоза Микротрубочки нитей веретена деления Образование новых клеток дерматомицета Образование нитей веретена деления
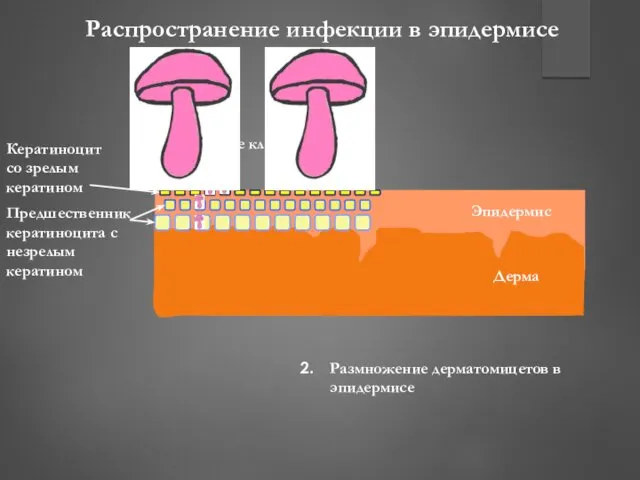
- 195. Эпидермис Дерма Кератиноцит со зрелым кератином Предшественник кератиноцита с незрелым кератином Распространение инфекции в эпидермисе Размножение
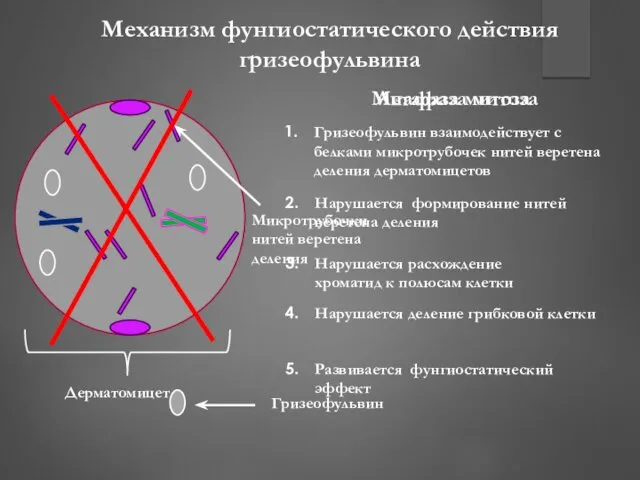
- 196. Метафаза митоза Анафаза митоза Механизм фунгиостатического действия гризеофульвина Микротрубочки нитей веретена деления Гризеофульвин Нарушается формирование нитей
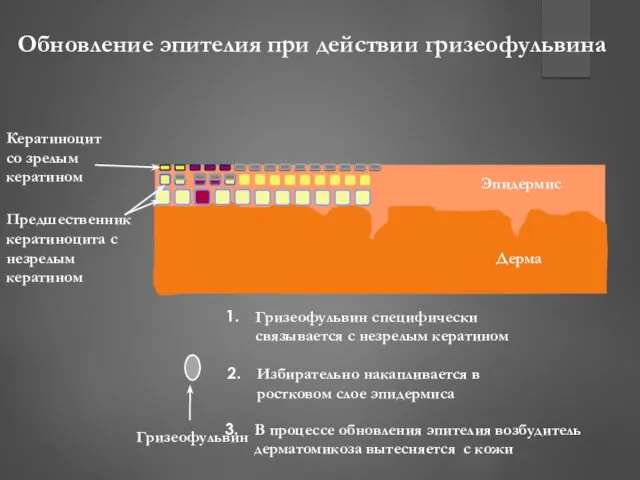
- 197. Эпидермис Дерма Кератиноцит со зрелым кератином Предшественник кератиноцита с незрелым кератином В процессе обновления эпителия возбудитель
- 198. Избирательность противомикробного действия гризеофульвина белки микротрубочек веретена деления у дерматомицетов и человека отличаются по строению концентрация
- 199. Фармакокинетика гризеофульвина специфически связывается с кератином при его образовании в предшественниках кератиноцитов кожи, волос и ногтей,
- 200. Нежелательные эффекты химиотерапии
- 201. Классификация нежелательных эффектов химиотерапии по механизму возникновения токсические эффекты, раздражающее действие аллергические эффекты биологические эффекты
- 202. Токсическое действие токсическое действие – нежелательное действие препарата, связанное с абсолютным или относительным, тотальным или местным
- 203. Раздражающее действие* раздражающеее действие – нежелательное действие препарата на пути его введения или выведения * Термин
- 204. Виды раздражающего действия при приеме внутрь тошнота, рвота, понос дискомфорт в животе запоры при подкожном и
- 205. Нейротоксические эффекты антибиотиков
- 206. Токсические эффекты антибиотиков (кроме нейротоксических)
- 207. Аллергические эффекты антибиотиков могут возникнуть при применении любого антибиотика наиболее часто возникают при использовании пенициллинов и
- 208. Биологические нежелательные эффекты антибиотиков Дисбактериоз (дисбиоценоз) – качественное и количественное нарушение естественной микрофлоры Дисбактериоз обычно возникает
- 209. Степени тяжести кишечного дисбактериоза I степень – функциональные нарушения II степень – клиническая картина энтерита, колита,
- 210. Направления борьбы с кишечным дисбактериозом Восстановление дефицита микрофлоры назначением пробиотиков Стимуляция роста микроорганизмов нормофлоры кишечника пребиотиками
- 211. Пробиотики Пробио́тики – живые культуры микроорганизмов, приём которых может быть полезен для здоровья В зависимости от
- 212. Пребиотики Пребио́тики – компоненты пищи, которые не перевариваются и не усваиваются в верхних отделах желудочно-кишечного тракта,
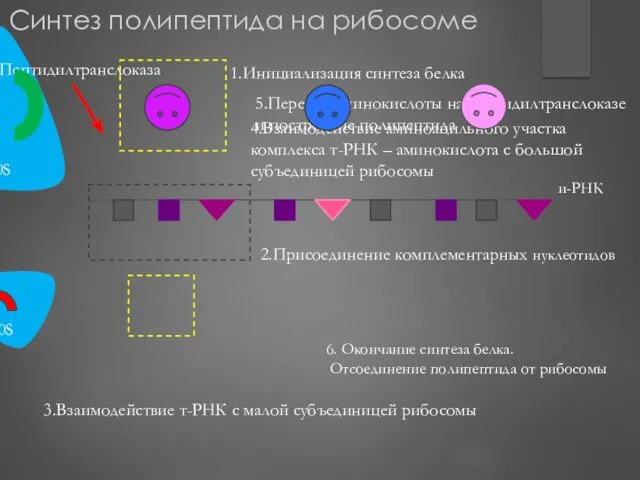
- 213. 50S 30S Пептидилтранслоказа 2.Присоединение комплементарных нуклеотидов 3.Взаимодействие т-РНК с малой субъединицей рибосомы 1.Инициализация синтеза белка 4.Взаимодействие
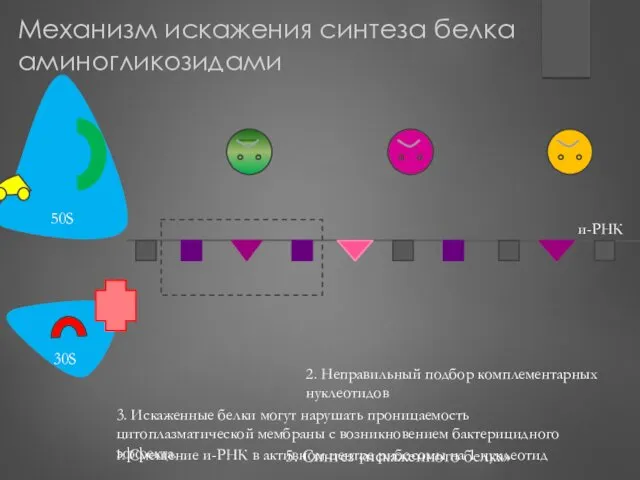
- 214. Механизм угнетения синтеза белка аминогликозидами (рифамицинами) 1.Присоединение аминогликозида к малой субъединице рибосомы 2.Нарушение инициализации синтеза белка
- 215. 5. Синтез «искаженного белка» 2. Неправильный подбор комплементарных нуклеотидов 1. Смещение и-РНК в активном центре рибосомы
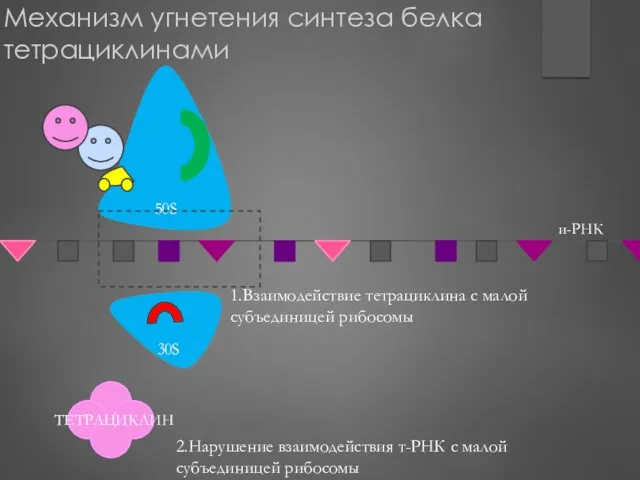
- 216. Механизм угнетения синтеза белка тетрациклинами 1.Взаимодействие тетрациклина с малой субъединицей рибосомы 2.Нарушение взаимодействия т-РНК с малой
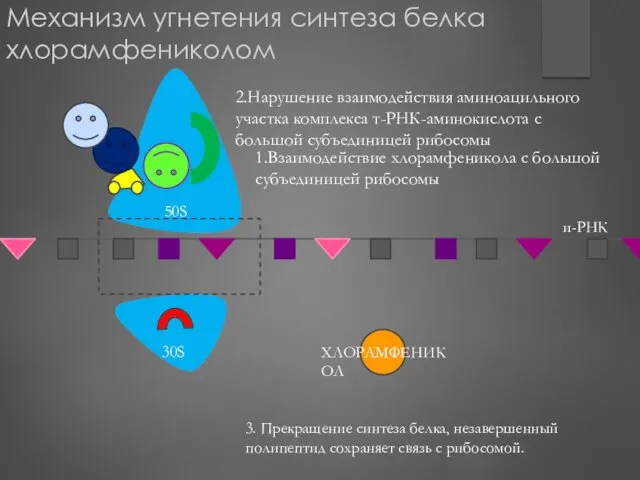
- 217. Механизм угнетения синтеза белка хлорамфениколом 1.Взаимодействие хлорамфеникола с большой субъединицей рибосомы 2.Нарушение взаимодействия аминоацильного участка комплекса
- 218. Механизм угнетения синтеза белка макролидами, азалидами и линкозамидами 1.Взаимодействие с пептидилтраслоказой 2.Разрушение комплекса рибосома - полипептид
- 219. Применение В качестве препарата выбора Сыпной тиф Бруцеллёз Холера Хламидиоз легких и мочеполовой системы Инфекциии, вызванные
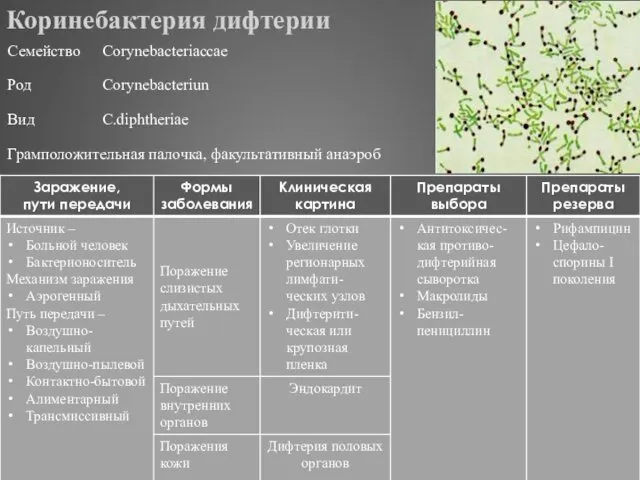
- 220. Применение В качестве препарата выбора Дифтерия зева Дифтерийный ларинготрахеит Пневмония В качестве препарата резерва Энтерит Уретрит
- 221. Формы выпуска Флаконы 0,25; 0,5 и 1,0 Применение В качестве препарата выбора Сепсис, вызванный E.coli Инфекции
- 222. Применение В качестве препарата выбора Чума Туляремия Фрамбезия В качестве препарата резерва Сепсис, вызванный E.coli Артрит
- 223. Флаконы 0,08 Ампулы 1%, 2%, 4% и 6% раствор 1 или 2мл Мазь 0,1% в тубах
- 224. Формы выпуска Таблетки 0,25 и 0,5 Капли глазные 0,25% раствор Флаконы 0,5 ;1,0 В качестве препарата
- 225. Формы выпуска Капсулы 0,15 и 0,3 по 20шт. Капсулы для детей 0,05 по 30шт. Ампулы 0,15
- 226. Применение В качестве препарата выбора Дифтерия зева Дифтерийный ларинготрахеит Пневмония В качестве препарата резерва Эризипелоид Энтерит
- 227. Формы выпуска Ампулы 2% раствор 2мл, 5мл и 10мл Таблетки буккальные 0,0015 (1500 ЕД) по 10шт.
- 228. Формы выпуска Таблетки 100 000 и 250 000ЕД по 10 и 12шт. Драже 100 000 ЕД
- 229. Формы выпуска Флаконы 100 000 ЕД, 125 000 ЕД, 250 000 ЕД, 300 000, 400 000
- 230. Флаконы 300 000ЕД, 600 000ЕД и 1 200 000ЕД Формы выпуска Применение В качестве препарата выбора
- 231. Формы выпуска Флаконы 600000 ЕД и 1200000 ЕД Применение В качестве препарата выбора Вторичная профилактика ревматизма
- 232. Формы выпуска Флаконы, содержащие бензатина бензилпенициллина 1200000 ЕД и бензилпенициллина новокаиновой соли 300000 ЕД Применение В
- 233. Формы выпуска Таблетки 0,25 и 0,5 по 20, 24 и 250шт. Желатиновые капсулы 0,25 по 10шт.
- 234. Формы выпуска Флаконы 0,250 или 0,5 по 10 и 100шт. Клоксациллин (Cloxacillinum) Применение В качестве препарата
- 235. Формы выпуска Капсулы 0,25 и 0,5 по 100 и 500шт. Порошок для приготовления суспензии — 0,125
- 236. Формы выпуска Таблетки 0,25 по 10шт. Капсулы 0,25 по 10, 16 или 25шт. и 0,5 по
- 237. Формы выпуска Таблетки 1,0 Капсулы 0,25 и 0,5 Применение В качестве препарата выбора Синусит Средний отит
- 238. Применение В качестве препарата выбора Пневмония Артрит Синусит Отит Инфекции, вызванные протеем В качестве препарата резерва
- 239. Цефалотин (Cefalotinum) Применение Перитонит Эндокардит Пневмония Абсцесс легкого Эмпиема плевры Бронхит Ангина Пиелонефрит Простатит Эндометрит Вульвовагинит
- 240. Формы выпуска Флаконы 1,0 по 20шт. Применение В качестве препарата выбора Инфекции органов малого таза Перитонит
- 241. Форма выпуска Таблетки 0,125 и 0,25 Применение В качестве препарата выбора В качестве препарата резерва Новобиоцин
- 242. Формы выпуска Капсулы 0,25 по 20шт. Применение Пиелонефрит Цистит Уретрит Простатит Карфециллин (Carphecillinum)
- 243. Формы выпуска Флаконы 50мл, 100мл и 250мл Применение В качестве препарата выбора Инфицированные раны Фурункулез Карбункулез
- 244. Флаконы 0,5; 1,0; 2,0 по 5 и 10шт. Формы выпуска Применение Бронхит Пневмония Абсцесс легких Эмпиема
- 245. Форма выпуска Флаконы 0,05; 0,15 и 1,0 Применение Конъюктивит Пиодермии Трофические язвы Фарингит Тонзиллит Гайморит Стоматит
- 246. Формы выпуска Флаконы 0,5;1,0; 2,0;5,0 и 10,0 по 10шт. Применение Бронхит Пневмония Сальмонеллёз Перитонит Менингит Эндокардит
- 247. Формы выпуска Флаконы 0,5; 1,0; 2,0 по 5 и 10шт. Применение Бронхит Пневмония Пиелит Цистит Пиелонефрит
- 248. Формы выпуска Капсулы 0,25 Применение В качестве препарата выбора Бронхит Пневмония Холангит Холецистит Пиелит Пиелонефрит Инфекции
- 249. Формы выпуска Применение В качестве препарата выбора Синусит Фарингит Средний отит Ларингит В качестве препарата резерва
- 250. Применение В качестве препарата выбора Синусит Средний отит Тонзиллит Фарингит Бронхит Пневмония Уретрит Цистит В качестве
- 251. Применение В качестве препарата выбора Тонзиллит Синусит Средний отит Бронхит Бронхопневмония Цистит Уретрит Периодонтит В качестве
- 252. Цефазолин (Cefazolinum) Формы выпуска Флаконы 0,25 Применение В качестве препарата выбора Фарингит Синусит Флегмона Рожа Эндокардит
- 253. Применение В качестве препарата выбора Хронический бронхит Внебольничная пневмония Острый отит Синусит Пиелонефрит Цистит Инфекцияии кожи
- 254. Применение В качестве препарата выбора Хронический бронхит Внебольничная пневмония Острый отит Синусит Пиелонефрит Цистит Инфекции кожи
- 255. Применение В качестве препарата выбора Хронический бронхит Внебольничная пневмония Острый отит Синусит Пиелонефрит Цистит Пиелит Эндометрит
- 256. Применение В качестве препарата выбора Пневмония Артрит Синусит Отит Инфекции мочевых путей и другие инфекции, вызванные
- 257. Применение В качестве препарата выбора Пневмония, артрит, синусит, отит, вызванные S.pneumoniae Инфекции мочевых путей и другие
- 258. Применение В качестве препарата выбора Пневмония,артрит, синусит,отит, вызванные S.pneumoniae Инфекции мочевых путей и другие инфекции, вызванные
- 259. Применение В качестве препарата выбора Пневмония, артрит, синусит, отит, вызванные S.pneumoniae Инфекции мочевых путей и другие
- 260. Применение Нозокомиальные инфекции, вызванные полирезистентной микрофлорой Пневмония Абсцесс легкого Эмпиема плевры Интраабдомиальные инфекции Сепсис Лечение инфекций
- 261. Применение В качестве препарата выбора Инфекция мочевых путей Сепсис Инфекции, вызванные E.coli В качестве препарата резерва
- 262. Применение В качестве препарата выбора Инфекции мочевых путей Сепсис Инфекции, вызванные E.coli В качестве препарата резерва
- 263. Применение В качестве препарата выбора Хронический бронхит Внебольничная пневмония Острые отиты и синуситы Пиелонефрит Цистит Инфекциях
- 264. Применение В качестве препарата выбора Пневмония Артрит Синусит Отит Инфекции мочевых путей и другие инфекции, вызванные
- 265. Применение В качестве препарата резерва Пиелонефрит Циститы Уретрит Простатиты Пневмония, Эмпиема плевры Менингит Сепсис Инфекции кожи
- 266. Формы выпуска Таблетки, покрытые оболочкой 0,05, 0,1, 0,15 и 0,3 по 10шт. Рокситромицин (Roxithromycinum)
- 267. Формы выпуска Флаконы 0,5 и 1,0 Применение Псевдомембранозный колит, вызванный C.difficile Инфекции, вызванные MRSA Ванкомицин (Vancomycinum)
- 268. Применение Псевдомембранозный колит, вызванный C.difficile Инфекции, вызванные MRSA Формы выпуска Флаконы 0,2 и 0,4 Тейкопланин (Teicoplaninum)
- 269. Применение В качестве препарата выбора Дифтерия зева Пневмония Дифтерийный ларинготрахеит В качестве препарата резерва Энтерит Уретрит
- 270. В качестве препарата резерва Энтерит Уретрит Атипичная пневмония Применение В качестве препарата выбора Дифтерия зева Дифтерийный
- 271. Формы выпуска Флаконы 1,0 Применение Абсцесс легкого и средостения Пиоторакс Инфекционный миозит Тубулоинтерстициальный нефрит Цистит Уретрит
- 272. Эртапенем (Ertapenemum) Формы выпуска Флаконы 1,0 Применение В качестве препарата резерва Интраабдоминальная хирургическая инфекция Гинекологические инфекции
- 273. Меропенем (Meropenum) Формы выпуска Флаконы 0,5 и 1,0 Применение В качестве препарата резерва Интраабдоминальная хирургическая инфекция
- 274. Имипенем (Imipenemum) Формы выпуска Флаконы, содержащие 0,5 имипенема и 0,5 циластатина натрия Применение В качестве препарата
- 275. Дорипенем (Doripenemum) Формы выпуска Флаконы 0,5 Применение В качестве препарата резерва Интраабдоминальная хирургическая инфекция Гинекологические инфекции
- 276. Даверцин (Davercinum) Формы выпуска Таблетки 0,25
- 277. Кишечная палочка (диареегенные штаммы)
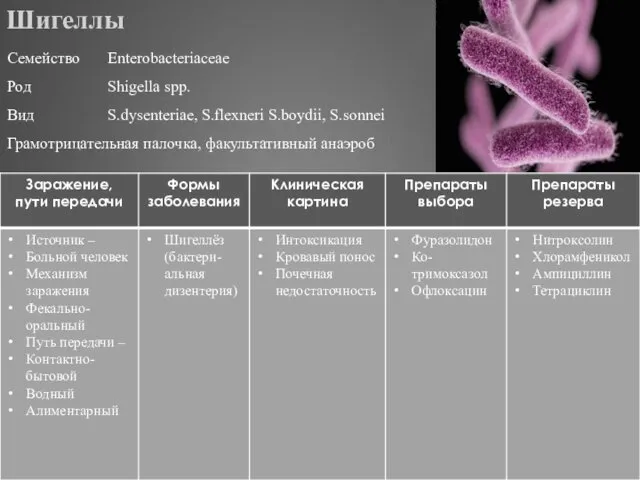
- 278. Шигеллы
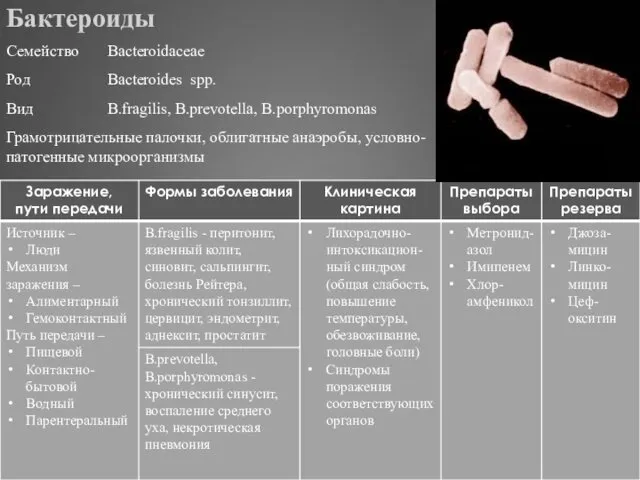
- 279. Бактероиды
- 280. Золотистый стафилококк
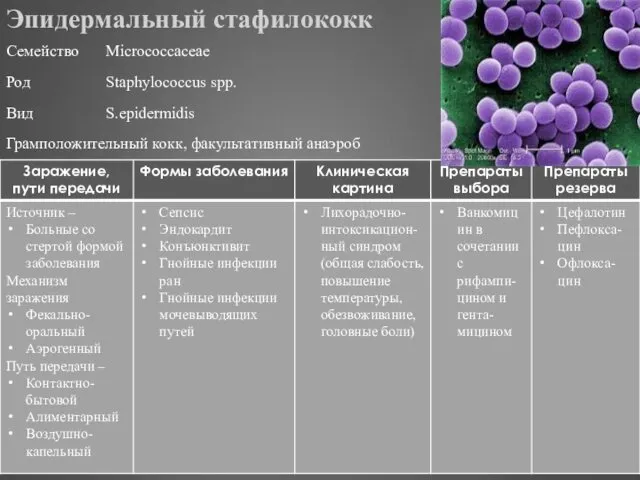
- 281. Эпидермальный стафилококк
- 282. β-гемолитический стрептококк группы А
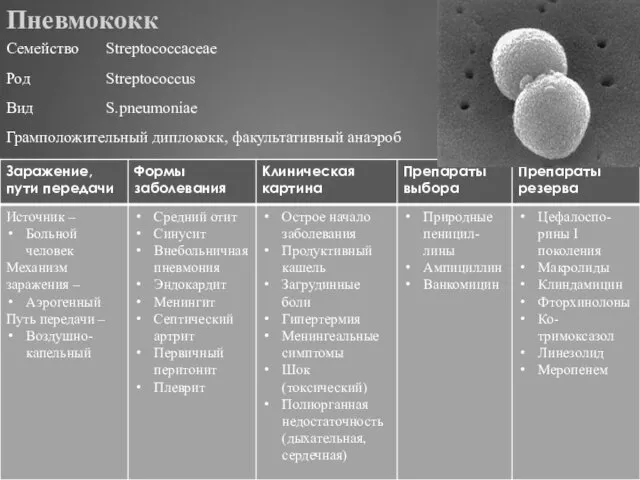
- 283. Пневмококк
- 284. Энтерококки
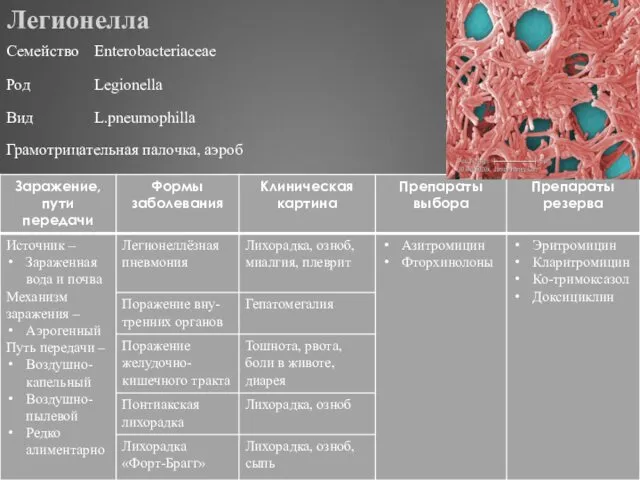
- 285. Легионелла
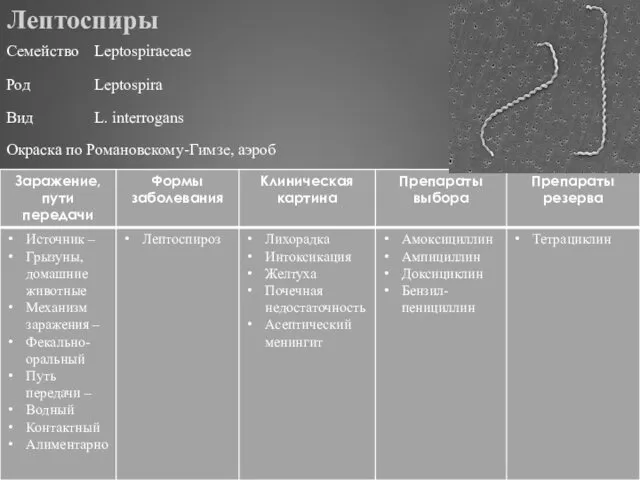
- 286. Лептоспиры
- 287. Микромоноспоры
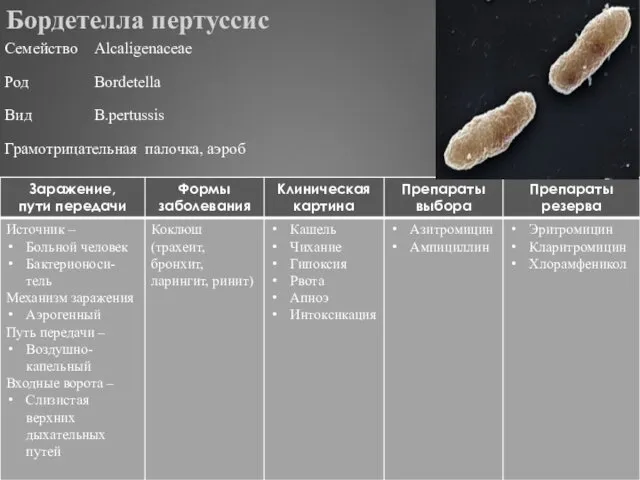
- 288. Бордетелла пертуссис
- 289. Коринебактерия дифтерии
- 290. Листерия
- 291. Бруцеллы
- 292. Боррелии
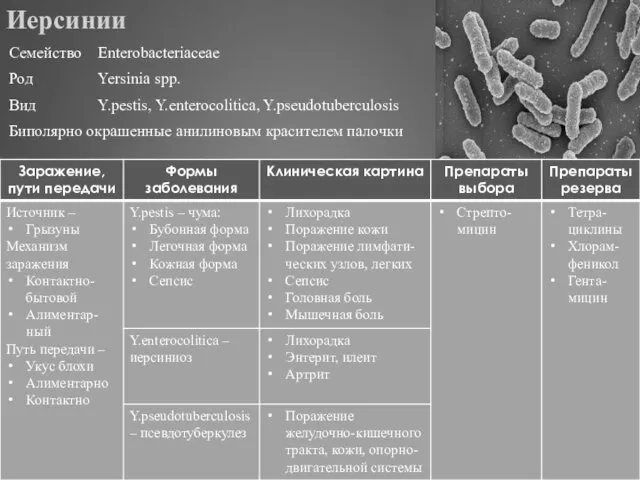
- 293. Иерсинии
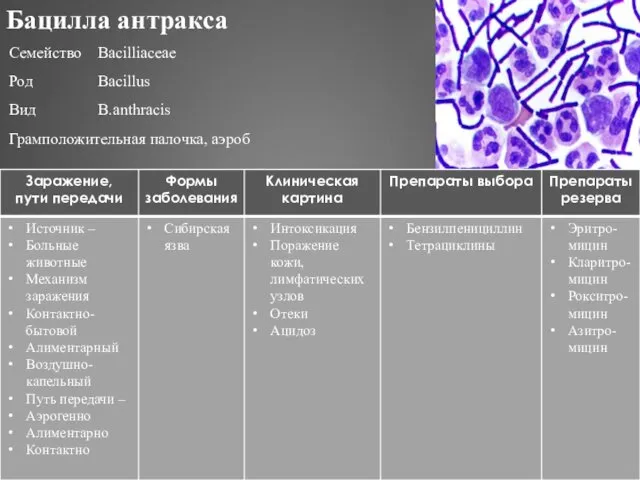
- 294. Бацилла антракса
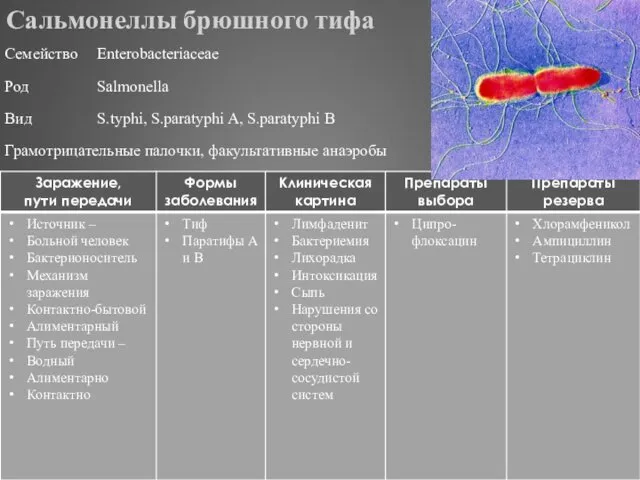
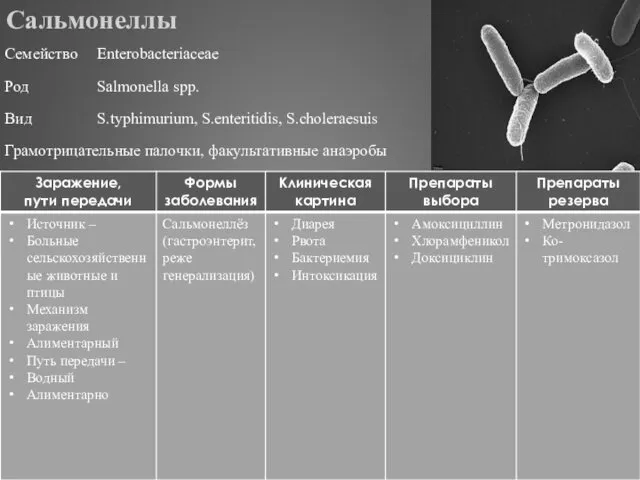
- 295. Сальмонеллы брюшного тифа
- 296. Сальмонеллы
- 297. Хеликобактер пилори
- 298. Гемофильная палочка
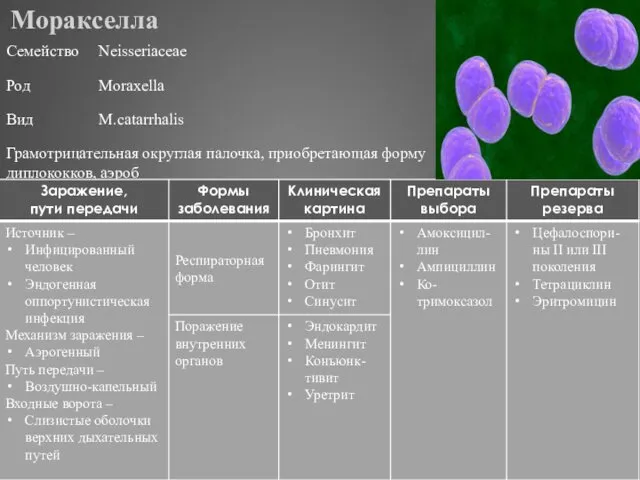
- 299. Моракселла
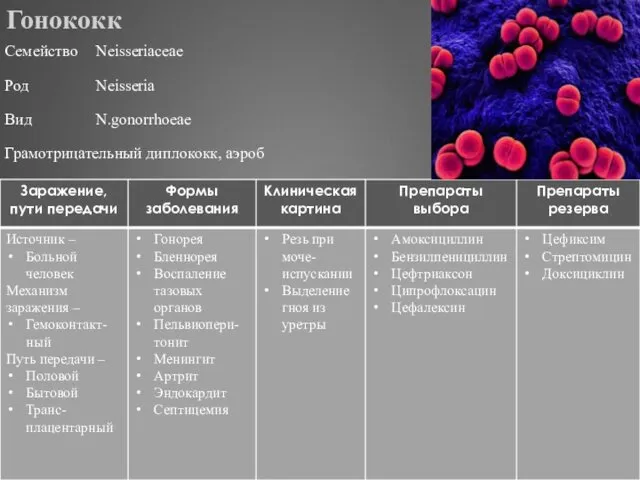
- 300. Гонококк
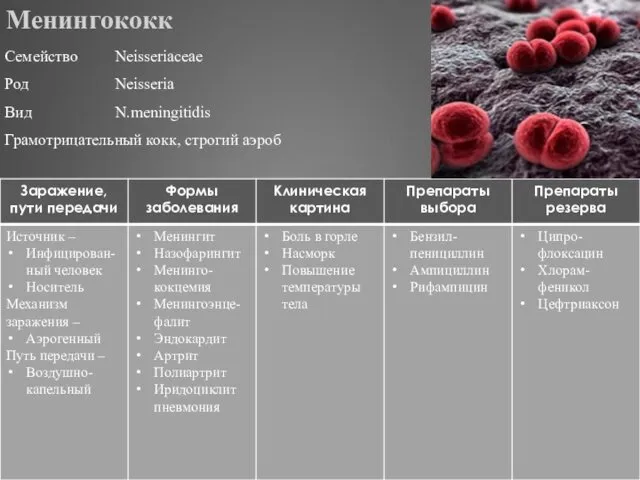
- 301. Менингококк
- 302. Цитробактер
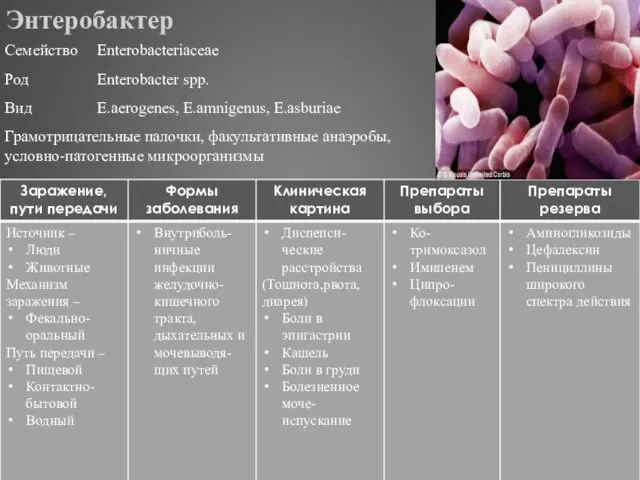
- 303. Энтеробактер
- 304. Протей
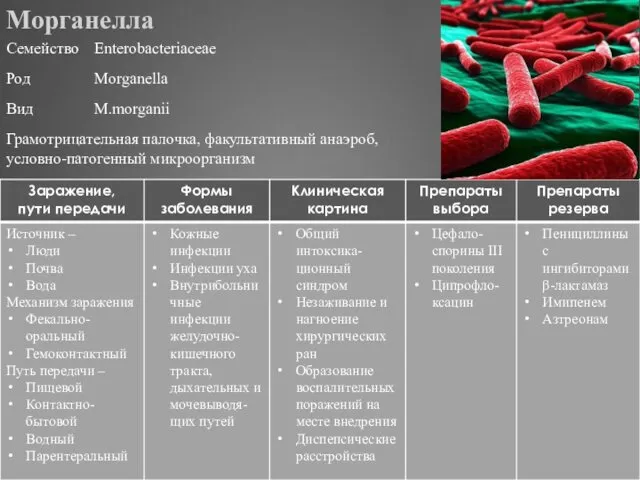
- 305. Морганелла
- 306. Ацинетобактер
- 307. Клебсиеллы
- 308. Серрации
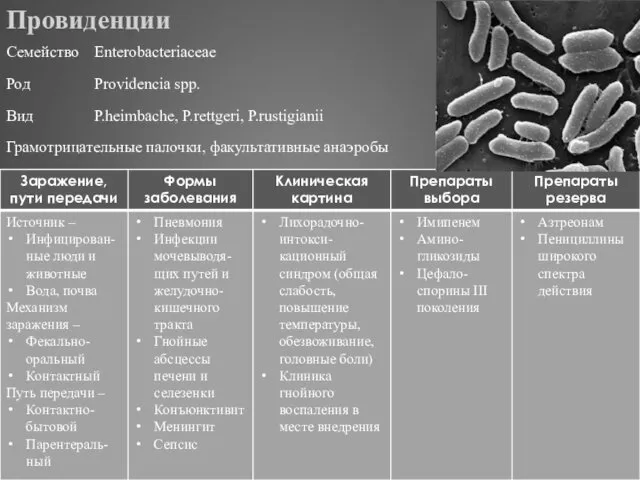
- 309. Провиденции
- 310. Пропионовокислые бактерии
- 311. Синегнойная палочка
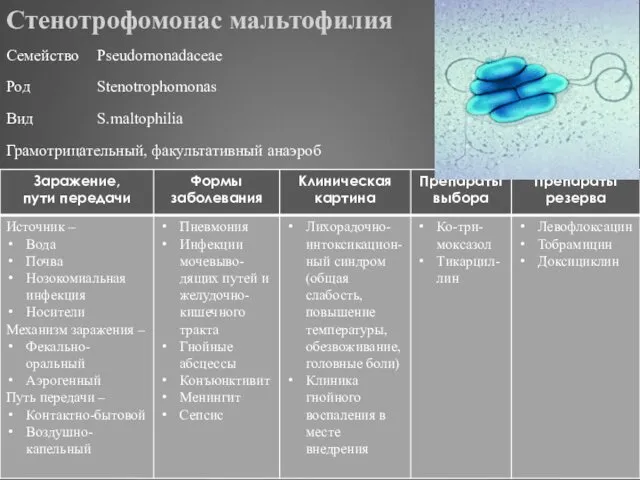
- 312. Стенотрофомонас мальтофилия
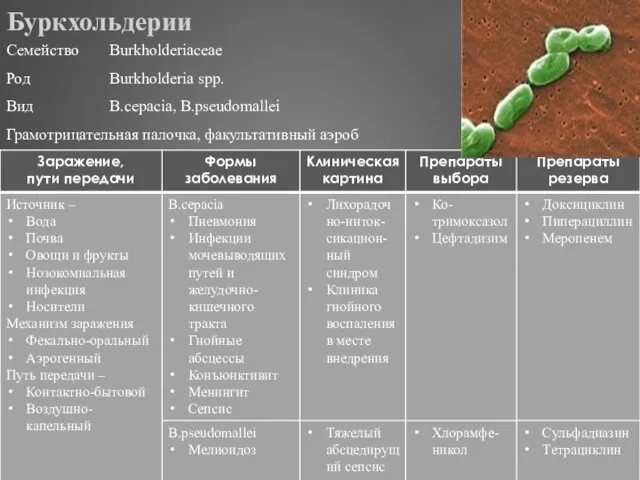
- 313. Буркхольдерии
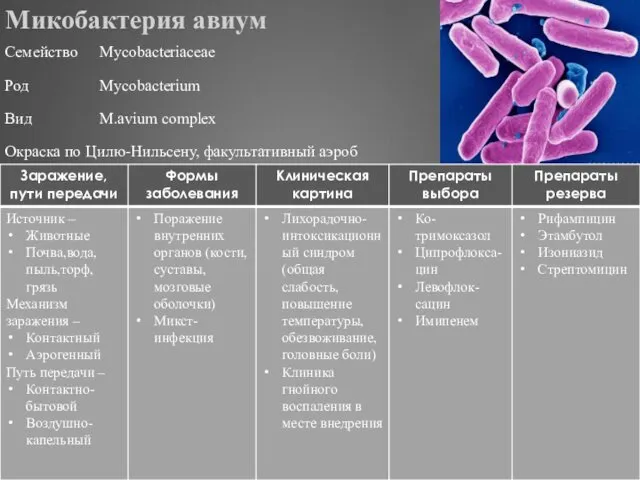
- 314. Микобактерия авиум
- 315. Криптоспоры
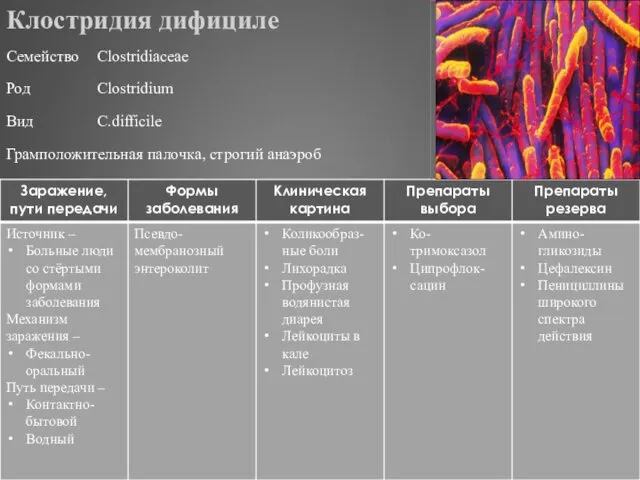
- 316. Клостридия дифициле
- 317. Клостридия ботулизма
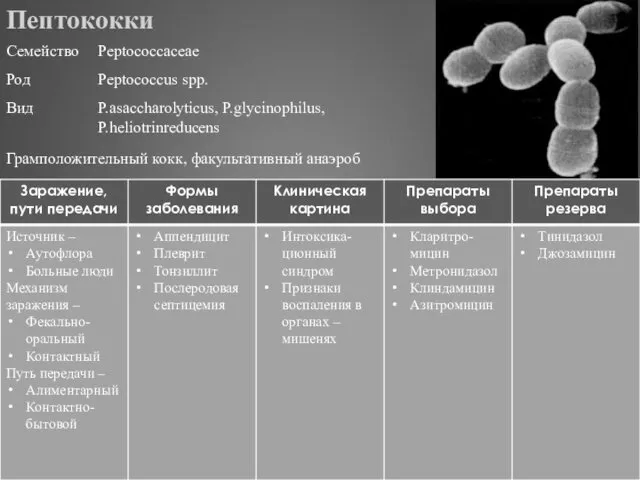
- 318. Пептококки
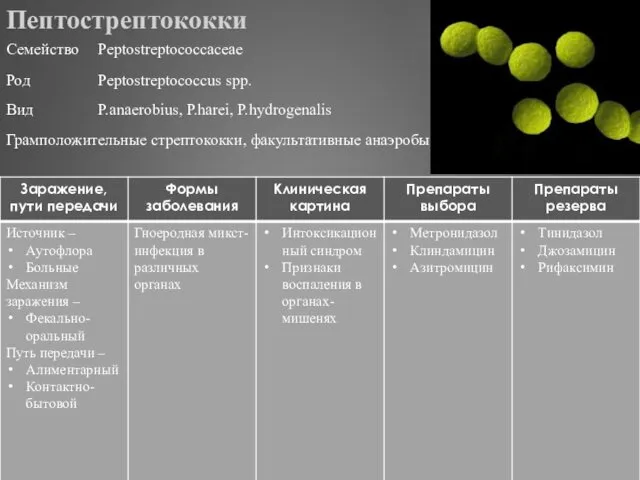
- 319. Пептострептококки
- 320. Фузобактерии
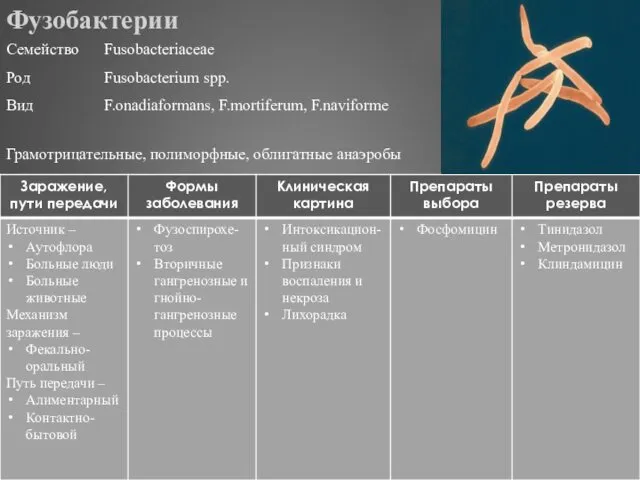
- 321. Микоплазмы
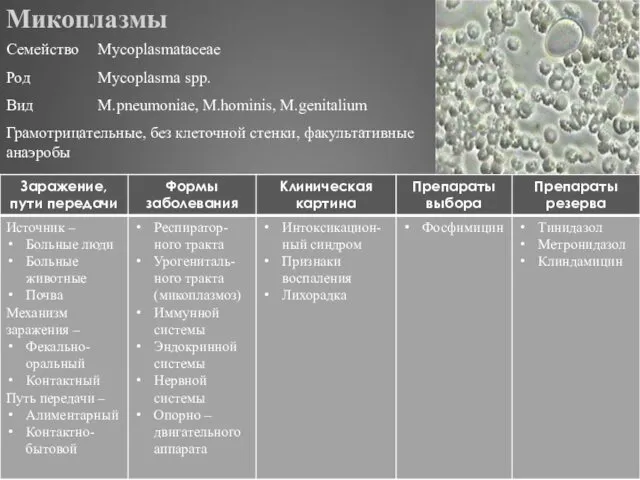
- 322. Риккетсии
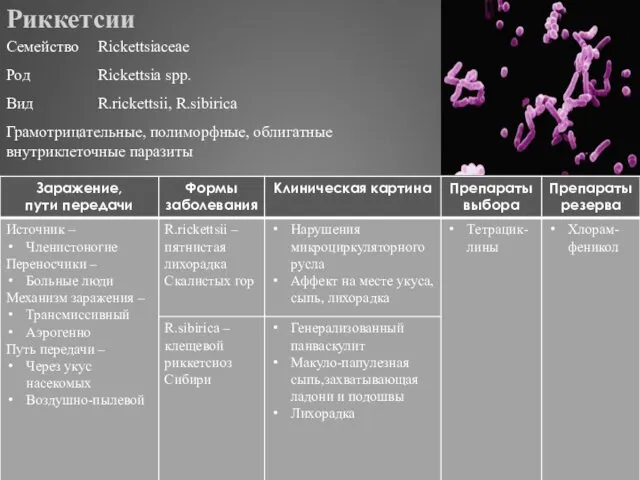
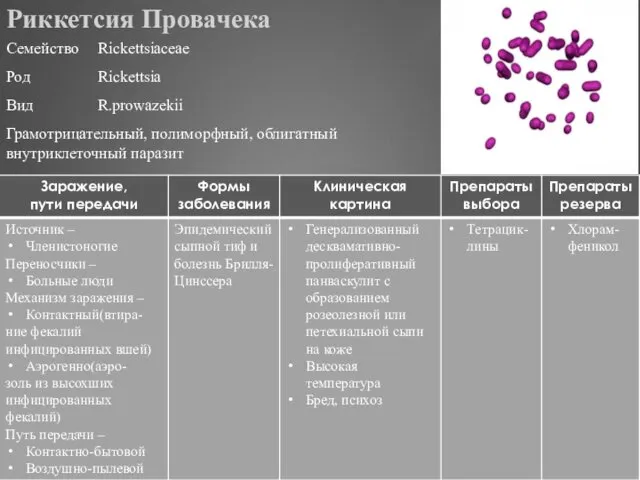
- 323. Риккетсия Провачека
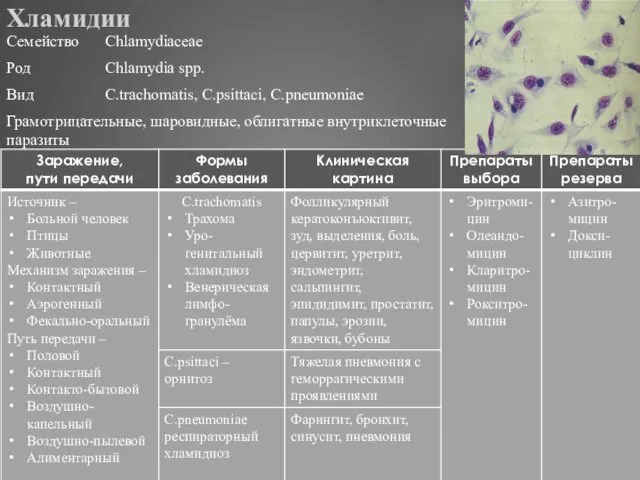
- 324. Хламидии
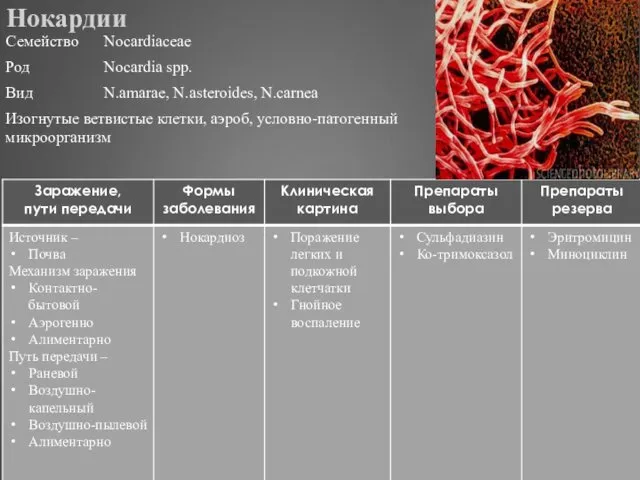
- 325. Нокардии
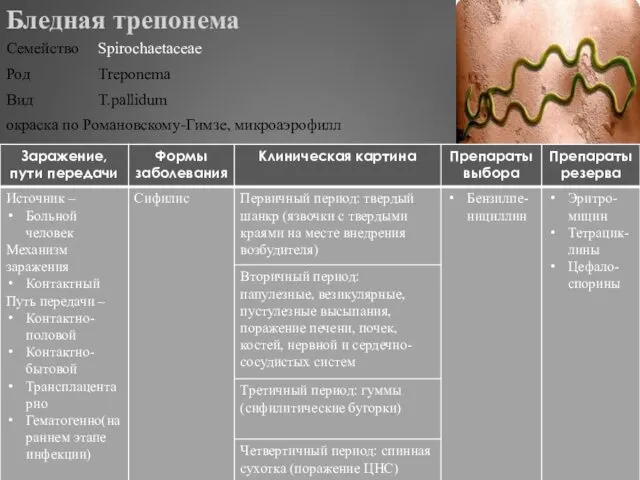
- 326. Бледная трепонема
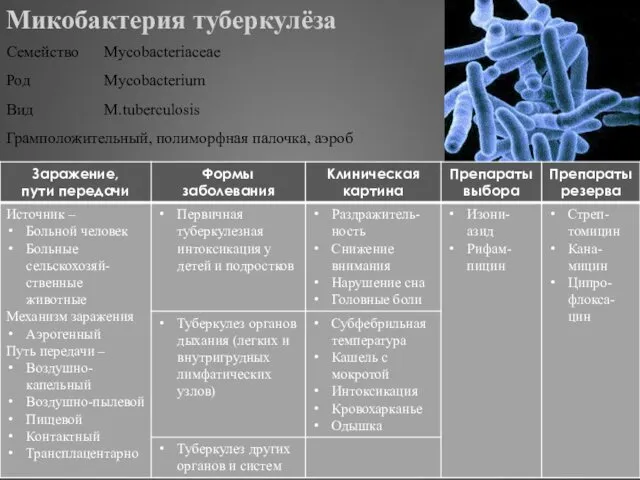
- 327. Микобактерия туберкулёза
- 328. Холерный вибрион
- 329. Франциселла
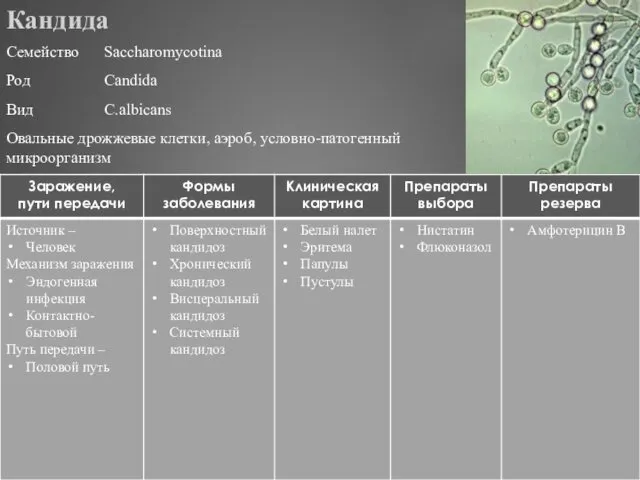
- 330. Кандида
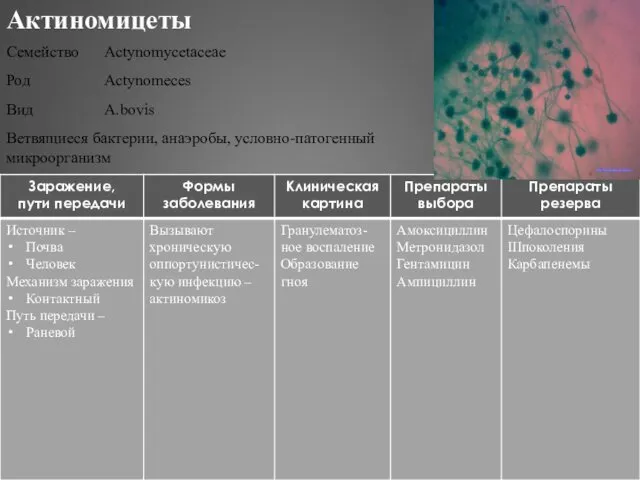
- 331. Актиномицеты
- 332. spp. spp. - это сокращение от латинского «speciales» (виды) Пишется после названия семейства или рода организма,
- 334. Скачать презентацию
















































































































































































































































 Современные представления о миоме матки
Современные представления о миоме матки Лекарственные средства, применяемые при заболеваниях ЖКТ
Лекарственные средства, применяемые при заболеваниях ЖКТ Виды повязок
Виды повязок Методы диагностики гипертрофии миокарда
Методы диагностики гипертрофии миокарда Модели врачевания
Модели врачевания Желтухи новорождённых и детей раннего возраста
Желтухи новорождённых и детей раннего возраста Современный подход к лечению метастатической меланомы кожи
Современный подход к лечению метастатической меланомы кожи Исследовательская работа на тему: Здоровый образ жизни и нетрадиционная медицина
Исследовательская работа на тему: Здоровый образ жизни и нетрадиционная медицина Вирусы и бактериофаги
Вирусы и бактериофаги Жарақат, түрлері, негізгі белгілері, инфицирленуі, асқынулары, ағымы, жазылу этаптары, емі, асқынудың алдын алу шаралары
Жарақат, түрлері, негізгі белгілері, инфицирленуі, асқынулары, ағымы, жазылу этаптары, емі, асқынудың алдын алу шаралары Гомеопатия
Гомеопатия Гипогонадизм. Гирсутизм
Гипогонадизм. Гирсутизм Травматизм и профессиональные заболевания в отрасли
Травматизм и профессиональные заболевания в отрасли Неотложная помощь при бронхообструктивном синдроме
Неотложная помощь при бронхообструктивном синдроме Ауруларды зерделеудегі эпидемиологиялық тәсіл. Жұқпалы және паразитарлы ауруларды тіркеу және есепке алу
Ауруларды зерделеудегі эпидемиологиялық тәсіл. Жұқпалы және паразитарлы ауруларды тіркеу және есепке алу Презентация Шестакова Ф-21
Презентация Шестакова Ф-21 ҚР бала тұрғындарына амбулаторлық көмек көрсетуді ұйымдастыру. Ана және нәресте қлімін
ҚР бала тұрғындарына амбулаторлық көмек көрсетуді ұйымдастыру. Ана және нәресте қлімін Метод использования виртуальной реальности для коррекции осанки у детей с синдромом гипермобильности суставов
Метод использования виртуальной реальности для коррекции осанки у детей с синдромом гипермобильности суставов Инфекционный контроль и профилактика внутрибольничных инфекций (ВБИ)
Инфекционный контроль и профилактика внутрибольничных инфекций (ВБИ) Қазақстандағы әлеуметтік медициналық сақтандыру туралы
Қазақстандағы әлеуметтік медициналық сақтандыру туралы Синдром респираторных расстройств у новорожденных
Синдром респираторных расстройств у новорожденных Протезирование на имплантатах
Протезирование на имплантатах Кардиотоники. Сердечные гликозиды
Кардиотоники. Сердечные гликозиды Здоровое питание
Здоровое питание Физиология вегетативной нервной системы
Физиология вегетативной нервной системы Сердечный цикл, проводящая система сердца, распространение возбуждения по миокарду
Сердечный цикл, проводящая система сердца, распространение возбуждения по миокарду Ортаңғы және ішкі құлақ аурулары. Саңыраулық және мылқаулық орта кұлактың жедел және созылмалы кабынуы мастоидит
Ортаңғы және ішкі құлақ аурулары. Саңыраулық және мылқаулық орта кұлактың жедел және созылмалы кабынуы мастоидит Особенности операции удаления временных и постоянных зубов у детей
Особенности операции удаления временных и постоянных зубов у детей