Серологические маркеры парентеральных вирусных гепатитов: диагностическая значимость и интерпретация результатов презентация
Содержание
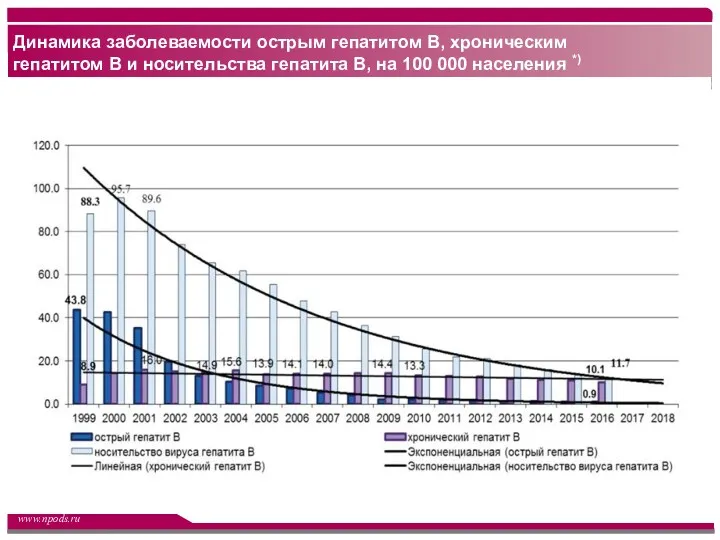
- 2. Динамика заболеваемости острым гепатитом В, хроническим гепатитом В и носительства гепатита В, на 100 000 населения
- 3. ООО «НПО «Диагностические системы», 2017г Диагностика оккультного гепатита В и выявление мутантных форм HВsAg
- 4. Латентная HBV инфекция Низкий уровень репликации HBV, сниженный синтез и экспрессия вирусных антигенов. Адекватный ответ иммунной
- 5. Клинический случай № 1 Пациент, мужчина, 20 лет, не злоупотребляющий алкоголем. Поступил в стационар с признаками
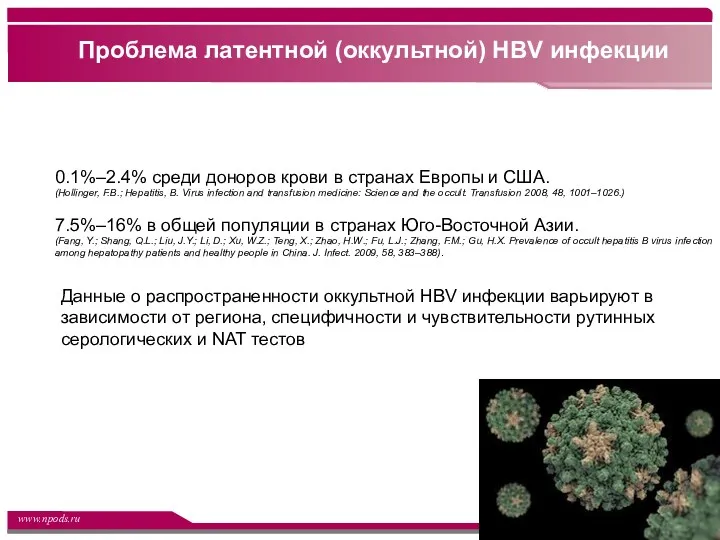
- 6. Проблема латентной (оккультной) HBV инфекции 0.1%–2.4% среди доноров крови в странах Европы и США. (Hollinger, F.B.;
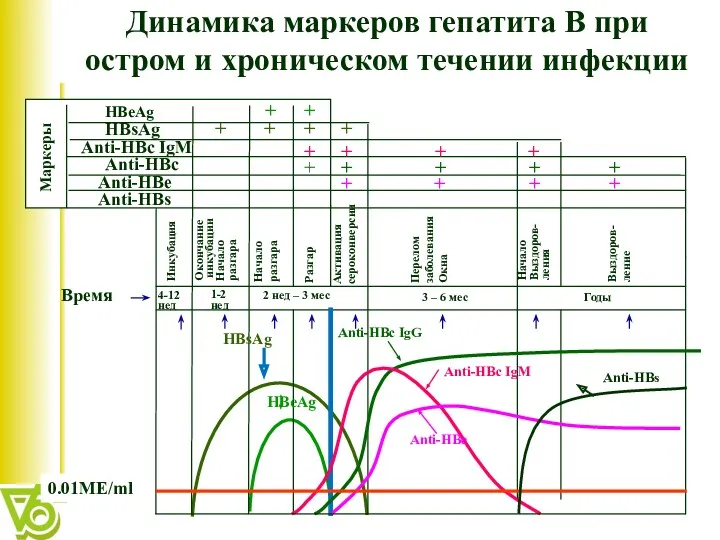
- 7. Динамика маркеров гепатита В при остром и хроническом течении инфекции Время Инкубация Окончание инкубации Начало разгара
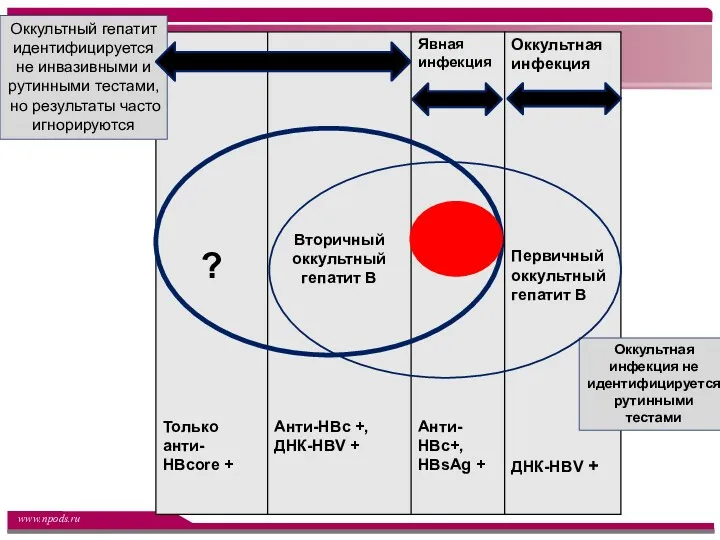
- 8. Оккультный гепатит идентифицируется не инвазивными и рутинными тестами, но результаты часто игнорируются Оккультная инфекция не идентифицируется
- 9. Проблема латентной (оккультной) HBV инфекции 2004 г. HBV ДНК “+” HBsAg “-” с/без антиHBs[1] 2006 г.
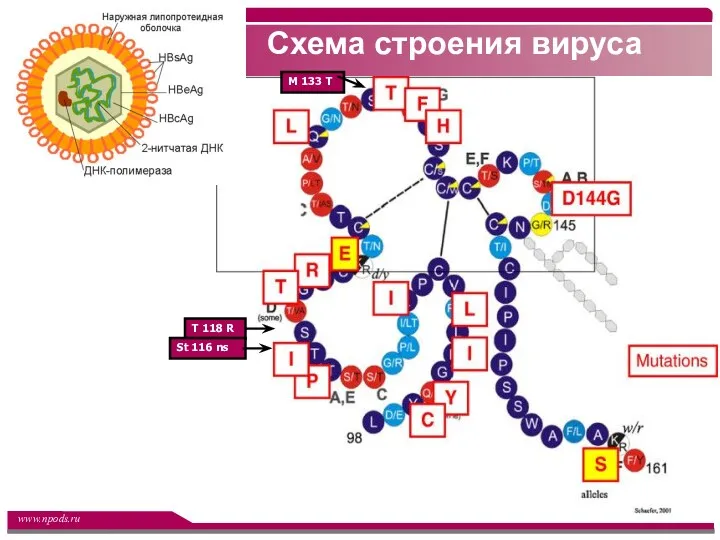
- 10. Схема строения вируса M 133 T Т 118 R St 116 ns
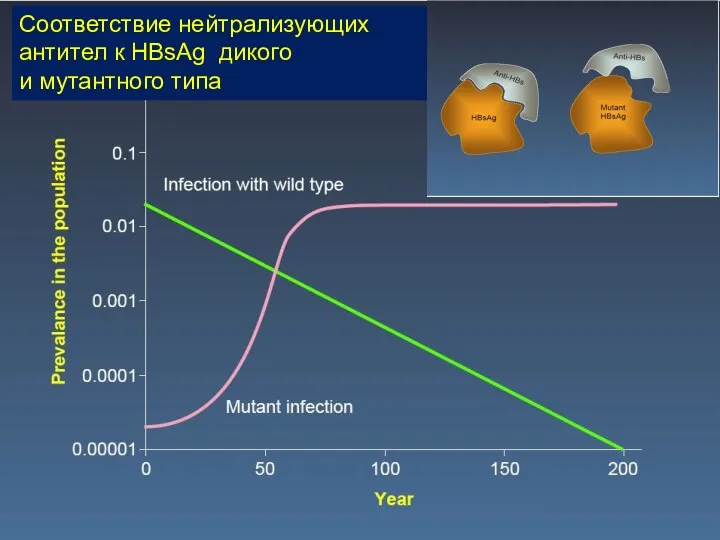
- 11. Соответствие нейтрализующих антител к HBsAg дикого и мутантного типа
- 12. «Мутантные формы вируса гепатита B могут возникать у пациентов под воздействием иммунного ответа или лечения. Мутантные
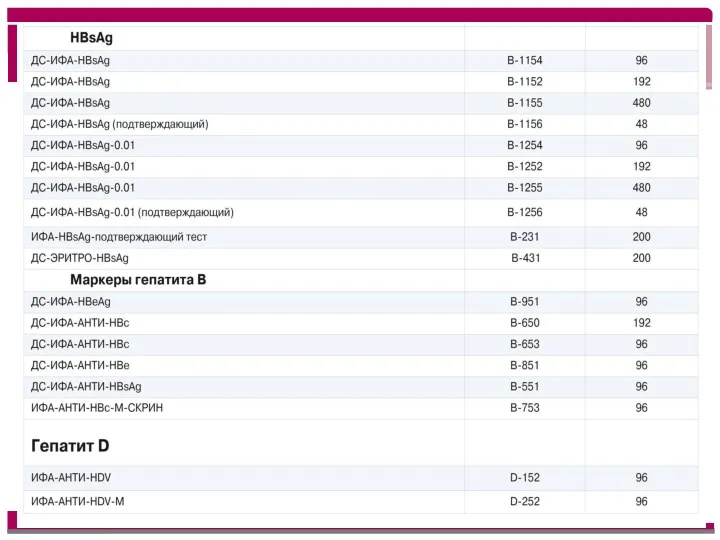
- 13. «ДС-ИФА-HBsAg-0,01» ИММУНОФЕРМЕНТНАЯ ТЕСТ-СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ HBsAg С ПОВЫШЕННОЙ ЧУВСТВИТЕЛЬНОСТЬЮ к HBsAg, равной 0,01 МЕ/мл
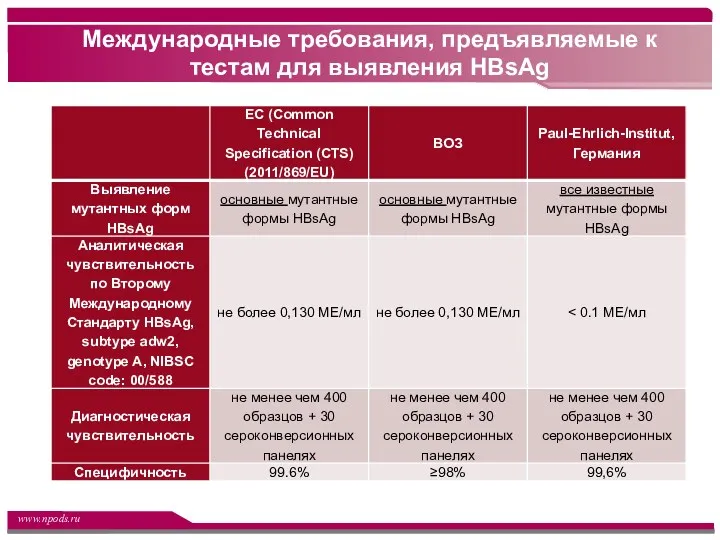
- 14. Международные требования, предъявляемые к тестам для выявления HBsAg
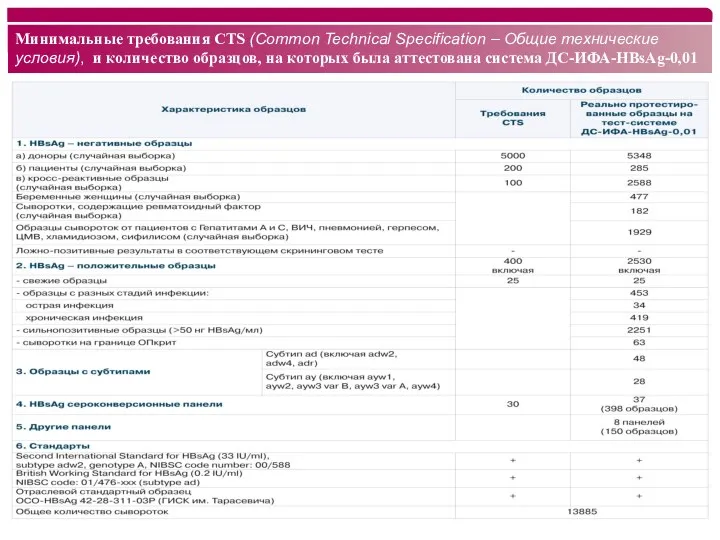
- 15. Минимальные требования CTS (Common Technical Specification – Общие технические условия), и количество образцов, на которых была
- 16. Prüflabor für In-vitro Diagnostika beim Paul-Ehrlich-Institut (PEI-IVD) Paul-Ehrlich-Straße 51-59 D-63225 Langen Evaluation Report for DS-EIA-HBsAg-0,01 Manufacturer:
- 17. For six seroconversion panels DS‐EIA‐HBsAg‐0.01 assay detected HBsAg seroconversion on average 1.3 specimens earlier than the
- 18. Согласно требованиям ведущих международных организаций, работающих в области здравоохранения (ВОЗ, PEI), оценка чувствительности тестов, применяемых для
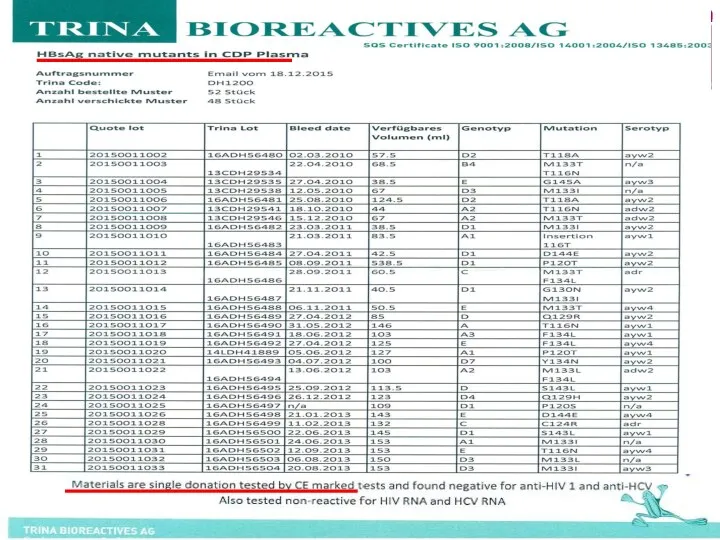
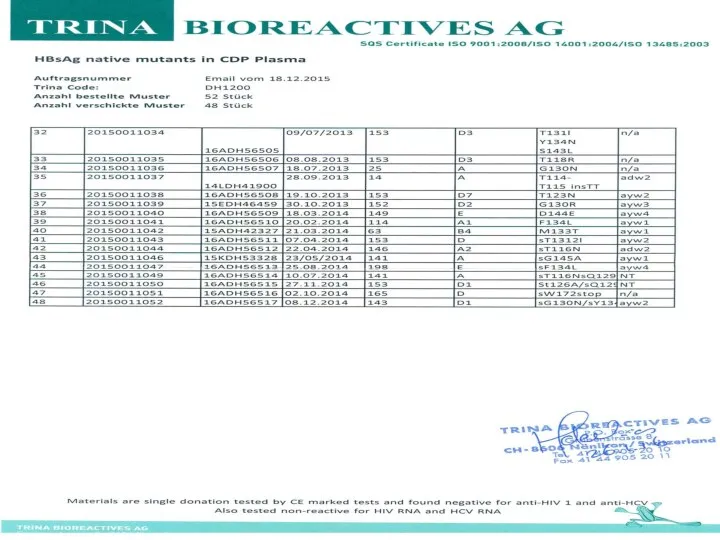
- 19. НВsAg native mutants in CDP Plasma (Trina Code: DH1200)
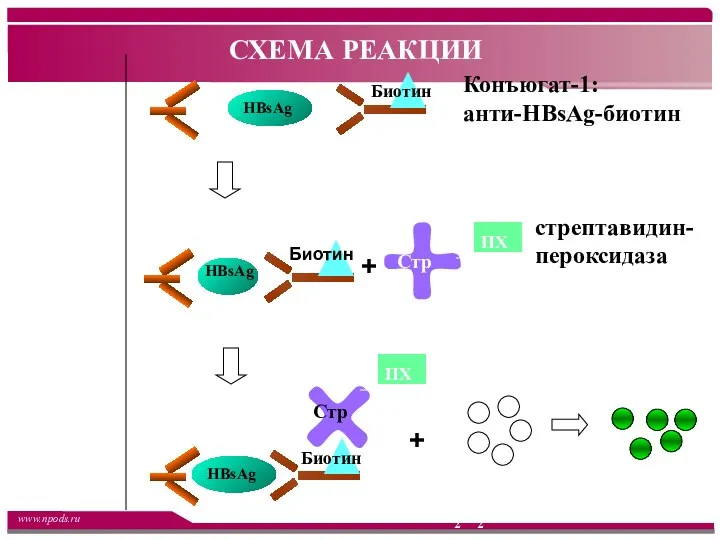
- 21. Конъюгат-1: анти-HBsAg-биотин Монокло-нальные антитела к HBsAg + ПХ Стр стрептавидин-пероксидаза хрена + + + Стр ПХ
- 22. ДС-ИФА-HBsAg-0,01 Единственная Российская тест-система сетифицированная по EC, рекомендованная ВОЗ и институтом Пауля-Эрлиха для диагностики вирусного гепатита
- 23. Скрининг на анти-HBc: делать или не делать? Аргументы «за»: Период “core window” – второе серологическое окно
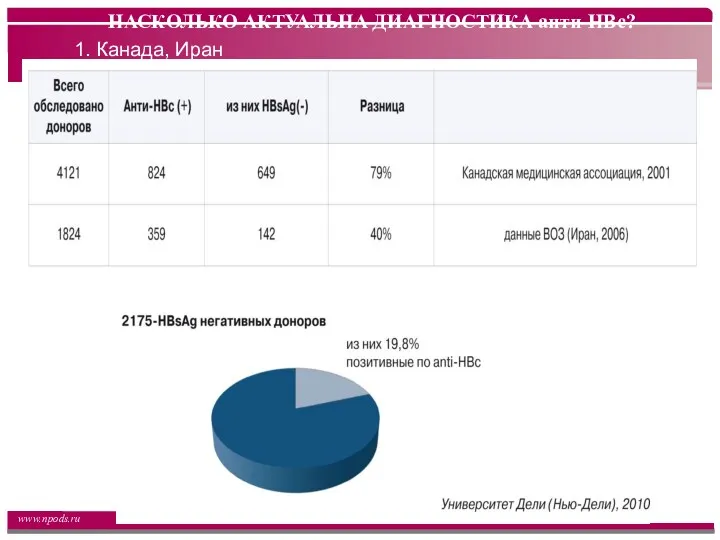
- 24. НАСКОЛЬКО АКТУАЛЬНА ДИАГНОСТИКА анти-HBc? 1. Канада, Иран 2. Индия
- 25. «…Частота выявления только анти-HBc напрямую связана с распространенностью ВГB-инфекции. К примеру, среди доноров в районах с
- 26. Скрининг на анти-HBc Скрининг обязателен: США Япония Франция Страны Латинской Америки (Бразилия, Уругвай, Колумбия) Отдельные регионы
- 28. Диагностика Вирусного Гепатита С с помощью тест-системы для одновременного определения Антигена и Антител к HCV ООО
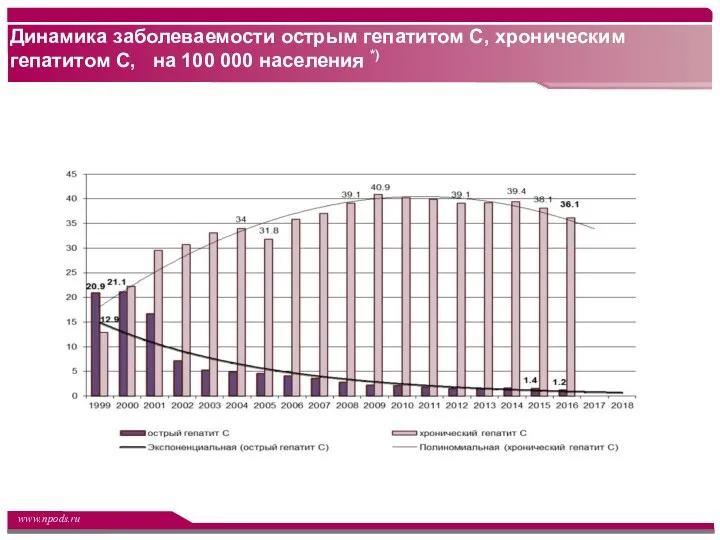
- 29. Динамика заболеваемости острым гепатитом С, хроническим гепатитом С, на 100 000 населения *)
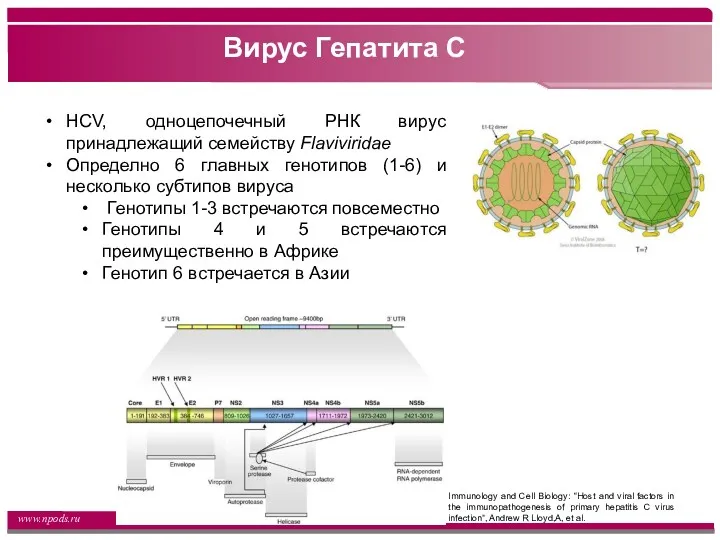
- 30. Вирус Гепатита С HCV, одноцепочечный РНК вирус принадлежащий семейству Flaviviridae Определно 6 главных генотипов (1-6) и
- 31. Введение тестирования с использованием технологий по определению нуклеиновых кислот (NAT) позволяет и дальше уменьшать период окна
- 32. Тесты для диагностики Гепатита С ИФА Доступная цена Высокая чувствительность Простота постановки Ложно-позитивные результаты Аутоиммунные процессы
- 33. 2010 – Компания ООО НПО Диагностические системы подписала соглашение о совместной работы с Центром по контроля
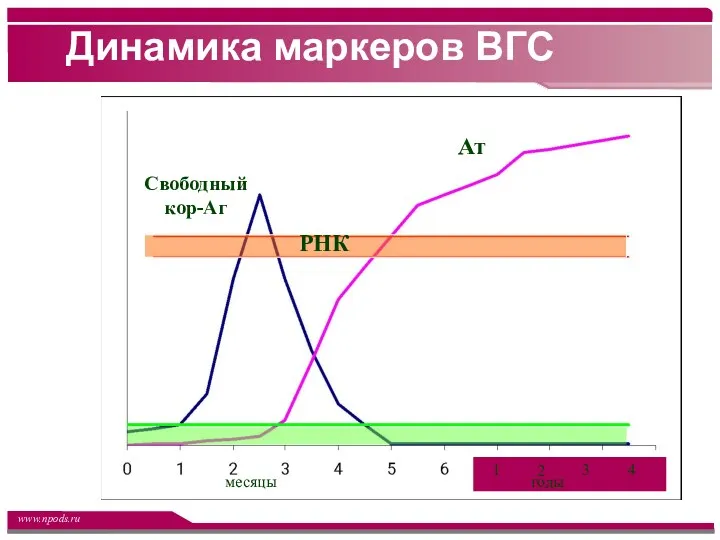
- 34. Динамика маркеров ВГС
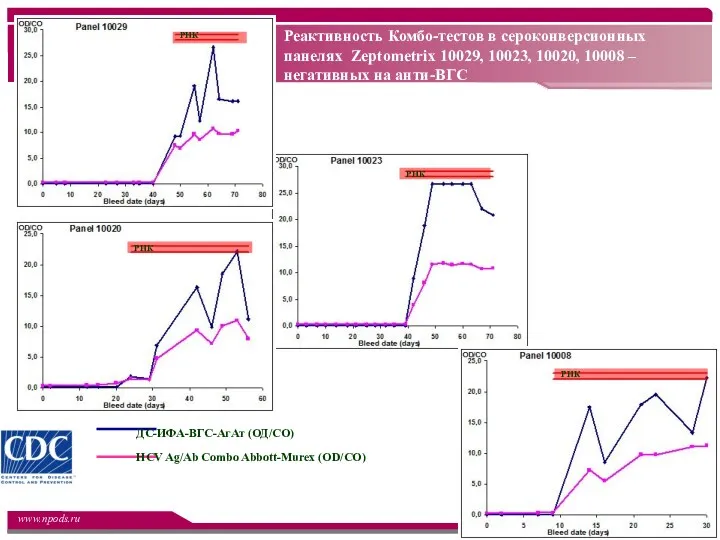
- 35. Реактивность Комбо-тестов в сероконверсионных панелях Zeptometrix 10029, 10023, 10020, 10008 – негативных на анти-ВГС
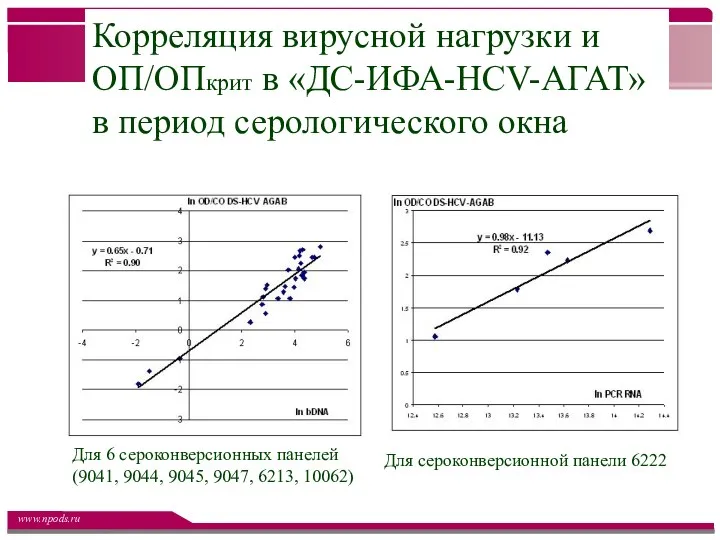
- 36. Корреляция вирусной нагрузки и ОП/ОПкрит в «ДС-ИФА-HCV-АГАТ» в период серологического окна Для 6 сероконверсионных панелей (9041,
- 37. ДС-ИФА-HCV-АГАТ Формат теста: 50 мкл конъюгата 1 (анти-кор Маб меченые биотином) + 50 мкл образца 30
- 38. УТВЕРЖДЕНЫ постановлением Правительства Российской Федерации от 31 декабря 2010 г. № 1230 Правила и методы исследований
- 39. ДС-ИФА-HCV-АГ Суммарное время инкубации – 1час 15 мин (шейкер), Срок годности – 13 месяцев
- 40. Общая цель Плана действий – к 2030 г. добиться элиминации вирусных гепатитов как угрозы общественному здоровью
- 42. Скачать презентацию





















 СПИД - чума ХХI века
СПИД - чума ХХI века Гинекологиялық операциялардан кейінгі науқастардың тамақтануы
Гинекологиялық операциялардан кейінгі науқастардың тамақтануы Диагностика и лечение постменопаузального остеопороза 45
Диагностика и лечение постменопаузального остеопороза 45 Воздействие сотовой связи на человека
Воздействие сотовой связи на человека Роль фельдшера в диагностике и лечении бронхиальной астмы у детей
Роль фельдшера в диагностике и лечении бронхиальной астмы у детей Обязательное медицинское страхование
Обязательное медицинское страхование ҚР бала тұрғындарына амбулаторлық көмек көрсетуді ұйымдастыру. Ана және нәресте қлімін
ҚР бала тұрғындарына амбулаторлық көмек көрсетуді ұйымдастыру. Ана және нәресте қлімін Профессиональная гигиена полости рта
Профессиональная гигиена полости рта Сборник патанатомических микропрепаратов
Сборник патанатомических микропрепаратов Іріңді паротит. Мастит. Парапроктит, лимфангаит, лимфаденит, тромбофлебит
Іріңді паротит. Мастит. Парапроктит, лимфангаит, лимфаденит, тромбофлебит Профессиональная гигиена полости рта
Профессиональная гигиена полости рта Средства, влияющие на функцию органов дыхания
Средства, влияющие на функцию органов дыхания Диагностика цервикальных неоплазий у женщин репродуктивного возраста
Диагностика цервикальных неоплазий у женщин репродуктивного возраста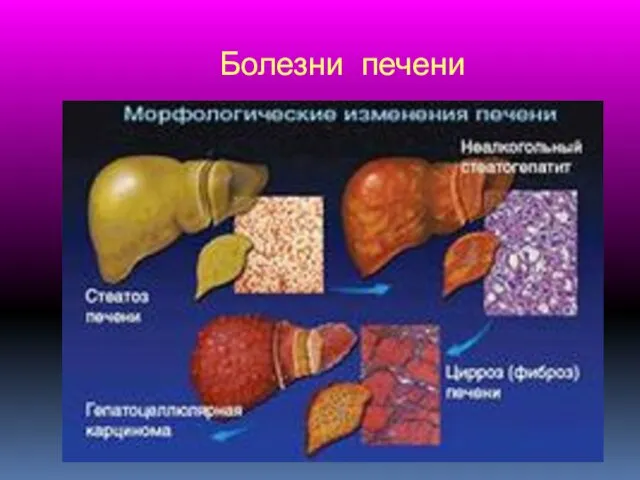 Болезни печени. Острая печеночная неодостаточность
Болезни печени. Острая печеночная неодостаточность Акушерские кровотечения
Акушерские кровотечения Бейспецификалық жаралы колит
Бейспецификалық жаралы колит Заболевания гипоталамогипофизарно-надпочечниковой системы
Заболевания гипоталамогипофизарно-надпочечниковой системы Введение в медицинскую информатику
Введение в медицинскую информатику Гибридные методы лучевой диагностики
Гибридные методы лучевой диагностики Виды костей человека и их соединения
Виды костей человека и их соединения Гигиена голоса
Гигиена голоса Мази №3
Мази №3 Жүкті әйелдердің, балалардың, қарт адамдардың тыныс алу жүйесінің визуальді диагностикасыны ерекшеліктерің
Жүкті әйелдердің, балалардың, қарт адамдардың тыныс алу жүйесінің визуальді диагностикасыны ерекшеліктерің Местное лечение заболеваний пародонта
Местное лечение заболеваний пародонта Контагиозный моллюск
Контагиозный моллюск Вирусты дерматоздар
Вирусты дерматоздар Физиологические роды. Обезболивание родов
Физиологические роды. Обезболивание родов Организация сестринской помощи при термических поражениях
Организация сестринской помощи при термических поражениях