Содержание
- 2. Адаптивный B-клеточный иммунный ответ работает по принципу клональной селекции. - Стволовая клетка дает начало огромному разнообразию
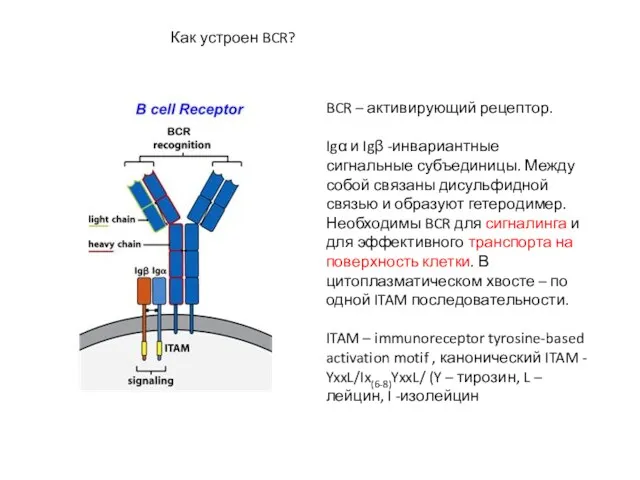
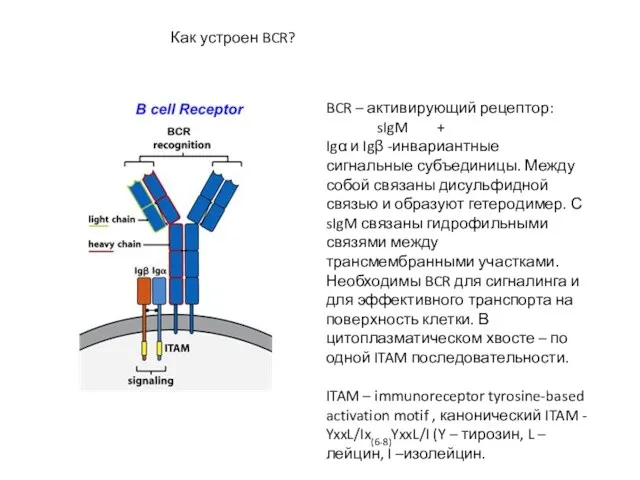
- 3. BCR – активирующий рецептор. Igα и Igβ -инвариантные сигнальные субъединицы. Между собой связаны дисульфидной связью и
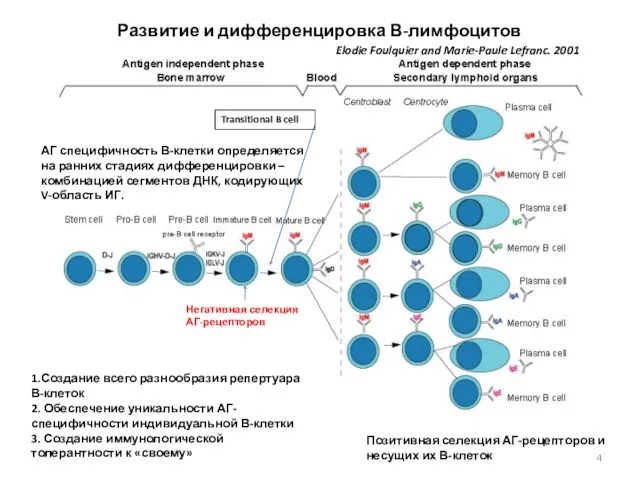
- 4. Развитие и дифференцировка В-лимфоцитов Elodie Foulquier and Marie-Paule Lefranc. 2001 АГ специфичность В-клетки определяется на ранних
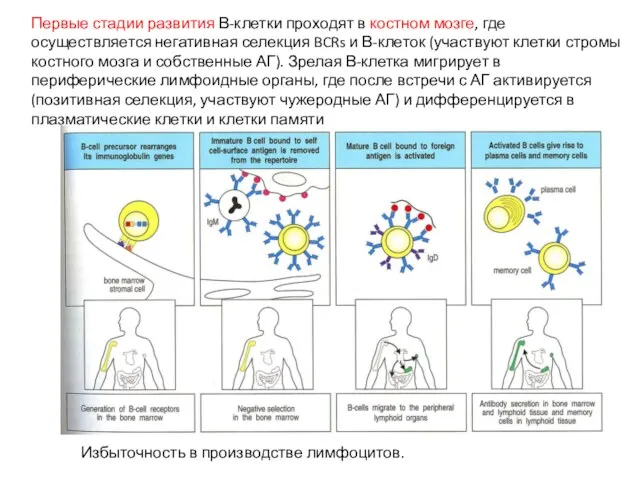
- 5. Первые стадии развития В-клетки проходят в костном мозге, где осуществляется негативная селекция BCRs и В-клеток (участвуют
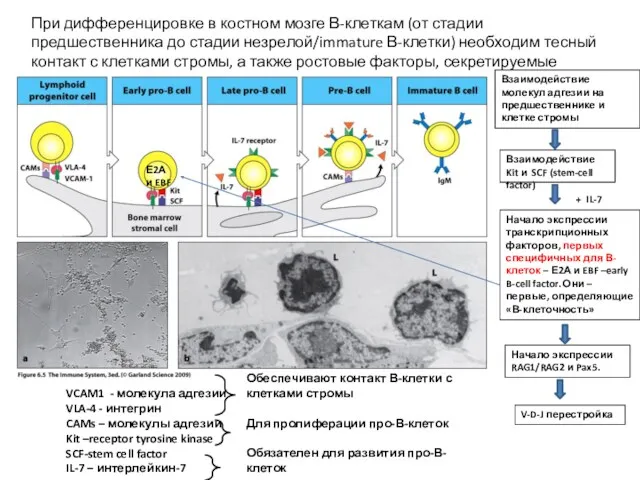
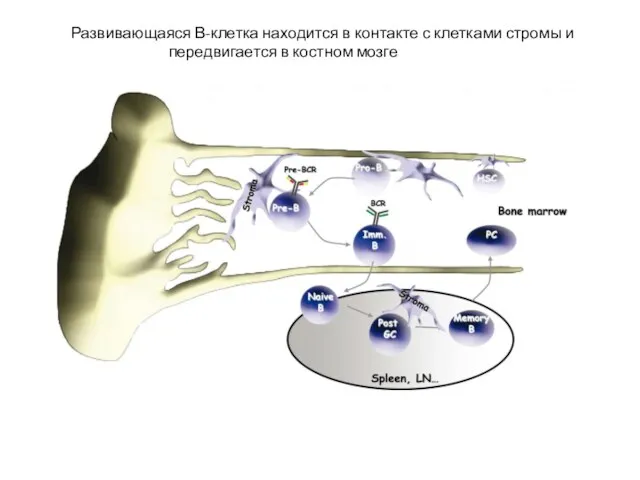
- 6. При дифференцировке в костном мозге В-клеткам (от стадии предшественника до стадии незрелой/immature В-клетки) необходим тесный контакт
- 7. Развивающаяся В-клетка находится в контакте с клетками стромы и передвигается в костном мозге
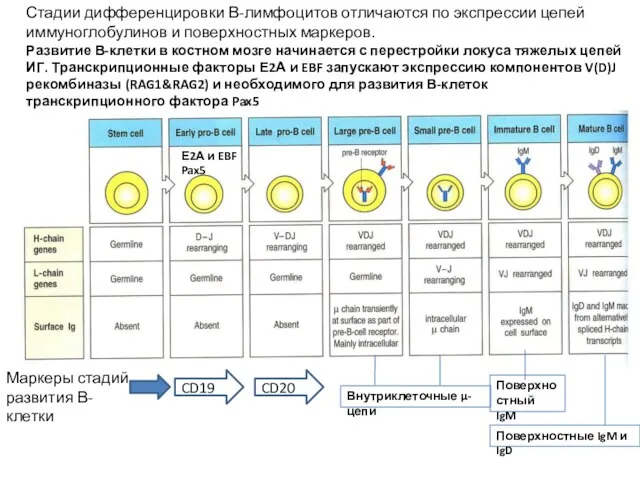
- 8. Стадии дифференцировки В-лимфоцитов отличаются по экспрессии цепей иммуноглобулинов и поверхностных маркеров. Развитие В-клетки в костном мозге
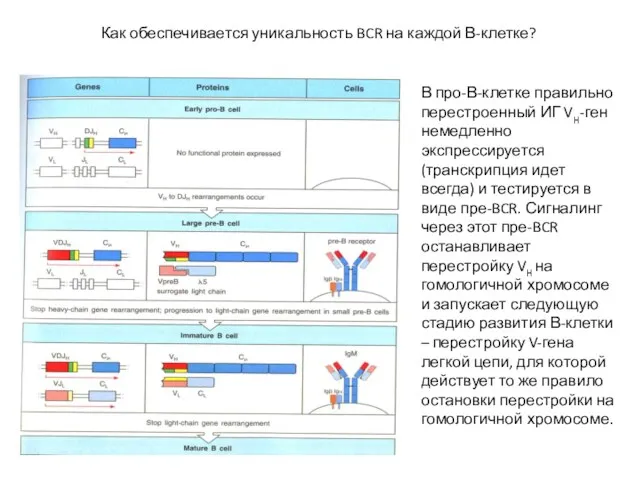
- 9. В про-В-клетке правильно перестроенный ИГ VH-ген немедленно экспрессируется (транскрипция идет всегда) и тестируется в виде пре-BCR.
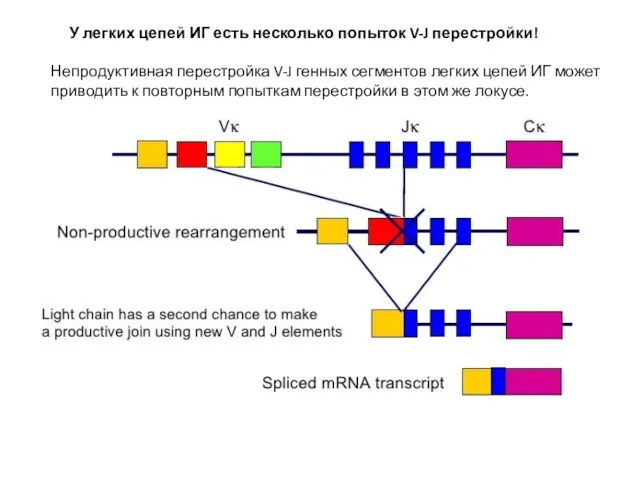
- 10. У легких цепей ИГ есть несколько попыток V-J перестройки! Непродуктивная перестройка V-J генных сегментов легких цепей
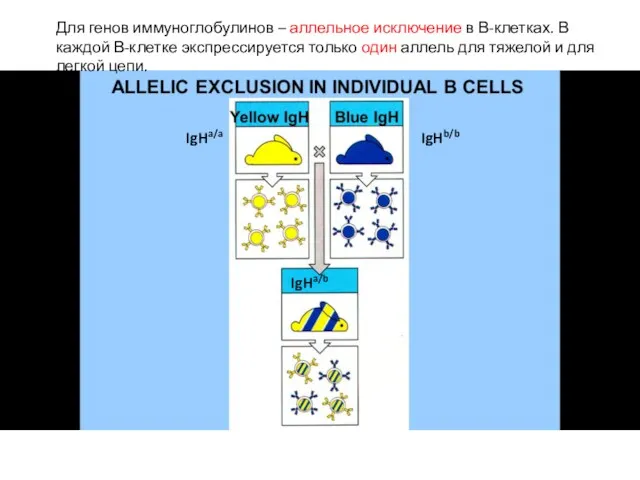
- 11. IgHa/a IgHb/b IgHa/b Для генов иммуноглобулинов – аллельное исключение в В-клетках. В каждой В-клетке экспрессируется только
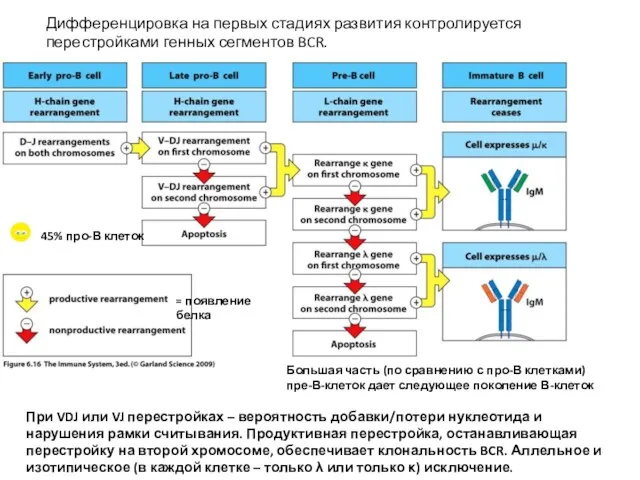
- 12. Дифференцировка на первых стадиях развития контролируется перестройками генных сегментов BCR. При VDJ или VJ перестройках –
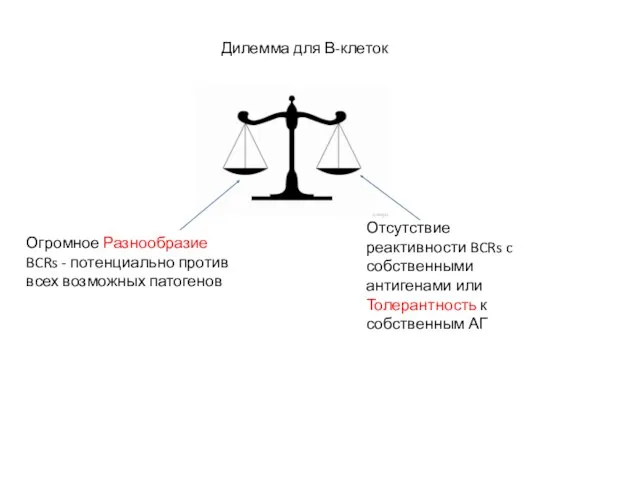
- 13. Дилемма для В-клеток Огромное Разнообразие BCRs - потенциально против всех возможных патогенов Отсутствие реактивности BCRs c
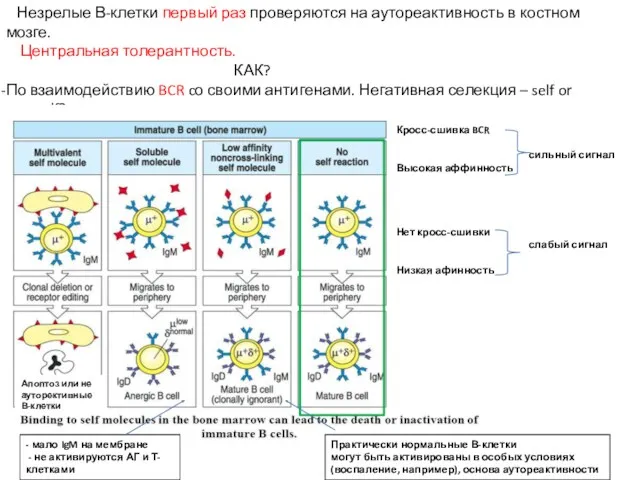
- 14. Незрелые В-клетки первый раз проверяются на аутореактивность в костном мозге. Центральная толерантность. КАК? По взаимодействию BCR
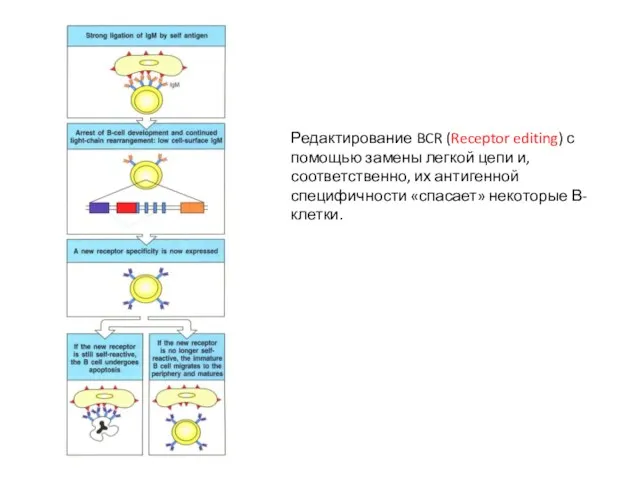
- 15. Редактирование BCR (Receptor editing) с помощью замены легкой цепи и, соответственно, их антигенной специфичности «спасает» некоторые
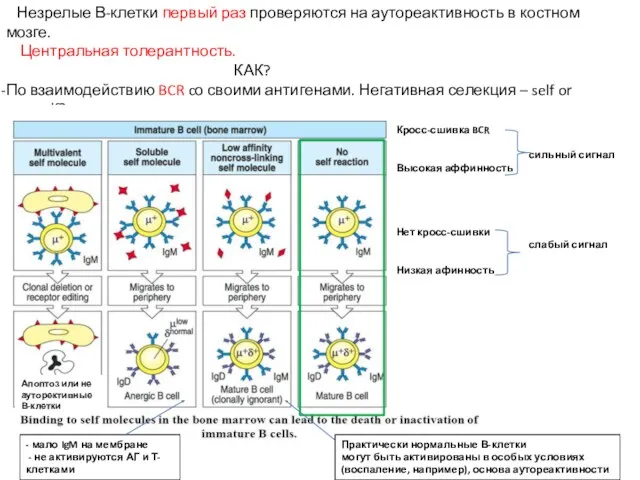
- 16. Незрелые В-клетки первый раз проверяются на аутореактивность в костном мозге. Центральная толерантность. КАК? По взаимодействию BCR
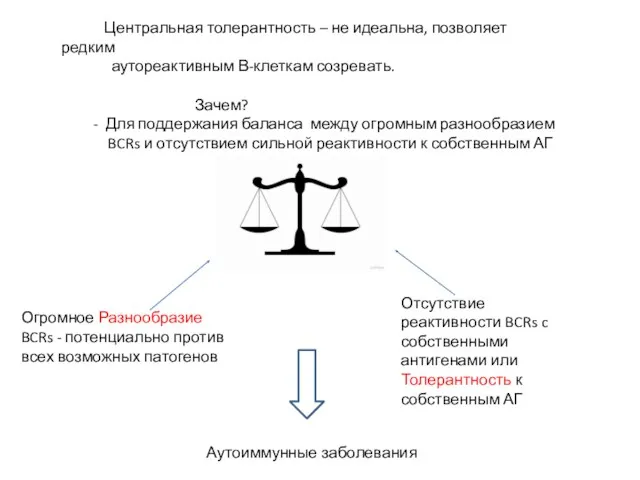
- 17. Центральная толерантность – не идеальна, позволяет редким аутореактивным В-клеткам созревать. Зачем? - Для поддержания баланса между
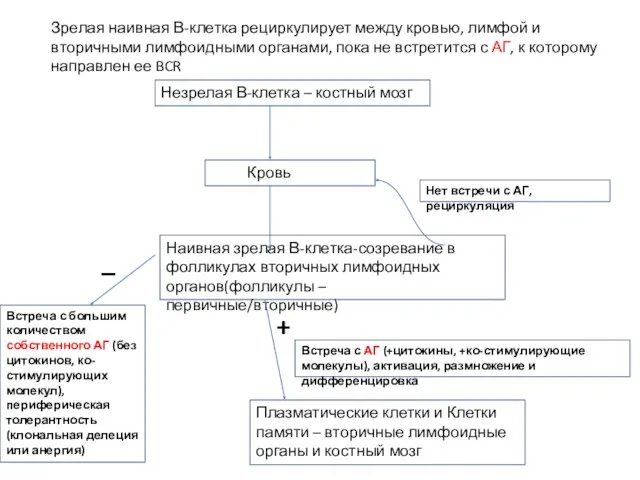
- 18. Наивная зрелая В-клетка-созревание в фолликулах вторичных лимфоидных органов(фолликулы – первичные/вторичные) Кровь Встреча с АГ (+цитокины, +ко-стимулирующие
- 19. BCR – В-клеточный рецептор Для чего нужен BCR? - Для взаимодействия В-клетки с окружающей внеклеточной средой.
- 20. BCR – активирующий рецептор: sIgM + Igα и Igβ -инвариантные сигнальные субъединицы. Между собой связаны дисульфидной
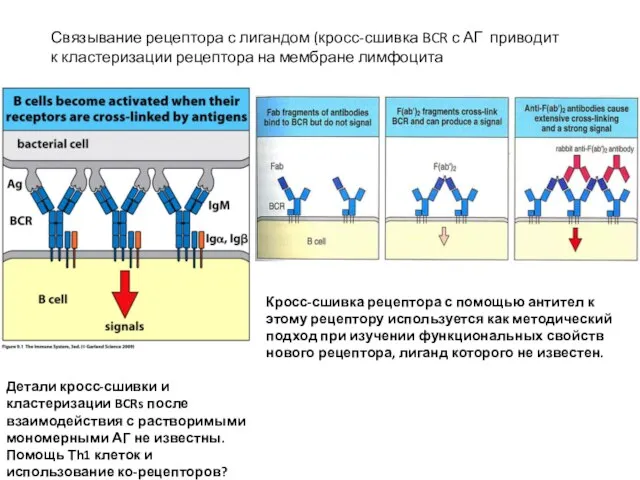
- 21. Связывание рецептора с лигандом (кросс-сшивка BCR с АГ приводит к кластеризации рецептора на мембране лимфоцита Кросс-сшивка
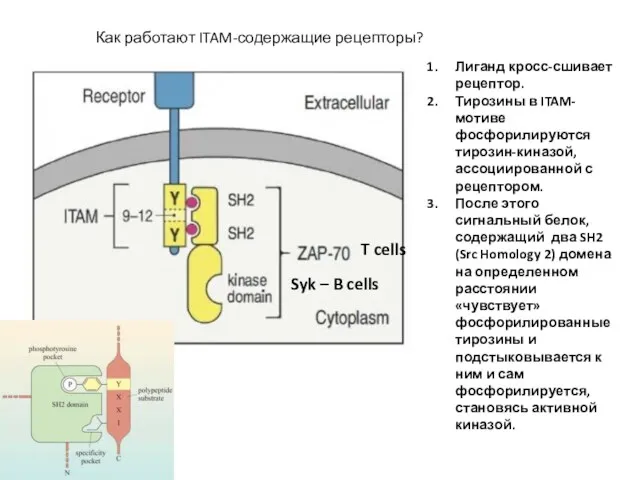
- 22. Как работают ITAM-содержащие рецепторы? Лиганд кросс-сшивает рецептор. Тирозины в ITAM-мотиве фосфорилируются тирозин-киназой, ассоциированной с рецептором. После
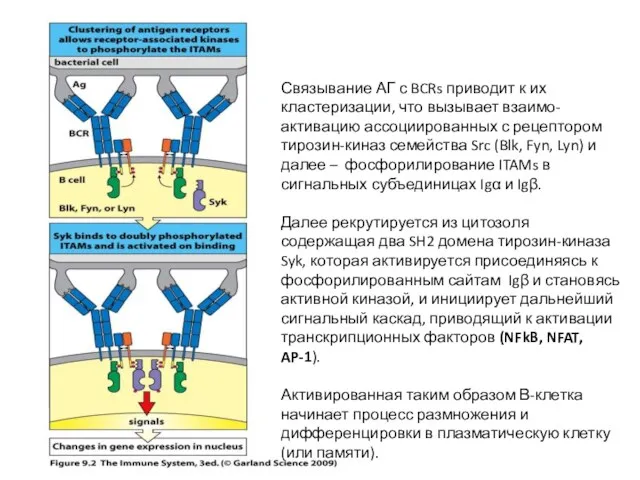
- 23. Связывание АГ с BCRs приводит к их кластеризации, что вызывает взаимо-активацию ассоциированных с рецептором тирозин-киназ семейства
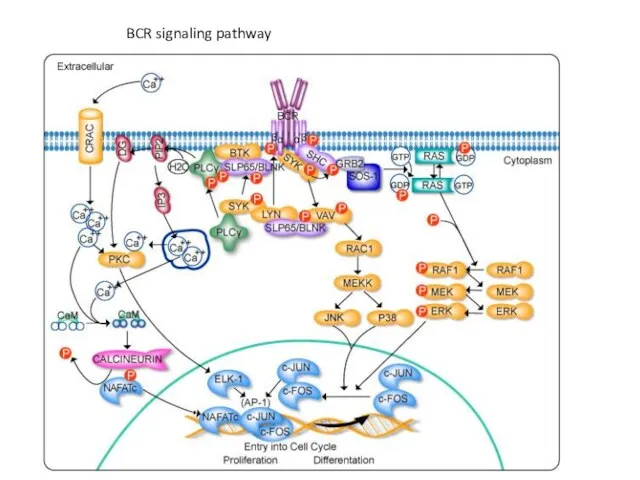
- 24. BCR signaling pathway
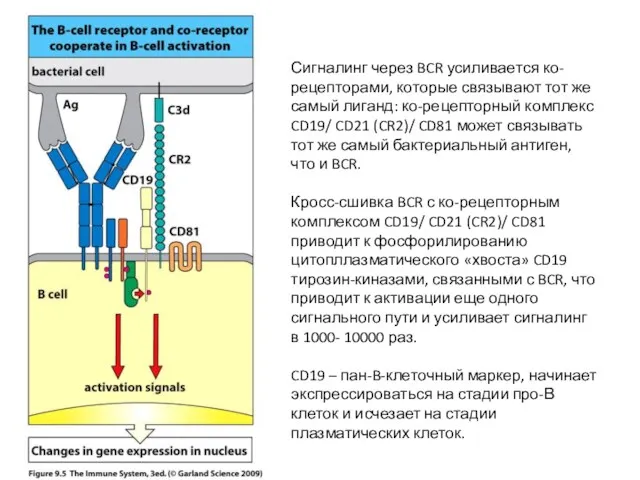
- 25. Сигналинг через BCR усиливается ко-рецепторами, которые связывают тот же самый лиганд: ко-рецепторный комплекс CD19/ CD21 (CR2)/
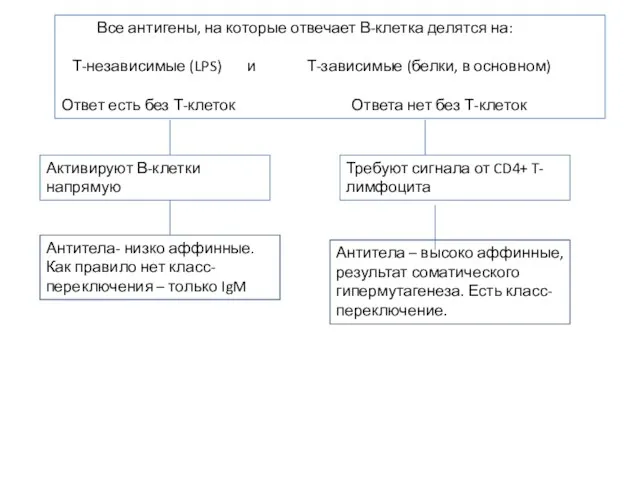
- 26. Все антигены, на которые отвечает В-клетка делятся на: Т-независимые (LPS) и Т-зависимые (белки, в основном) Ответ
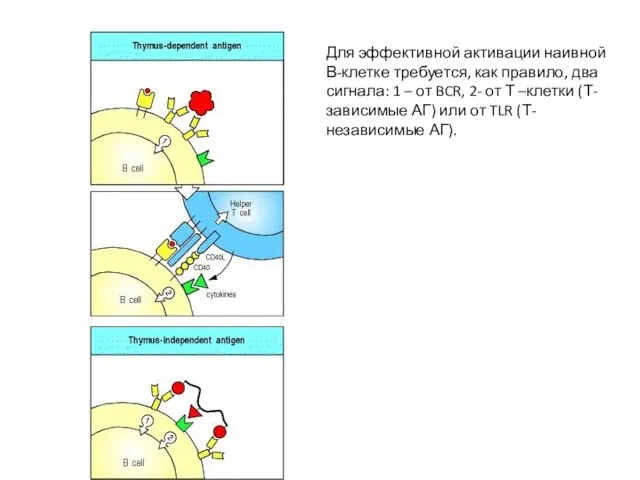
- 27. Для эффективной активации наивной В-клетке требуется, как правило, два сигнала: 1 – от BCR, 2- от
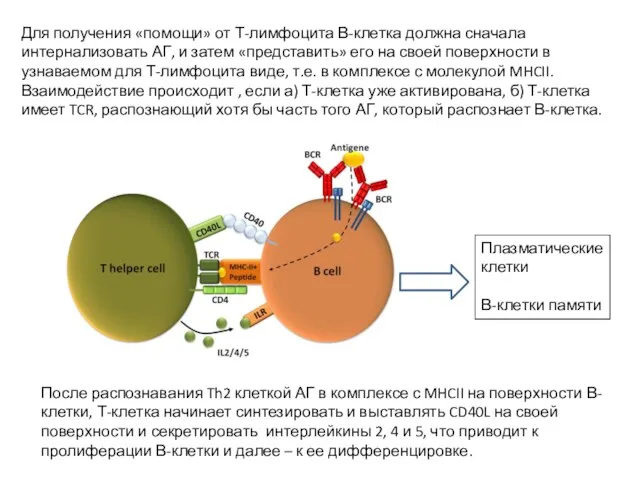
- 28. Для получения «помощи» от Т-лимфоцита В-клетка должна сначала интернализовать АГ, и затем «представить» его на своей
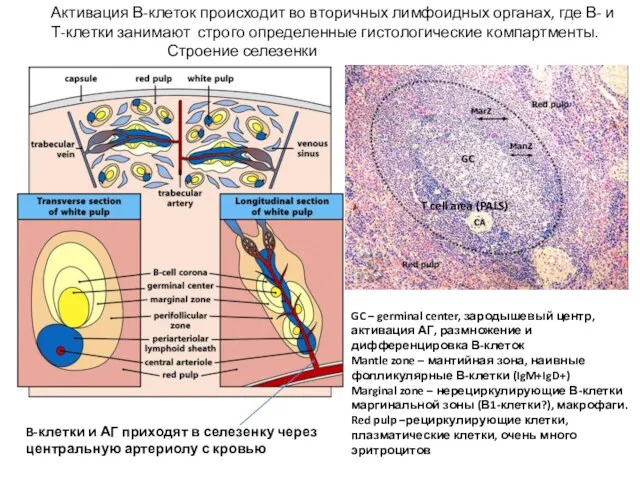
- 29. Активация В-клеток происходит во вторичных лимфоидных органах, где В- и Т-клетки занимают строго определенные гистологические компартменты.
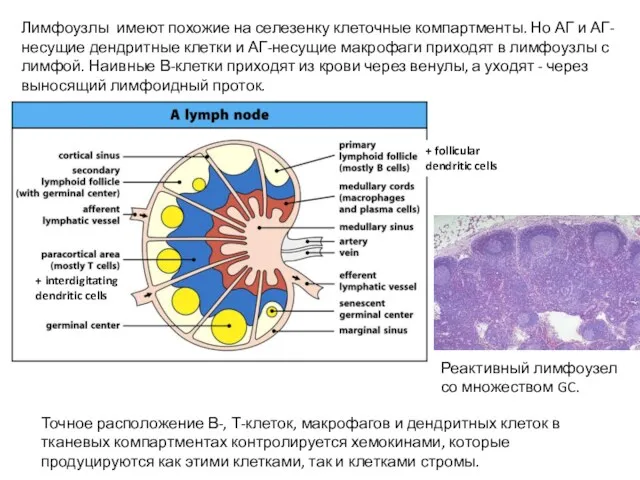
- 30. Лимфоузлы имеют похожие на селезенку клеточные компартменты. Но АГ и АГ-несущие дендритные клетки и АГ-несущие макрофаги
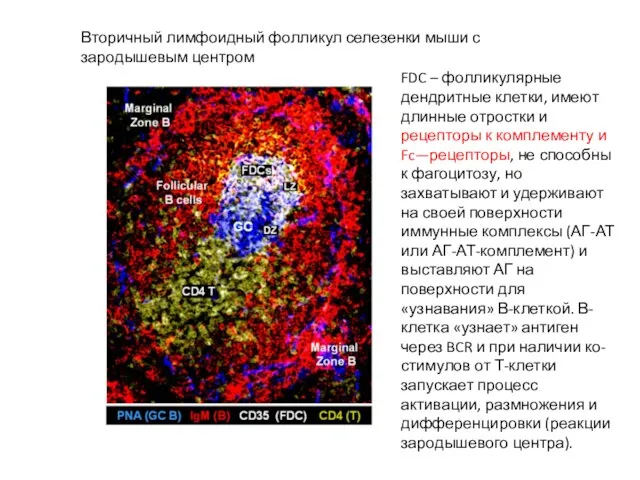
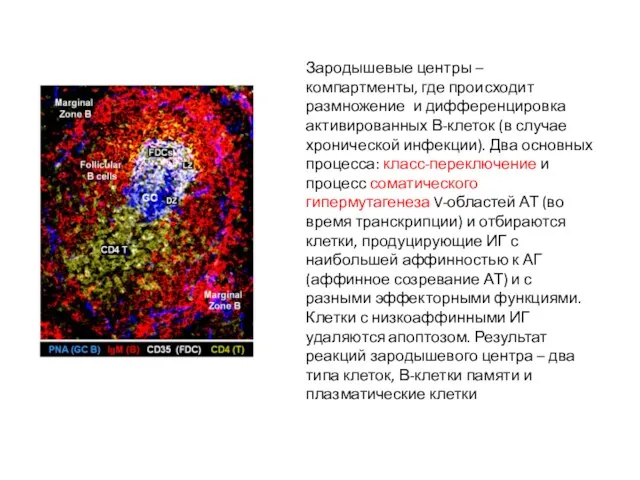
- 31. Вторичный лимфоидный фолликул селезенки мыши с зародышевым центром FDC – фолликулярные дендритные клетки, имеют длинные отростки
- 32. Зародышевые центры – компартменты, где происходит размножение и дифференцировка активированных В-клеток (в случае хронической инфекции). Два
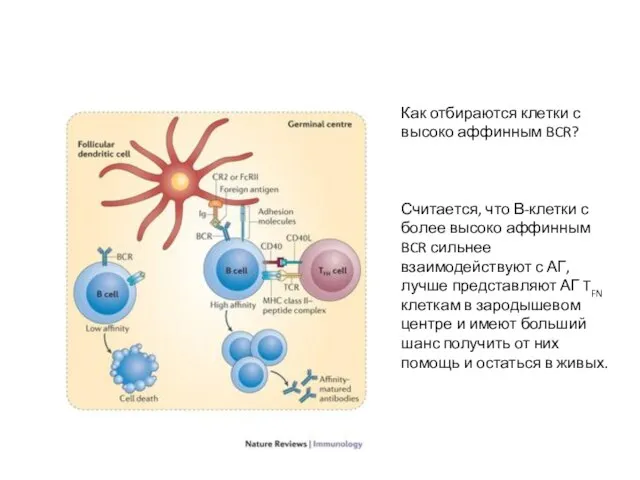
- 33. Как отбираются клетки с высоко аффинным BCR? Считается, что В-клетки с более высоко аффинным BCR сильнее
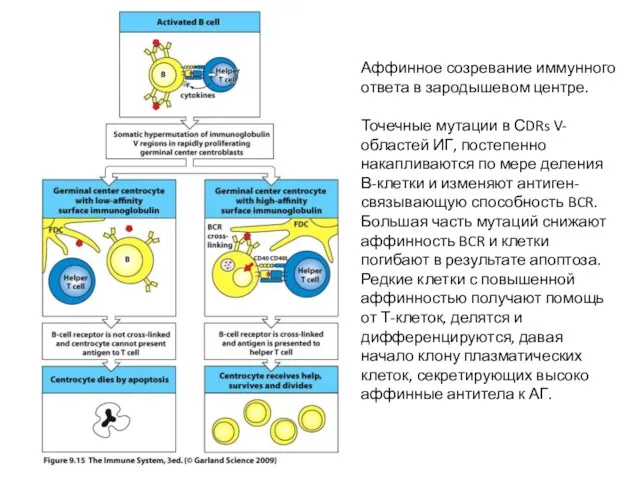
- 34. Аффинное созревание иммунного ответа в зародышевом центре. Точечные мутации в СDRs V-областей ИГ, постепенно накапливаются по
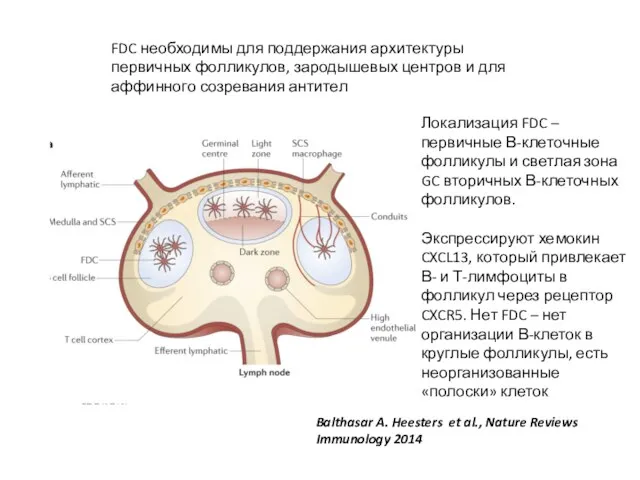
- 35. ФОЛЛИКУЛЯРНЫЕ ДЕНДРИТНЫЕ КЛЕТКИ (FDC) – уникальная популяция клеток, необходимая для развития зародышевого центра и продукции высоко
- 36. Локализация FDC – первичные В-клеточные фолликулы и светлая зона GC вторичных В-клеточных фолликулов. Экспрессируют хемокин CXCL13,
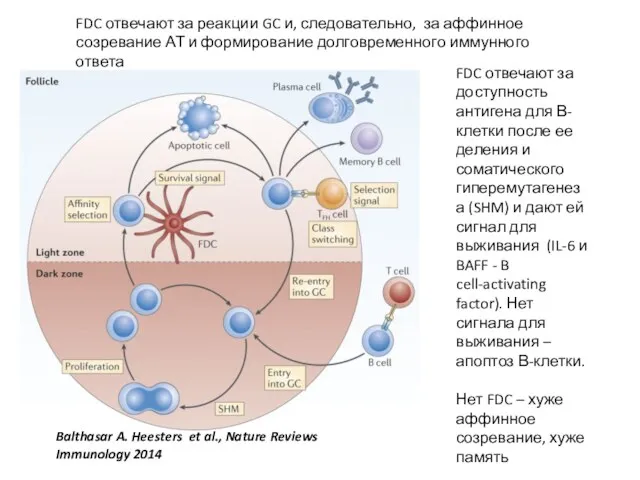
- 37. Balthasar A. Heesters et al., Nature Reviews Immunology 2014 FDC отвечают за доступность антигена для В-клетки
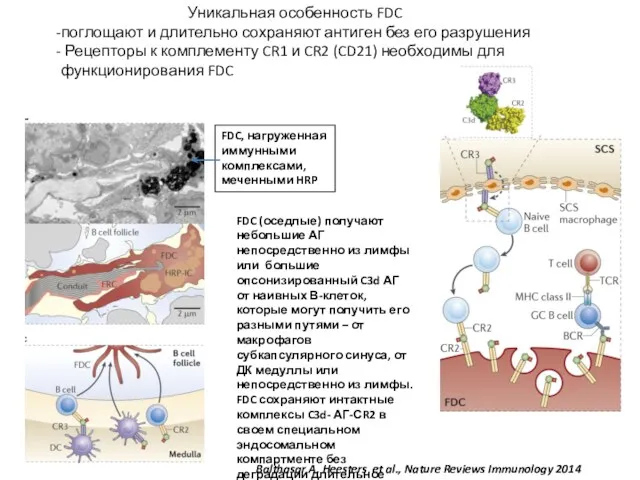
- 38. Balthasar A. Heesters et al., Nature Reviews Immunology 2014 Уникальная особенность FDC поглощают и длительно сохраняют
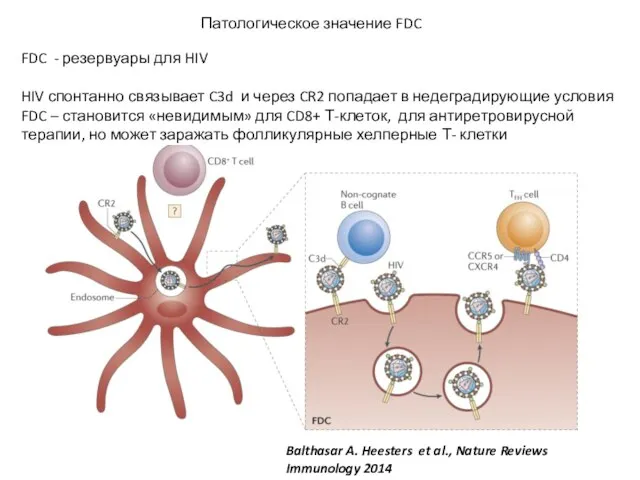
- 39. FDC - резервуары для HIV HIV спонтанно связывает C3d и через CR2 попадает в недеградирующие условия
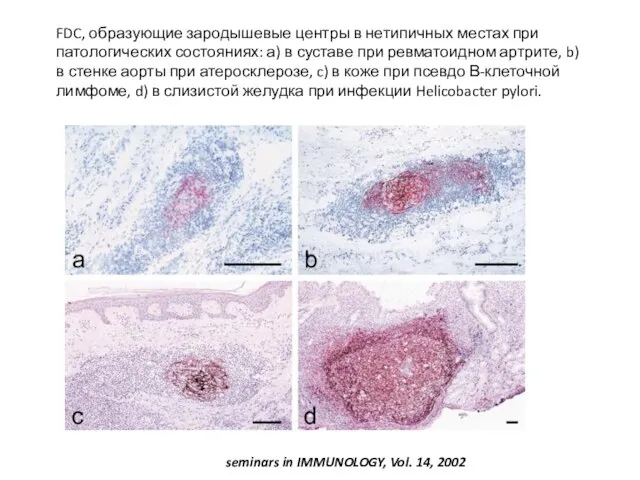
- 40. FDC, образующие зародышевые центры в нетипичных местах при патологических состояниях: а) в суставе при ревматоидном артрите,
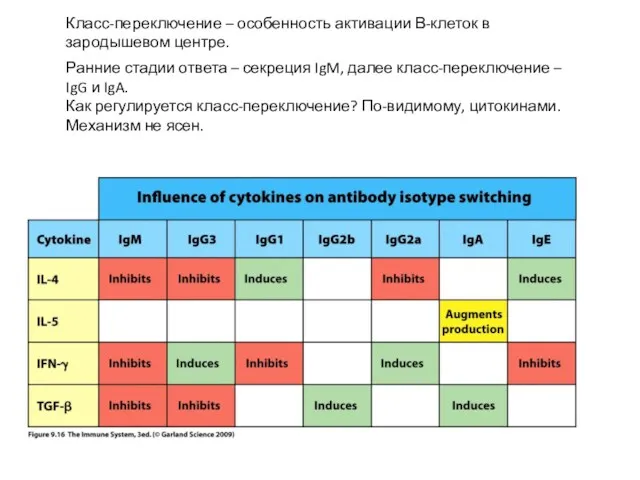
- 41. Ранние стадии ответа – секреция IgM, далее класс-переключение – IgG и IgA. Как регулируется класс-переключение? По-видимому,
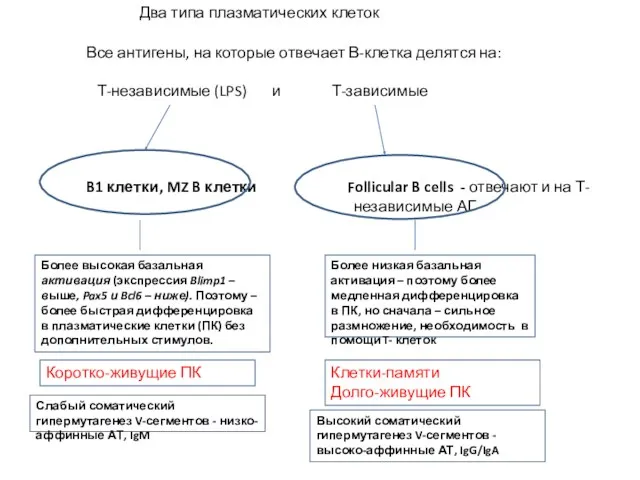
- 42. Все антигены, на которые отвечает В-клетка делятся на: Т-независимые (LPS) и Т-зависимые B1 клетки, MZ B
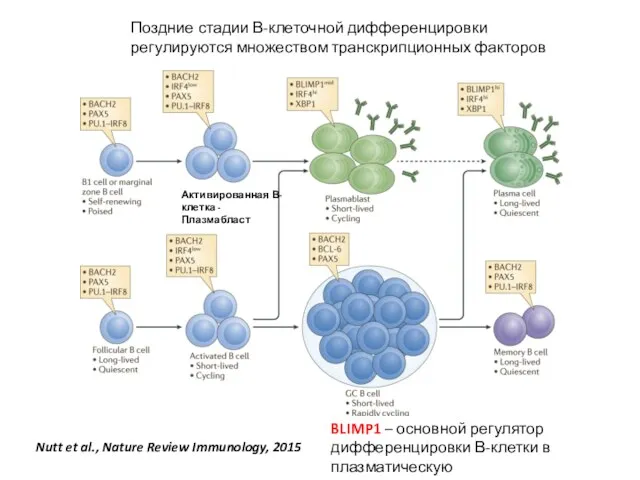
- 43. Поздние стадии В-клеточной дифференцировки регулируются множеством транскрипционных факторов Nutt et al., Nature Review Immunology, 2015 Активированная
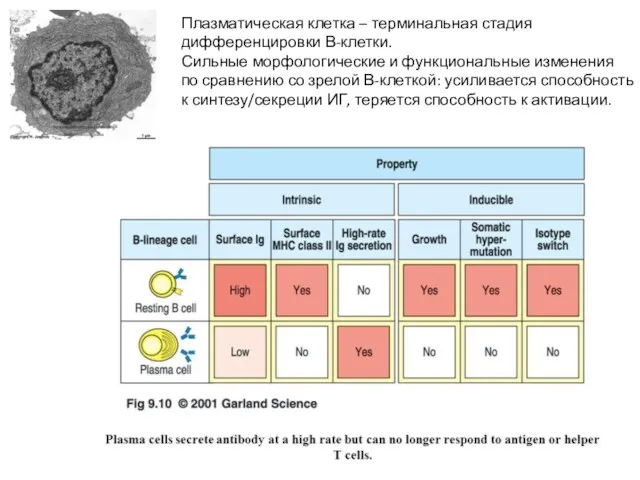
- 44. Плазматическая клетка – терминальная стадия дифференцировки В-клетки. Сильные морфологические и функциональные изменения по сравнению со зрелой
- 46. Скачать презентацию



 Гигиенаның қалыптасуы және даму тарихы
Гигиенаның қалыптасуы және даму тарихы Ишемическая болезнь сердца
Ишемическая болезнь сердца Осложнения острого хоолецистита. Механическая желтуха
Осложнения острого хоолецистита. Механическая желтуха Молекулярно-генетические механизмы онтогенеза. Нарушения онтогенеза и их место в патологии человека
Молекулярно-генетические механизмы онтогенеза. Нарушения онтогенеза и их место в патологии человека Питание дома. Питание в школьной столовой. Поведение в школьной столовой
Питание дома. Питание в школьной столовой. Поведение в школьной столовой Балалардағы В 12 тапшылықты анемия
Балалардағы В 12 тапшылықты анемия Патофизиология липидного обмена. Атеросклероз
Патофизиология липидного обмена. Атеросклероз Наборы инстрементов на операции
Наборы инстрементов на операции Загальна характеристика вірусних гепатитів. Вірусні гепатити з фекально-оральним механізмом зараження
Загальна характеристика вірусних гепатитів. Вірусні гепатити з фекально-оральним механізмом зараження Эпидемиология как наука. Предмет, задачи и методы
Эпидемиология как наука. Предмет, задачи и методы Асептика и антисептика. История вопроса. Виды антисептики
Асептика и антисептика. История вопроса. Виды антисептики Строение тазобедренного сустава
Строение тазобедренного сустава Недоношенные новорожденные
Недоношенные новорожденные Сюрпризы погоды и их влияние на здоровье человека
Сюрпризы погоды и их влияние на здоровье человека Энцефалиты
Энцефалиты Ранняя реабилитация пациентов, перенесших инсульт. Роль медицинской сестры
Ранняя реабилитация пациентов, перенесших инсульт. Роль медицинской сестры Геморрагический васкулит
Геморрагический васкулит ДТЗ (Диффузно-токсический зоб)
ДТЗ (Диффузно-токсический зоб) Гиподинамия, гипердинамия
Гиподинамия, гипердинамия Энтеральные вирусные гепатиты
Энтеральные вирусные гепатиты Современные методы обследования больных с опухолями головы и шеи
Современные методы обследования больных с опухолями головы и шеи Пародонт аурулары. Түсінік, жүйесі, этиологиясы, патогенезі. Терминдер
Пародонт аурулары. Түсінік, жүйесі, этиологиясы, патогенезі. Терминдер Coagularea intravasculară diseminată
Coagularea intravasculară diseminată Диагностика варикозной болезни и облитерирующего атеросклероза вен нижних конечностей
Диагностика варикозной болезни и облитерирующего атеросклероза вен нижних конечностей Волосатоклеточный лейкоз
Волосатоклеточный лейкоз ОРВИ у детей
ОРВИ у детей Искусственный интеллект (ИИ) в медицине (примеры использования)
Искусственный интеллект (ИИ) в медицине (примеры использования) Заболевания, передающиеся половым путём
Заболевания, передающиеся половым путём