Содержание
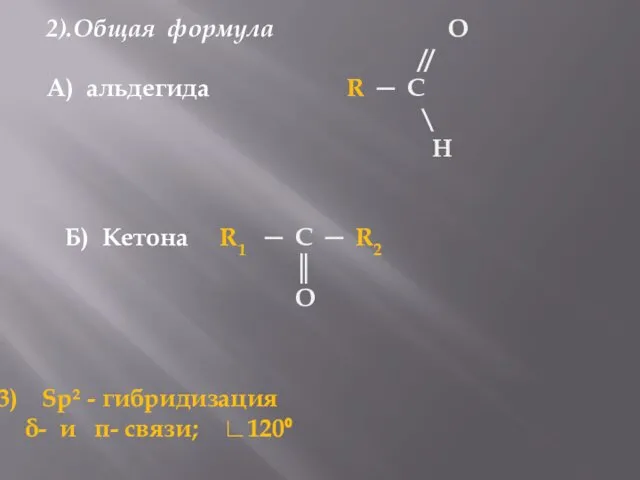
- 2. 2).Общая формула O // А) альдегида R ─ C \ H Б) Кетона R1 ─ C
- 3. Приложение № 2. Виды изомерии А) для предельных альдегидов: Изомерия УГ (углеродного скелета) Межклассовая изомерия (с
- 4. Упр. 2 стр. 159-160 Изомеры: С5Н10О - А) В) Д) Е) С6Н12О - Б) Г) Ж)
- 5. Приложение № 3. Номенклатура. Название альдегидов образуется из: Названия соответствующего углеводорода с прибавлением суффикса – аль-
- 6. Название кетонов образуется из названий: соответствующих углеводородов (алканов) + суффикс – он- + цифра атома углерода
- 7. Упр. 3 стр. 160 О 5 4 3 2 1 // А) СН3 – СН –
- 8. Приложение № 4 Физические свойства.
- 9. Приложение № 5. Химические свойства. Реакции восстановления - гидрирование: А) альдегидов O // Ni R –
- 10. Реакции окисления: O O Общая схема процесса: // {O} // R – C → R -
- 11. Кетоны не окисляются ни кислородом воздуха, ни аммиачным раствором оксида серебра. Окисление кетонов идет значительно труднее,
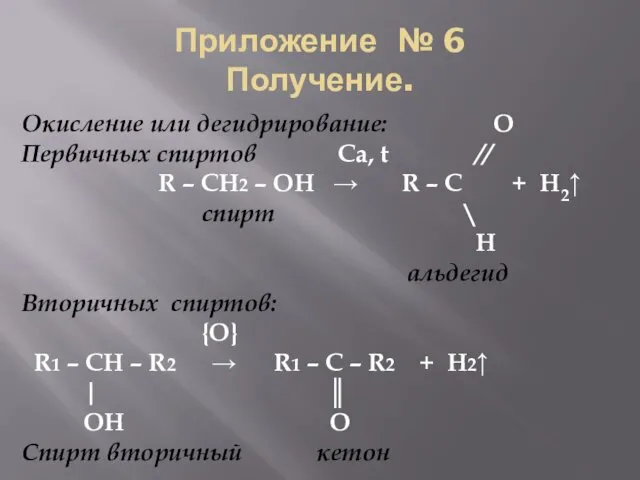
- 12. Приложение № 6 Получение. Окисление или дегидрирование: O Первичных спиртов Ca, t // R – CH2
- 13. Реакция Кучерова (получение ацетальдегида) O HgSO4, H2SO4, t // HC ≡ CH + H2O CH3 –
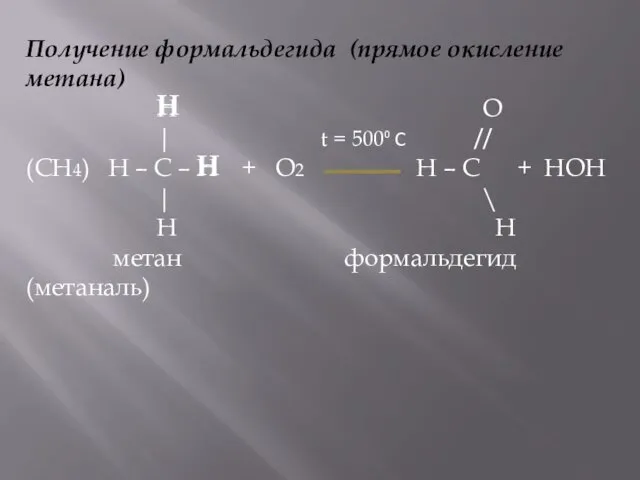
- 14. Получение формальдегида (прямое окисление метана) H O | t = 500⁰ C // (CH4) H –
- 15. Приложение № 7 Применение. формальдегид Получение фенолформальдегидных смол Кожевенное производство В с/х – для протравливания семян
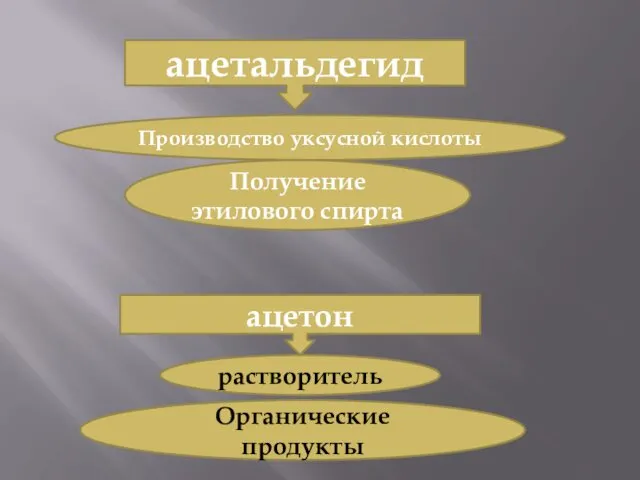
- 16. ацетальдегид Производство уксусной кислоты Получение этилового спирта ацетон растворитель Органические продукты
- 18. Скачать презентацию











 Холодная штамповка
Холодная штамповка Рыночная экономика как система
Рыночная экономика как система Дослідження технічних засобів системи контролю і діагностики тягових підстанцій
Дослідження технічних засобів системи контролю і діагностики тягових підстанцій Конструктивная характеристика одежды, обуви и кожгалантерейных изделий
Конструктивная характеристика одежды, обуви и кожгалантерейных изделий Обзор новых возможностей. Знакомство с Рowerpoint 2010
Обзор новых возможностей. Знакомство с Рowerpoint 2010 класс. Сфера духовной культуры
класс. Сфера духовной культуры Методы познания, принципы познания. Портфолио как способ самопознания личности
Методы познания, принципы познания. Портфолио как способ самопознания личности Охрана окружающей среды
Охрана окружающей среды Қазіргі әлемдегі нанотехнология
Қазіргі әлемдегі нанотехнология Автоматты қайта қосылу
Автоматты қайта қосылу Презентация Художественное выпиливание
Презентация Художественное выпиливание Средства угнетающие ЦНС. Средства для наркоза
Средства угнетающие ЦНС. Средства для наркоза 20231112_moralnyy_vybor_i_moralnaya_otsenka
20231112_moralnyy_vybor_i_moralnaya_otsenka Произведение двух последовательных отрицательных чисел
Произведение двух последовательных отрицательных чисел Моё хобби
Моё хобби Родительское собрание в 3 классе по теме: Как воспитывать у ребёнка любовь к чтению
Родительское собрание в 3 классе по теме: Как воспитывать у ребёнка любовь к чтению Подвиг восстановления Ленинграда
Подвиг восстановления Ленинграда Изделия из газетных трубочек
Изделия из газетных трубочек Организация учебной дискуссии: методика и управление
Организация учебной дискуссии: методика и управление Приборы определения скорости корабля и пройденного им расстояния. (Тема 6)
Приборы определения скорости корабля и пройденного им расстояния. (Тема 6) Игра- лабиринт по теме Первоначальные химические понятия, 8 класс.
Игра- лабиринт по теме Первоначальные химические понятия, 8 класс. Михаил Лямин
Михаил Лямин Расстройства восприятия и злоупотребление психоактивными веществами
Расстройства восприятия и злоупотребление психоактивными веществами Система кровообращения человека
Система кровообращения человека Проект на проведение сейсморазведочных работ МОГТ-3D с целью уточнения структурно-тектонического строения Песчанской площади
Проект на проведение сейсморазведочных работ МОГТ-3D с целью уточнения структурно-тектонического строения Песчанской площади Инновационная образовательная программа Теремок для детей от 2 месяцев до 3 лет
Инновационная образовательная программа Теремок для детей от 2 месяцев до 3 лет Словo Жыцця. Красавiк 2016. “Тое, што вы зрабілі аднаму з гэтых братоў Маіх меншых, вы Мне зрабілі” (Мц 25,40)
Словo Жыцця. Красавiк 2016. “Тое, што вы зрабілі аднаму з гэтых братоў Маіх меншых, вы Мне зрабілі” (Мц 25,40) Правила движения в походе. Часть 2
Правила движения в походе. Часть 2