Слайд 2

Белки – высокомолекулярные природные соединения (биополимеры), состоящие из остатков аминокислот, которые
соединены пептидной связью.
Слайд 3

В состав белков входят:
Углерод
Водород
Кислород
Азот
Сера
Фосфор
Железо
Другие элементы
Гемоглобин - С3032H4816O872N780S8Fe4
Mr белка яйца
= 36 000,
Mr белка мышц = 1 500 000.
Слайд 4
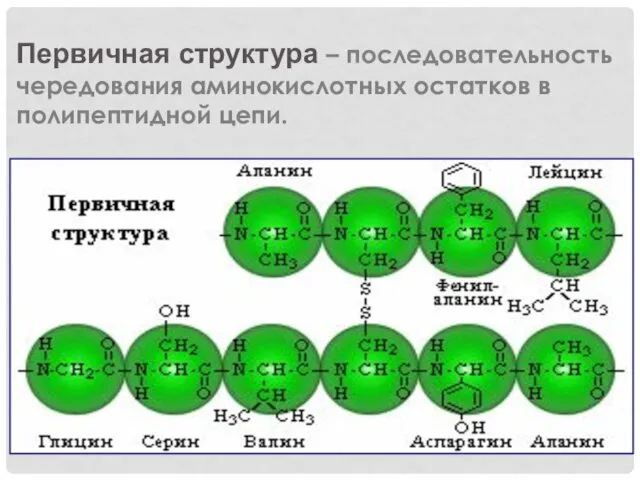
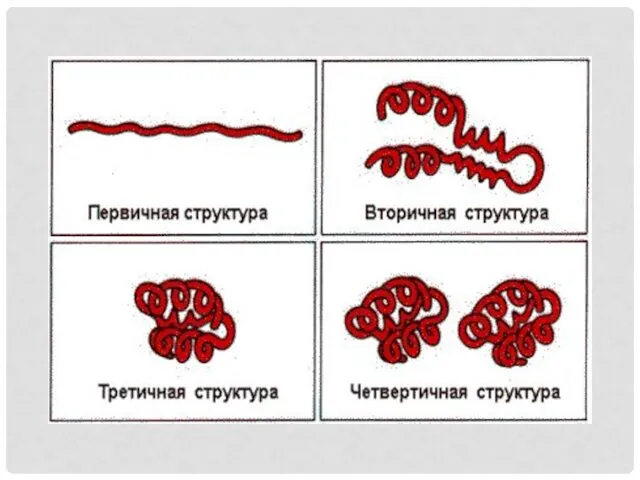
Первичная структура – последовательность чередования аминокислотных остатков в полипептидной цепи.
Слайд 5
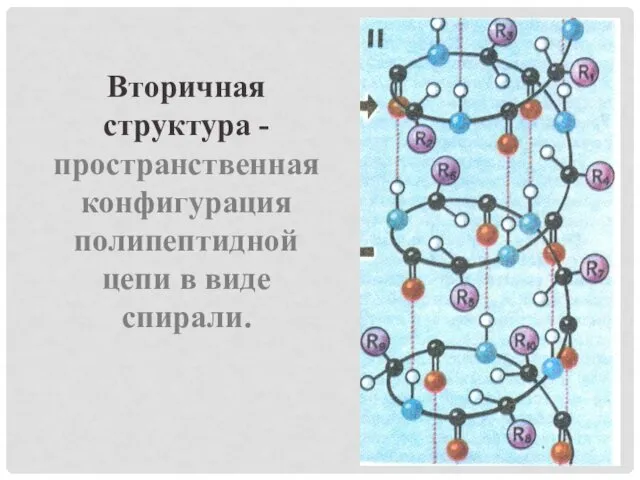
Вторичная структура -пространственная конфигурация полипептидной цепи в виде спирали.
Слайд 6
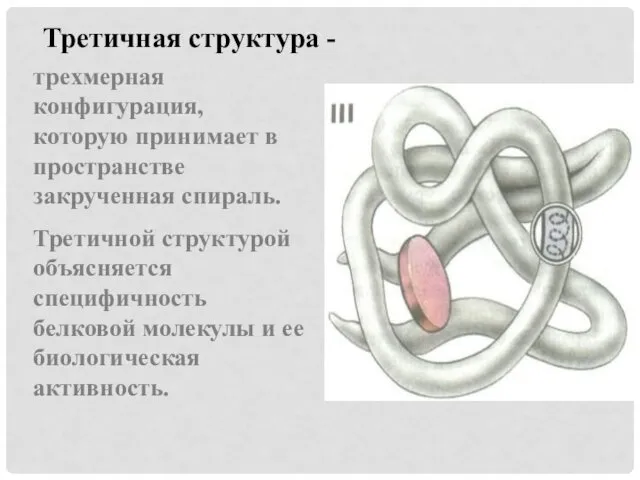
Третичная структура -
трехмерная конфигурация, которую принимает в пространстве закрученная спираль.
Третичной структурой
объясняется специфичность белковой молекулы и ее биологическая активность.
Слайд 7
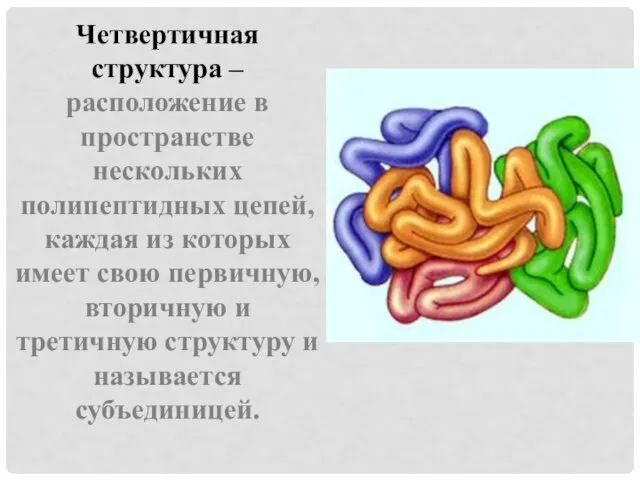
Четвертичная структура – расположение в пространстве нескольких полипептидных цепей, каждая из
которых имеет свою первичную, вторичную и третичную структуру и называется субъединицей.
Слайд 8
Слайд 9

ФУНКЦИИ БЕЛКОВ
1. Строительная – белки участвуют в образовании оболочки клетки,
органоидов и мембран клетки. Из белков построены кровеносные сосуды, сухожилия, волосы
2. Каталитическая – все клеточные катализаторы –
белки (активные центры фермента).
3.Двигательная – сократительные белки вызывают
всякое движение.
4. Транспортная – белок крови гемоглобин присоединяет кислород и разносит его по всем тканям.
5. Защитная – выработка белковых тел и антител для обезвреживания чужеродных веществ.
6. Энергетическая – 1 г белка эквивалентен 17,6 кДж.
7. Рецепторная – реакция на внешний раздражитель.
Слайд 10
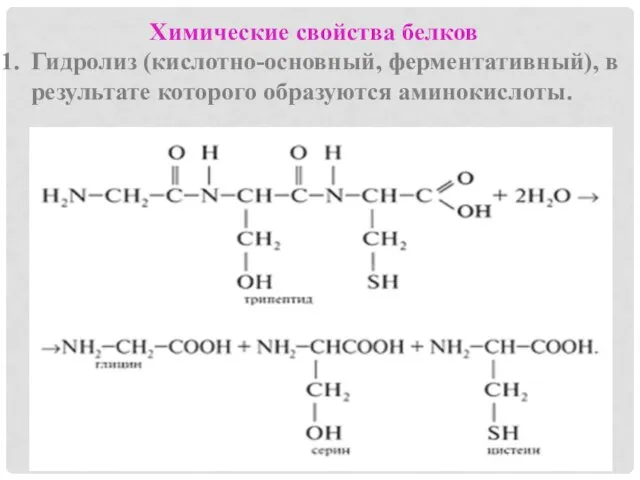
Химические свойства белков
Гидролиз (кислотно-основный, ферментативный), в результате которого образуются аминокислоты.
Слайд 11

ДЕНАТУРИРОВАННЫЙ БЕЛОК ТЕРЯЕТ СВОИ БИОЛОГИЧЕСКИЕ СВОЙСТВА.
Денатурация – нарушение природной структуры белка
под действием нагревания и химических реагентов.
а) высокая или низкая температура
б) механическое воздействие;
в) облучение;
г) яды;
д) действие спирта;
б) действие солей тяжелых металлов (Pb, Hg и др.)
Слайд 12

3. Цветные качественные реакции белков
а) Биуретовая реакция– взаимодействие слабощелочных растворов
белков с раствором сульфата меди (II), в результате которой появляется фиолетово-синяя окраска.
б) Ксантопротеиновая реакция– взаимодействие с концентрированной азотной кислотой, которое сопровождается появлением желтой окраски.
Слайд 13
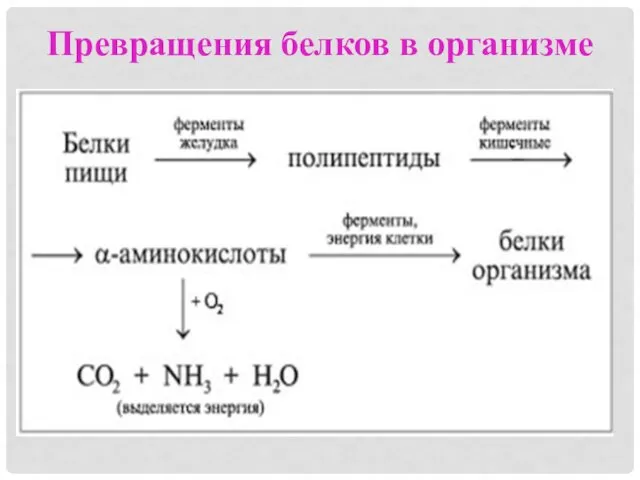
Превращения белков в организме
Слайд 14

Значение белков
Отдельные белки находят применение в народном хозяйстве, например белки шерсти,
шелка, кожи и рогов животных.
Выяснение структуры белков, их многообразных функций в организме позволяет понять механизм наследственности, что в свою очередь, имеет большое значение для выведения высокопродуктивных пород животных и сортов растений.
Изучение белков важно и для выяснения природы заболеваний, наблюдаемых у человека и животных













 Н.И.Роговцева. Технология. 3 класс. Ателье мод.Одежда. Пряжа и ткани. Вязание.
Н.И.Роговцева. Технология. 3 класс. Ателье мод.Одежда. Пряжа и ткани. Вязание. Введение в раздел дисциплины. Нормативные требования к аэродромным сооружениям
Введение в раздел дисциплины. Нормативные требования к аэродромным сооружениям Передача товаров на ответственное хранение с целью продажи
Передача товаров на ответственное хранение с целью продажи Презентация к мероприятию День семьи
Презентация к мероприятию День семьи Наркозға арналған дәрілер
Наркозға арналған дәрілер Журова Музыкотерапия
Журова Музыкотерапия Поговорим о толерантности
Поговорим о толерантности Зиянкестерден интеграцияланған өсімдіктерді қорғау. Биологиялық қорғаудағы агротехникалық әдістер. (Лекция 14)
Зиянкестерден интеграцияланған өсімдіктерді қорғау. Биологиялық қорғаудағы агротехникалық әдістер. (Лекция 14) Презентация ОФПО 30мая22
Презентация ОФПО 30мая22 Телевизор - друг, телевизор - враг? Диск
Телевизор - друг, телевизор - враг? Диск Адаптация детей к ДОУ. презентация
Адаптация детей к ДОУ. презентация 20230825_yunosheskiy_vozrast
20230825_yunosheskiy_vozrast В весеннем лесу (объёмная аппликация)
В весеннем лесу (объёмная аппликация) Электротехника и электроника
Электротехника и электроника Медикэр және Медикейд бағдарламалары
Медикэр және Медикейд бағдарламалары Сложение чисел с помощью координатной прямой. 6 класс
Сложение чисел с помощью координатной прямой. 6 класс Купеческий город Сарапул
Купеческий город Сарапул интерактивный тест по географии
интерактивный тест по географии Электрические аппараты и приборы, электрические цепи тепловоза, электрические цепи электровоза
Электрические аппараты и приборы, электрические цепи тепловоза, электрические цепи электровоза Проведение чайной церемонии в Японии
Проведение чайной церемонии в Японии Проект возникновения чисел
Проект возникновения чисел География транспорта мира
География транспорта мира презентация Великой Победе посвящается
презентация Великой Победе посвящается Личностно-ориентированный подход при подготовке и проведении классных часов
Личностно-ориентированный подход при подготовке и проведении классных часов Игра по творчеству Э. Грига. Сюита Пер Гюнт
Игра по творчеству Э. Грига. Сюита Пер Гюнт Проектирование электрической части главной понизительной подстанции нефтеперерабатывающего завода 220/10 кВ
Проектирование электрической части главной понизительной подстанции нефтеперерабатывающего завода 220/10 кВ Силикатная промышленность. Керамика
Силикатная промышленность. Керамика Презентация проекта
Презентация проекта