Содержание
- 2. Бұл типтегі қосылыстардың жалпы формуласы: Сілтілік металдардың иондары (Na, K) немесе органикалық негіздер (моно-, ди- және
- 3. Екіншілік алкил-сульфаттарды олефинді көмірсутектерге күкірт қышқылымен әсер ету арқылы келесі реакция арқылы алады: RCH=CH2+ H2SO4 R(CH3)OSO3
- 4. Қос байланыстың изомеризациясы күкірт қышқылының концентрациясына, температураға және реакцияның жүру ұзақтығына байланысты. Сульфаттаушы агент күші шешуші
- 5. Сульфатирлеудің оптималды шарттары. Бастапқы шикізат – олефиндер, қатты парафиндердің крекингі кезінде алынған, парафинді көмірсутектердің дәл сондай
- 6. Қолданылатын күкірт қышқылының концентрациясы мен мөлшерін сульфоэфирлердің сапа көрсеткіші мен шығымы көрсетеді. Олардың көбеюімен сульфаттаудың толықтығы
- 7. Екіншілік алкилсульфаттар және олардың тұздары
- 8. Екіншілік алкилсульфаттар және олардың тұздарын алу 2 реакцияға негізделеді: а. жоғарғы алкендерге күкірт қышқылын қосу: б.
- 9. Алкендерге күкірт қышқылының қосылуы Марковников ережесі бойынша және электрофильді қосылу механизмі бойынша оңай жүреді. Реакция механизмі
- 10. Екіншілік алкилсульфаттарды алу жанама реакциялармен: диалкилсульфаттар түзілуі, алкендер және т.б. олигомерленуі жүреді. Диалкилсульфаттар карбкатионға қатысты нуклеофильді
- 11. Алкиларенсульфонаттар Алкиларенсульфонаттар алкил ароматты қосылыстардың сульфоқышқылдарының тұздары болып саналады. СМС құрамында натрий алкилбензолсульфонаты – сульфанолдар болады.
- 12. Алкилхлоридтер негізіндегі алкилбензолсульфонаттар Процесс келесі сатылардан тұрады: деароматталған керосин немесе н-алкандарды хлорлау, алкилбензолдарды алу, алкилбензолдарды сульфирлеу,
- 13. Хлор радикалдары қасиеті жағынан электронға ұқсас, сол себепті алкандардан бос алкил радикалын түзе отырып сутегі атомын
- 14. Барлық бос радикалдардың жойылуынан кейін аяқталатын тізбекті процесс осылай жүреді. Әдетте н-алкандармен жүретін реакцияларды изомерлі хлоралкандар
- 15. Метил тобындағы (СН3) С-Н байланыстарының энергиясы 390 кДж/моль құрағандықтан, метилен тобындағы (СН2) байланыс энергиясы 368 кДж/моль,
- 16. Бензолды алкилхлоридтермен алкилдеу Сульфанолды алу процесінің келесі сатысы бензолды алкилхлорид-термен алкилдеу болып табылады. Процесс Фридель-Крафтс реакциясы
- 17. Бензолды алкилхлорид-термен алкилдеу реакциясы электрофильді орынбасу механмзміне бағынады. Процесс катализаторлары ретінде протонды қышқылдар немесе Льюис қышқылдары
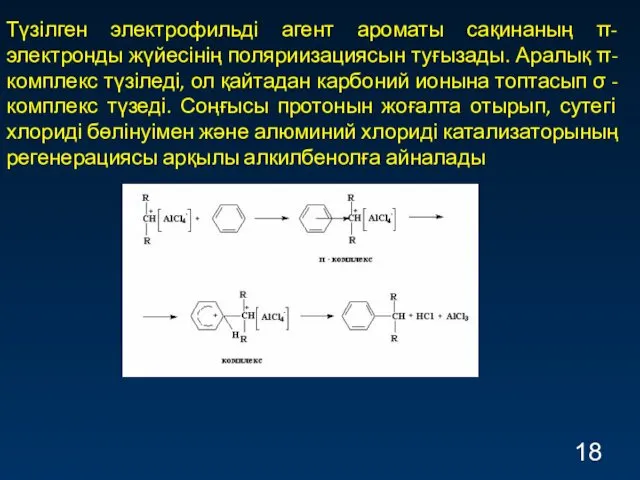
- 18. Түзілген электрофильді агент ароматы сақинаның π-электронды жүйесінің поляриизациясын туғызады. Аралық π- комплекс түзіледі, ол қайтадан карбоний
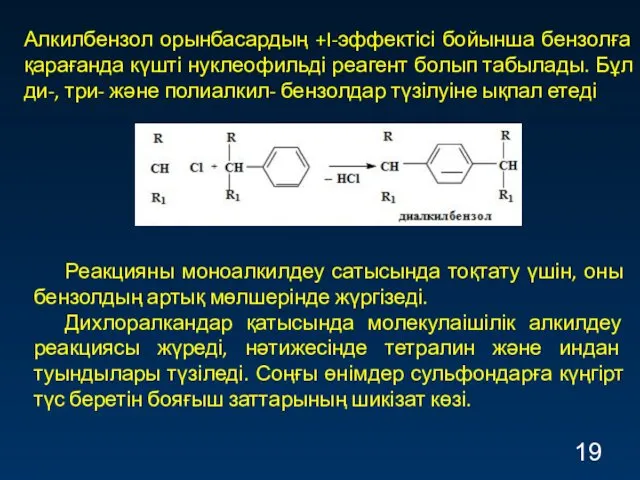
- 19. Алкилбензол орынбасардың +I-эффектісі бойынша бензолға қарағанда күшті нуклеофильді реагент болып табылады. Бұл ди-, три- және полиалкил-
- 20. Алкилбензолдарды сульфирлеу Алкилбензолдарды сульфирлеудің келесі сатылары: сульфоқышқыл-дарды бейтараптау және тауарлық алкилбензолсульфонат алу. Сульфирлеуші агент ретінде күкірт
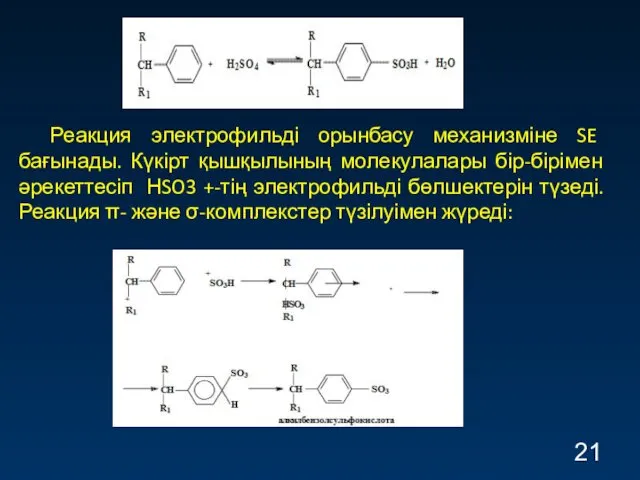
- 21. Реакция электрофильді орынбасу механизміне SE бағынады. Күкірт қышқылының молекулалары бір-бірімен әрекеттесіп НSO3 +-тің электрофильді бөлшектерін түзеді.
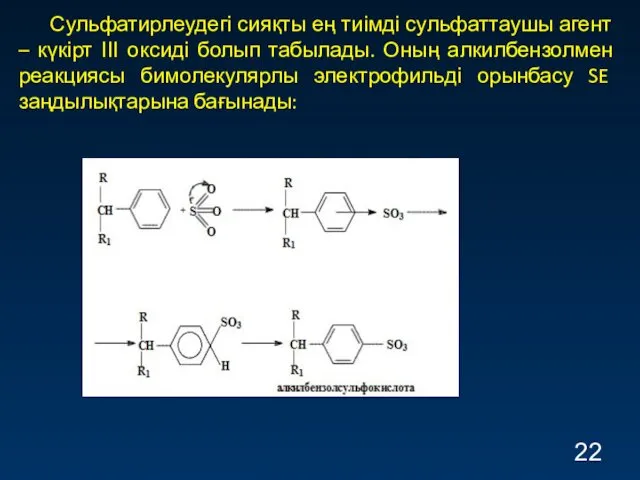
- 22. Сульфатирлеудегі сияқты ең тиімді сульфаттаушы агент – күкірт ІІІ оксиді болып табылады. Оның алкилбензолмен реакциясы бимолекулярлы
- 23. Алкилсульфонаттар Алкилсульфонаттарды әдетте біріншілік және екіншілік туындылардың қоспасы түрінде: RSO3Na және R`R``CHSO3Na. Бұл өнімді екінші дүниежүзілік
- 24. Бұл синтез төмен молеулалы алкилдермен тез жүреді. С8-С16 ұзын тізбекті алкилсульфонатын алу үшін ең жақсы нәтижені
- 25. Алкилсульфонаттарды практика жүзінде алу 1936 жылғы Рид пен Хорнның ашқан парафинді көмірсутектердің сульфохлорлау реакциясынан кейін мүмкін
- 26. Сульфототығудың қолданылатын инициаторларына байланысты сулы-ашық және сірке ангидридті әдістері бар. Реакция бос радикалды механизммен бірнеше сатыда
- 27. Алкандардың сульфототығуы Алкандар оттегі қатысында УК сәулелену кезінде күкірт ангидридімен әрекеттеседі. Шикізат ретінде мұқият тазаланған көмірсутектерді
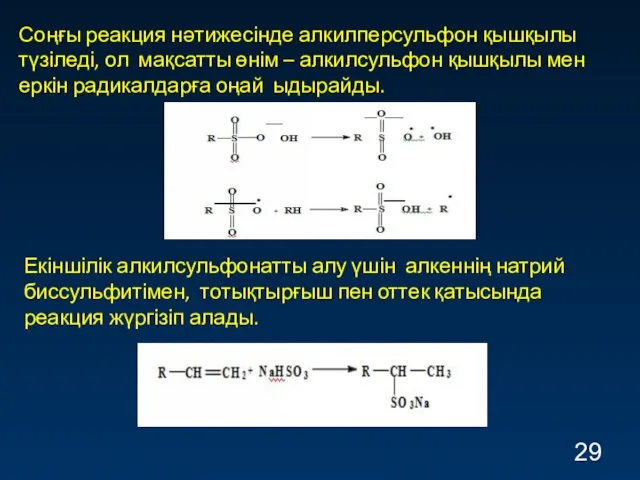
- 29. Соңғы реакция нәтижесінде алкилперсульфон қышқылы түзіледі, ол мақсатты өнім – алкилсульфон қышқылы мен еркін радикалдарға оңай
- 31. Скачать презентацию























 Советы родителям будущих первоклассников.
Советы родителям будущих первоклассников. Танкисты – добровольцы из Тувинской Народной Республики
Танкисты – добровольцы из Тувинской Народной Республики Презентация Пальчиковые игрушки
Презентация Пальчиковые игрушки Где вода-там жизнь
Где вода-там жизнь Основы программирования на языке Python
Основы программирования на языке Python Пристрій керування каналом (Заняття № 7.9)
Пристрій керування каналом (Заняття № 7.9) КузнецовВВ_Презентация
КузнецовВВ_Презентация Игрушки из прищепок. Технология. 2 урок
Игрушки из прищепок. Технология. 2 урок Использование метода проекта в образовательном процессе МБДОУ
Использование метода проекта в образовательном процессе МБДОУ Расписание учебных занятий
Расписание учебных занятий Практика применения законодательства о контрактной системе. Подходы антимонопольного органа и арбитражных судов
Практика применения законодательства о контрактной системе. Подходы антимонопольного органа и арбитражных судов Скоростные поезда
Скоростные поезда Компетентностно-ориентированные задачи по химии для 8 класса
Компетентностно-ориентированные задачи по химии для 8 класса Беларусь в составе Российской империи в конце XVIII - середине XIX вв. (Занятие 7)
Беларусь в составе Российской империи в конце XVIII - середине XIX вв. (Занятие 7) Разработка мероприятий по снижению безработицы в Ставропольском крае
Разработка мероприятий по снижению безработицы в Ставропольском крае Ярмарки в России
Ярмарки в России Презентация к уроку географии на тему Изображение высот и глубин на картах.
Презентация к уроку географии на тему Изображение высот и глубин на картах. Личное и групповое снаряжение
Личное и групповое снаряжение Производство армированных изделий методом намотки
Производство армированных изделий методом намотки Фенилхромановые соединения. Флавоноиды
Фенилхромановые соединения. Флавоноиды Должностные положения бухгалтерского, финансового и экономического отделов
Должностные положения бухгалтерского, финансового и экономического отделов Творческая мастерская. Пасхальный дар
Творческая мастерская. Пасхальный дар Занимательная химия
Занимательная химия Патріотизм
Патріотизм Ниткопись - инновационный игровой метод работы с детьми дошкольного возраста
Ниткопись - инновационный игровой метод работы с детьми дошкольного возраста Страны Евразии. Обобщение. Задания
Страны Евразии. Обобщение. Задания Лабиринты 5-6 классы
Лабиринты 5-6 классы Лирика Пушкина
Лирика Пушкина