Содержание
- 2. «Фосфор…- элемент жизни и мысли.» академик А.Е. Ферсман. P
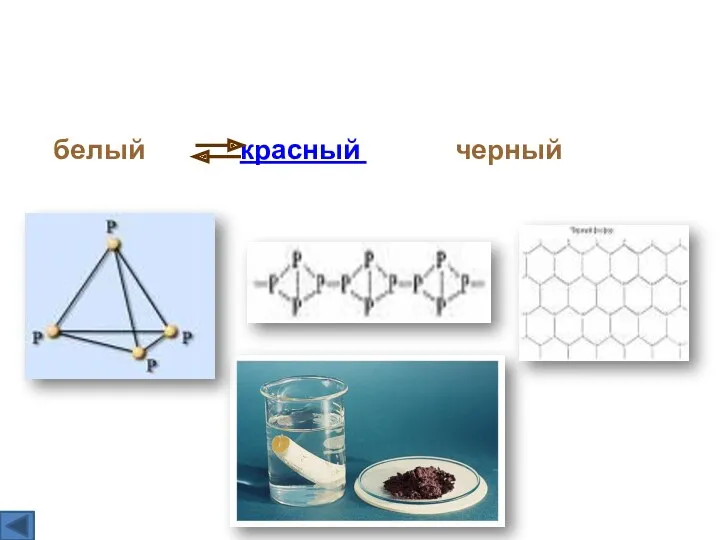
- 3. белый красный черный Аллотропные модификации фосфора
- 4. Состоит из молекул P4. Белое мягкое кристаллическое вещество. Чесночный запах. t плавления 44 oC, самовоспламеняющийся порошок.
- 5. Черный фосфор: Похож на графит. Проводит электрический ток. t плавления 597 оС. Атомная кристаллическая решетка. Нерастворим
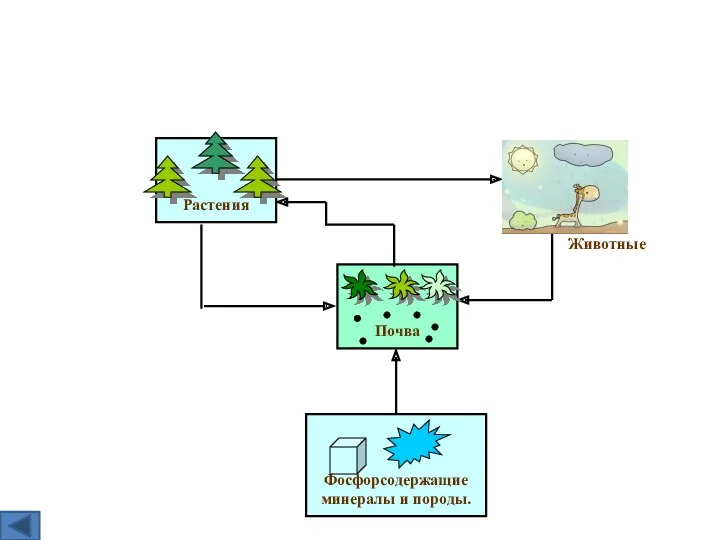
- 6. Фосфорсодержащие минералы и породы. Почва Растения Животные Круговорот фосфора в природе
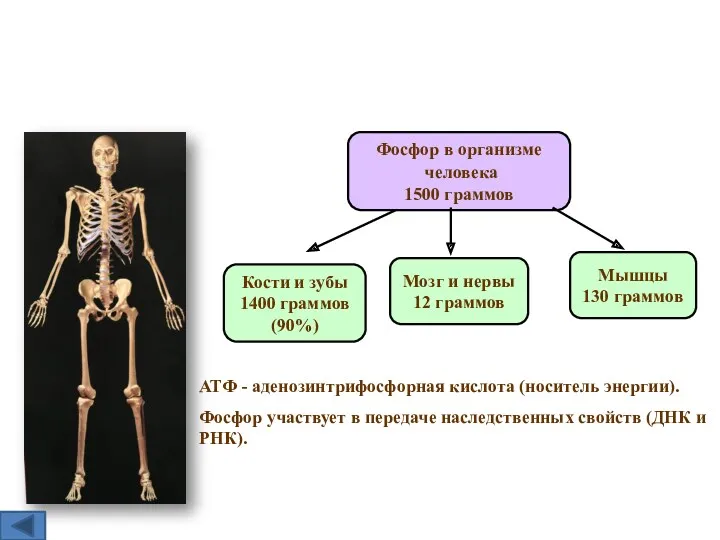
- 7. Фосфор в организме человека 1500 граммов Кости и зубы 1400 граммов (90%) Мышцы 130 граммов Мозг
- 8. Химические свойства фосфора Р0 Р-3 Р+5 окислитель восстановитель I. Фосфор – окислитель: При реакции с активными
- 10. Скачать презентацию




 Классный час(1 класс) В мире животных
Классный час(1 класс) В мире животных ЭКО-селение Родное
ЭКО-селение Родное Основные причины и виды деформаций зданий
Основные причины и виды деформаций зданий Советы логопеда по развитию речи неговорящих детей
Советы логопеда по развитию речи неговорящих детей Проектирование автоматической телефонной станции на железнодорожном транспорте
Проектирование автоматической телефонной станции на железнодорожном транспорте Гордость театральной сцены Башкортостана
Гордость театральной сцены Башкортостана Общевоинские уставы Вооруженных Сил РФ – закон воинской жизни
Общевоинские уставы Вооруженных Сил РФ – закон воинской жизни Юридическая ответственность и ее задачи. Лекция №7
Юридическая ответственность и ее задачи. Лекция №7 Подготовка к походу. Личное снаряжение
Подготовка к походу. Личное снаряжение Витоки української культури
Витоки української культури День Знаний для первоклассников.
День Знаний для первоклассников. Животный Мир Тундры
Животный Мир Тундры Урок 32. Поняття мови програмування
Урок 32. Поняття мови програмування Универсальный самоходный снегоуборочный робот
Универсальный самоходный снегоуборочный робот Речевая готовность детей к школе.
Речевая готовность детей к школе. Проектирование корпуса Лукояновского молочного завода,
Проектирование корпуса Лукояновского молочного завода, Здоровый образ жизни
Здоровый образ жизни Слитное и раздельное написание приставок в наречиях
Слитное и раздельное написание приставок в наречиях Основы объективно-ориентированного программирования в среде Lazarus
Основы объективно-ориентированного программирования в среде Lazarus Гипертоническая болезнь (ГБ)
Гипертоническая болезнь (ГБ) Психика және сана
Психика және сана Искусственный интеллект. Эволюционные алгоритмы
Искусственный интеллект. Эволюционные алгоритмы Дупликация. Самая простая схема выхода на бонус > 20 000 рублей
Дупликация. Самая простая схема выхода на бонус > 20 000 рублей преемственность детского сада и школы
преемственность детского сада и школы Понятие и классификация теорий менеджмента
Понятие и классификация теорий менеджмента Статистика туризма. (Лекции 3-4)
Статистика туризма. (Лекции 3-4) Как строят дома (презентация)
Как строят дома (презентация) Требования предъявляемые к оборудованию подстанций работающему в составе Цифровых ПС
Требования предъявляемые к оборудованию подстанций работающему в составе Цифровых ПС