Содержание
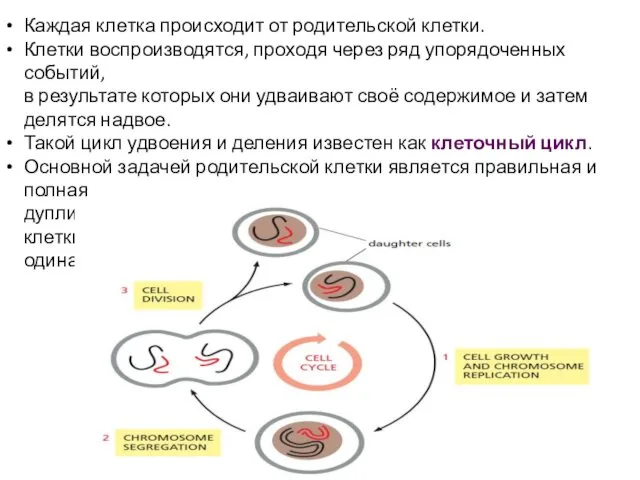
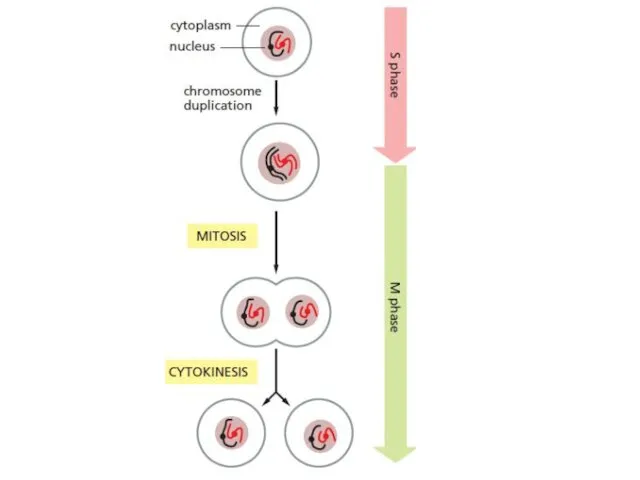
- 2. Каждая клетка происходит от родительской клетки. Клетки воспроизводятся, проходя через ряд упорядоченных событий, в результате которых
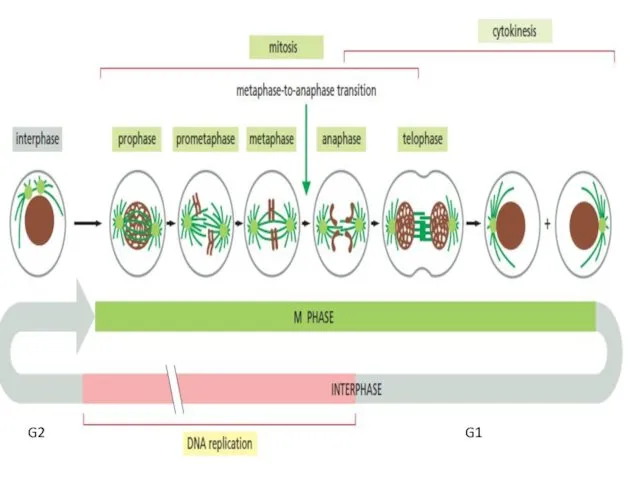
- 4. G1 G2
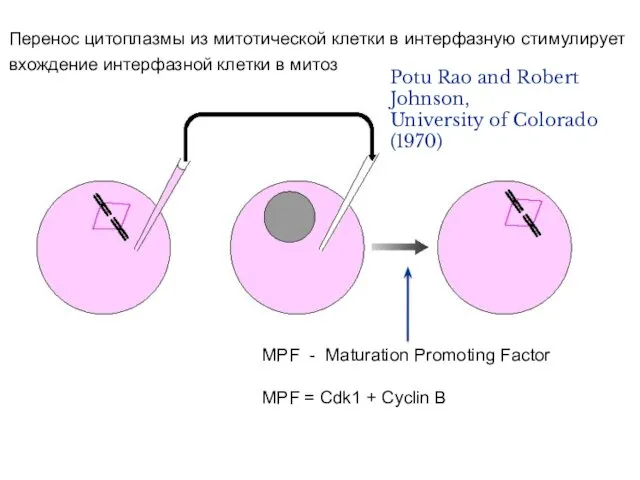
- 5. Перенос цитоплазмы из митотической клетки в интерфазную стимулирует вхождение интерфазной клетки в митоз MPF - Maturation
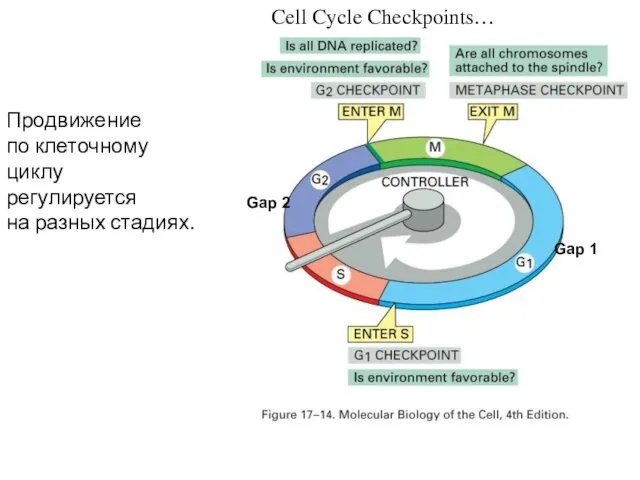
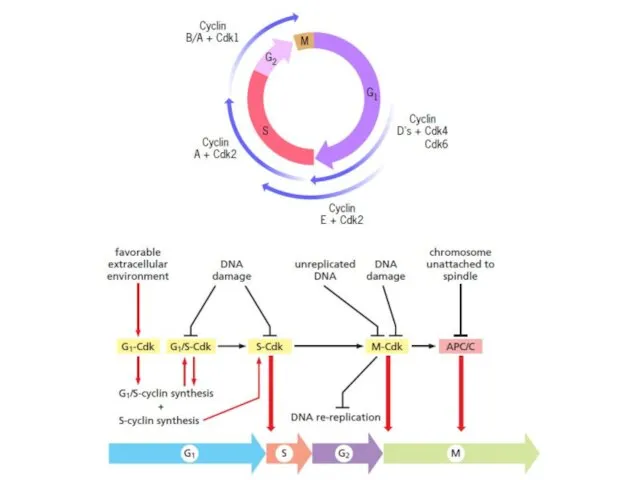
- 6. Cell Cycle Checkpoints… Gap 1 Gap 2 Продвижение по клеточному циклу регулируется на разных стадиях.
- 7. Cdk - cyclin-dependent kinases Saccharomyces cerevisiae (budding yeast) Schizosaccharomyces pombe (fission yeast) Leland Hartwell (University of
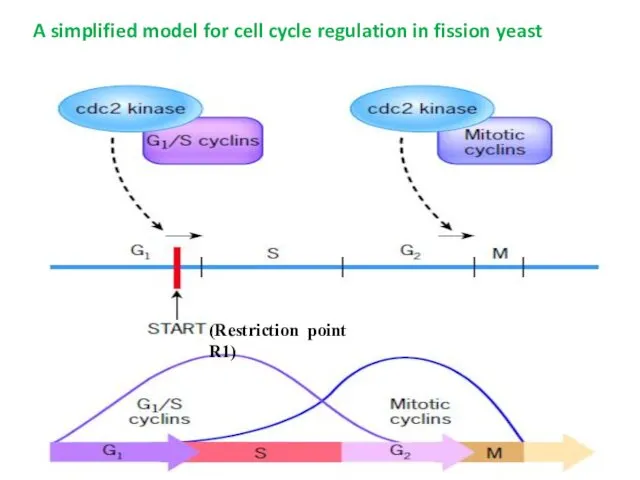
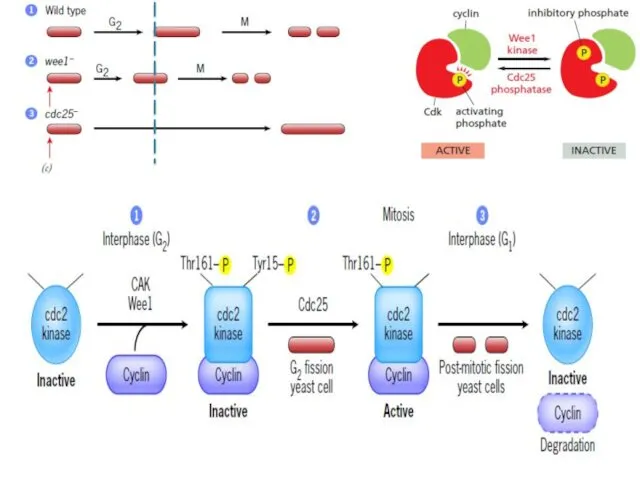
- 8. (Restriction point R1) A simplified model for cell cycle regulation in fission yeast
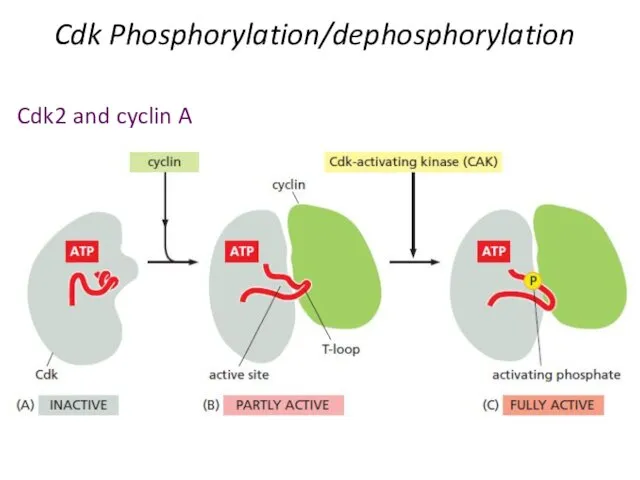
- 10. Cdk Phosphorylation/dephosphorylation Cdk2 and cyclin A
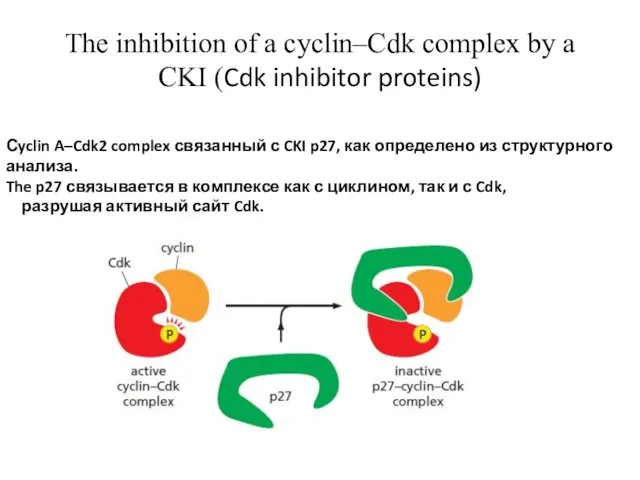
- 12. The inhibition of a cyclin–Cdk complex by a CKI (Cdk inhibitor proteins) Сyclin A–Cdk2 complex связанный
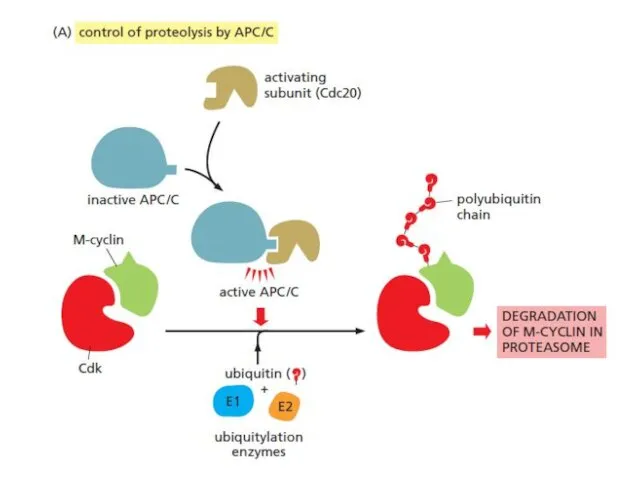
- 13. metaphase-to-anaphase transition Anaphase promoting complex, or cyclosome (APC/C) = ubiquitin ligase Продвижение через R1 (START) и
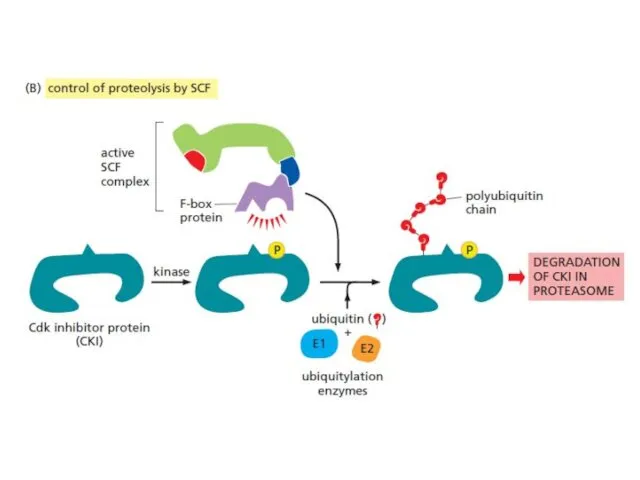
- 14. SCF убиквитинирует: Определенные CKI в поздней G1, что позволяет активировать S-Cdk’s и запустить репликацию DNA. SCF
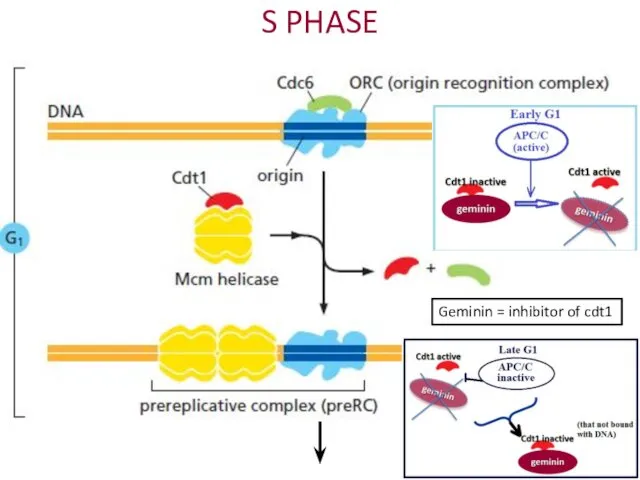
- 18. S PHASE Geminin = inhibitor of cdt1
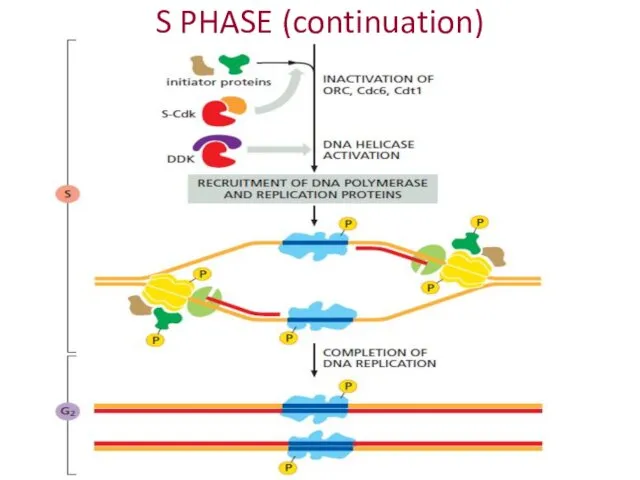
- 19. S PHASE (continuation)
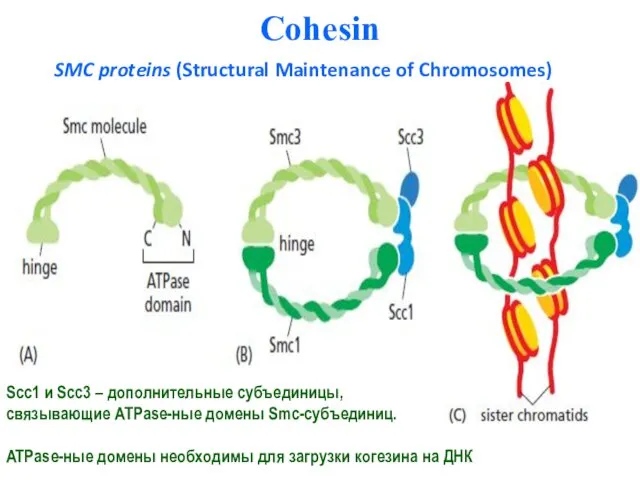
- 20. Cohesin SMC proteins (Structural Maintenance of Chromosomes) Scc1 и Scc3 – дополнительные субъединицы, связывающие ATPase-ные домены
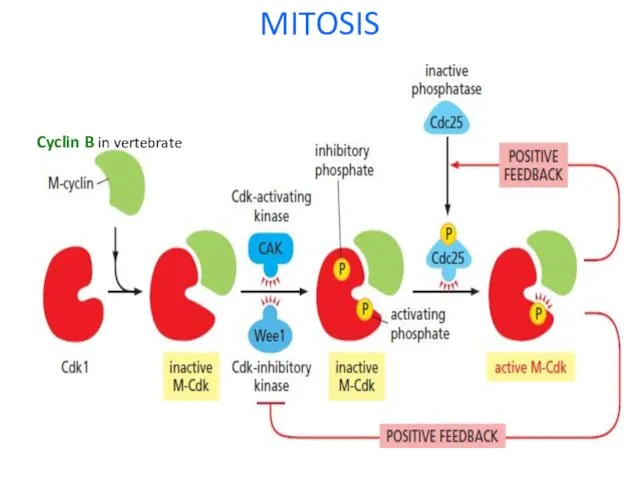
- 21. MITOSIS Cyclin B in vertebrate
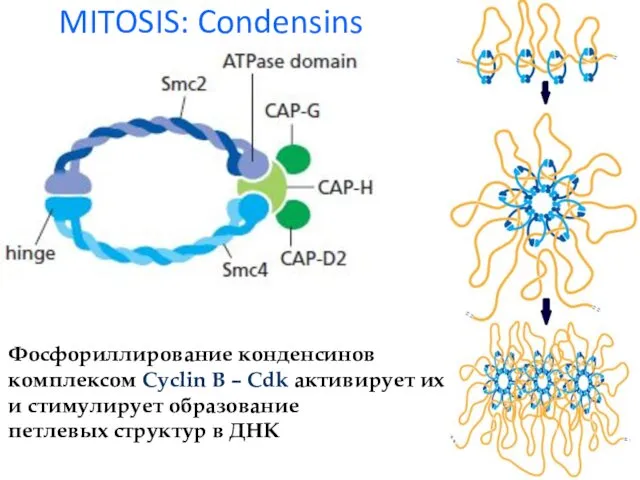
- 22. MITOSIS: Condensins Фосфориллирование конденсинов комплексом Cyclin B – Cdk активирует их и стимулирует образование петлевых структур
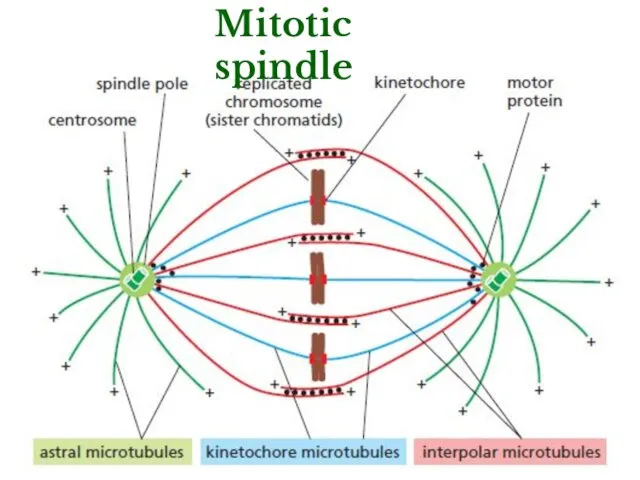
- 23. Mitotic spindle
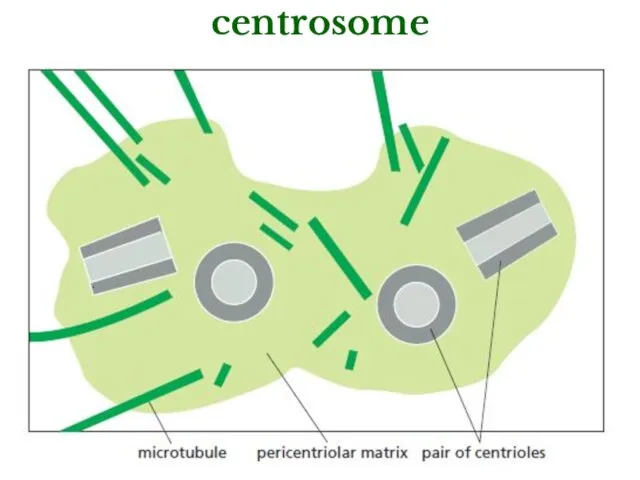
- 24. centrosome
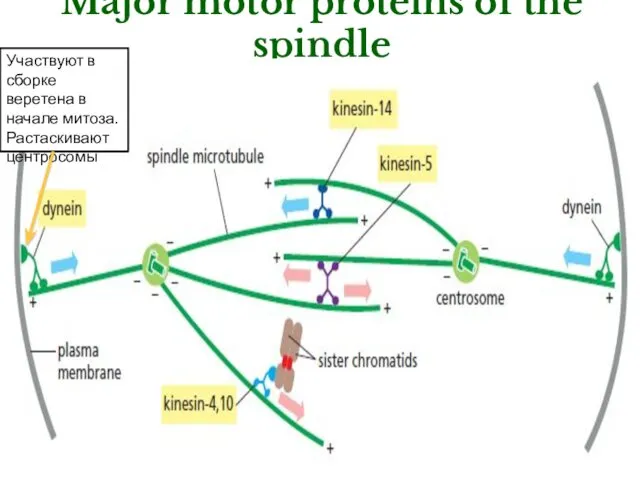
- 25. Major motor proteins of the spindle
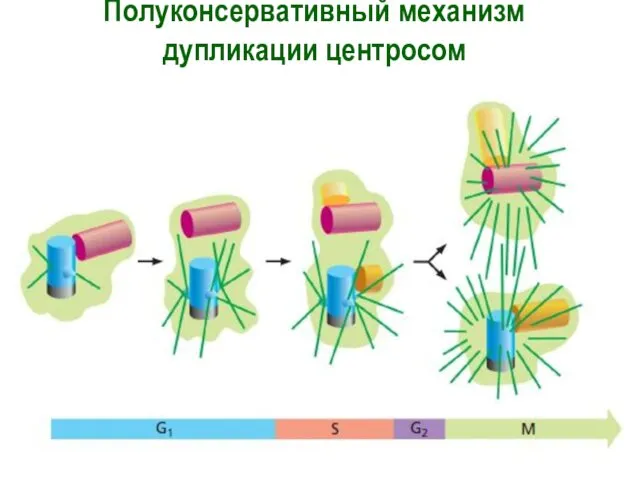
- 26. Полуконсервативный механизм дупликации центросом
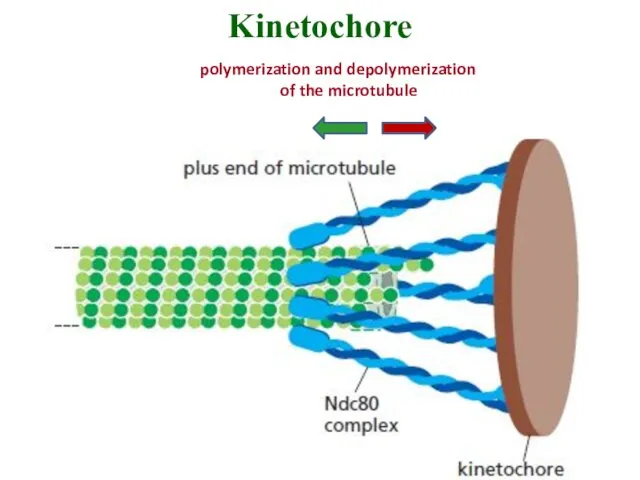
- 27. Kinetochore polymerization and depolymerization of the microtubule
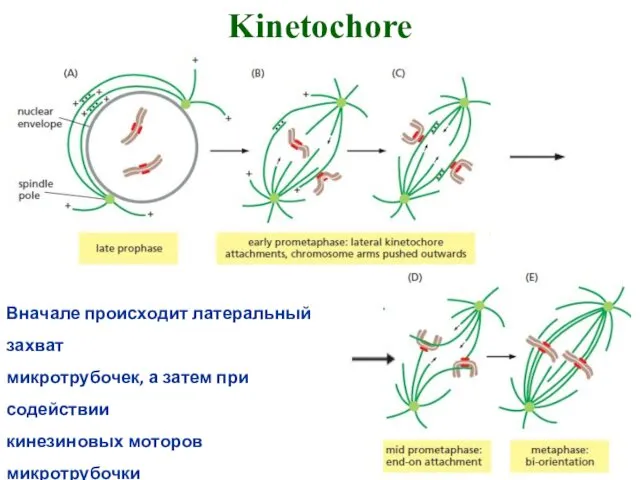
- 28. Kinetochore Вначале происходит латеральный захват микротрубочек, а затем при содействии кинезиновых моторов микротрубочки ориентируются в правильное
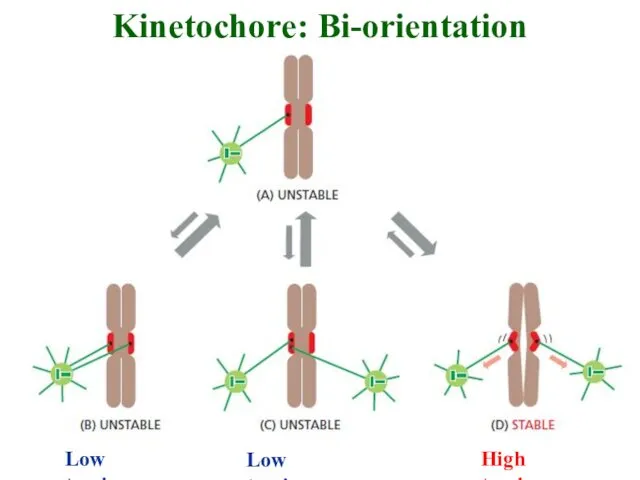
- 29. Kinetochore: Bi-orientation Low tension Low tension High tension
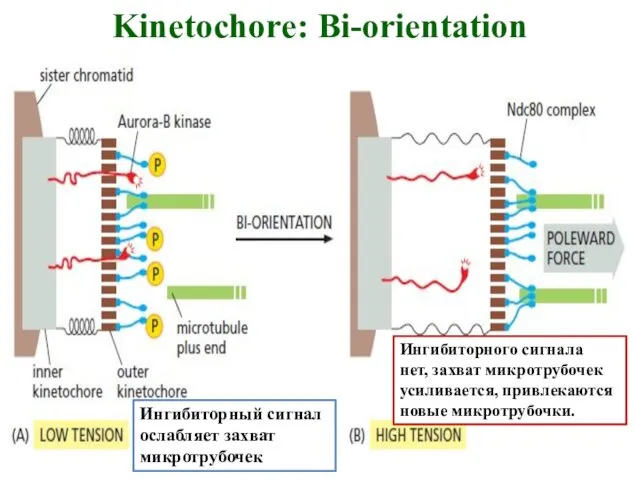
- 30. Kinetochore: Bi-orientation Ингибиторный сигнал ослабляет захват микротрубочек Ингибиторного сигнала нет, захват микротрубочек усиливается, привлекаются новые микротрубочки.
- 31. Сила, направляющая кинетохор к полюсу (разборка микротрубочек в месте прикрепления к кинетохору). К полюсу Движение самих
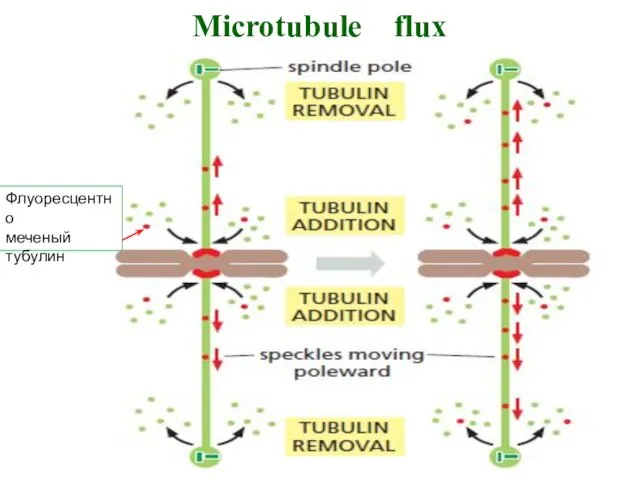
- 32. Флуоресцентно меченый тубулин Microtubule flux
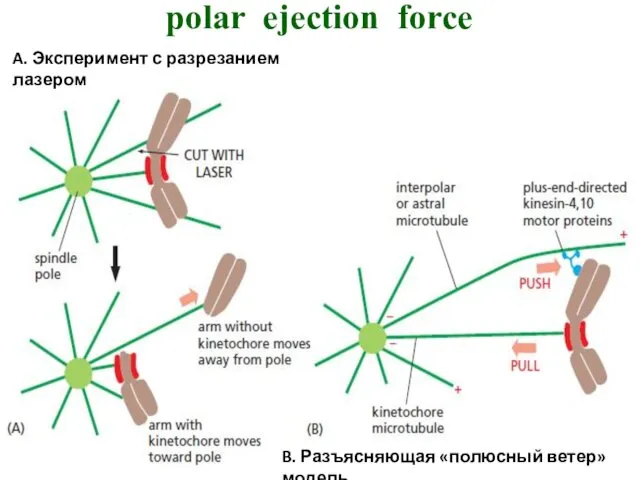
- 33. polar ejection force A. Эксперимент с разрезанием лазером B. Разъясняющая «полюсный ветер» модель
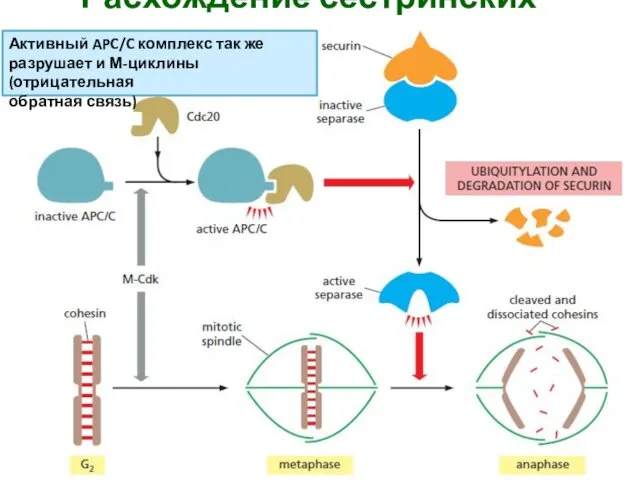
- 34. Расхождение сестринских хроматид Активный APC/C комплекс так же разрушает и М-циклины (отрицательная обратная связь)
- 35. Mad2 белок является проверочным механизмом присоединения к кинетохору трубочек. Если напряжения на микротрубочках, связанных с кинетохором
- 36. Разборка веретена; Фрагменты ядерной мембраны ассоциируются с отдельными хромосомами и затем соединяются друг с другом; комплекс
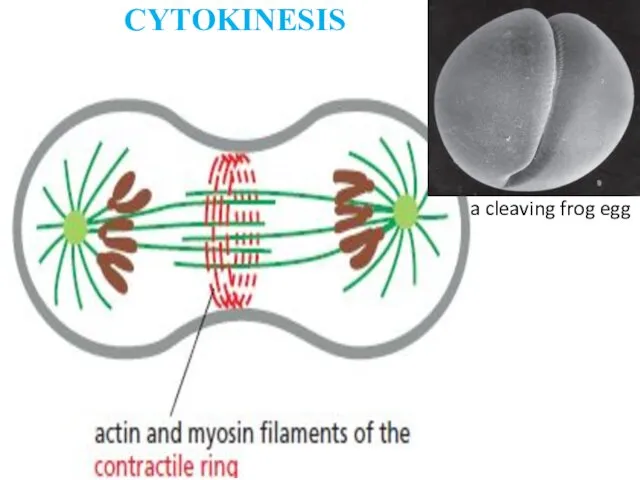
- 37. CYTOKINESIS Обычно митоз заканчивается цитокинезом. Некоторые клетки (ранние эмбрионы дрозофилы, гепатоциты и кардиомиоциты) проходят митоз без
- 38. CYTOKINESIS a cleaving frog egg
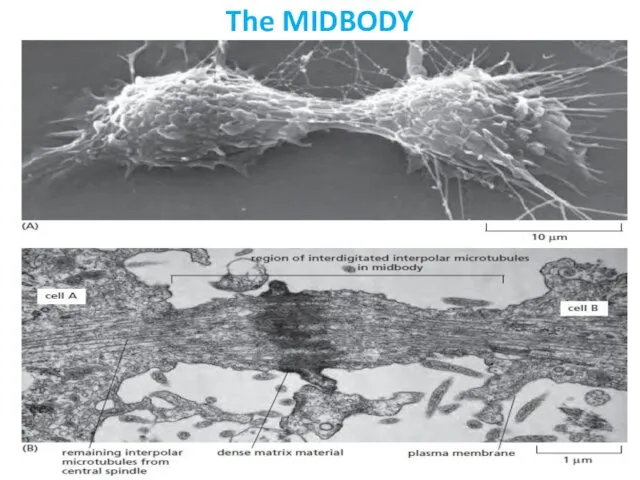
- 39. The MIDBODY
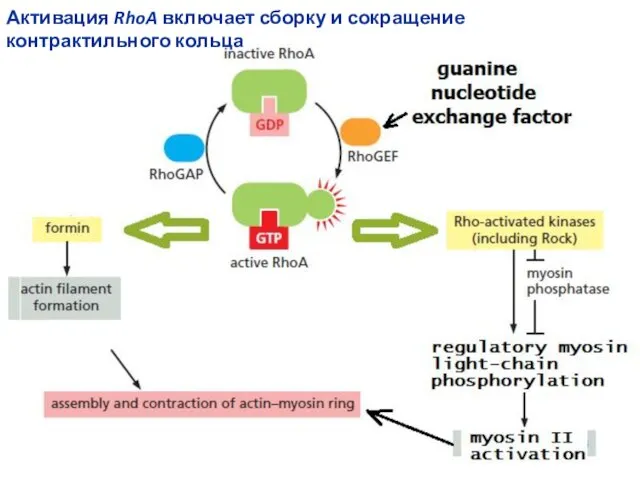
- 40. Активация RhoA включает сборку и сокращение контрактильного кольца
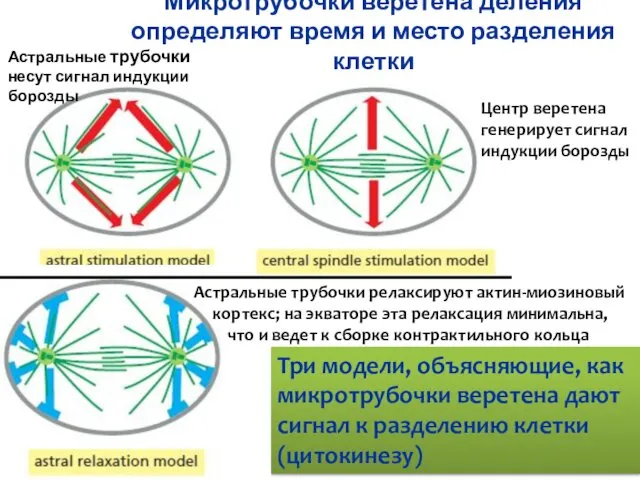
- 41. Микротрубочки веретена деления определяют время и место разделения клетки Три модели, объясняющие, как микротрубочки веретена дают
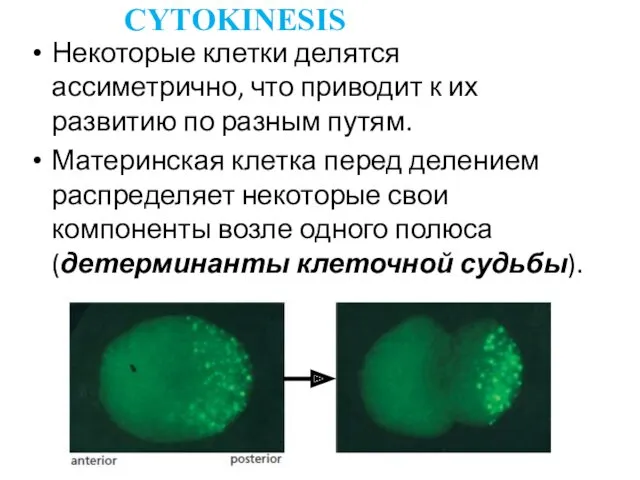
- 42. Некоторые клетки делятся ассиметрично, что приводит к их развитию по разным путям. Материнская клетка перед делением
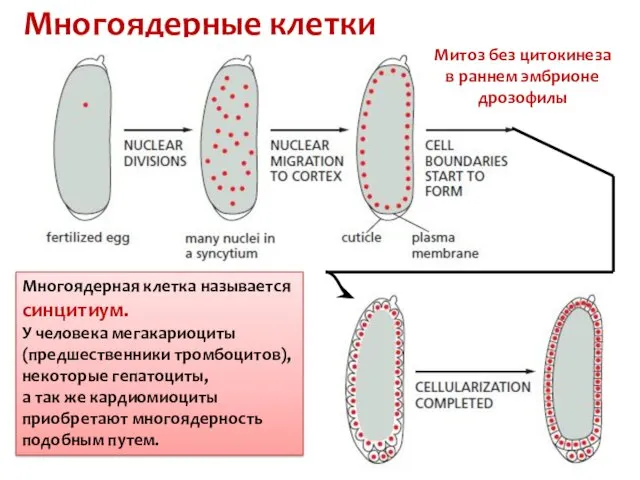
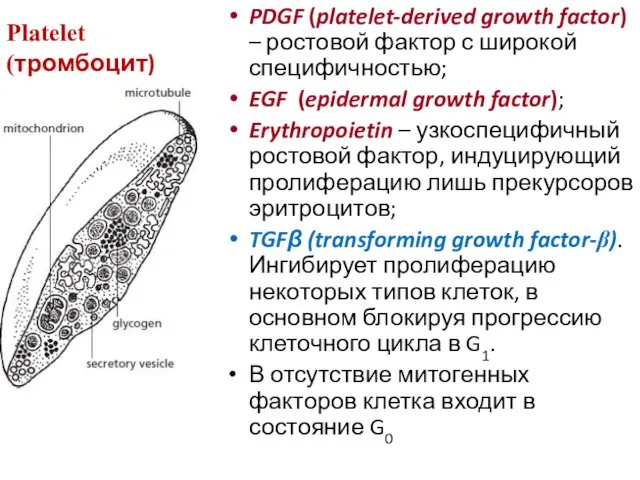
- 43. Многоядерные клетки Многоядерная клетка называется синцитиум. У человека мегакариоциты (предшественники тромбоцитов), некоторые гепатоциты, а так же
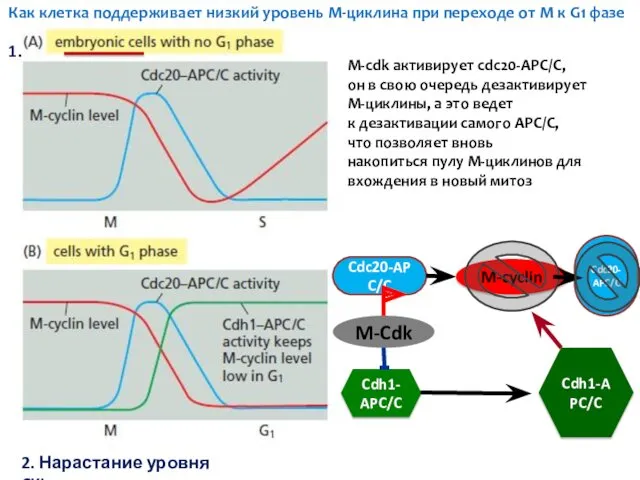
- 44. М-cdk активирует cdc20-APC/C, он в свою очередь дезактивирует М-циклины, а это ведет к дезактивации самого APC/C,
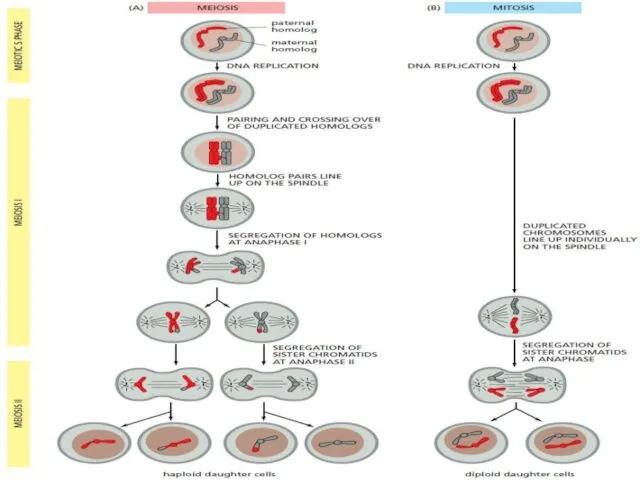
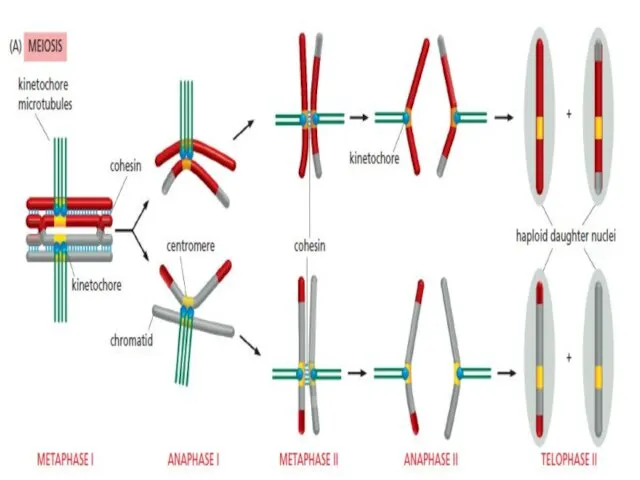
- 45. MEIOSIS
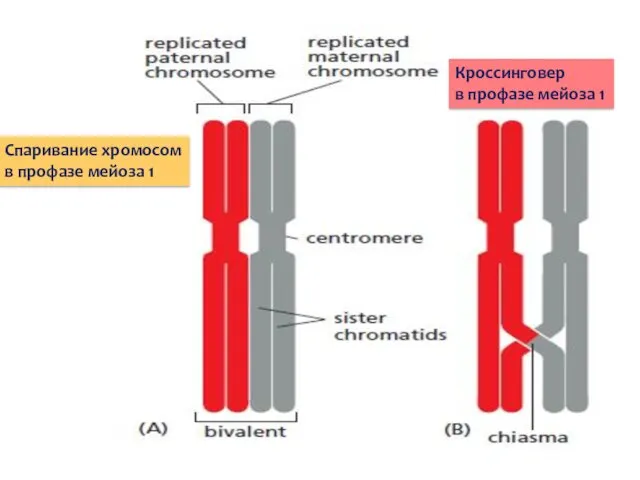
- 47. Спаривание хромосом в профазе мейоза 1 Кроссинговер в профазе мейоза 1
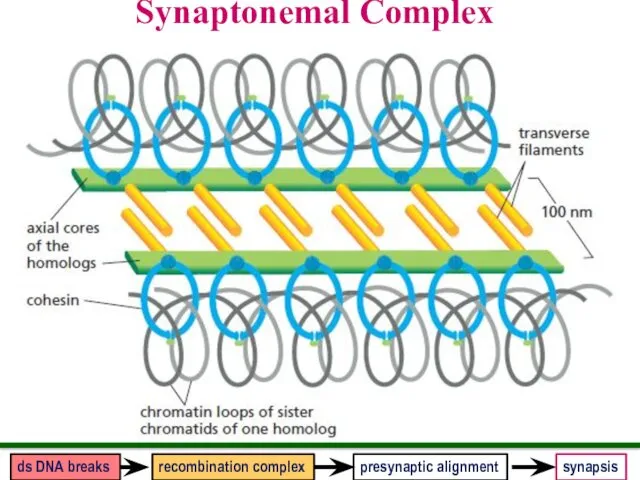
- 48. Synaptonemal Complex presynaptic alignment synapsis ds DNA breaks recombination complex
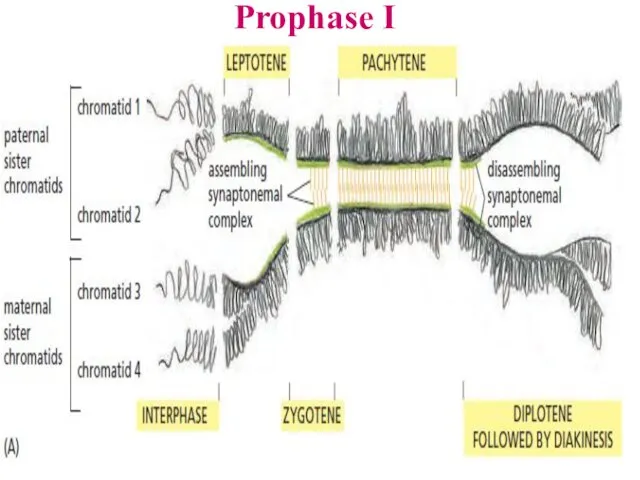
- 49. Prophase I
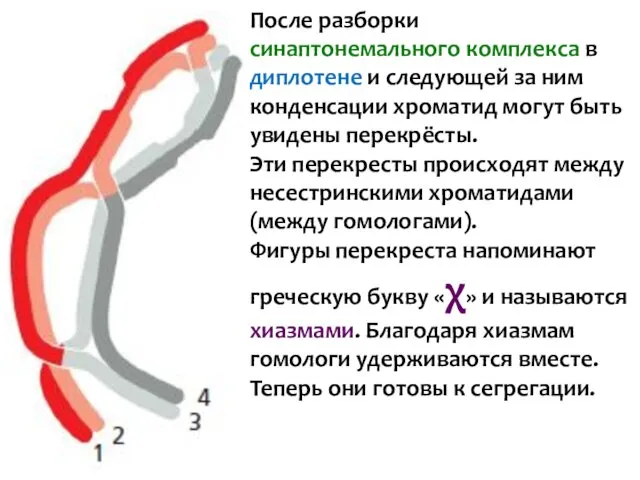
- 50. После разборки синаптонемального комплекса в диплотене и следующей за ним конденсации хроматид могут быть увидены перекрёсты.
- 51. 1. Оба сестринских кинетохора в гомологе должны быть соединены с ОДНИМ и тем же полюсом веретена.
- 53. Кроссинговер тщательно регулируется: на каждую гомологичную пару хромосом приходится не менее одного (поскольку гомологи должны удерживаться
- 54. Контроль клеточного деления и роста Внеклеточные сигналы, регулирующие клеточный рост, деление и «выживание», могут быть разделены
- 55. PDGF (platelet-derived growth factor) – ростовой фактор с широкой специфичностью; EGF (epidermal growth factor); Erythropoietin –
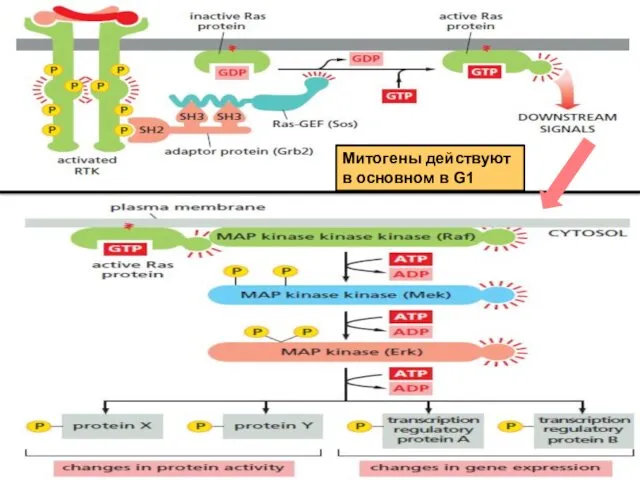
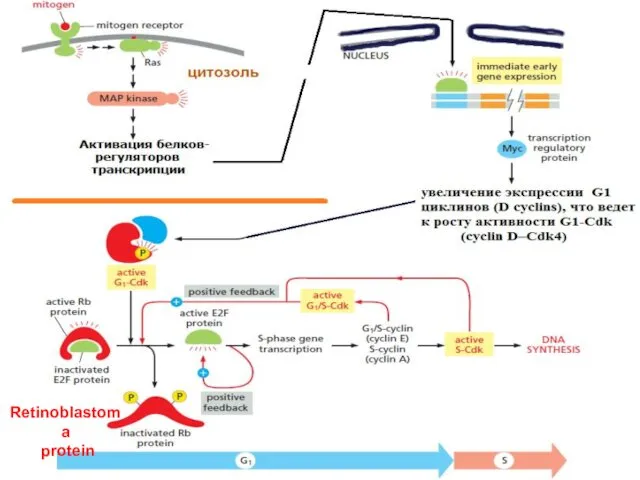
- 56. Митогены действуют в основном в G1
- 57. Retinoblastoma protein
- 60. Клетки имеют ограниченное число делений (предел Хейфлика). После этого предела клетки входят в неделящееся состояние, из
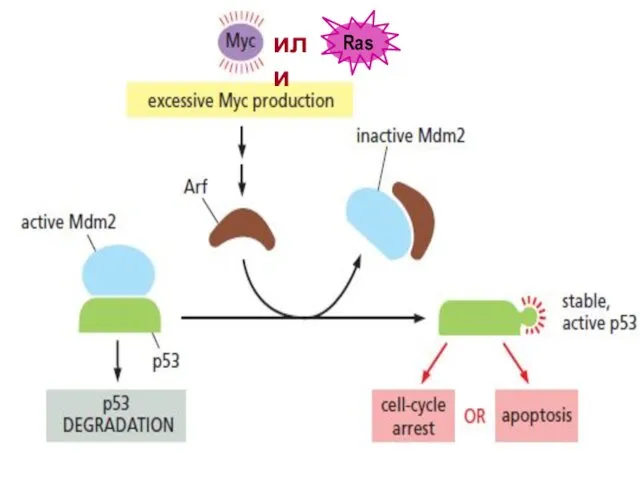
- 61. или Ras
- 63. Скачать презентацию












 Презентация Коллективная разработка ПО
Презентация Коллективная разработка ПО Невынашивание беременности
Невынашивание беременности Мікропроцесорна техніка (лекція 7)
Мікропроцесорна техніка (лекція 7)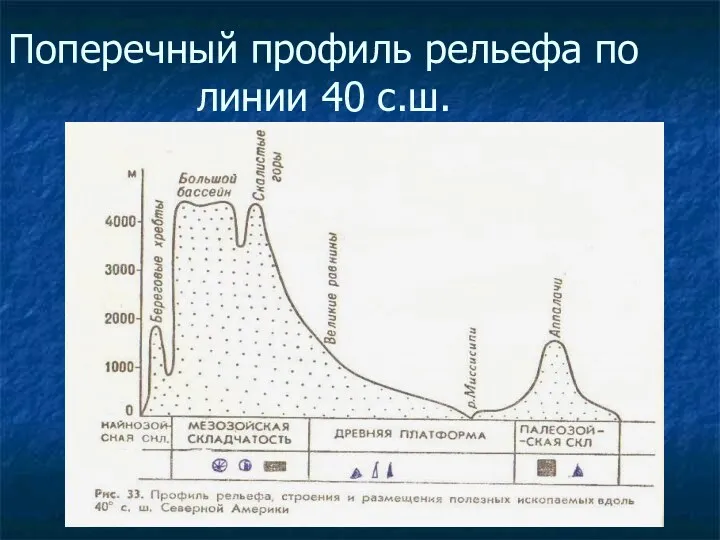 7 класс: Оледенение С.Америки
7 класс: Оледенение С.Америки Чем археолог отличается от криминалиста. Социальные ландшафты: вещи в динамике прошлого
Чем археолог отличается от криминалиста. Социальные ландшафты: вещи в динамике прошлого Functional styles of the english language: newspaper style
Functional styles of the english language: newspaper style Статус - отчет по ремонту Сормовский 3060
Статус - отчет по ремонту Сормовский 3060 К юбилею В.Г. Распутина, Героя Социалистического Труда, дважды лауреата Государственной премии СССР
К юбилею В.Г. Распутина, Героя Социалистического Труда, дважды лауреата Государственной премии СССР Планиметрия. Повторение. Часть 1
Планиметрия. Повторение. Часть 1 Мартеновский способ производства стали. Выплавка стали в электропечах
Мартеновский способ производства стали. Выплавка стали в электропечах How to present in English
How to present in English Интеллектуальные роботы состояние и перспективы
Интеллектуальные роботы состояние и перспективы Презентация С правом по жизни.
Презентация С правом по жизни. особенности изображения Земли на глобусе и на карте
особенности изображения Земли на глобусе и на карте Декоративные злаки
Декоративные злаки Мы вместе. Часть 2
Мы вместе. Часть 2 Рисуем пластилином
Рисуем пластилином Монтаж и эксплуатация ПВО. Противовыбросовое оборудование иностранных производителей
Монтаж и эксплуатация ПВО. Противовыбросовое оборудование иностранных производителей Философия Августина Блаженного
Философия Августина Блаженного Классный час 1сентября Эхо Бесланской печали
Классный час 1сентября Эхо Бесланской печали Конспект урока географии в 6 классе Тайны подземных бурь.
Конспект урока географии в 6 классе Тайны подземных бурь. Закрепление изученного в 4 классе
Закрепление изученного в 4 классе Стандартизация свойств. Физические, механические, физико-химические свойства СМ. Долговечность и надежность
Стандартизация свойств. Физические, механические, физико-химические свойства СМ. Долговечность и надежность презентация
презентация Биосфера Земли. Тест
Биосфера Земли. Тест Презентация Автоматизация звука Л в словах
Презентация Автоматизация звука Л в словах Священная Библейская история Ветхого Завета. Грехопадение и его последствия (Быт.3)
Священная Библейская история Ветхого Завета. Грехопадение и его последствия (Быт.3) Нарушения обмена хромопротеидов
Нарушения обмена хромопротеидов