Содержание
- 2. ОПРЕДЕЛЕНИЕ Корро́зия (от лат.corrosio - разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического
- 3. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде.
- 5. ТИПЫ КОРРОЗИИ Главная классификация производится по механизму протекания процесса. Различают два вида: - химическую коррозию -
- 6. Химическая коррозия Химическая коррозия — взаимодействие поверхности металла с коррозионно-активной средой ( сухой газ – Cl₂,
- 7. Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. При электрохимической коррозии
- 8. По типу агрессивных сред, в которых протекает процесс разрушения, коррозия может быть следующих видов: газовая коррозия
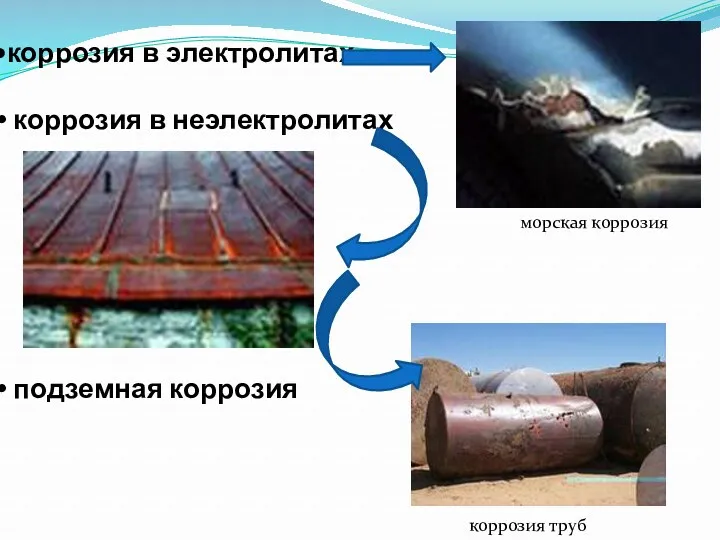
- 9. коррозия в электролитах коррозия в неэлектролитах подземная коррозия морская коррозия коррозия труб
- 10. биокоррозия коррозия под воздействием блуждающих токов. коррозия на древесине коррозия на бетоне
- 11. По характеру разрушения: сплошная коррозия, охватывающая всю поверхность: равномерная неравномерная; локальная (местная) коррозия, охватывающая отдельные участки:
- 12. БОРЬБА С КОРРОЗИЕЙ Основной ущерб, заключается в огромной стоимости изделий, разрушаемых коррозией. Истинные убытки : стоимость
- 13. МЕТОДЫ БОРЬБЫ С КОРРОЗИЕЙ. Шлифование поверхностей изделия Применение легированных сплавов «нержавейка»
- 14. Нанесение защитных покрытий - неокисляющиеся масла , лак , краска , эмаль - оксидных, нитридных, полимерных
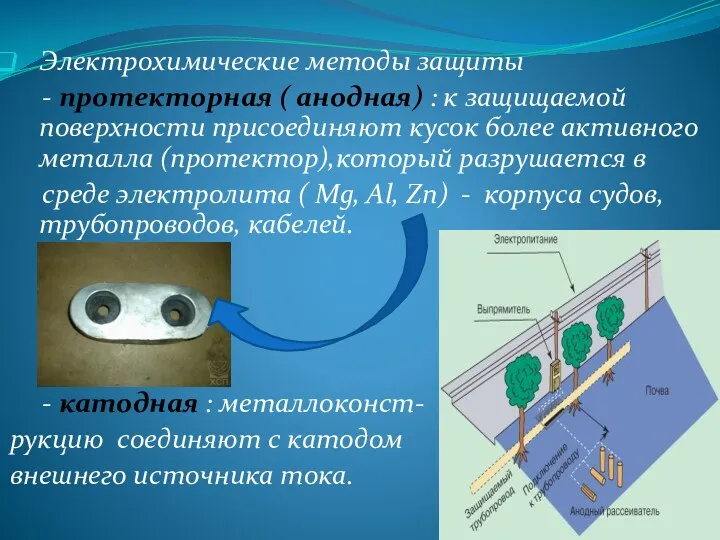
- 15. Электрохимические методы защиты - протекторная ( анодная) : к защищаемой поверхности присоединяют кусок более активного металла
- 17. Скачать презентацию












 Бронхиальная астма и статус
Бронхиальная астма и статус Hello september
Hello september Падежи имен существительных
Падежи имен существительных Организация комплекса просветительских мероприятий на приходе св. прав. Симеона Верхотурского
Организация комплекса просветительских мероприятий на приходе св. прав. Симеона Верхотурского Е1 біріншілік цифрлық ағынынның циклының құрылуы
Е1 біріншілік цифрлық ағынынның циклының құрылуы Фритредерские тенденции в таможенной политике в начале XIX века
Фритредерские тенденции в таможенной политике в начале XIX века Презентация ВГЛТУ
Презентация ВГЛТУ Личность и коллектив
Личность и коллектив Строение скелета и мышц головы и туловища
Строение скелета и мышц головы и туловища Модернизм в русской литературе
Модернизм в русской литературе Где живут слоны
Где живут слоны Мультивибраторы и триггеры
Мультивибраторы и триггеры Геокешинг. Удивительные приключения Солнышка в библиотеке
Геокешинг. Удивительные приключения Солнышка в библиотеке Металлургический комплекс. Черная и цветная металлургия России
Металлургический комплекс. Черная и цветная металлургия России Введение в профессию по направлению подготовки бакалавров
Введение в профессию по направлению подготовки бакалавров Социально - нравственное воспитание
Социально - нравственное воспитание Шаруашылық аумақтық ұйымдастырылуы. Ішкі айырмашылықтары
Шаруашылық аумақтық ұйымдастырылуы. Ішкі айырмашылықтары Производство чугуна и стали
Производство чугуна и стали На какие вопросы может дать ответ астрология?
На какие вопросы может дать ответ астрология? Обозначение парных глухих и звонких согласных звуков на конце слова
Обозначение парных глухих и звонких согласных звуков на конце слова Современный компьютер. Перспективы развития
Современный компьютер. Перспективы развития краеведческая игра Я горжусь тобой, мой Липецкий край!
краеведческая игра Я горжусь тобой, мой Липецкий край! Возникновение ислама. Арабский халифат и его распад
Возникновение ислама. Арабский халифат и его распад Бурильна колона. Лекція 5
Бурильна колона. Лекція 5 Прилагательные, отвечающие на вопрос: чей
Прилагательные, отвечающие на вопрос: чей В мире басен И.А.Крылова 2 часть
В мире басен И.А.Крылова 2 часть Пограничное расстройство личности
Пограничное расстройство личности Хроническая сердечная недостаточность
Хроническая сердечная недостаточность