Содержание
- 2. АЗОТИСТЫЙ БАЛАНС Азотистый баланс — разница между количеством азота, поступающего с пищей, и количеством выделяемого азота
- 3. Если количество поступающего азота равно количеству выделяемого, то наступает азотистое равновесие. Такое состояние бывает у здорового
- 4. Белковая недостаточность Известно, что даже длительное исключение из рациона человека жиров или углеводов не вызывает тяжёлых
- 5. В организме человека в сутки распадается на аминокислоты около 400 г белков, примерно такое же количество
- 6. Фонд свободных аминокислот организма составляет примерно 35 г. Содержание свободных аминокислот в крови в среднем равно
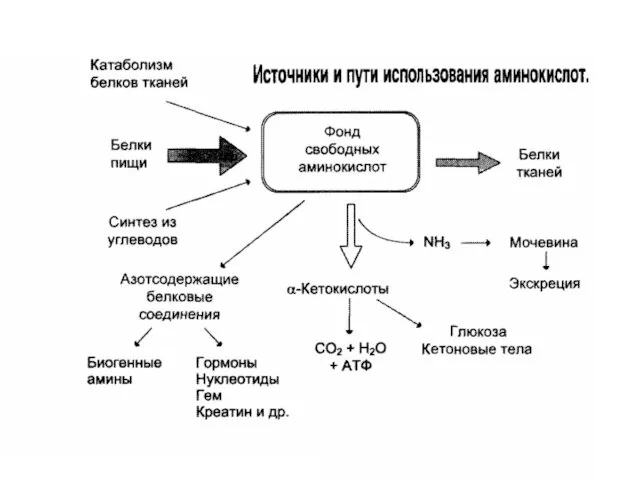
- 7. Источники аминокислот 1. Белки корма 2. Белки тканей при распаде в процессе их обновления ( при
- 8. Пути использования аминокислот в организме Биосинтез белков Синтез биологически активных веществ Синтез углеводов, липидов Окисление для
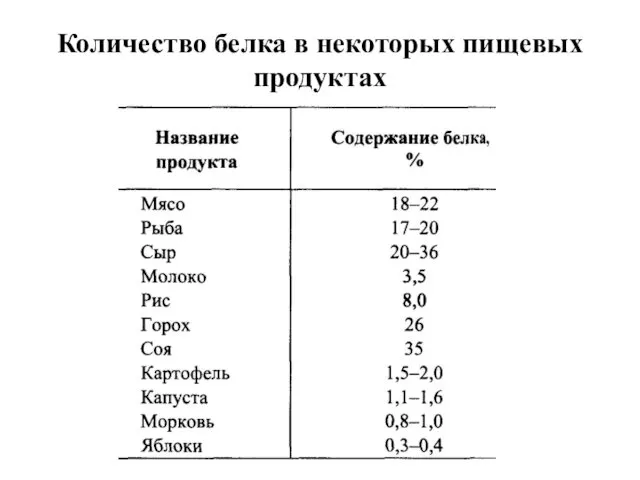
- 10. Количество белка в некоторых пищевых продуктах
- 11. ПЕРЕВАРИВАНИЕ БЕЛКОВ В пищевых продуктах содержание свободных аминокислот очень мало. Подавляющее их количество входит в состав
- 12. Переваривание белков в желудке Желудочный сок — продукт нескольких типов клеток. Обкладочные (париетальные) клетки стенок желудка
- 13. Под действием НС1 происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей
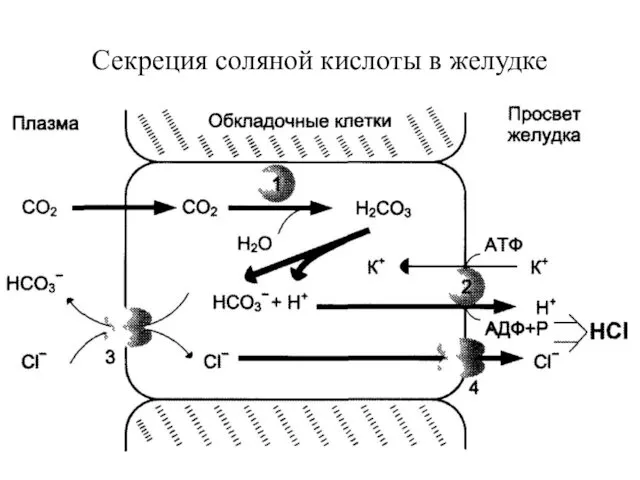
- 14. Секреция соляной кислоты в желудке
- 15. Механизм активации пепсина Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена
- 16. Особенности переваривания белков в желудке У детей грудного возраста в желудке находится фермент реннин (химозин) ,
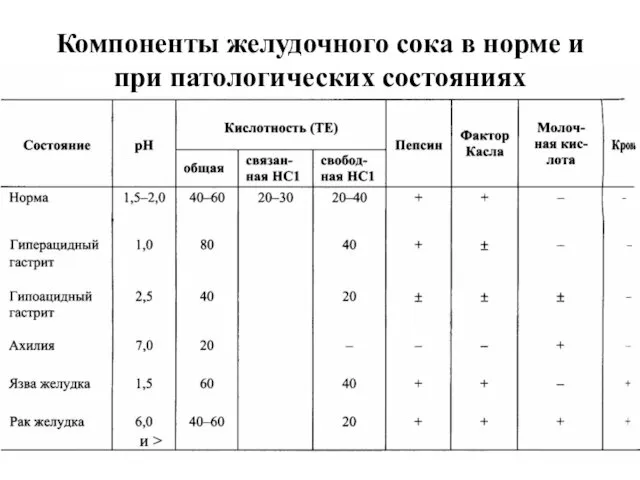
- 17. Компоненты желудочного сока в норме и при патологических состояниях
- 18. Активация панкреатических ферментов В поджелудочной железе синтезируются проферменты ряда протеаз: трипсиноген, химотрипсиноген, проэластаза, прокарбоксипептидазы А и
- 19. Активация трипсиногена происходит под действием фермента эпителия кишечника энтериептидазы. Этот фермент отщепляет с N-конца молекулы трипсиногена
- 20. Образовавшийся трипсин активирует химотрипсиноген, из которого получается несколько активных ферментов. Химотрипсиноген состоит из одной полипептидной цепи,
- 21. Активация химотрипсиногена
- 22. Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного протеолиза.
- 23. Специфичность действия протеаз Трипсин преимущественно гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина. Химотрипсины наиболее
- 24. Карбоксипептидазы А и В — цинксодержащие ферменты, отщепляют С-концевые остатки аминокислот. Причём карбоксипептидаза А отщепляет преимущественно
- 25. Аминопептидазы последовательно отщепляют N-концевые аминокислоты пептидной цепи. Наиболее известна лейцинаминопептидаза — Zn2+ - или Мn2+ -
- 26. Защита клеток от действия протеаз Клетки поджелудочной железы защищены от действия пищеварительных ферментов тем, что: эти
- 27. Защита от действия протеаз В полости желудка и кишечника протеазы не контактируют с белками клеток, поскольку
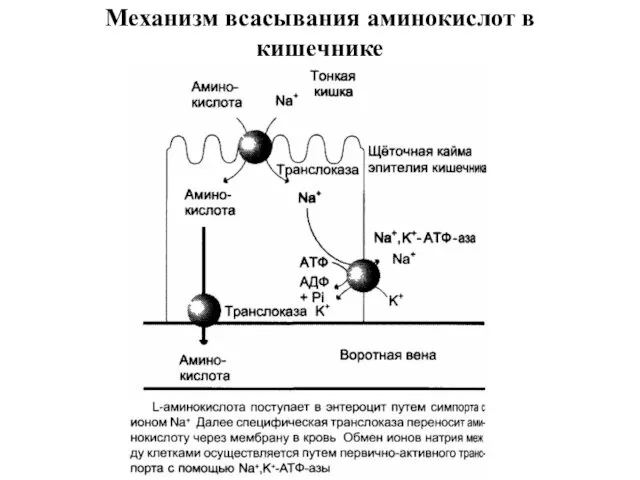
- 28. Механизм всасывания аминокислот в кишечнике
- 29. В настоящёе время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для
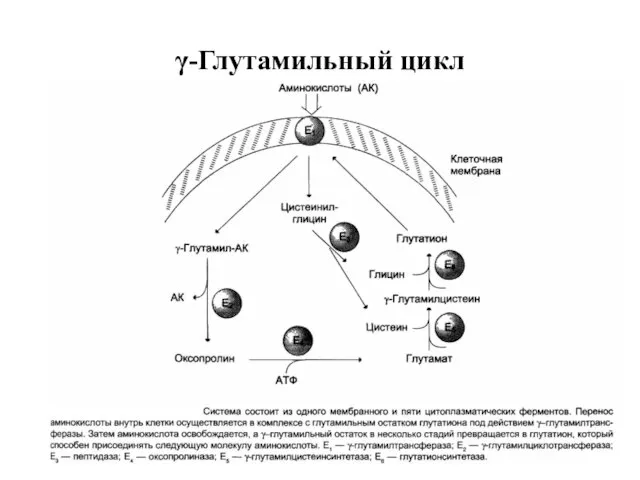
- 30. γ-Глутамильный цикл
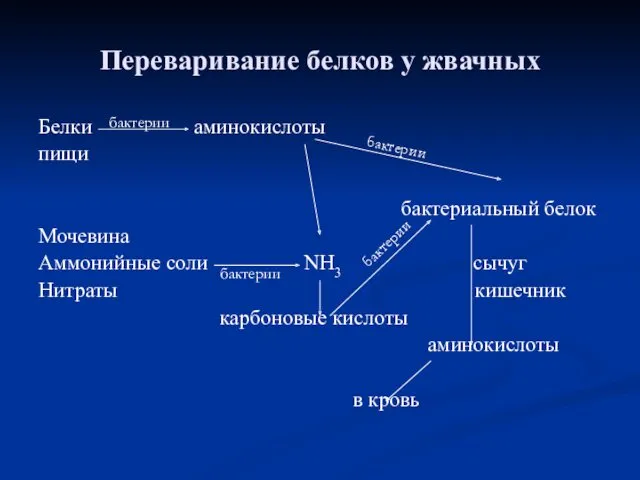
- 31. Переваривание белков у жвачных Белки аминокислоты пищи бактериальный белок Мочевина Аммонийные соли NH3 сычуг Нитраты кишечник
- 32. КАТАБОЛИЗМ АМИНОКИСЛОТ Аминокислоты, образующиеся при переваривании белков и поступающие в клетки тканей, подвергаются катаболизму и анаболизму,
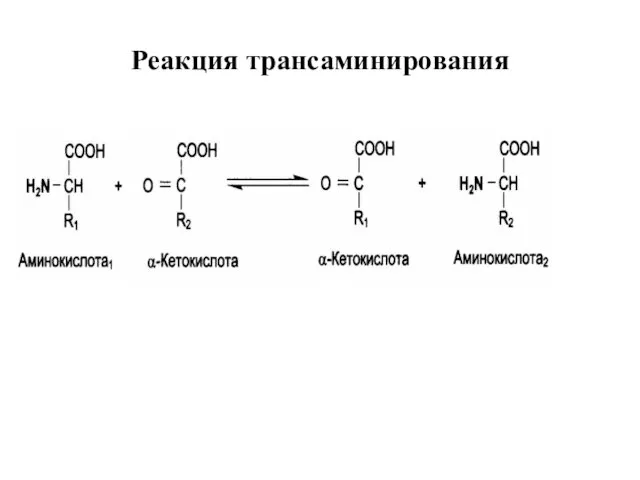
- 33. Трансаминирование Трансаминирование — реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту, в результате чего образуются новая кетокислота
- 34. Аминотрансферазы Аминотрансферазы обнаружены как в цитоплазме, так и в митохондриях клеток эукариот. Причём митохондриальные и цитоплазматические
- 35. Реакция трансаминирования
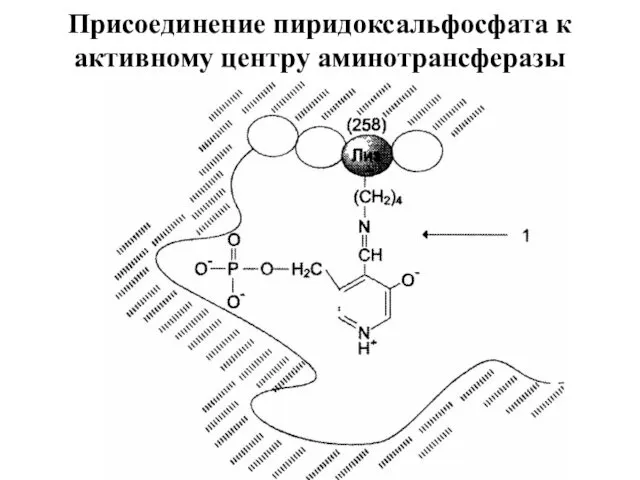
- 36. Присоединение пиридоксальфосфата к активному центру аминотрансферазы
- 37. Основной путь трансаминирования Чаще всего в реакциях трансаминированиш участвуют аминокислоты, содержание которых в тканях значительно выше
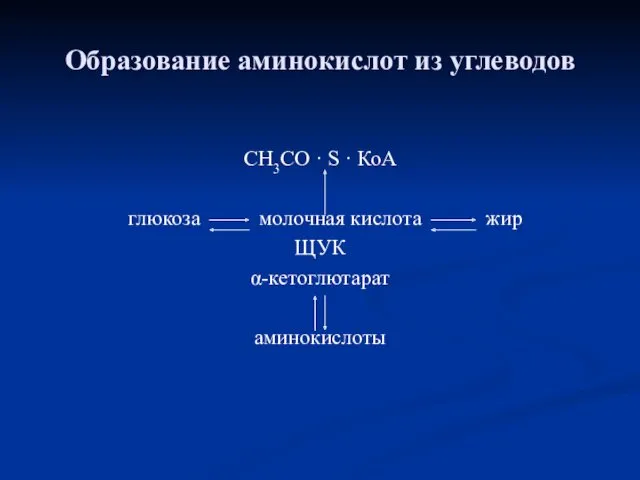
- 38. Образование аминокислот из углеводов СН3СО · S · КоА глюкоза молочная кислота жир ЩУК α-кетоглютарат аминокислоты
- 39. Аминотрансферазы обладают субстратной специфичностью к разным аминокислотам. В тканях человека обнаружено более 10 разных аминотрансфераз. Наиболее
- 40. Аланинаминотрансфераза АЛТ (АлАТ) катализирует реакцию трансаминирования между аланином и α-кетоглутаратом. Локализован этот фермент в цитозоле клеток
- 41. ACT (АсАТ) катализирует реакцию трансаминирования между аспартатом и α-кетоглутаратом аналогично предыдущей. В результате образуются оксалоацетат и
- 42. Биологическое значение трансаминирования Реакции трансаминирования играют большую роль в обмене аминокислот. Поскольку этот процесс обратим, ферменты
- 43. Дезаминирование аминокислот Дезаминирование аминокислот — реакция отщепления α-аминогруппы от аминокислоты, в результате чего образуется соответствующая α-кетокислота
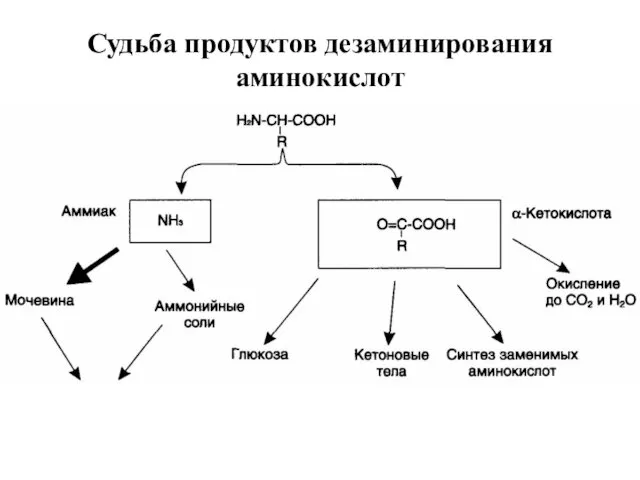
- 44. Судьба продуктов дезаминирования аминокислот
- 45. R R В) COOH +NH3 COONH4 органическая аммонийная кислота соль органич. к-ты
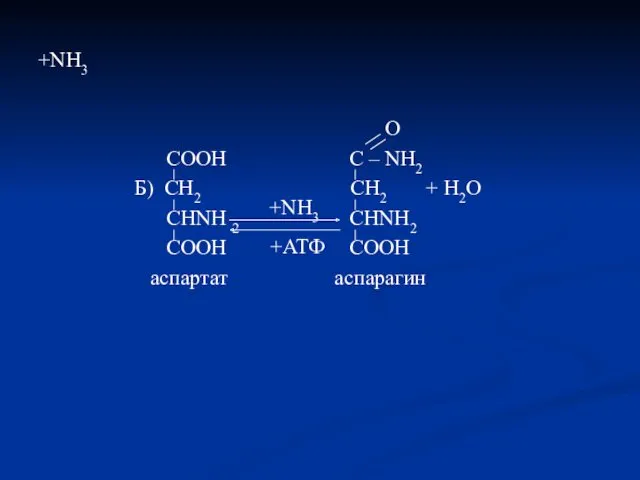
- 46. +NH3 O COOH C – NH2 Б) CH2 CH2 + H2O CHNH 2 CHNH2 COOH COOH
- 47. Виды дезаминирования аминокислот 1. Гидролитическое 2. Окислительное 3. Восстановительное 4. Внутримолекулярное
- 48. Гидролитическое дезаминирование CH3 CH3 CHNH2 CHOH COOH COOH (у бактерий) +HOH -NH3
- 49. Окислительное дезаминирование Окислительное дезаминирование может происходить при участии ФМН и ФАД –зависимых оксидаз аминокислот: А)D-аминокислоты иминокислоты
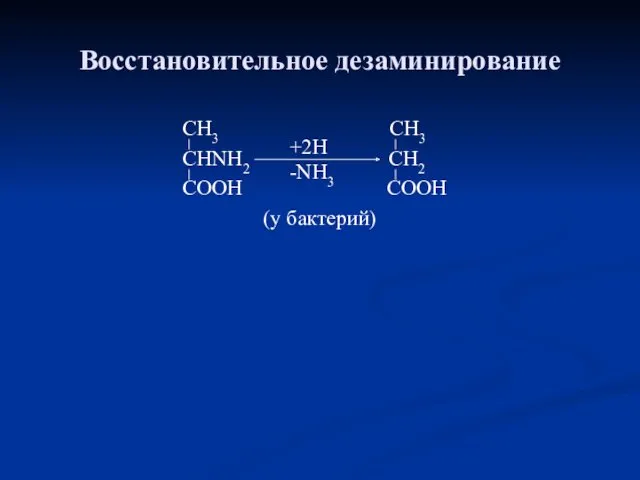
- 50. Восстановительное дезаминирование CH3 CH3 CHNH2 CH2 COOH COOH (у бактерий) +2Н -NH3
- 51. Внутримолекулярное дезаминирование СН СН2 СНNH2 СН СООН СООН (у бактерий) У высших животных таким путем дезаминируется
- 52. Большая часть безазотистых остатков аминокислот превращается в пируват, либо в результате более сложного пути, в один
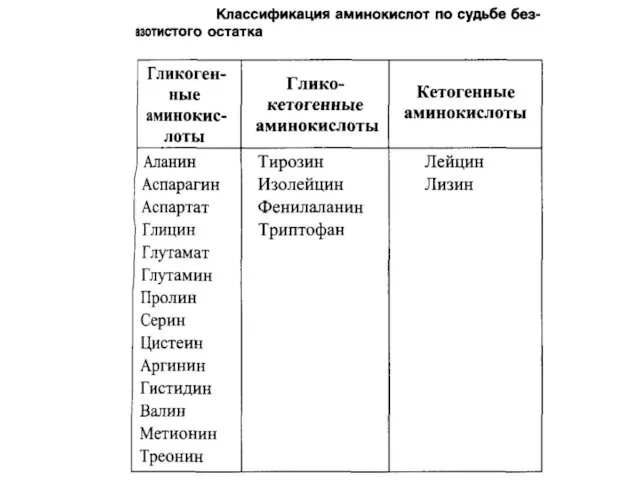
- 53. ГЛИКОГЕННЫЕ и кетогенные АМИНОКИСЛОТЫ Катаболизм всех аминокислот сводится к образованию шести веществ, вступающих в путь катаболизма:
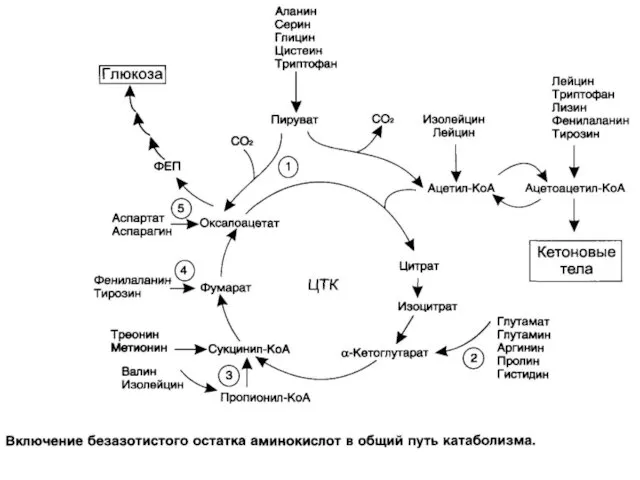
- 54. Пути использования безазотистого остатка аминокислот: 1. Окисляются → энергия + Н2О + СО2 2. Синтез углеводов
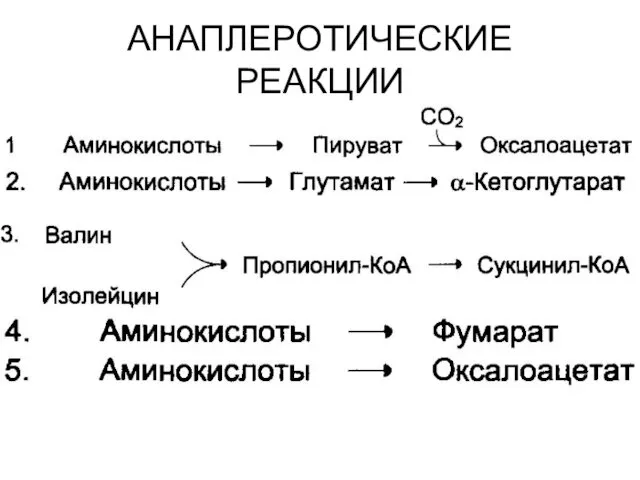
- 57. АНАПЛЕРОТИЧЕСКИЕ РЕАКЦИИ
- 59. БИОСИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ В организме человека возможен синтез восьми заменимых аминокислот: Ала, Асп, Арг, Сер, Гли,
- 60. Кроме восьми перечисленных заменимых аминокислот, в организме млекопитающих могут синтезироваться ещё четыре аминокислоты. Частично заменимые аминокислоты
- 61. Пути обезвреживания NH3 Временное - образование амидов аминокислот, образование аммонийных солей – во всех тканях. Окончательное
- 62. Окислительное дезаминирование Наиболее активно в тканях происходит деза-минирование глутаминовой кислоты. Реакцию катализирует фермент глутаматдегидрогеназа, коферментом глутаматдегидрогеназы
- 63. Дезаминирование глутамата
- 64. Непрямое дезаминирование (трансдезаминирование) Большинство аминокислот не способно дезаминироваться в одну стадию, подобно Глу. Аминогруппы таких аминокислот
- 65. трансдезаминирование непрямое дезаминироваше — основной способ дезаминирования большинства аминокислот. Обе стадии непрямого дезаминирования обратимы, что обеспечивает
- 66. Обратимость трансдезаминирования
- 67. Неокислительное дезаминирование В печени человека присутствуют специфические ферменты, катализирующие реакции дезаминирования аминокислот серина, треонина и гистидина
- 68. Дезаминирование серина
- 69. Токсичность аммиака Аммиак легко проникает через мембраны в клетки и в митохондриях сдвигает реакцию, катализируемую глутаматдегидрогеназой,
- 70. Токсичность аммиака Повышение концентрации аммиака в кро ви сдвигает рН в щелочную сторону (вызы вает алкалоз).
- 71. Связывание аммиака Основной реакцией связывания аммиака, протекающей во всех тканях организма, является синтез глутамина под действием
- 72. Глутамин — основной донор азота в организме. 'Высокий уровень глутамина в крови и лёгкость его поступления
- 73. Орнитиновый цикл Мочевина — основной конечный продукт азотистого обмена, в составе которого из организма выделяется до
- 74. Орнитиновый цикл
- 75. Орнитиновый цикл
- 76. Орнитиновый цикл
- 77. Орнитиновый цикл
- 78. Орнитиновый цикл
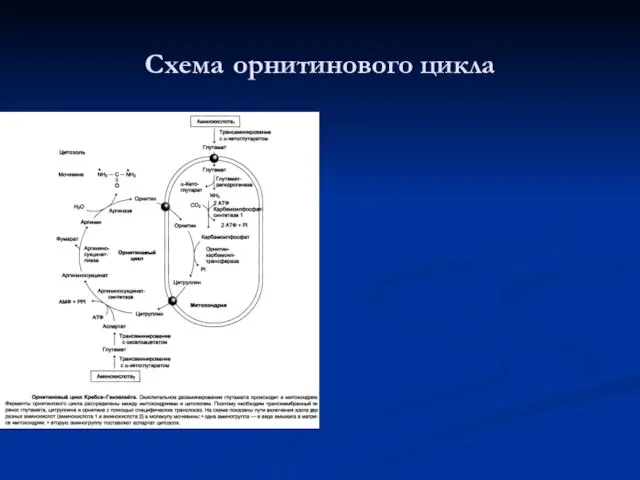
- 79. Схема орнитинового цикла
- 80. При образовании мочевины используется А) аммиак – одна молекула Б) СО2 – одна молекула В) аминогруппа
- 81. Кроме аминокислот источником аммиака в организме являются: А) биогенные амины – гистамин, серотонин и др. Б)
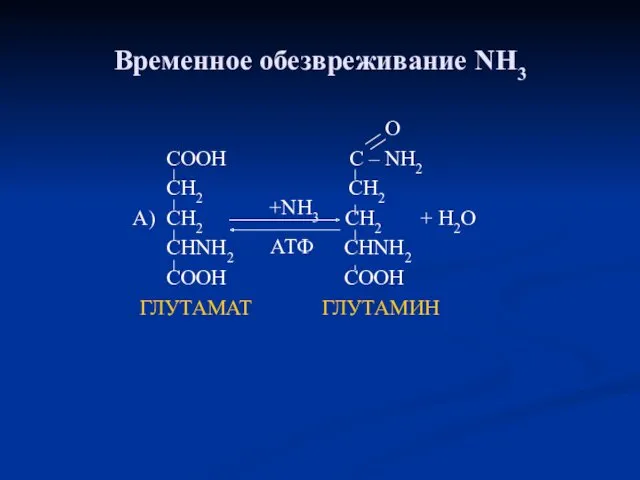
- 82. Временное обезвреживание NH3 O COOH C – NH2 CH2 CH2 A) CH2 CH2 + H2O CHNH2
- 83. Превращение белков в толстом кишечнике БЕЛКИ АМИНОКИСЛОТЫ гнилостные бактерии ЯДОВИТЫЕ ВЕЩЕСТВА аммиак, сероводород, путресцин, кадаверин, фенол,
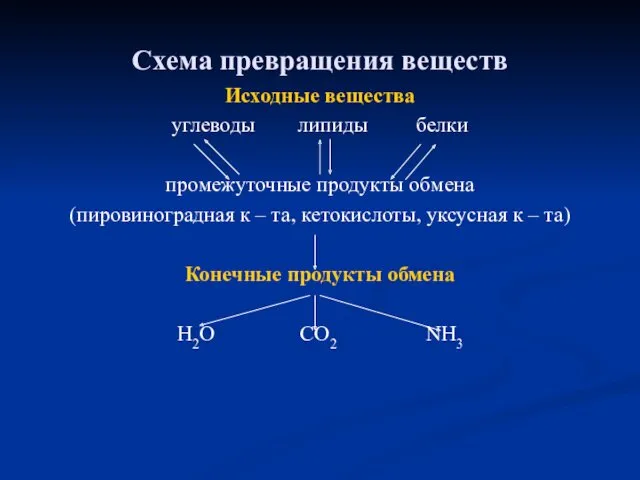
- 84. Схема превращения веществ Исходные вещества углеводы липиды белки промежуточные продукты обмена (пировиноградная к – та, кетокислоты,
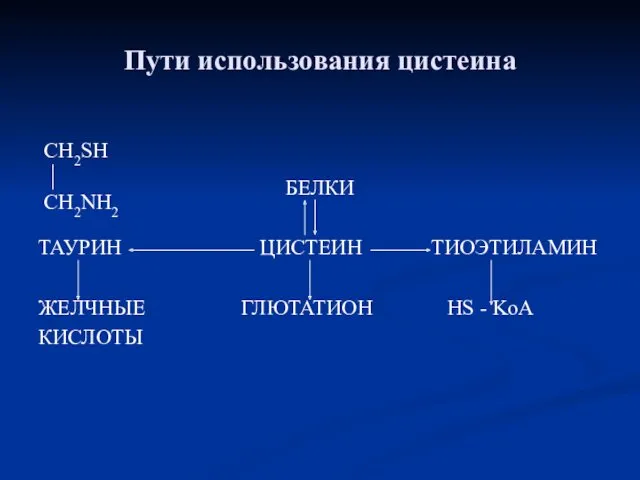
- 85. Пути использования цистеина БЕЛКИ ТАУРИН ЦИСТЕИН ТИОЭТИЛАМИН ЖЕЛЧНЫЕ ГЛЮТАТИОН HS - KoA КИСЛОТЫ CH2SH CH2NH2
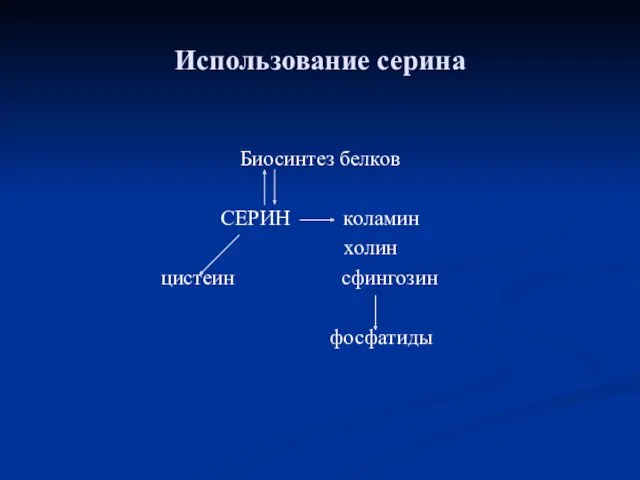
- 86. Использование серина Биосинтез белков СЕРИН коламин холин цистеин сфингозин фосфатиды
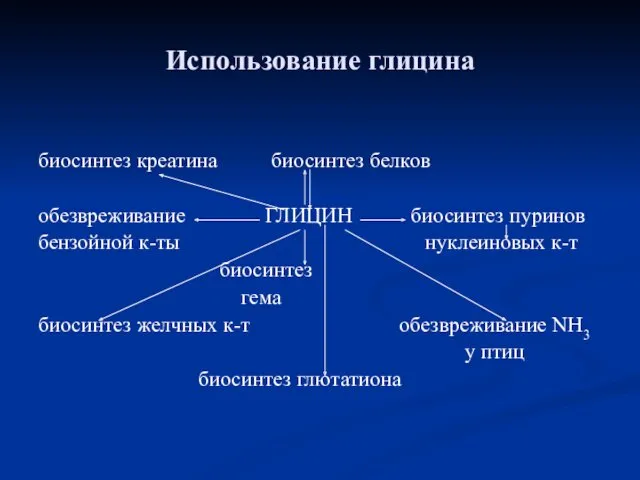
- 87. Использование глицина биосинтез креатина биосинтез белков обезвреживание ГЛИЦИН биосинтез пуринов бензойной к-ты нуклеиновых к-т биосинтез гема
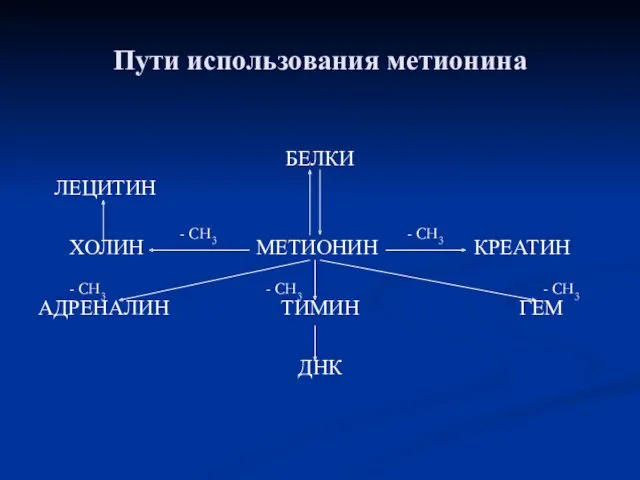
- 88. Пути использования метионина БЕЛКИ ЛЕЦИТИН ХОЛИН МЕТИОНИН КРЕАТИН АДРЕНАЛИН ТИМИН ГЕМ ДНК - СН3 - СН3
- 90. Скачать презентацию
































































 Монтаж многоэтажных каркасных зданий
Монтаж многоэтажных каркасных зданий Южная Африка
Южная Африка Тағам микрофлорасы
Тағам микрофлорасы Состав слова. Суффикс
Состав слова. Суффикс Петрушка
Петрушка Проект Цифровая образовательно-проектная среда рынка maринет. Направление ДК: Развитие человеческого капитала
Проект Цифровая образовательно-проектная среда рынка maринет. Направление ДК: Развитие человеческого капитала План-конспект непосредственно образовательной деятельности в подготовительной группе
План-конспект непосредственно образовательной деятельности в подготовительной группе Персонал предприятия как объект управления
Персонал предприятия как объект управления Технология обработки наружных фасонных поверхностей деталей из древесины
Технология обработки наружных фасонных поверхностей деталей из древесины Проблемы электроснабжения крупных городов и мегаполисов. Электроснабжение городов
Проблемы электроснабжения крупных городов и мегаполисов. Электроснабжение городов Презентация педагогического проекта Волшебный мир красок
Презентация педагогического проекта Волшебный мир красок Оконный блок
Оконный блок Уголовное право Нового времени
Уголовное право Нового времени Упражнения для закрепления правильного употребления в речи предлогов.
Упражнения для закрепления правильного употребления в речи предлогов. Конкуренция на отраслевых рынках
Конкуренция на отраслевых рынках Петр Первый
Петр Первый Система зарядки АКБ
Система зарядки АКБ Современная компьютерная техника
Современная компьютерная техника Иммунопатологиялық үрдістер
Иммунопатологиялық үрдістер герои советского союза -солдаты победы.герои советского союза города тулуна
герои советского союза -солдаты победы.герои советского союза города тулуна Построение чертежей воротников женской одежды
Построение чертежей воротников женской одежды Презентация к уроку Высотная поясность
Презентация к уроку Высотная поясность История развития прокуратуры земли Калужской
История развития прокуратуры земли Калужской Презентация к уроку РиКО в 5 классе Точность речи.
Презентация к уроку РиКО в 5 классе Точность речи. Исковое требование. Компенсация морального вреда. Пример
Исковое требование. Компенсация морального вреда. Пример Традиции празднования Нового Года
Традиции празднования Нового Года презентация Здоровьесбережение в воспитательном процессе
презентация Здоровьесбережение в воспитательном процессе Четыре замечательные точки треугольника
Четыре замечательные точки треугольника