Содержание
- 2. ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО МАТЕРИАЛА Выполним задание « Найди родственников» Из перечня формул составьте генетический ряд.(вопросы…) Ca(OH)2, CI2,
- 3. Общий вывод: Признаки которые характеризуют генетический ряд: Вещества разных классов; Разные вещества образованные одним химическим элементом,
- 4. Вспомним … 1.Валентность. 2.Степень окисления. 3.Восстановитель. 4.Окислитель. 5.Типы химических реакций.
- 5. Окислительно –восстановительные Реакции Выполнила: Бригаденко Надежда Александровна - учитель химии.
- 6. Цель урока: 1.Сформировать понятие об окислительно-восстановительных реакциях. 2.Научиться уравнивать записи ОВР методом электронного баланса.
- 7. Пример: 2Cu0 + O2 =2 Cu2+O2- 2H+CL- + Zn0 = Zn2+CL2- + H20 Реакции, в резултате
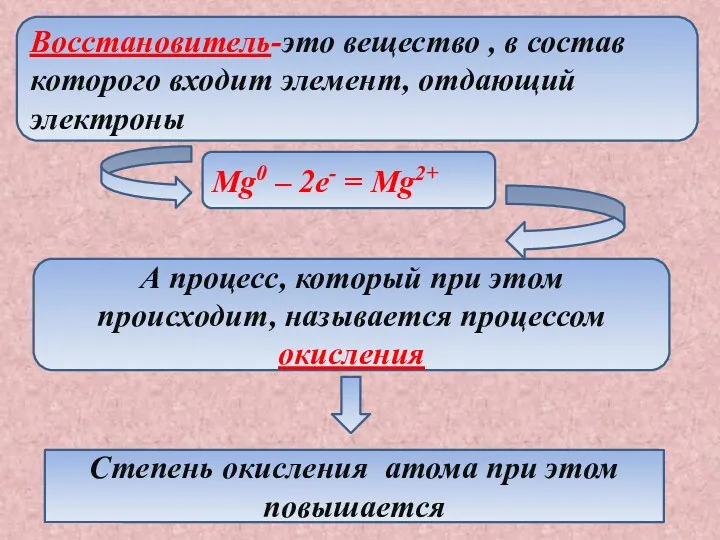
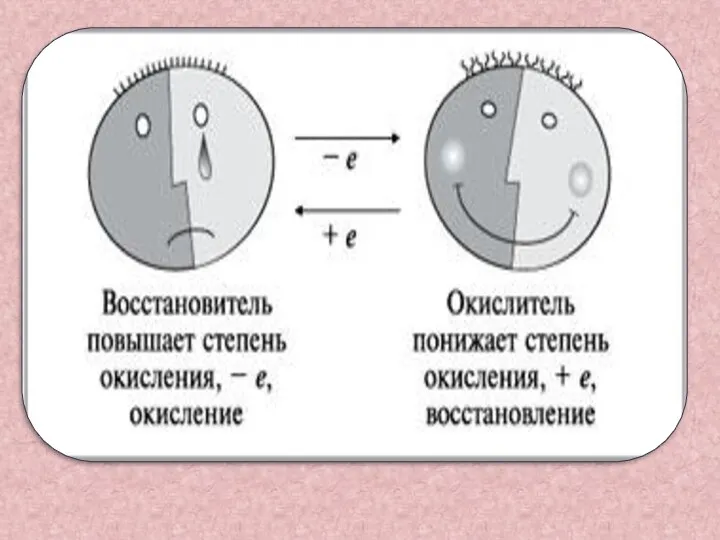
- 8. Восстановитель-это вещество , в состав которого входит элемент, отдающий электроны Mg0 – 2e- = Mg2+ А
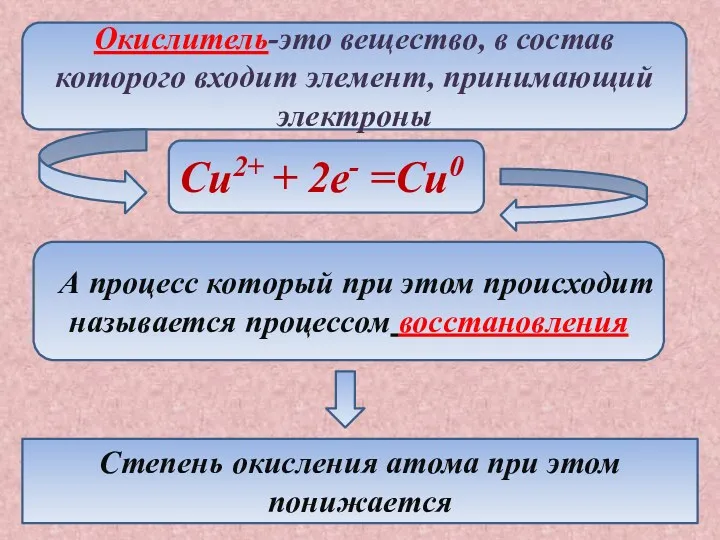
- 9. Окислитель-это вещество, в состав которого входит элемент, принимающий электроны Cu2+ + 2e- =Cu0 А процесс который
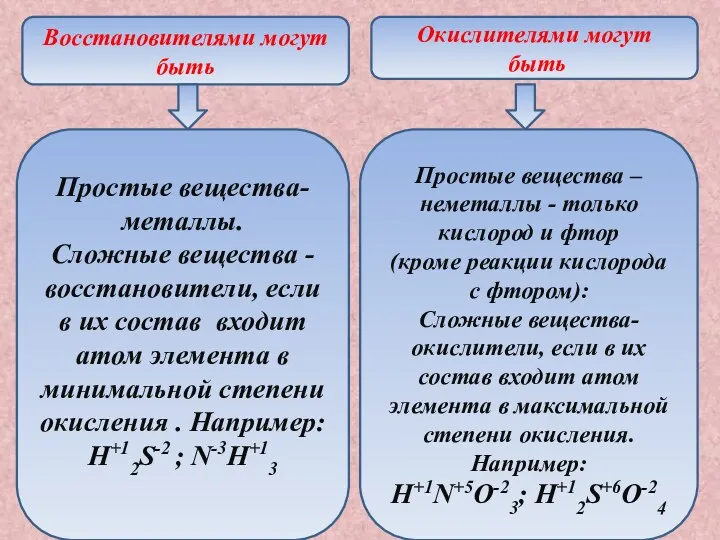
- 11. Восстановителями могут быть Окислителями могут быть Простые вещества-металлы. Сложные вещества - восстановители, если в их состав
- 12. Различают: минимальную (низшую) степень окисления S-2 2e- 8e- 8e- промежуточную степень окисления S0 2e- 8e- 6e-
- 13. Закрепление… Итог….
- 14. Д/З п.43 до стр.232 Стр.235№1,3.
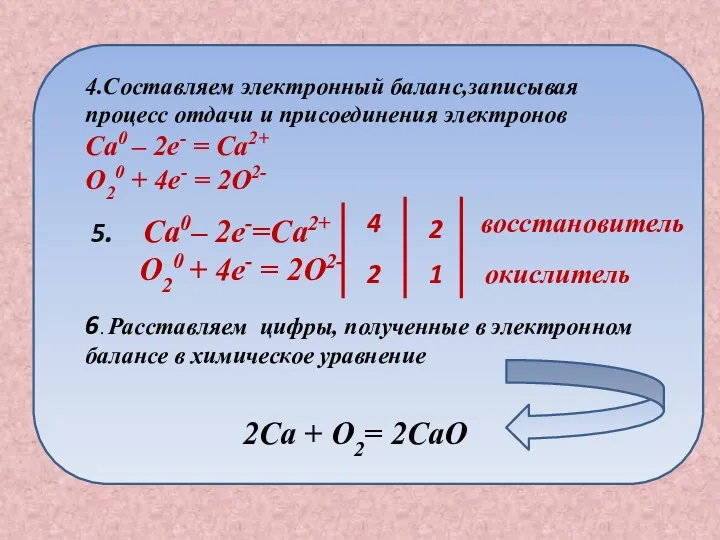
- 15. План составления окислительно -восстановительной реакции Записываем схему химической реакции Ca + O2 2. Расставляем степени окисления
- 16. 5. Ca0– 2e-=Ca2+ O20 + 4e- = 2O2- 4 2 2 1 восстановитель окислитель 6. Расставляем
- 17. Используя метод электронного баланса, допишите схемы и составьте уравнения, расставив коэффициенты Mg + O2 HCL +
- 19. Скачать презентацию











 Разработка занятия по внеурочной деятельности Станем волшебниками в 3 классе Волшебная глина дымковской игрушки
Разработка занятия по внеурочной деятельности Станем волшебниками в 3 классе Волшебная глина дымковской игрушки Административный процесс
Административный процесс Эксплуатация нефтяных скважин погружными центробежными электронасосами. Общая схема установки, ее элементы и их назначение
Эксплуатация нефтяных скважин погружными центробежными электронасосами. Общая схема установки, ее элементы и их назначение Острый живот
Острый живот Детство опаленное войной
Детство опаленное войной Эко-мебель
Эко-мебель Сюжеты Ветхого и Нового завета в искусстве
Сюжеты Ветхого и Нового завета в искусстве Атмосферное давление
Атмосферное давление : Вежливость.
: Вежливость. первый узкофюзеляжный гражданский самолёт SSJ100
первый узкофюзеляжный гражданский самолёт SSJ100 Программа развития медицинской реабилитации в России как система мероприятий по снижению смертности и инвалидизации
Программа развития медицинской реабилитации в России как система мероприятий по снижению смертности и инвалидизации World Wide Web – всемирная паутина
World Wide Web – всемирная паутина Методическая разработка урока.
Методическая разработка урока. Пори року
Пори року Активные и пассивные дома
Активные и пассивные дома Система двох рівнянь як математична модель прикладної задачі. 9 клас . Алгебра
Система двох рівнянь як математична модель прикладної задачі. 9 клас . Алгебра Овощи
Овощи Внеклассное мероприятие по технологии
Внеклассное мероприятие по технологии Приймання та відправлення поїздів. Обов’язки ДСП
Приймання та відправлення поїздів. Обов’язки ДСП Әлеуметтік медициналық көмектер
Әлеуметтік медициналық көмектер Первая медицинская помощь при обморожении и переохлаждении
Первая медицинская помощь при обморожении и переохлаждении Общение родителей и детей как условие успеха воспитания
Общение родителей и детей как условие успеха воспитания Викторина к празднику 8 марта
Викторина к празднику 8 марта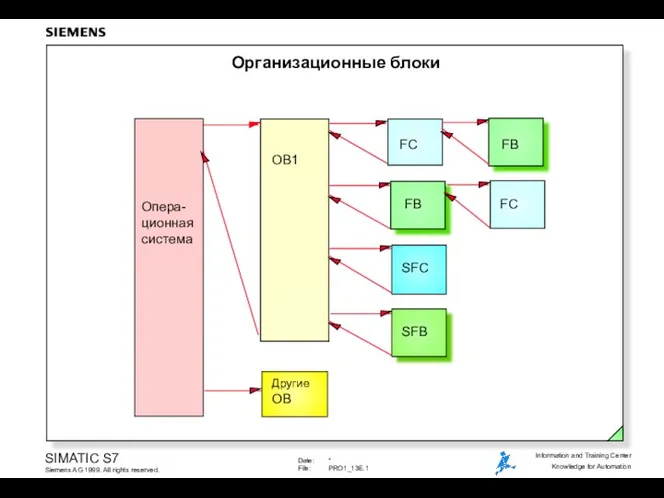 Организационные блоки
Организационные блоки Пазлы в инфографике
Пазлы в инфографике Compartiendo Aplicaciones Application Sharing
Compartiendo Aplicaciones Application Sharing Калфаклы сандугач
Калфаклы сандугач Доказательства и результаты эволюции
Доказательства и результаты эволюции