Содержание
- 2. Тепловая энергия – форма энергии, связанная с движением атомов, молекул или других частиц, из которых состоит
- 3. Механическая энергия может переходить в тепловую энергию и обратно. Превращение механической энергии в тепловую и обратно
- 4. Термодинамика Термодинамика – раздел физики, изучающий соотношения и превращения теплоты и других форм энергии. Термодинамика изучает:
- 5. Термодинамика — наука, изучающая взаимные превращения различных видов энергии, связанные с переходом энергии в форме теплоты
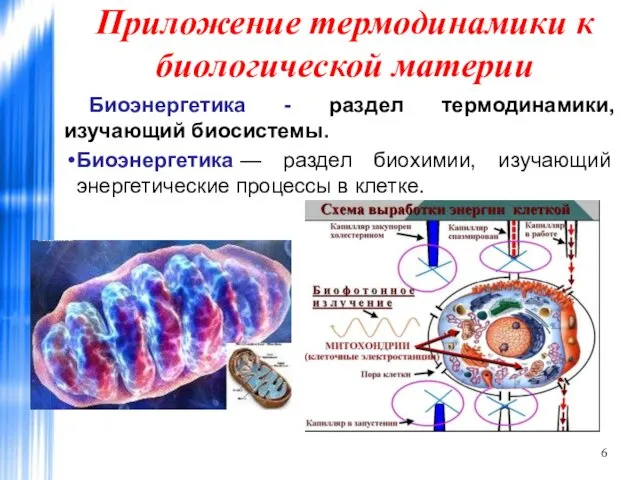
- 6. Приложение термодинамики к биологической материи Биоэнергетика - раздел термодинамики, изучающий биосистемы. Биоэнергетика — раздел биохимии, изучающий
- 7. Термохимия Термохимия - это раздел химии, изучающий тепловые эффекты химических процессов. Изобарные процессы – проходят при
- 8. ТЕРМИНЫ И ПОНЯТИЯ Система — это совокупность материальных объектов, отделённых от окружающей среды. Окружающая среда —
- 9. Термодинамическими параметры : экстенсивные и интенсивные. Если система изменяет свои параметры, то в ней происходит термодинамический
- 10. Нулевой закон термодинамики Если каждая из двух термодинамических систем находится в тепловом равновесии с некоторой третьей,
- 11. 1-й закон термодинамики 1-й закон термодинамики – это закон сохранения энергии. Впервые он был сформулирован Ломоносовым
- 12. 1-й закон термодинамики II. Невозможно создать перпетум-мобиле, или двигатель первого рода, т.е. осуществлять работу, не затрачивая
- 13. III. Теплота, подведенная к системе (или выделенная ею) расходуется на изменения внутренней энергии системы и совершение
- 14. IV. Увеличение внутренней энергии системы равно теплоте, которую система получает извне, за исключением работы, которую совершила
- 15. А= р ∆ V Для изохорного процесса: A=0 и Qv=U2- U1 = ∆U Для изобарного: Qp
- 16. Природа теплового эффекта химических реакций. Термохимические уравнения. Тепловой эффект химической реакции - это количество теплоты, которая
- 17. Энтальпией сгорания называется тепловой эффект реакции взаимодействия 1 моля вещества с кислородом с образованием высших устойчивых
- 18. Закон Гесса В 1840 г. Н. Г. Гесс сформулировал закон постоянства суммы тепла: Тепловой эффект реакции
- 19. Закон Гесса Тепловые эффекты реакций в термохимии рассчитывают, используя следствия из закона Гесса. I-е следствие: тепловой
- 20. Закон Гесса II-е - следствие: тепловой эффект реакции равен разности между суммой теплот сгорания исходных веществ
- 21. Закон Гесса III - следствие: Тепловой эффект прямой реакции равен тепловому эффекту обратной реакции с противоположным
- 22. Исследование термохимических расчетов для энергетической характеристики биохимических процессов В приложении к живому организму закон сохранения энергии
- 23. Предполагается, что теплозатрата организма человека при условии умеренного климата в среднем равна 7100 кДж в сутки.
- 24. Энергию дают, в основном, жиры, белки, углеводы: 39 кДж/г, 18 кДж/г, 22 кДж/г соответственно. Несмотря на
- 25. 2-й закон термодинамики 1) теплота не может сама собой переходить от холодного тепла к горячему, не
- 26. 2-й закон термодинамики Все реальные самопроизвольные процессы – необратимые. Обратим только идеальный процесс. В реальных необратимых
- 27. «Жизнь – это борьба с энтропией». А. Шредингер Энтропия связана с термодинамической вероятностью реализации данного состояния
- 28. 2-й закон термодинамики Чем больше неупорядоченность системы тем больше ее энтропия. Самопроизвольно идущие процессы идут с
- 29. В изолированных системах при обратимых процессах S = const, ∆S = 0; Энтропия связана с тепловой
- 30. называется приведенной теплотой, - связанной энергией. Абсолютное значение энтропии можно вычислить, исходя из постулата Планка, являющегося
- 31. 2-й закон термодинамики Следствие второго закона термодинамики: суммарное изменение энтропии, необходимое для формирования живого организма и
- 32. 2-й закон термодинамики - характера связи Sков. >Sмет. - чем сложнее химический состав, тем больше S.
- 33. Изобарно- изотермический потенциал или энергия Гиббса. На ход химической реакции могут влиять два фактора: энтальпийный ∆Н
- 34. F – энергия Гельмгольца (изохорно - изотермический потенциал) ΔF°=∆U°-T∆S°
- 35. Применение законов термодинамики к живым системам Теплота, выделяющаяся из организма, равна теплоте, найденной путём подсчёта по
- 36. 1-й закон термодинамики
- 38. Скачать презентацию

































 De compras — покупки
De compras — покупки Презентация по МХК Жилища древних людей
Презентация по МХК Жилища древних людей История освоения Арктики
История освоения Арктики Презентации к праздникам.
Презентации к праздникам. Алгебра высказываний. Логические операции
Алгебра высказываний. Логические операции Вера
Вера Палеонтология. Схема соподчиненности основных систематических единиц. Царство животные простейшие (одноклеточные)
Палеонтология. Схема соподчиненности основных систематических единиц. Царство животные простейшие (одноклеточные) Презентация Готовность ребенка к школе
Презентация Готовность ребенка к школе 20231012_stat_futbolistom
20231012_stat_futbolistom Планирование работы в отделении организации медицинской помощи детям и подросткам в образовательных учреждениях
Планирование работы в отделении организации медицинской помощи детям и подросткам в образовательных учреждениях Типовые узлы комбинационного типа
Типовые узлы комбинационного типа Презентация к конспекту интегрированного занятия КОСМИЧЕСКОЕ ПУТЕШЕСТВИЕ
Презентация к конспекту интегрированного занятия КОСМИЧЕСКОЕ ПУТЕШЕСТВИЕ Правила оформления презентаций
Правила оформления презентаций Конспект бинарного урока Открытое письмо ветеранам
Конспект бинарного урока Открытое письмо ветеранам Промывочные агрегаты
Промывочные агрегаты Нормативно-правовые акты, гарантирующие право получения детям с ограниченными возможностями здоровья адекватного их возможностям образования
Нормативно-правовые акты, гарантирующие право получения детям с ограниченными возможностями здоровья адекватного их возможностям образования Требования безопасности при эксплуатации теплового оборудования на кухне
Требования безопасности при эксплуатации теплового оборудования на кухне Древнееврейское царство
Древнееврейское царство Презентация к уроку географии Иркутской области в 8 классе по теме Почвы
Презентация к уроку географии Иркутской области в 8 классе по теме Почвы органическая химия(Жиры)
органическая химия(Жиры) ПрезентацияОткуда в снежинках берётся грязь?
ПрезентацияОткуда в снежинках берётся грязь? Зинаида Гиппиус
Зинаида Гиппиус Назначение, боевые характеристики и устройство ручных осколочных и противотанковых гранат
Назначение, боевые характеристики и устройство ручных осколочных и противотанковых гранат кл Греческая культураl
кл Греческая культураl Акция Птицы Кубани. Операция День птиц
Акция Птицы Кубани. Операция День птиц Reasons to learning English
Reasons to learning English Презентация Визитная карточка воспитателя Храмовой Елены Витальевны
Презентация Визитная карточка воспитателя Храмовой Елены Витальевны Онлайн курс. Магия денег
Онлайн курс. Магия денег