Содержание
- 2. 1)познакомить учащихся с понятием аморфные и кристаллические решетки; 2)дать понятие о типах кристаллических решеток 3)рассмотреть свойства
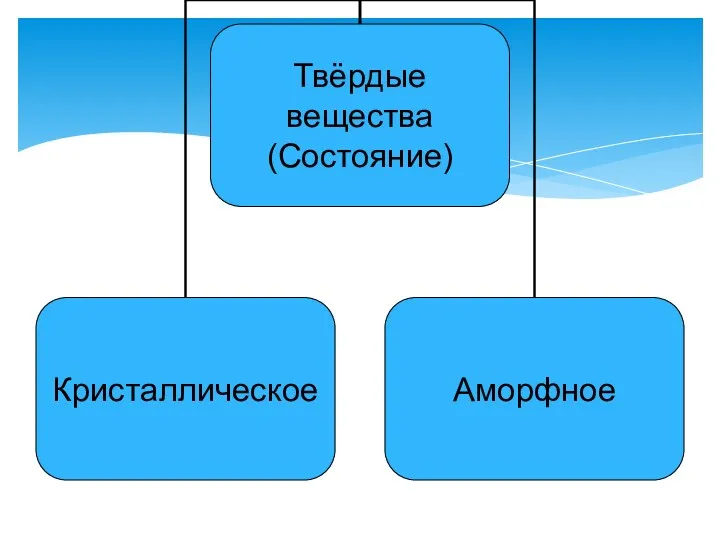
- 4. Кристаллическое состояние характеризуется упорядоченной структурой. Упорядоченность в кристаллах обусловливается правильным геометрическим расположением частиц, из которых состоит
- 5. Например, кристаллы поваренной соли имеют форму куба, калийной селитры - форму призмы, алюминиевых квасцов - форму
- 6. Некоторые вещества могут находиться и в кристаллическом, и в аморфном состояниях, - например сера, оксид кремния
- 7. Аморфные вещества особенно сильно отличаются от кристаллических по своим физическим свойствам: -нет определенной температуры плавления -меняют
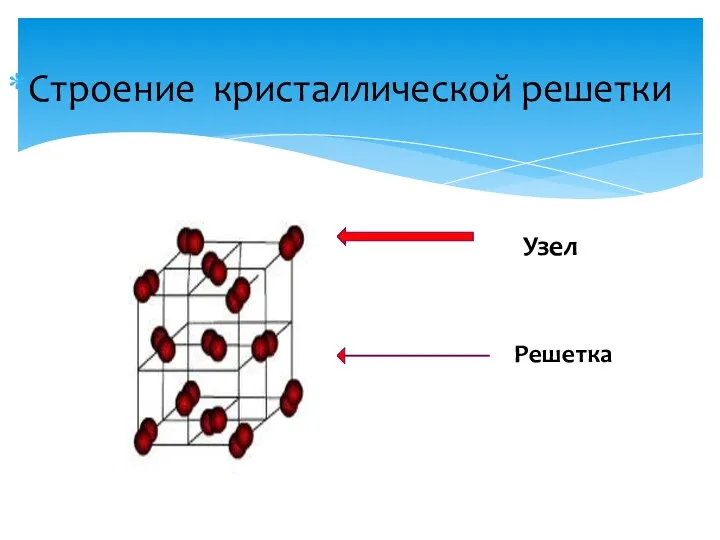
- 8. Строение кристаллической решетки Узел Решетка
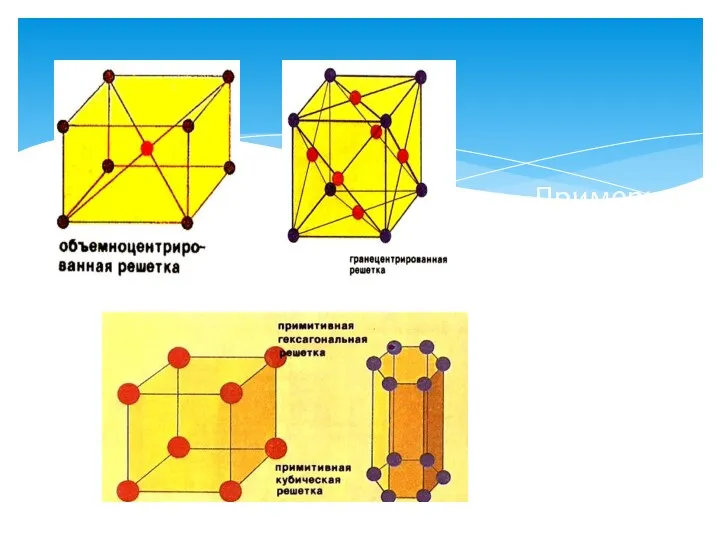
- 9. Примеры кристаллических решеток
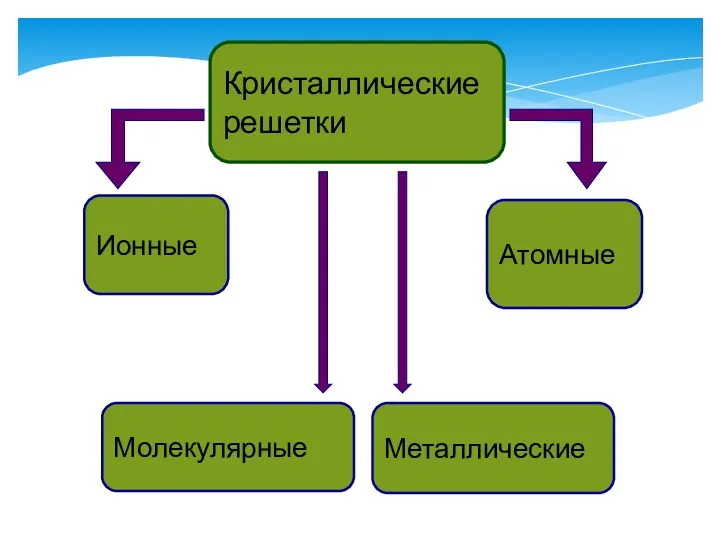
- 10. Кристаллические решетки Металлические Молекулярные Атомные Ионные
- 11. Свойства твёрдых веществ Определяются видом кристаллической решетки. Вещества с ионной кристаллической решеткой имеют высокие температуры плавления
- 12. Вещества с молекулярной кристаллической решеткой имеют низкие температуры плавления и кипения; высоко летучи и менее твердые,
- 13. Атомная решетка Вещества с атомной кристаллической решеткой тугоплавки и практически нерастворимы ни в каких жидкостях. Для
- 14. Аморфное состояние (от греч. а - отрицательная частица и morphē - форма), твёрдое состояние вещества, обладающее
- 15. Примеры аморфных веществ: стекла, смолы, воск, шоколад, янтарь В Аморфное состояние могут находиться не только вещества,
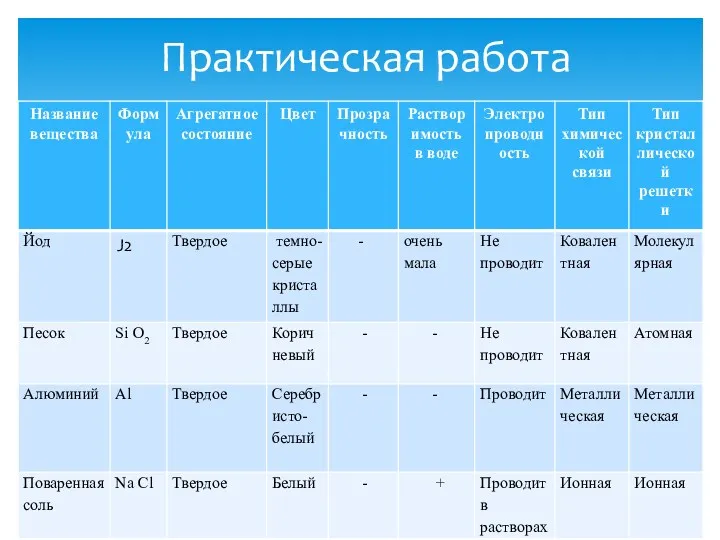
- 16. Практическая работа
- 17. Тест «Проверь себя»: 1.В узлах разных кристаллических решеток могут находиться а)атомы б)электроны в)протоны г)ионы д)молекулы 2.Выберите
- 19. Скачать презентацию











 How It Works - the global leader in innovative lifting solutions
How It Works - the global leader in innovative lifting solutions 300 лет Полтавской битве
300 лет Полтавской битве презентация Ферменты
презентация Ферменты Приключения Буратино
Приключения Буратино An intellectual contest for the 8-th formers What do you know about fashion in britain
An intellectual contest for the 8-th formers What do you know about fashion in britain Where i want to go
Where i want to go Асинхронный двигатель с частотным управлением как объект автоматического регулирования
Асинхронный двигатель с частотным управлением как объект автоматического регулирования Класифікація дестабілізуючих факторів
Класифікація дестабілізуючих факторів Поэтическая тетрадь. Проверочная работа
Поэтическая тетрадь. Проверочная работа математика
математика Моё электронное портфолио Диск Диск Диск
Моё электронное портфолио Диск Диск Диск Етика і деонтологія в професійній діяльності лікаря
Етика і деонтологія в професійній діяльності лікаря Дружба. Отличительные черты дружбы
Дружба. Отличительные черты дружбы Бизнес-стратегия: мифы и реальность
Бизнес-стратегия: мифы и реальность Готовность к школьному обучению
Готовность к школьному обучению Центр творчества студентов
Центр творчества студентов Recent Advances of High Power 1 µm Lasers
Recent Advances of High Power 1 µm Lasers Пророчий ярус у давніх українських іконостасах: Іконографія та поезія
Пророчий ярус у давніх українських іконостасах: Іконографія та поезія Жилой дом. Этапы строительства
Жилой дом. Этапы строительства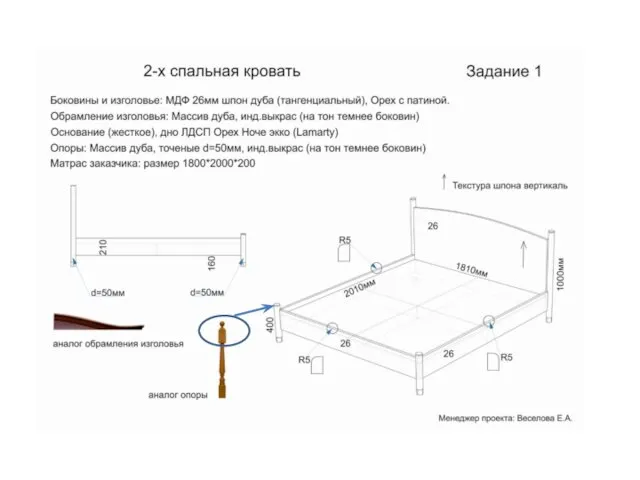 2-х спальная кровать
2-х спальная кровать ТРУД В ПРИРОДЕ В ДОУ
ТРУД В ПРИРОДЕ В ДОУ British Stereotypes
British Stereotypes Дорожный мастер
Дорожный мастер Восстание казахов Младшего жуза под предводительством Сырыма Датулы
Восстание казахов Младшего жуза под предводительством Сырыма Датулы Презентация Последняя семья Романовых
Презентация Последняя семья Романовых Ситуационный анализ рынка
Ситуационный анализ рынка Engetronics. Internet datacenter
Engetronics. Internet datacenter Біоорганічна хімія. Реакційна здатність біоорганічних сполук
Біоорганічна хімія. Реакційна здатність біоорганічних сполук