Содержание
- 2. Цели урока: Сформировать у учащихся знаний о фосфоре как о химическом элементе и простом веществе; аллотропных
- 3. Открытие фосфора Гамбургский алхимик Хеннинг Бранд 1669 год «Фосфор» - от греческого «светоносный»
- 4. период Фосфор как химический элемент группа валентных электронов степени окисления высший оксид водородное соединение
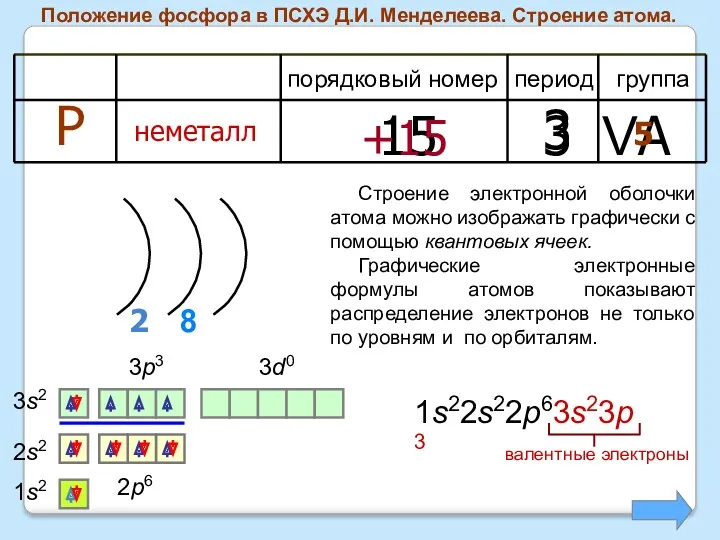
- 5. Положение фосфора в ПСХЭ Д.И. Менделеева. Строение атома. период группа порядковый номер Р неметалл 15 3
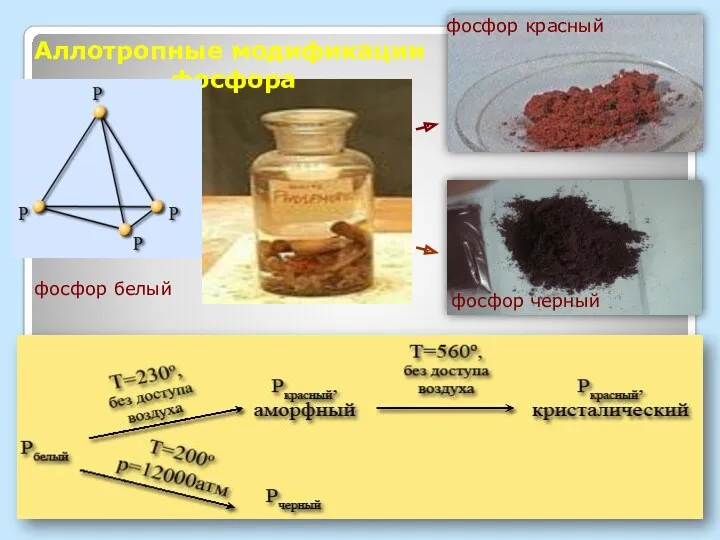
- 6. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ Р БЕЛЫЙ КРАСНЫЙ ЧЕРНЫЙ Сравните физические свойства АЛЛОТРОПНЫХ МОДИФИКАЦИЙ ФОСФОРА
- 7. Аллотропные модификации фосфора фосфор белый фосфор черный фосфор красный
- 8. Белый фосфор - твердое кристаллическое вещество, плотность его 1,82 г/см3. На воздухе самовоспламеняется, в темноте светится.
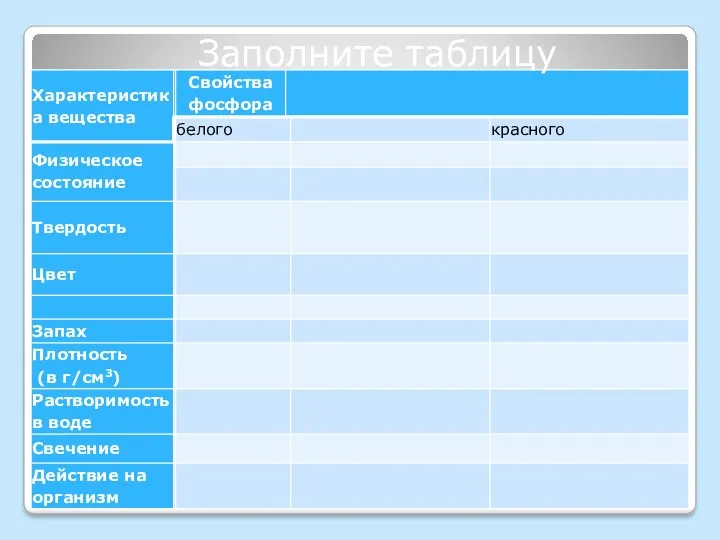
- 9. Заполните таблицу
- 10. ХИМИЧЕСКИЕ СВОЙСТВА С металлами: Ca + P = C неметаллами: P + O2 = P +
- 11. с бертолетовой солью при ударе взрывается, воспламеняется: KClO3 + P = P2O5 + KCl (уравнять!)
- 12. Физиологическое действие белого фосфора Результат применения чрезмерного количества фосфора Появление лягушек с уродствами -результат применения фосфорных
- 13. Применение фосфора 1 2 7 8 9 3 6 4 5 Белый фосфор применяется для получения
- 14. Получение фосфора нагреванием смеси фосфорита, угля и песка в электропечи: Ca3(PO4)2 + C + SiO2 →
- 16. Скачать презентацию










 Суть процесу виховання. Закономірності і принципи виховання (тема 7)
Суть процесу виховання. Закономірності і принципи виховання (тема 7) Проверка качества подгузников для взрослых
Проверка качества подгузников для взрослых Аксонометрия и песпектива. Построение трехмерных изображений
Аксонометрия и песпектива. Построение трехмерных изображений Поисковые системы. Правила поиска информации
Поисковые системы. Правила поиска информации Стихотворение М.Ю. Лермонтова Бородино - отклик на 25-летнюю годовщину Бородинского сражения
Стихотворение М.Ю. Лермонтова Бородино - отклик на 25-летнюю годовщину Бородинского сражения Использование невербальных средств в речевом общении
Использование невербальных средств в речевом общении International Trade Centre
International Trade Centre Моя семья
Моя семья Презентация КВН Я здоровье берегу - быть здоровым я хочу!
Презентация КВН Я здоровье берегу - быть здоровым я хочу! Точение конических и фасонных поверхностей. Изготовление ручки напильника. 7 класс
Точение конических и фасонных поверхностей. Изготовление ручки напильника. 7 класс Проект Источники энергии
Проект Источники энергии Как воспитать футболиста
Как воспитать футболиста Классный час по теме Моя малая Родина
Классный час по теме Моя малая Родина OSB / ОСП Ориентированно-стружечная плита
OSB / ОСП Ориентированно-стружечная плита Подвижная игра, как средство здоровьесбережения у дошкольников. Деловая игра с воспитателями ДОУ.
Подвижная игра, как средство здоровьесбережения у дошкольников. Деловая игра с воспитателями ДОУ. Профессиональный стандар -инструмент реализации стратегии образования в меняющемся мире
Профессиональный стандар -инструмент реализации стратегии образования в меняющемся мире Книги - юбиляры 2021 года
Книги - юбиляры 2021 года Храмы Санкт-Петербурга
Храмы Санкт-Петербурга Организационное заседание ШНО.
Организационное заседание ШНО. ООО Аптека Исцеление
ООО Аптека Исцеление Параллелепипед
Параллелепипед Основы строительной акустики и звукоизоляции ограждающих конструкций зданий
Основы строительной акустики и звукоизоляции ограждающих конструкций зданий Л 4 Т 4 З 1 Боевая группа
Л 4 Т 4 З 1 Боевая группа Аналоговый и цифровой звук
Аналоговый и цифровой звук По музеям
По музеям Публичное выступление
Публичное выступление УМК нового поколения по русскому языку и литературе
УМК нового поколения по русскому языку и литературе Управление талантами как фактор конкурентоспособности современных организаций
Управление талантами как фактор конкурентоспособности современных организаций