Содержание
- 2. «Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры
- 3. Железо: ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА.
- 4. Особенности строения атома железа Fe 26 2е 8е 14е 2е 1s22s22р63s23р63d64s2 возможные степени окисления: +2 и
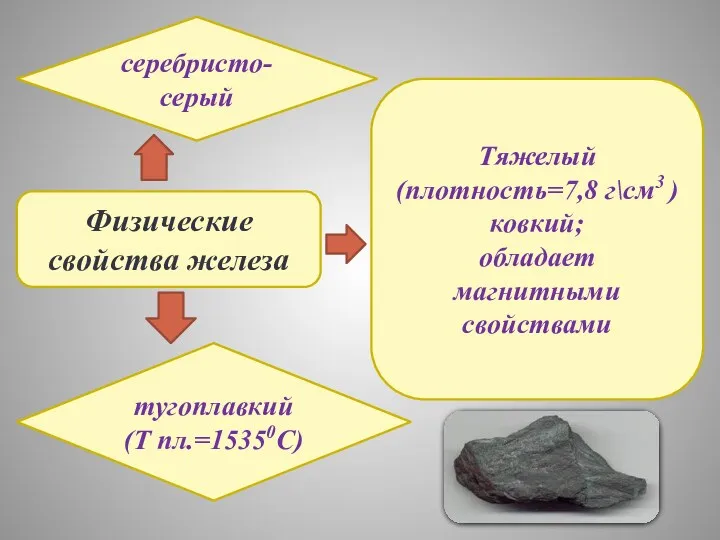
- 5. Физические свойства железа серебристо-серый тугоплавкий (Т пл.=15350C) Тяжелый (плотность=7,8 г\см3 ) ковкий; обладает магнитными свойствами
- 6. Железо сегодня Гидроэлектро- станции и опоры линий электропередач Трубопроводы для воды, нефти и газа Автомобили ,
- 7. Железо как материал искусства
- 8. Железо как материал искусства
- 9. Железо как материал искусства
- 11. Железо Химически чистое (0,01% примесей) Технически чистое (0,02-0,04% примесей)
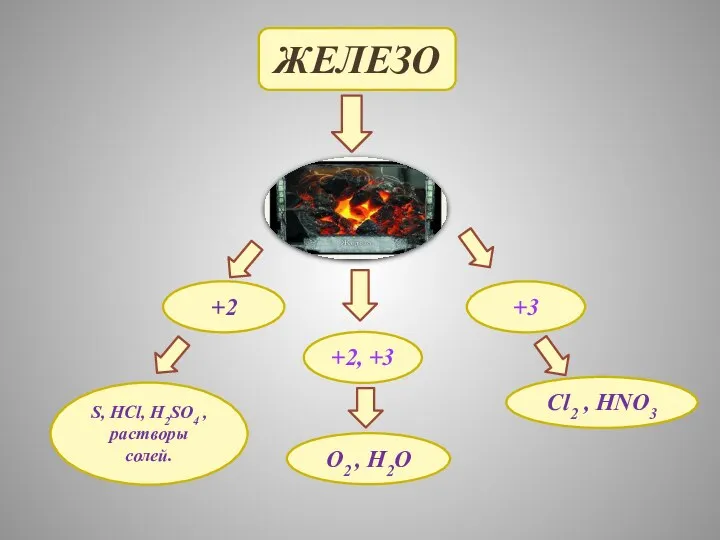
- 12. Железо +2 +3 S, HCl, H2SO4 , растворы солей. O2 , H2O +2, +3 Cl2 ,
- 13. Химические свойства Реакции с простыми веществами Железо сгорает в чистом кислороде при нагревании:3Fe +2O2=Fe3O4 Реагирует с
- 14. Химические свойства Реакции со сложными веществами С кислотами: А) с соляной кислотой 2HCl + Fe =
- 15. Железо разрушается под действием окружающей среды, т.е. подвергается коррозии – «ржавлению». При этом на поверхности образуется
- 17. Железо в организме Железо в виде ионов присутствует в организмах всех животных и, конечно же, человека.
- 18. Основная роль железа в организме – участие в «рождении» красных (эритроцитов) и белых (лимфоцитов) кровяных клеток.
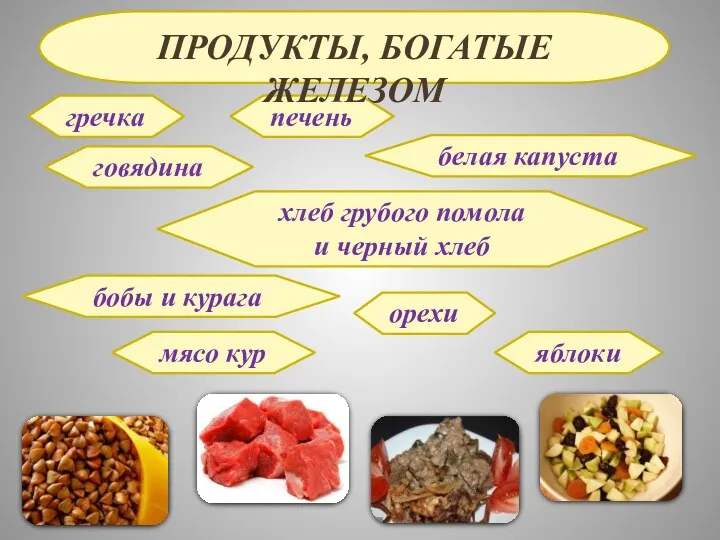
- 19. гречка говядина печень белая капуста хлеб грубого помола и черный хлеб бобы и курага орехи мясо
- 21. Скачать презентацию














 Действия с дробями
Действия с дробями Югорский автомобильный вантовый мост
Югорский автомобильный вантовый мост Электронная презентация к интегрированному занятию В гостях у сказки Диск
Электронная презентация к интегрированному занятию В гостях у сказки Диск К выпускному вечеру в 4 классе
К выпускному вечеру в 4 классе Памятники природы Новосибирской области
Памятники природы Новосибирской области Диагностика и лечение тиреотоксикоза с диффузным зобом
Диагностика и лечение тиреотоксикоза с диффузным зобом Знаменитые иконописцы
Знаменитые иконописцы Санитарно - защитные зоны предприятий
Санитарно - защитные зоны предприятий Образотворче мистецтво XIV-XVІ століття
Образотворче мистецтво XIV-XVІ століття Классный час Славная осень
Классный час Славная осень № 90. Я и мои друзья
№ 90. Я и мои друзья Портфолио ученика(образец)
Портфолио ученика(образец) Региональная экономика. Природно-ресурсный потенциал
Региональная экономика. Природно-ресурсный потенциал Система координат
Система координат Подготовка к ГИА (С1)
Подготовка к ГИА (С1) Технология выполнения то и ремонт переднего ведущего моста трактора МТЗ-80
Технология выполнения то и ремонт переднего ведущего моста трактора МТЗ-80 Благоустройство повседневности монопрофильного муниципального образования Город Кирово-Чепецк Кировской области
Благоустройство повседневности монопрофильного муниципального образования Город Кирово-Чепецк Кировской области Принятие решений в условиях определенности
Принятие решений в условиях определенности Техническое регулирование в Российской Федерации
Техническое регулирование в Российской Федерации семинары
семинары Другие методы расчета коэффициента активности
Другие методы расчета коэффициента активности Аналық жыныс жүйесі мүшелерінің гистологиясы
Аналық жыныс жүйесі мүшелерінің гистологиясы USairB. Новітня технологія, яка змінить все і навіть більше
USairB. Новітня технологія, яка змінить все і навіть більше Закономерности размещения промышленности: основные тенденции
Закономерности размещения промышленности: основные тенденции Обобщение по теме: Гидросфера
Обобщение по теме: Гидросфера алгоритм одевания и раздевания
алгоритм одевания и раздевания Шахматные фигуры. Начальная позиция.
Шахматные фигуры. Начальная позиция. Забытые азы кораблестроения. О чем не говорят, чему не учат в школе. Сахалинский госуниверситет
Забытые азы кораблестроения. О чем не говорят, чему не учат в школе. Сахалинский госуниверситет