Содержание
- 2. СТРУКТУРА УЧЕБНОГО СОДЕРЖАНИЯ Клиническая фармакология антимикробных лекарственных средств (ЛС) Классификация и фармакодинамика основных групп антимикробных препаратов
- 3. КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ АНТИМИКРОБНЫХ ЛС
- 4. Основные положения Антимикробные препараты – это лекарственные средства (ЛС), действие которых избирательно направлено на подавление жизнедеятельности
- 5. Основные положения Тип действия антимикробных ЛС бывает: цидным (бактерицидным, фунгицидным, вирицидным или протозоацидным), под которым понимается
- 6. Основные положения Все антимикробные ЛС объединяет ряд уникальных качеств: Мишень (рецептор) ЛС находится не в тканях
- 7. Основные механизмы резистентности к антимикробным ЛС Изменение мишени действия Ферментативную инактивацию ЛС Активное выведение ЛС из
- 8. КЛАССИФИКАЦИЯ И ФАРМАКОДИНАМИКА ОСНОВНЫХ ГРУПП АНТИМИКРОБНЫХ ПРЕПАРАТОВ
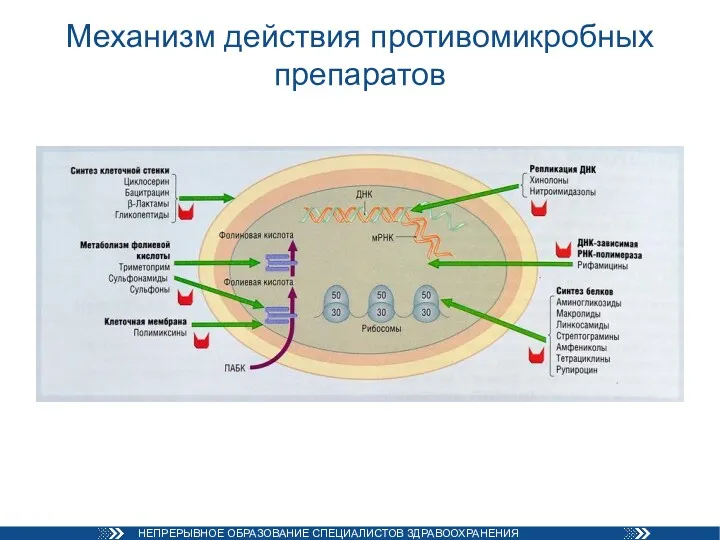
- 9. Механизм действия противомикробных препаратов
- 10. Классификация антимикробных препаратов по механизму действия β-лактамы – ингибируют поперечную сшивку пептидогликана: Пенициллины Цефалоспорины Карбапенемы Монобактамы
- 11. Классификация антимикробных препаратов
- 12. Ингибиторы синтеза клеточной стенки
- 13. Пенициллины
- 14. Цефалоспорины
- 15. Карбапенемы и монобактамы
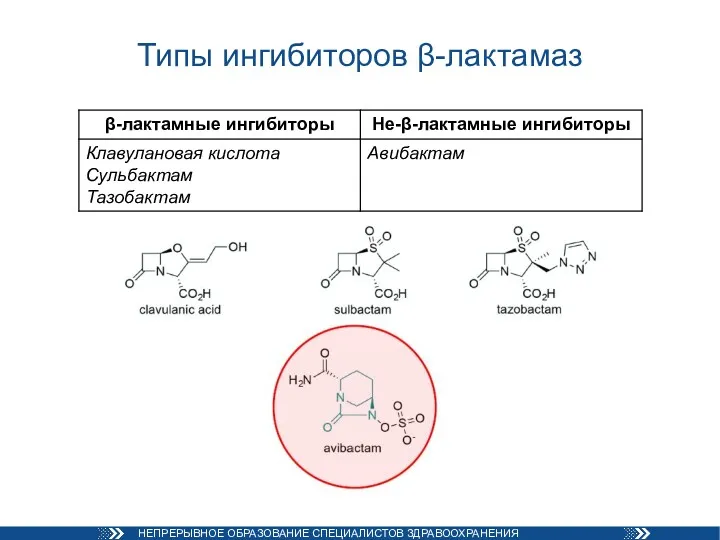
- 16. Типы ингибиторов β-лактамаз
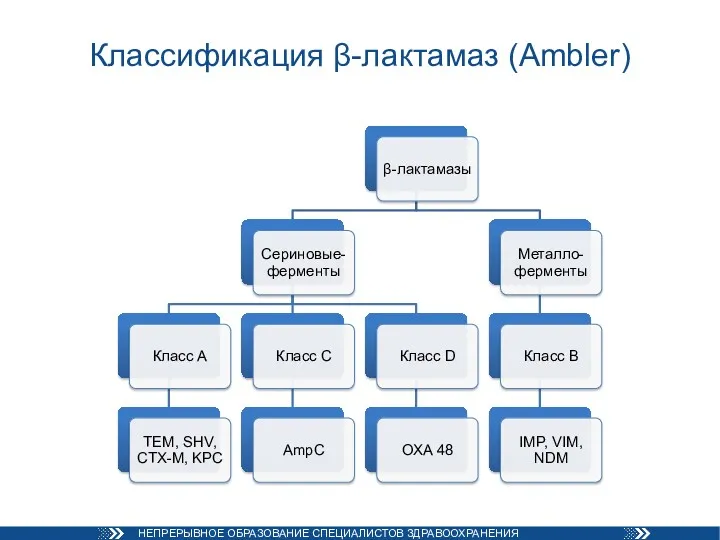
- 17. Классификация β-лактамаз (Ambler)
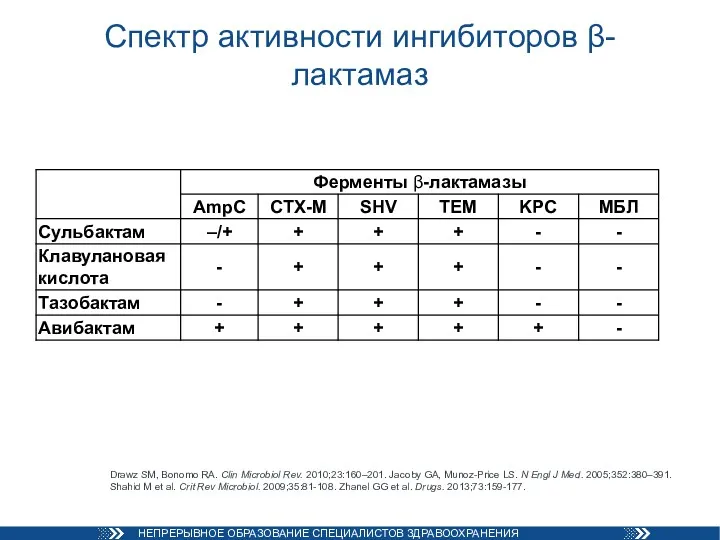
- 18. Спектр активности ингибиторов β-лактамаз Drawz SM, Bonomo RA. Clin Microbiol Rev. 2010;23:160–201. Jacoby GA, Munoz-Price LS.
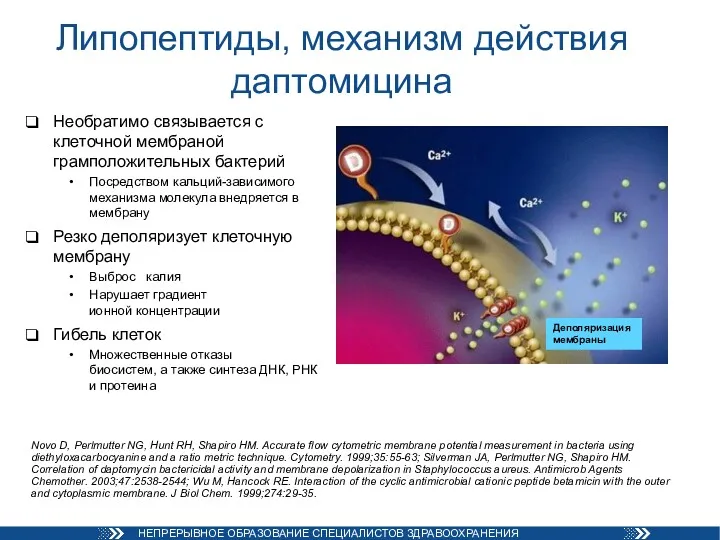
- 19. Липопептиды, механизм действия даптомицина Необратимо связывается с клеточной мембраной грамположительных бактерий Посредством кальций-зависимого механизма молекула внедряется
- 20. Ингибиторы синтеза нуклеиновых кислот
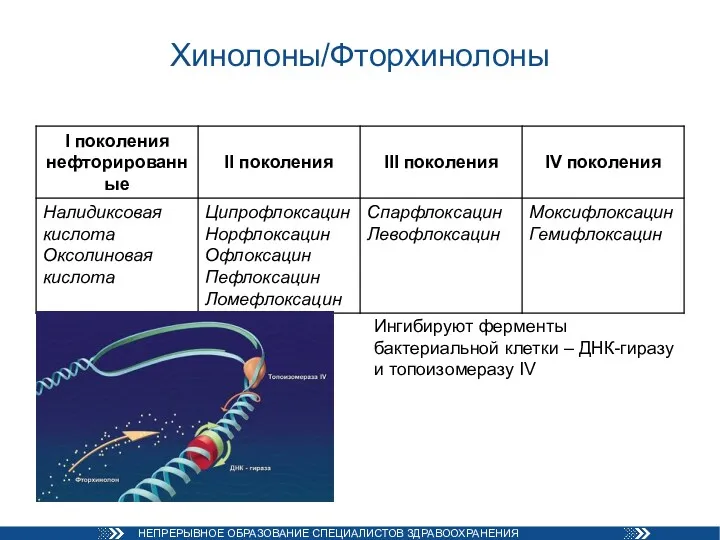
- 21. Хинолоны/Фторхинолоны Ингибируют ферменты бактериальной клетки – ДНК-гиразу и топоизомеразу IV
- 22. Ингибиторы синтеза белка
- 23. Аминогликозиды Присоединяются к 30S субъединице рибосом, повышают вероятность включения ошибочных аминокислот в растущую полипептидную цепь. Это
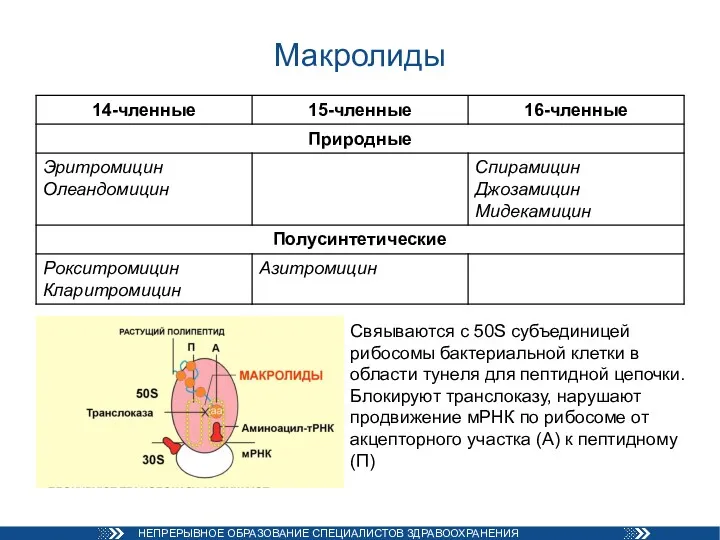
- 24. Макролиды Свяываются с 50S субъединицей рибосомы бактериальной клетки в области тунеля для пептидной цепочки. Блокируют транслоказу,
- 25. Противогрибковые препараты
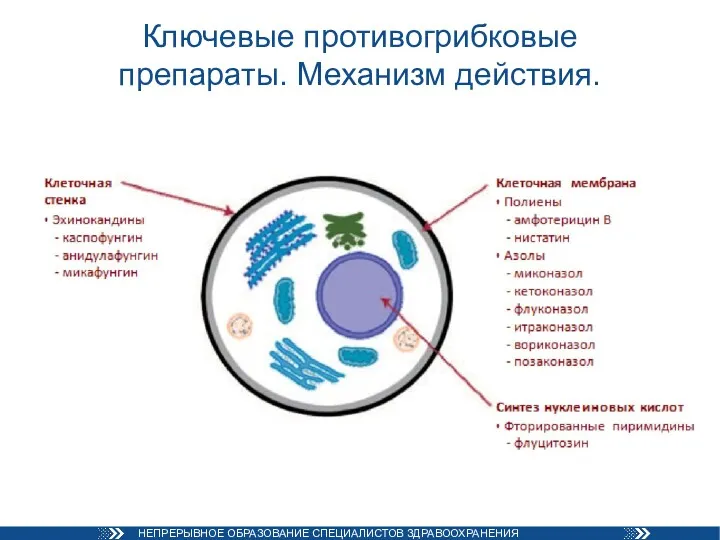
- 26. Ключевые противогрибковые препараты Полиены (нарушают целостность клеточной мембраны): Амфотерицин В Липосомальные формы Амфотерицина В Триазолы (нарушают
- 27. Ключевые противогрибковые препараты. Механизм действия.
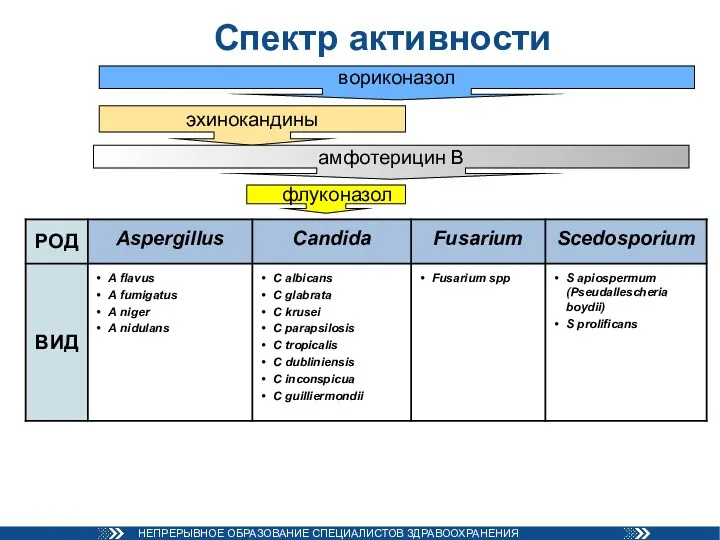
- 28. Спектр активности эхинокандины вориконазол флуконазол амфотерицин В
- 29. ФАРМАКОКИНЕТИКА ОСНОВНЫХ ГРУПП АНТИМИКРОБНЫХ ПРЕПАРАТОВ
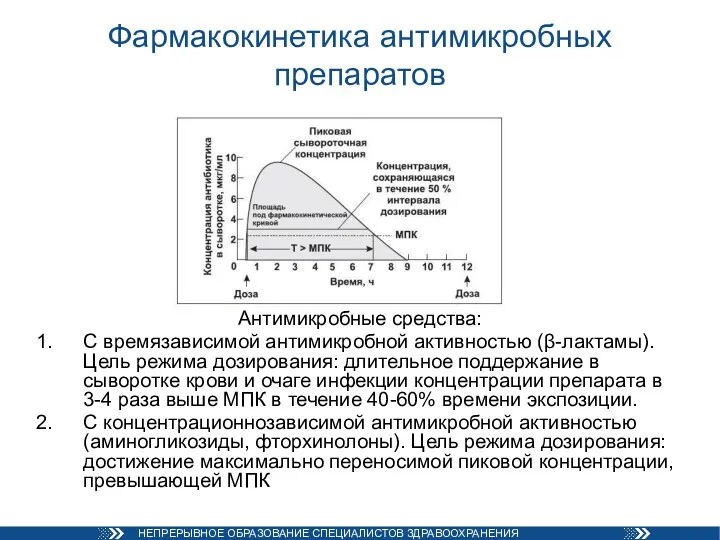
- 30. Фармакокинетика антимикробных препаратов Основные фармакокинетические термины: МПК (минимальная подавляющая концентрация) – минимальные концентрации антибиотика (мкг/мл или
- 31. Фармакокинетика антимикробных препаратов Антимикробные средства: С времязависимой антимикробной активностью (β-лактамы). Цель режима дозирования: длительное поддержание в
- 32. Особенности фармакокинетики пенициллинов Создают высокие концентрации в легких, почках, слизистой оболочке кишечника, половых органах, плевральной и
- 33. Особенности фармакокинетики цефалоспоринов Создают высокие концентрации в легких, почках, печени, мышцах, коже, костях, синовиальной, плевральной и
- 34. Особенности фармакокинетики карбапенемов Вводятся только парэнтерально Хорошо распределяются в организме, создавая терапевтические концентрации во многих органах
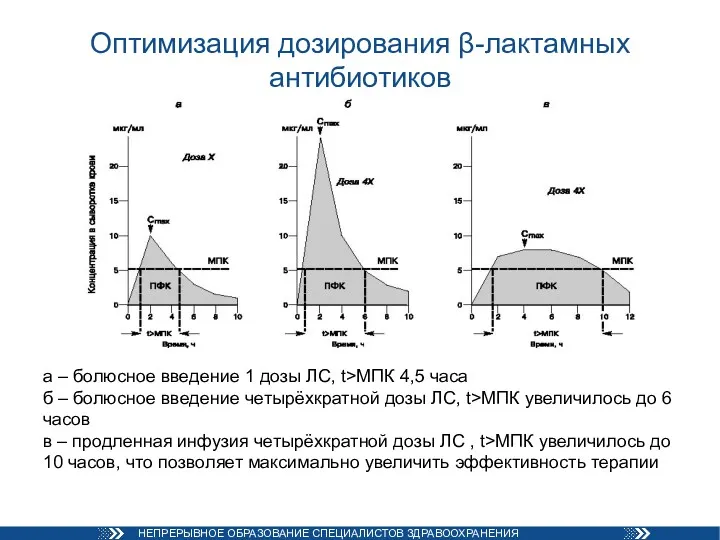
- 35. Оптимизация дозирования β-лактамных антибиотиков а – болюсное введение 1 дозы ЛС, t>МПК 4,5 часа б –
- 36. Особенности фармакокинетики аминогликозидов Низкая биодоступность при приеме внутрь Около 10% дозы связывается с альбумином Распределяются в
- 37. Особенности дозирования аминогликозидов Дозы всех аминогликозидов должны расчитываться на килограмм массы тела при парэнтеральном введении. Суточная
- 38. Особенности фармакокинетики хинолонов и фторхинолонов Хорошо всасываются в ЖКТ, высокая биодоступность Фторхинолоны создают высокие концентрации во
- 39. Особенности фармакокинетики макролидов Биодоступнось при пероральном приеме 80-95% Хорошо проникают в ткани, высокие внутриклеточные концентрации, плохо
- 40. ПРОБЛЕМА РЕЗИСТЕНТНОСТИ МИКРООРГАНИЗМОВ К АНТИБИОТИКАМ
- 41. Патогены группы ESCAPE: E - Enterococcus faecium S - Staphylococcus aureus (MRSA) C - Clostridium difficile
- 42. ВОЗ: наиболее опасные резистентные патогены Acinetobacter baumanii Устойчивые к карбапененмам Pseudomonas aeruginosa Устойчивые к карбапененмам Enterobacteriaceae
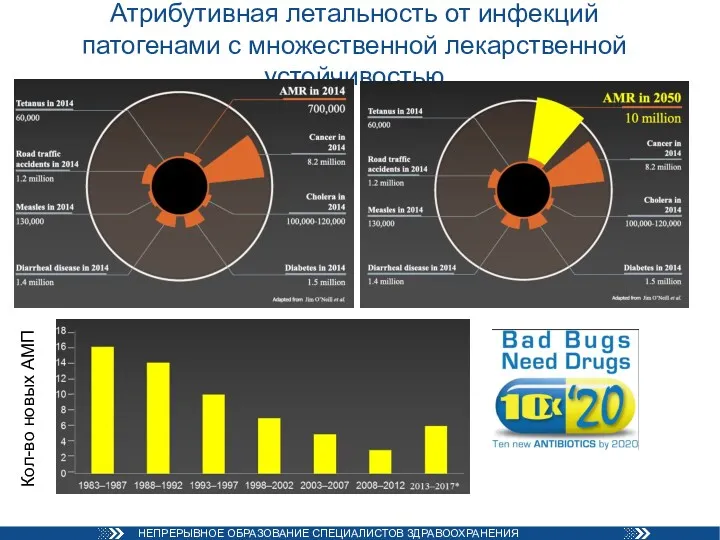
- 43. Атрибутивная летальность от инфекций патогенами с множественной лекарственной устойчивостью Кол-во новых АМП
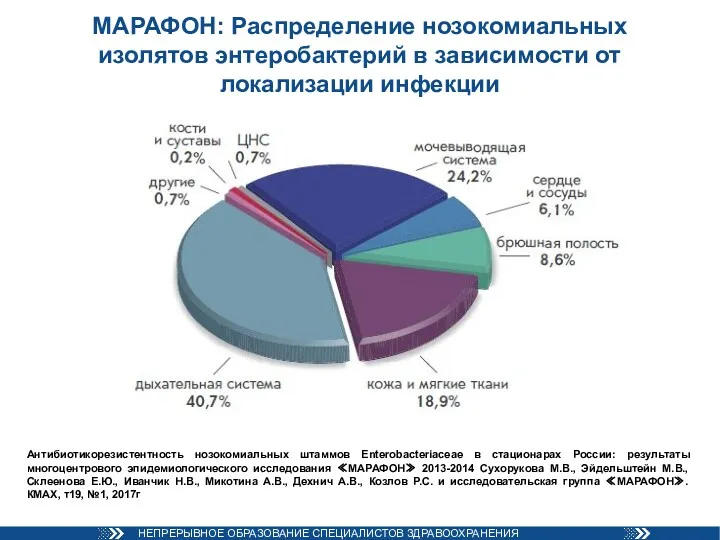
- 44. МАРАФОН: Распределение нозокомиальных изолятов энтеробактерий в зависимости от локализации инфекции Антибиотикорезистентность нозокомиальных штаммов Enterobacteriaceae в стационарах
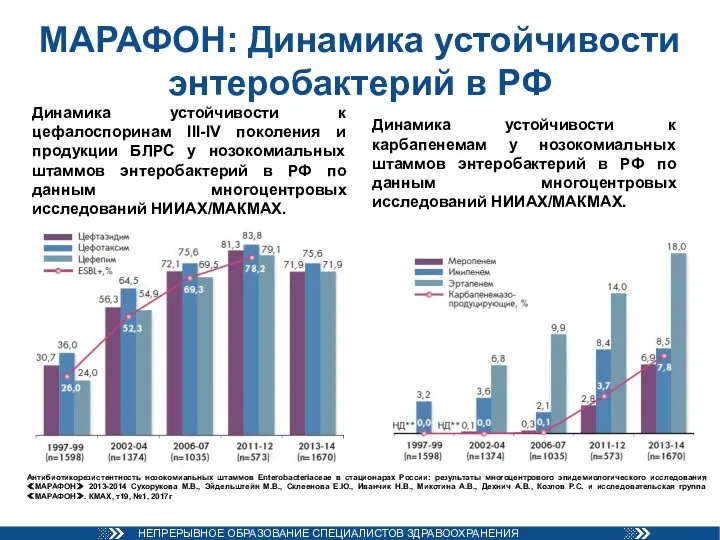
- 45. МАРАФОН: Динамика устойчивости энтеробактерий в РФ Динамика устойчивости к цефалоспоринам III-IV поколения и продукции БЛРС у
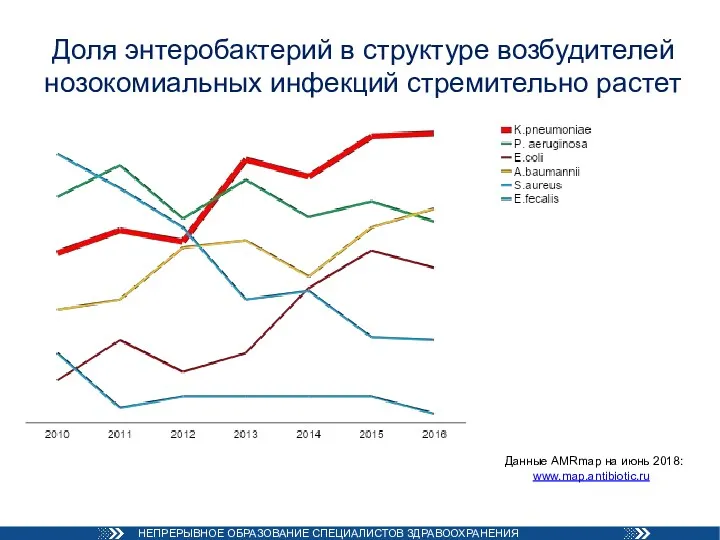
- 46. Доля энтеробактерий в структуре возбудителей нозокомиальных инфекций стремительно растет Данные AMRmap на июнь 2018: www.map.antibiotic.ru
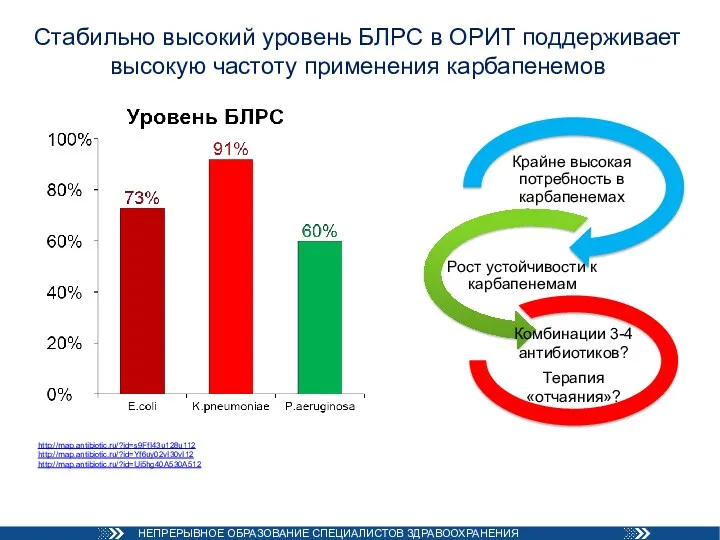
- 47. Стабильно высокий уровень БЛРС в ОРИТ поддерживает высокую частоту применения карбапенемов http://map.antibiotic.ru/?id=s9FfI43u128u112 http://map.antibiotic.ru/?id=Yf6uy02vI30vI12 http://map.antibiotic.ru/?id=Ui5hg40A530A512
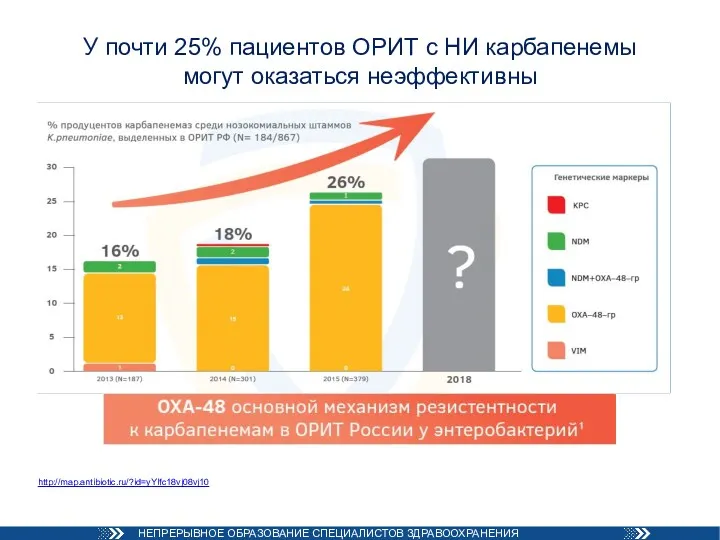
- 48. У почти 25% пациентов ОРИТ с НИ карбапенемы могут оказаться неэффективны http://map.antibiotic.ru/?id=yYIfc18vj08vj10
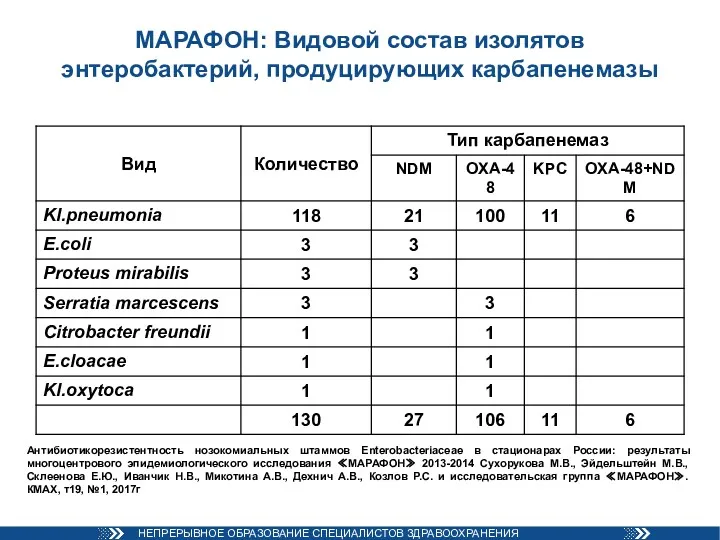
- 49. МАРАФОН: Видовой состав изолятов энтеробактерий, продуцирующих карбапенемазы Антибиотикорезистентность нозокомиальных штаммов Enterobacteriaceae в стационарах России: результаты многоцентрового
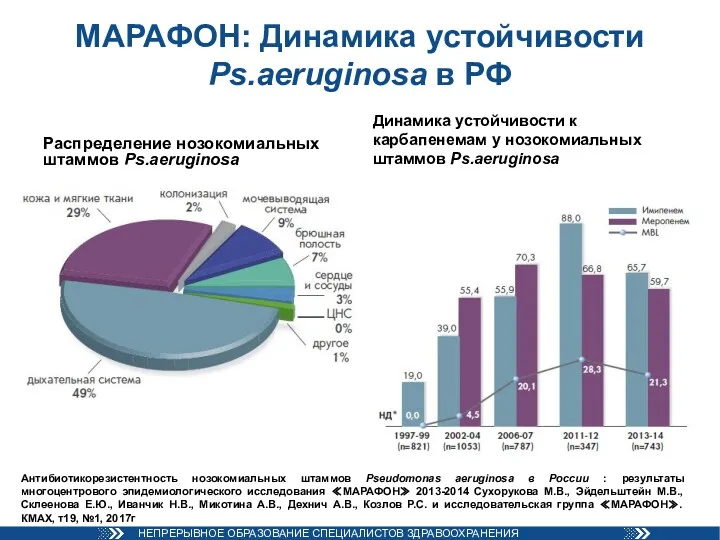
- 50. МАРАФОН: Динамика устойчивости Ps.aeruginosa в РФ Распределение нозокомиальных штаммов Ps.aeruginosa Динамика устойчивости к карбапенемам у нозокомиальных
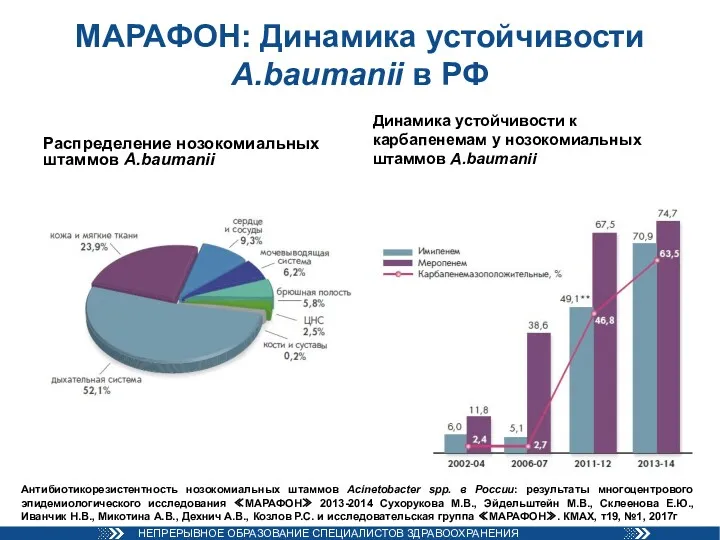
- 51. МАРАФОН: Динамика устойчивости A.baumanii в РФ Распределение нозокомиальных штаммов A.baumanii Динамика устойчивости к карбапенемам у нозокомиальных
- 52. ОСНОВЫ РАЦИОНАЛЬНОЙ АНТИМИКРОБНОЙ ТЕРАПИИ
- 53. Основные положения Выбор стартового препарата должен учитывать: микрофлору, вызвавшую инфекционный процесс; проникновение препарата в очаг инфекции
- 54. Основные положения Правильное использование антибиотиков имеет особое значение на фоне повышения резистентности грамотрицательных микроорганизмов Рациональная антибиотикотерапия
- 55. “Collateral Damage”- сопутствующий ущерб “Сопутствующий ущерб - экологические побочные эффекты антимикробной терапии … проводящие к селекции
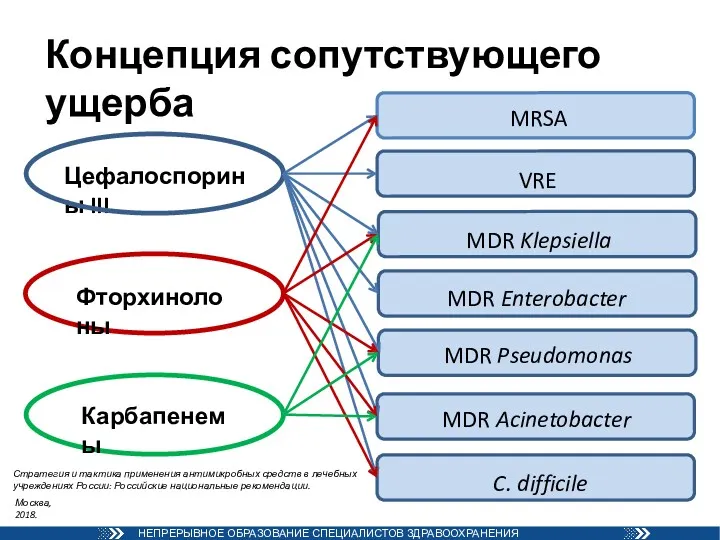
- 56. Концепция сопутствующего ущерба Цефалоспорины III Фторхинолоны Карбапенемы C. difficile MDR Acinetobacter MDR Pseudomonas MDR Enterobacter MDR
- 57. Концепция «параллельного ущерба» при применении цефалоспоринов и фторхинолонов “Collateral Damage” from Cephalosporin or Quinolone Antibiotic Therapy.
- 58. Критерии достаточности антимикробной терапии Нормализация температуры Положительная динамика основных симптомов инфекции Положительная динамика основных лабораторных показателей
- 59. Критерии достаточности антимикробной терапии Сохранение отдельных симптомов инфекции (субфебрильная лихорадка, умеренный лейкоцитоз без сдвига, повышение СОЭ),
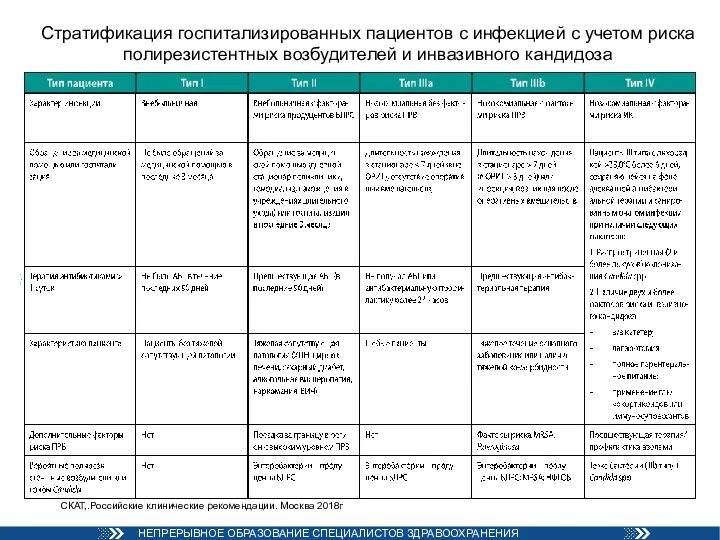
- 60. Стратификация госпитализированных пациентов с инфекцией с учетом риска полирезистентных возбудителей и инвазивного кандидоза СКАТ,.Российские клинические рекомендации.
- 61. Рекомендации по антимикробной терапии
- 62. Mario Tumbarello et al. Identifying Patients Harboring Extended-Spectrum-β-Lactamase-Producing Enterobacteriaceae on Hospital Admission: Derivation and Validation of
- 63. Алгоритм выбора антимикробной терапии у пациентов с тяжелой инфекцией и признакаами сепсиса Индекс Tumbarello et al
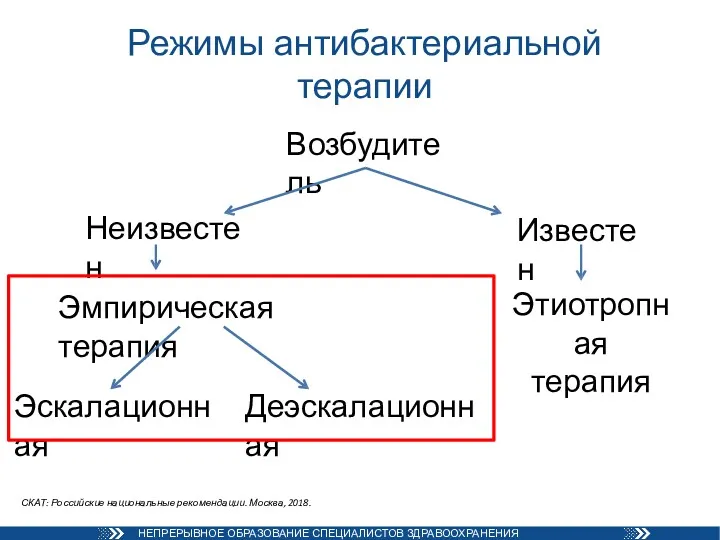
- 64. Режимы антибактериальной терапии Возбудитель Известен Неизвестен Эмпирическая терапия Этиотропная терапия Эскалационная Деэскалационная СКАТ: Российские национальные рекомендации.
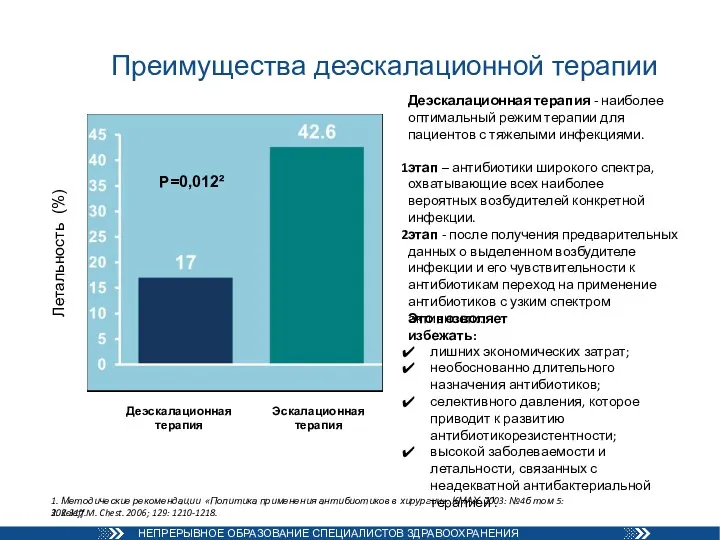
- 65. Преимущества деэскалационной терапии Летальность (%) 2. Koleff M. Chest. 2006; 129: 1210-1218. Деэскалационная терапия Деэскалационная терапия
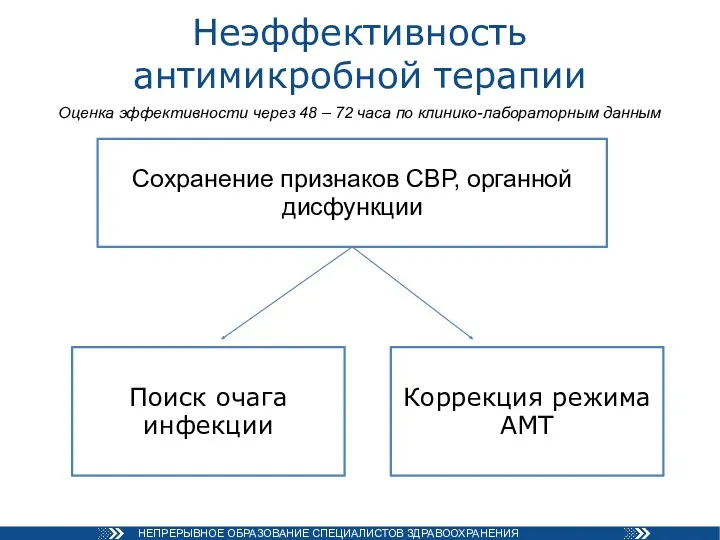
- 66. Неэффективность антимикробной терапии Сохранение признаков СВР, органной дисфункции Поиск очага инфекции Коррекция режима АМТ Оценка эффективности
- 67. Факторы оказывающие влияние на исходы терапии
- 68. Факторы риска полирезистентных возбудителей Антимикробная терапия в предшествующие 90 дней Настоящая госпитализацие в течение ≥ 5
- 69. Факторы риска БЛРС Нахождение в ОРИТ более 4 суток Перевод из другого стационара Лечение цефалоспоринами или
- 70. Факторы риска карбапенемазо – продуцирующих энтеробактерий Применение нескольких антимикробных препаратов (особенно комбинаций, включающих карбапенемы и ФХ)
- 71. Факторы риска P.aeruginosa Длительное нахождение в ОРИТ (> 5 суток), ИВЛ Иммуносупрессия (цитостатики, глюкокортикоиды, нейтропения) Бронхоэктазы
- 72. Факторы риска MRSA Предшествующая госпитализация Предшествующие антибиотики Нахождение в ОРИТ ИВЛ Внутрисосудистые катетеры Назофаренгиальное носительство MRSA
- 73. Факторы риска VRE Длительное применение ванкомицина Длительное применение антибиотиков широкого спектра Длительное пребывание в ОРИТ Иммуносупрессия,
- 74. Факторы риска инвазивных микозов EORTC/MSG 2008 Факторы риска инвазивного аспергиллеза Нейтропения менее 0,5х109/л ( Реципиент аллогенного
- 75. 1. León C, Ruiz-Santana S, Saavedra P, et al. Usefulness of the "Candida score" for discriminating
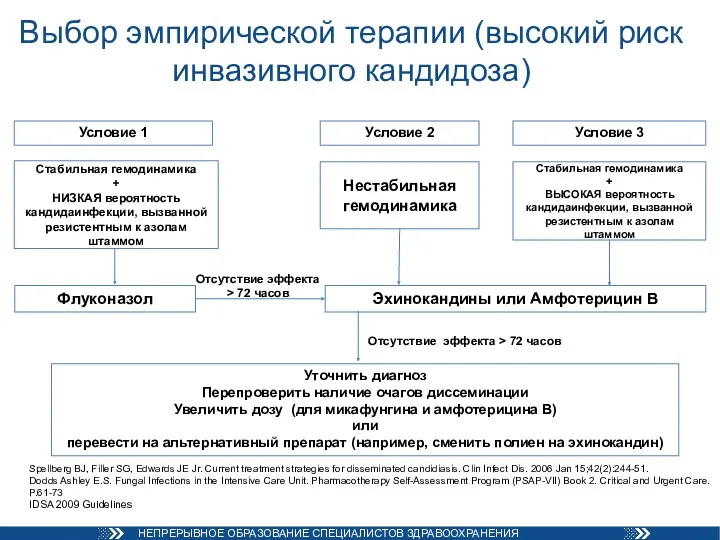
- 76. Выбор эмпирической терапии (высокий риск инвазивного кандидоза) Нестабильная гемодинамика Эхинокандины или Амфотерицин В Флуконазол Отсутствие эффекта
- 77. СОВРЕМЕННЫЕ ВОЗМОЖНОСТИ ЛЕЧЕНИЯ ПОЛИРЕЗИСТЕНТНЫХ ИНФЕКЦИЙ, ВЫЗВАННЫХ ГРАМОТРИЦАТЕЛЬНЫМИ БАКТЕРИЯМИ
- 78. Антимикробные препараты для лечения бактерий с экстремальной устойчивостью Бактерии, продуцирующие карбапенемазы: класса А – KPC; класса
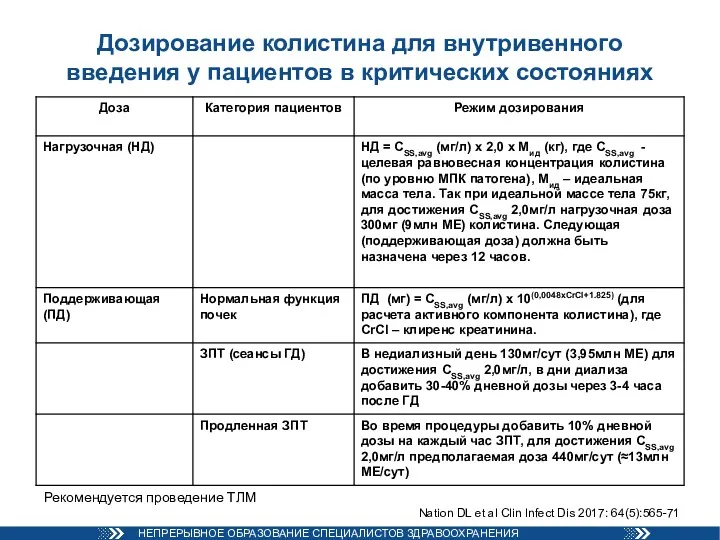
- 79. Дозирование колистина для внутривенного введения у пациентов в критических состояниях Nation DL et al Clin Infect
- 80. Дозирование полимиксина В для внутривенного введения у пациентов в критических состояниях International Consensus Guidelines for the
- 81. Оценка опыта применения полимиксина B: Примерно половина пациентов, выживших после терапии полимиксином B погибли в течении
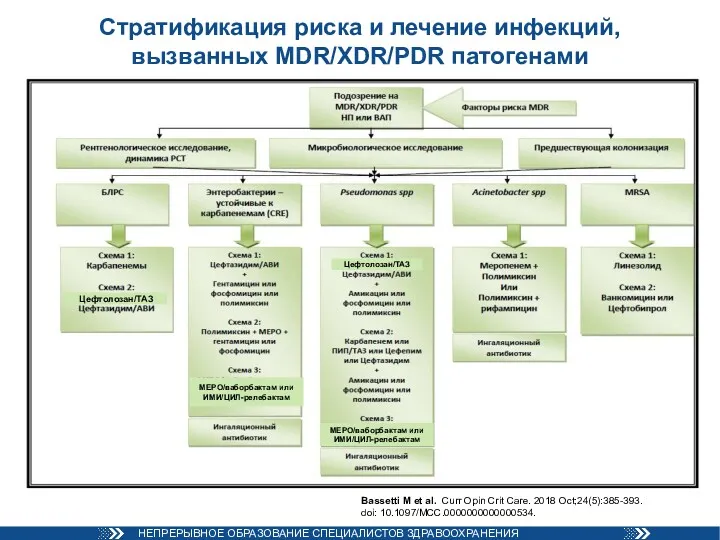
- 82. Стратификация риска и лечение инфекций, вызванных MDR/XDR/PDR патогенами Bassetti M et al. Curr Opin Crit Care.
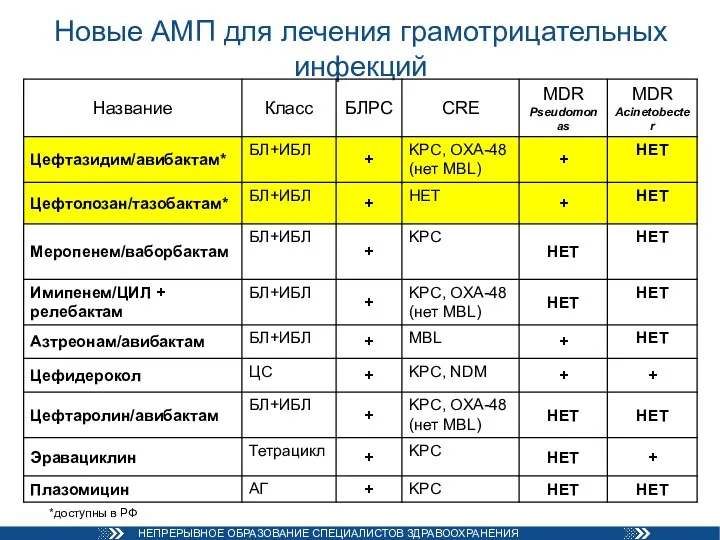
- 83. Новые АМП для лечения грамотрицательных инфекций *доступны в РФ
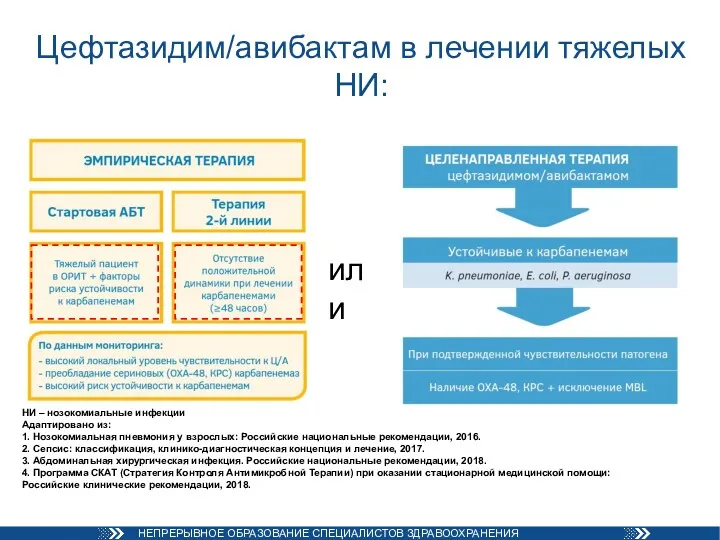
- 84. Цефтазидим/авибактам в лечении тяжелых НИ: НИ – нозокомиальные инфекции Адаптировано из: 1. Нозокомиальная пневмония у взрослых:
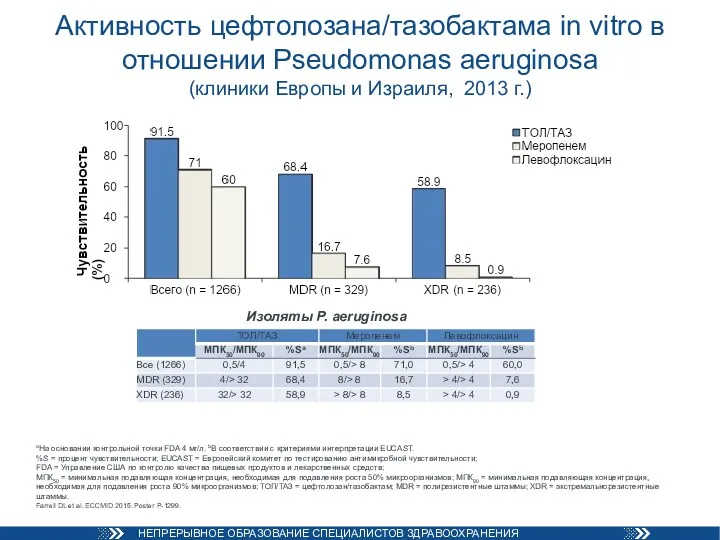
- 85. Активность цефтолозана/тазобактама in vitro в отношении Pseudomonas aeruginosa (клиники Европы и Израиля, 2013 г.) Изоляты P.
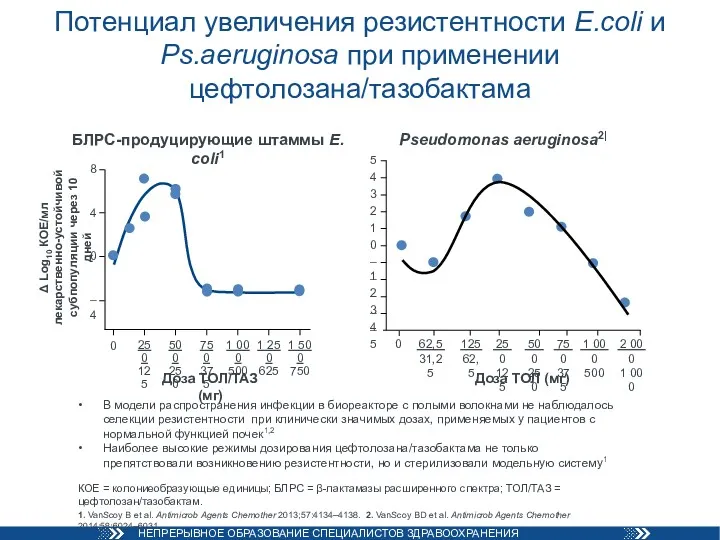
- 86. Потенциал увеличения резистентности E.coli и Ps.aeruginosa при применении цефтолозана/тазобактама В модели распространения инфекции в биореакторе с
- 87. РЕКОМЕНДАЦИИ ПО ЭТИОТРОПНОЙ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ ПОЛИРЕЗИСТЕНТНЫХ ИНФЕКЦИЙ
- 89. Скачать презентацию






















































 Prezentatsia
Prezentatsia Образовательная ситуация с использованием информационно-коммуникационных технологий В гостях у сказки для детей средней группы.
Образовательная ситуация с использованием информационно-коммуникационных технологий В гостях у сказки для детей средней группы. Родительный, дательный, творительный и предложный падежи имен прилагательных женского рода
Родительный, дательный, творительный и предложный падежи имен прилагательных женского рода Процессуальные теории мотивации
Процессуальные теории мотивации Шаблоны для изготовления презнтаций на зимнюют тематику.
Шаблоны для изготовления презнтаций на зимнюют тематику. Проект: Этих дней не смолкнет слава
Проект: Этих дней не смолкнет слава Бизнес-план. Индивидуальное предприятие
Бизнес-план. Индивидуальное предприятие Қаймақ технологиясы оларды нормалау және гомогенизациялау
Қаймақ технологиясы оларды нормалау және гомогенизациялау Операция Зёрнышко (презентация)
Операция Зёрнышко (презентация) Принцип действия и схема рт-252 рт-253 рт-255
Принцип действия и схема рт-252 рт-253 рт-255 Лист. Общие понятия о листе, его развитие, анатомическое строение, видоизменения, морфология и классификация
Лист. Общие понятия о листе, его развитие, анатомическое строение, видоизменения, морфология и классификация Викторина История Олимпийских игр
Викторина История Олимпийских игр Обобщение опыта по теме Психология общения
Обобщение опыта по теме Психология общения Доклад на РМО воспитателей разновозрастных групп по теме: Система мониторинга реализации ООП ДОУ
Доклад на РМО воспитателей разновозрастных групп по теме: Система мониторинга реализации ООП ДОУ Технические каналы утечки информации
Технические каналы утечки информации Участие медсестры в подготовке к инструментальным методам исследования
Участие медсестры в подготовке к инструментальным методам исследования Резцы. Классификация резцов
Резцы. Классификация резцов Умная теплица
Умная теплица Зимняя олимпиада 2014
Зимняя олимпиада 2014 День Святой Троицы (Пятидесятница)
День Святой Троицы (Пятидесятница) Драматургия танца
Драматургия танца Когерентность. Монохроматические волны
Когерентность. Монохроматические волны Современное климатическое оборудование
Современное климатическое оборудование Мои ученики
Мои ученики Конспект интегрированного занятия по развитию речи для детей младшего дошкольного возраста с использованием мнемотехники и ИКТ
Конспект интегрированного занятия по развитию речи для детей младшего дошкольного возраста с использованием мнемотехники и ИКТ Методическая разработка Презентация ко Дню Победы Поклонимся великим тем годам... Диск Диск Диск Диск
Методическая разработка Презентация ко Дню Победы Поклонимся великим тем годам... Диск Диск Диск Диск Кім ақылды кім шапшаң кім тапқыр. Таныстыру
Кім ақылды кім шапшаң кім тапқыр. Таныстыру Антон Павлович Чехов
Антон Павлович Чехов