Содержание
- 2. Сера
- 3. Положение в Периодической системе: Сера: Порядковый номер № 16 Период : 3 период Группа: VI группа,
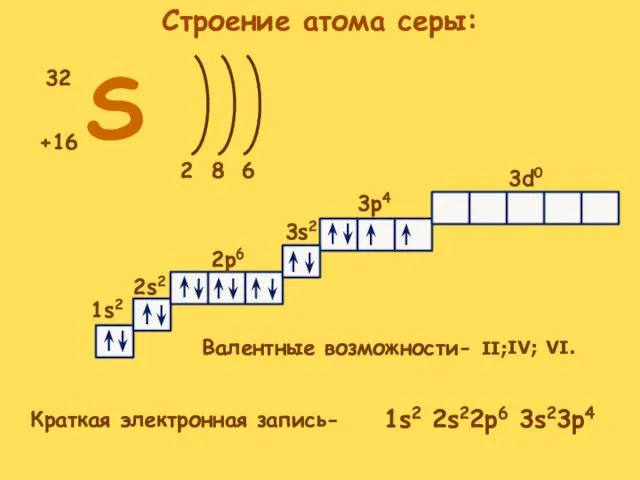
- 4. S +16 32 2 6 8 1s2 2s2 2p6 3s2 3p4 3d0 Краткая электронная запись- Валентные
- 5. Строение атома серы
- 6. Нахождение серы в природе. Сера самородная (S) Цинковая обманка (сфалерит ZnS) Киноварь (HgS) Свинцовый блеск (галенит
- 7. Сера самородная
- 8. Сера самородная
- 9. Сера самородная
- 10. Сера самородная
- 11. Сера самородная
- 12. Историческая справка. Cера встречается в природе в свободном (самородном) состоянии, поэтому она была известна человеку уже
- 13. Историческая справка Считалось, что горящая сера отгоняет нечистую силу. В Библии говорится об использовании серы для
- 14. Историческая справка В 11 в. алхимики полагали, что металлы, в том числе золото и серебро, состоят
- 15. Историческая справка. Практическое значение серы резко возросло после того, как изобрели черный порох (в состав которого
- 16. Аллотропия серы. Аллотропия – явление, когда один химический элемент образует несколько простых веществ. Сами простые вещества,
- 17. Аллотропия - ромбическая (α - сера) - S8 t°пл. = 113°C; ρ = 2,07 г/см3 Наиболее
- 18. Физические свойства. Твердое кристаллическое вещество желтого цвета, нерастворима в воде, водой не смачивается (плавает на поверхности
- 19. Химические свойства Окислительные свойства серы (S0 + 2ē → S-2) Сера реагирует со щелочными металлами без
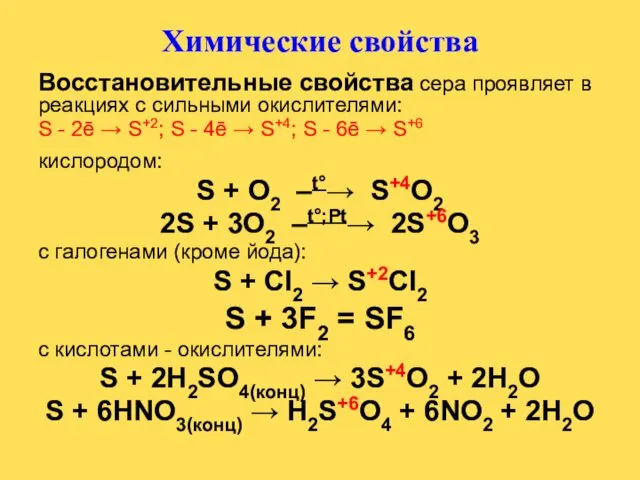
- 20. Химические свойства Восстановительные свойства сера проявляет в реакциях с сильными окислителями: S - 2ē → S+2;
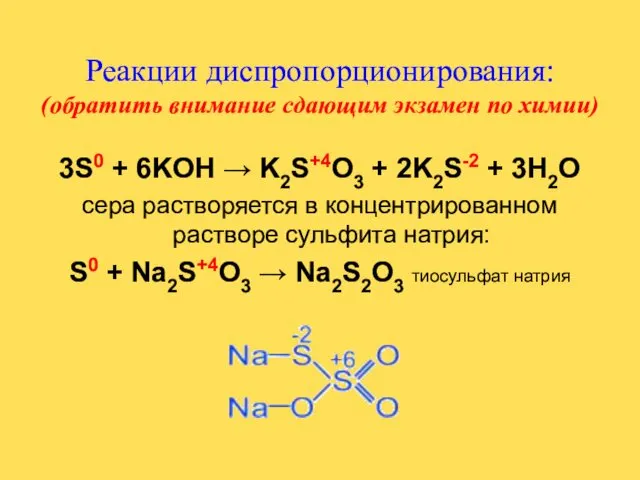
- 21. Реакции диспропорционирования: (обратить внимание сдающим экзамен по химии) 3S0 + 6KOH → K2S+4O3 + 2K2S-2 +
- 22. Применение серы. Производство спичек Медицина Борьба с вредителями
- 23. РЕШИТЕ ЗАДАЧУ В зернохранилищах для истребления насекомых сжигают серу, исходя из нормы 24 г на 1
- 25. Скачать презентацию


















 Пресмыкающиеся
Пресмыкающиеся Цветотерапия в ДОУ
Цветотерапия в ДОУ Минералы и кристаллы. Свойства минералов
Минералы и кристаллы. Свойства минералов Особенности социально-педагогического сопровождения детей-сирот и детей, оставшихся без попечения родителей
Особенности социально-педагогического сопровождения детей-сирот и детей, оставшихся без попечения родителей Способы обработки металлов давлением
Способы обработки металлов давлением создание парка моделей машин
создание парка моделей машин Черная металлургия
Черная металлургия Игры для коррекционно-развивающей работы с детьми. Раздел - фонематика.
Игры для коррекционно-развивающей работы с детьми. Раздел - фонематика. Путешествие по Тулате
Путешествие по Тулате Нагнетатели. Насосы, тягодутьевые машины и компрессоры
Нагнетатели. Насосы, тягодутьевые машины и компрессоры Правописание наречий с приставками
Правописание наречий с приставками Мазутные хозяйства ТЭС. Лекция 7
Мазутные хозяйства ТЭС. Лекция 7 Эпидемиологическая ситуация по ВИЧ-инфекции в Саратовской области на 01.07.2017 года
Эпидемиологическая ситуация по ВИЧ-инфекции в Саратовской области на 01.07.2017 года Поиск и отбор персонала
Поиск и отбор персонала Как выглядит Дед Мороз в разных странах
Как выглядит Дед Мороз в разных странах Классный час - презентация Год культуры в России
Классный час - презентация Год культуры в России Что такое хвоинки?
Что такое хвоинки? Раннее послеродовое кровотечение
Раннее послеродовое кровотечение экология
экология Іріңді паротит. Мастит. Парапроктит, лимфангаит, лимфаденит,тромбофлебит
Іріңді паротит. Мастит. Парапроктит, лимфангаит, лимфаденит,тромбофлебит Волейбол
Волейбол Спортивна фізіологія. Зміст, задачі, зародження, зв’язок з іншими науками, наукові сучасні перспективи
Спортивна фізіологія. Зміст, задачі, зародження, зв’язок з іншими науками, наукові сучасні перспективи ГТО - групповой товарооборот
ГТО - групповой товарооборот Арт-терапия. Загляни в себя
Арт-терапия. Загляни в себя Психологические аспекты межэтнического взаимодействия
Психологические аспекты межэтнического взаимодействия Составление планов контактной сети станции
Составление планов контактной сети станции IT сервис Build Network. Рабочая структура
IT сервис Build Network. Рабочая структура Сравнительный подход к оценке недвижимости. (Тема 8)
Сравнительный подход к оценке недвижимости. (Тема 8)