Содержание
- 2. Цель урока: обобщить и систематизировать знания учащихся об особенностях получении металлов; научных принципах производства металлов и
- 3. Методы: словесный – беседа, рассказ, наглядно - иллюстративные – демонстрация таблиц, практический – решение задач. Тип
- 4. Самым распространенным Ме в земной коре является алюминий. За ним следует железо, натрий, калий, магний и
- 5. Самородок платины Самородок серебра Самородок золота Самородок меди Нахождение металлов в природе
- 6. Способы получения металлов
- 7. Пирометаллургия - получение металлов и сплавов под действием высоких температур. Восстановление углем (угарным газом): 2PbO +
- 8. Гидрометаллургия - получение металлов из водных растворов. 1 стадия: растворение в кислоте нерастворимых минералов, содержащих металлы:
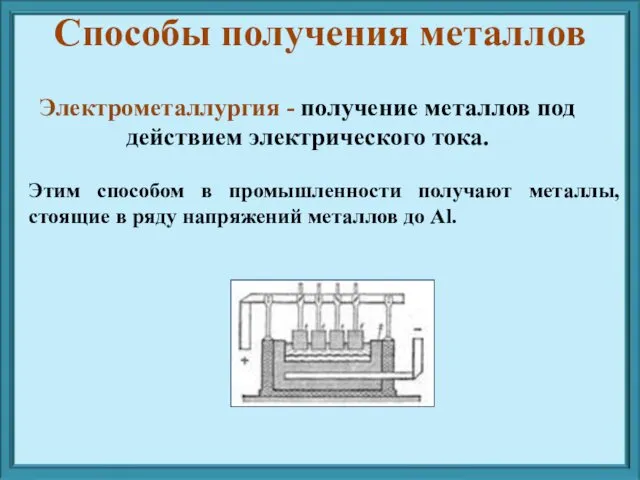
- 9. Электрометаллургия - получение металлов под действием электрического тока. Этим способом в промышленности получают металлы, стоящие в
- 10. Самопроизвольное разрушение металлических материалов, происходящее под воздействием окружающей среды, называется коррозией Коррозия металлов
- 11. Одним из наиболее широко распространенных коррозионных процессов является ржавление железа. Его можно описать суммарным уравнением: 4Fe
- 12. Коррозия может возникать и под влиянием радиационного излучения, а также продуктов жизнедеятельности бактерий и других организмов.
- 13. Защита поверхности металла металлическими покрытиями хромирование золочение никелирование Защита поверхности металлов неметаллическими покрытиями Защиты от коррозии:
- 14. Утечка газа, нефти и других опасных химических продуктов из разрушенных коррозией трубопроводов приводит к загрязнению окружающей
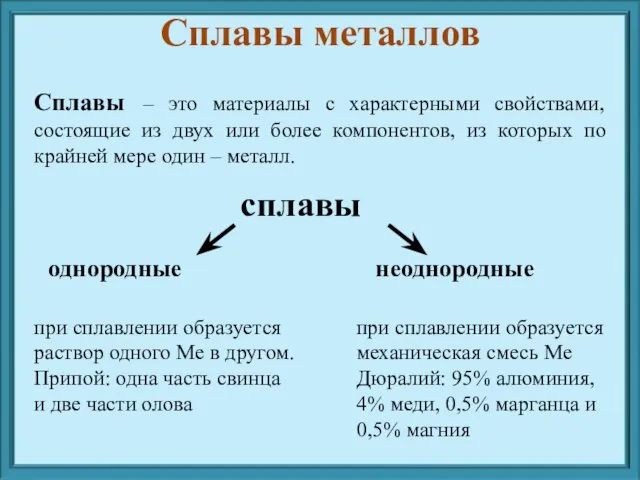
- 15. Сплавы – это материалы с характерными свойствами, состоящие из двух или более компонентов, из которых по
- 16. Сплавы на основе железа Чугун – это сплав железа, содержащий более 1,7 % углерода, а также
- 17. Бронза – сплав на основе меди с добавлением (20%) олова. Латунь – медный сплав, содержащий от
- 18. Примеры заданий по теме: «Общие способы получение металлов» Задания с выбором ответа А1. Реакция возможна между
- 19. A3. Какой из металлов вытесняет медь из сульфата меди (II)? 1) Zn 2) Ag 3) Hg
- 21. Скачать презентацию
















 Тема 3. Товарне виробництво. Товар і гроші. Лекція 2: Вартість товару, еволюція форм вартості
Тема 3. Товарне виробництво. Товар і гроші. Лекція 2: Вартість товару, еволюція форм вартості Презентация Рельеф дна Мирового океана 6 класс
Презентация Рельеф дна Мирового океана 6 класс Память. Как устроена память
Память. Как устроена память Артикуляционная гимнастика для девочек
Артикуляционная гимнастика для девочек Требования Камминз к диагностике, ремонту и оформлению рекламационных актов
Требования Камминз к диагностике, ремонту и оформлению рекламационных актов Использование творческих заданий на уроках музыки как фактор развития индивидуальности личности/
Использование творческих заданий на уроках музыки как фактор развития индивидуальности личности/ Гео-шоу: Покажи мне мою страну
Гео-шоу: Покажи мне мою страну родителям об электронном дневнике и журнале
родителям об электронном дневнике и журнале Внутренняя политика Николая II
Внутренняя политика Николая II Optics. Basic photometric values and their units
Optics. Basic photometric values and their units Кто такие динозавры?
Кто такие динозавры? Презентация Необычные памятники России
Презентация Необычные памятники России Самбо
Самбо особенности одаренных и проблемных детей
особенности одаренных и проблемных детей The Las Vegas Boulevard Tracker Interface
The Las Vegas Boulevard Tracker Interface Задержка психического развития
Задержка психического развития Внедрение технологических процессов изготовления деталей машин и осуществление технологического контроля
Внедрение технологических процессов изготовления деталей машин и осуществление технологического контроля Квадратичная функция
Квадратичная функция Безопасный локомотивный объединенный комплекс (БЛОК). Назначение, устройство, технические характеристики
Безопасный локомотивный объединенный комплекс (БЛОК). Назначение, устройство, технические характеристики Презентация основных тезисов программы Музыкальный калейдоскоп
Презентация основных тезисов программы Музыкальный калейдоскоп 8 МАРТА
8 МАРТА 20231016_zagovor_v_zerentuyskom_rudnike
20231016_zagovor_v_zerentuyskom_rudnike Рак легкого
Рак легкого Робота МЗС на консульському напрямі у 2017 році. Департамент консульської служби, 2018 рік
Робота МЗС на консульському напрямі у 2017 році. Департамент консульської служби, 2018 рік Функции управления
Функции управления Опыт работы кл.рук 2
Опыт работы кл.рук 2 Норма права
Норма права Лазер. Спонтанное (самопроизвольное) излучение
Лазер. Спонтанное (самопроизвольное) излучение