Слайд 2

При изучении курса органической химии использована методическая система УДЕ. На основе
УДЕ планируются темы:
«Углеводороды и их природные источники»,
«Кислородсодержащих соединений и их нахождение в живой природе,
«Азотсодержащие соединения и их нахождение в живой природе». При изучении этих тем одновременно рассматриваются: состав, строение, свойства, получение.
Слайд 3

Использование укрупненных дидактических единиц позволяет:
-активизировать познавательную деятельность обучающихся за счет выявления
сходств, применения обобщений и самостоятельной деятельности в текущей учебной работе.
-выявлять главное и существенное в большой дозе материала.
-устанавливать больше логических связей в материал;
-совместное и одновременное изучение родственных разделов ( блочное изучение материала)
-изучение противоположных явлений и процессов в единстве.
- использование обзорных способов выражения информации.
Слайд 4

Использование укрупненных дидактических единиц
Увеличения объема изученного материала, объединение в крупные
блоки, создают резерв времени для закрепления , повторения.
-активизировать познавательную деятельность обучающихся за счет выявления сходств, применения обобщений и самостоятельной деятельности в текущей учебной работе.
-выявлять главное и существенное в большой дозе материала.
-устанавливать больше логических связей в материал;
-совместное и одновременное изучение родственных разделов ( блочное изучение материала)
-изучение противоположных явлений и процессов в единстве.
- использование обзорных способов выражения информации.
Слайд 5

Основные этапы работы
1 этап – изучение нового материала
Теоретический материал в учебнике
представлен в 8 параграфах. Данный материал разделен на три основных единицы информации:
-строение и номенклатура углеводородов,
-химические свойства и применение углеводородов, ароматические углеводороды
Слайд 6

На уроке информация подается в виде сжатого конспекта – таблицы, в
виде работы с матрицей.
Ученик сам делает выбор: что ему записывать, а что легко запомнить
Слайд 7

2 этап- закрепление теоретического материала
Процесс решения ключевых задач осуществляется следующим образом:
учащийся вслух объясняют каждый свой шаг в решении задач, другой записывает под диктовку. Работая в группах они рассказывают и разъясняют друг другу материал составляют матрицы.
Слайд 8

Конспект к уроку «Строение углеводородов. (семинар)
1.Определите по приведенным общим формулам класс
соединений:
CnH2n-2 CnH2n CnH2n+2 CnH2n-6
2. Укажите формулы алканов и назовите эти соединения:
C6H12 C4H10 C2H2 C6H14 C6H6 C9H20
3. Составьте молекулярные и структурные формулы алканов, алкенов, алкинов с числом углеродных атомов а) 6, б) 8, в) 3. Назовите полученные вещества
4. Составьте структурные формулы по приведенным углеродным скелетам:
1) C – C – C – C 2) C – C – C = C – C 3) C ≡ C – C - С
4) C – C ≡C – C – C 5 ) C = C – C – C = C
| | | | |
C C – C C C C
5. Составьте формулы гомологов бутана, пропена, этина, гексана.
6.Составьте структурные формулы изомеров пентана, гексана.
Слайд 9

«Номенклатура углеводородов»
Номенклатура- система названий, применяемая в науке.
Выполнение по алгоритму названия органических
веществ.
7. Назовите по международной номенклатуре:
1) CH3– CH – CH – CH3 2 ) CH2= CH – CH – CH3
| | |
CH3 CH3 C2H5
8. напишите структурные формулы веществ:
1) 2-метилпентен-2 3) 3,4,4-триметилпентина-1
2) 2.3-диметилбутен-1 4) 2-метил-4этилгептен-2
9. Проверьте названия веществ, исправьте, если требуется.
CH3— CH2— C = CН2
CH3 — C = CН —CH3
│
СН3 │ │
2метил бутен -1 CH3 CH3 2 метилбутен
Слайд 10

Конспект урока « Химические свойства углеводородов» (семинар).
1. С какими из перечисленных
веществ будет взаимодействовать ацетилен: Вr2 , СН4, Н2, НL, О2. Напишите уравнения возможных реакций.
2. С какими веществами будет взаимодействовать метан: хлор, вода, водород, углерод, перманганат калия, кислород. Напишите уравнения возможных реакций.
3 . Осуществите схемы превращений:
a) CH4----> C2H6---> C2H5Br ---> C2H5OH
б) метан---> ацетилен---> этан---> хлорэтан---> этилен
в) СН4 → СН3CL →C2H6 → C2H4→ C2H6
Слайд 11

3 этап работы – самореализация
Конспект к уроку « Повторение темы «
Углеводороды» 1.Какие вещества, формулы которых приведены ниже относятся
К алканам: C4H10 C2H2 CH4 C6H6 C2H4;
к алкенам: C5H12 C3H6 C5H10 C6H6 C4H6 C7H14
2. Для углеводородов:
CH3– CH – CH3 CH2= CH – CH – CH3
| |
CH3 CH3
Составьте структурные формулы двух гомологов и двух изомеров.
Назовите полученные вещества.
3. Назовите вещества по международной номенклатуре:
a) CH3– CH – CH – CH3 б) CH2= CH – CH – CH3
| |
CH3 C2H5
Слайд 12
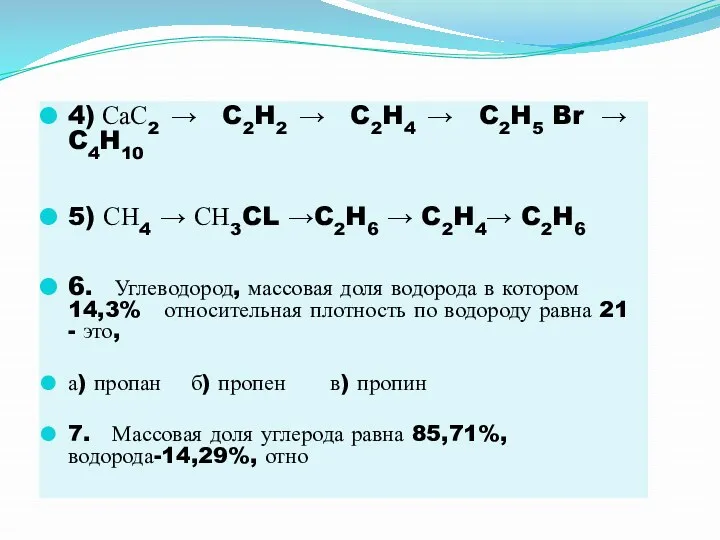
4) СаС2 → C2H2 → C2H4 → C2H5 Br → C4H10
5)
СН4 → СН3CL →C2H6 → C2H4→ C2H6
6. Углеводород, массовая доля водорода в котором 14,3% относительная плотность по водороду равна 21 - это,
а) пропан б) пропен в) пропин
7. Массовая доля углерода равна 85,71%, водорода-14,29%, отно
Слайд 13

4 этап работы - контрольная работа
Контрольная работа по теме «Углеводороды»
Задание1.
Для вещества, формула которого
CH3– CH – CH – CH3
| |
CH3 CH3
составьте структурные формулы двух изомеров и двух гомологов.
Дайте названия всех веществ по систематической номенклатуре.
Задание2. С какими из перечисленных веществ: азотная кислота, вода, хлор, хлороводород – будет реагировать метан? Напишите уравнения реакций, укажите условия их осуществления, составьте названия исходных веществ и продуктов реакций.
Задание 3. Напишите уравнения реакций, при помощи которых можно осуществить превращения по схеме:
C2H2 → C6H6 → C6H6C16
↓
C6H5NO2
Задание 4. Массовая доля углерода в углеводороде равна 92,31%, а его относительная плотность по воздуху– 0,897. Выведите его молекулярную формулу.












 Гражданская война в США (1861-1865). Империализм
Гражданская война в США (1861-1865). Империализм Николай Александрович Бердяев
Николай Александрович Бердяев Презентация № 3 Воздух, которым мы дышим
Презентация № 3 Воздух, которым мы дышим Діагностування пристроїв заземлення
Діагностування пристроїв заземлення Критерии оценивания курсовой и выпускной квалификационной работы
Критерии оценивания курсовой и выпускной квалификационной работы Деятельность руководителя по управлению деловой карьерой персонала
Деятельность руководителя по управлению деловой карьерой персонала Исследование и оценка физического развития. Функциональные пробы
Исследование и оценка физического развития. Функциональные пробы Государственная поддержка малого предпринимательства. ООО СтройЭкспертСтрелка
Государственная поддержка малого предпринимательства. ООО СтройЭкспертСтрелка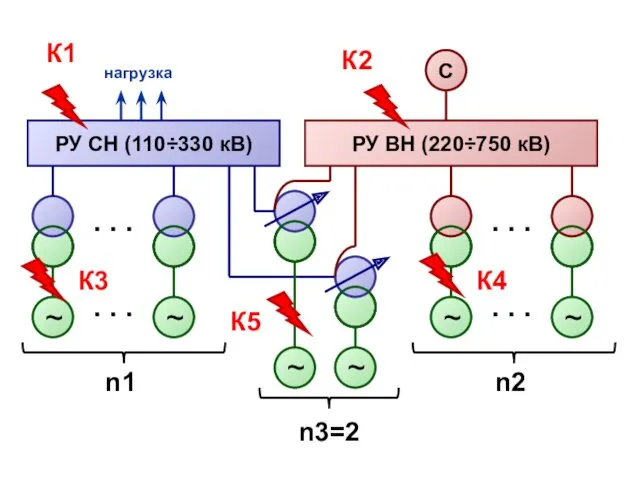 Расчёт ТКЗ схемы замещения
Расчёт ТКЗ схемы замещения Презентация 1
Презентация 1 Проект складной рыбацкий стулик
Проект складной рыбацкий стулик Сальмонеллалар, микробиологиялық диагностика, алдын-алу мен емдеу жолдары
Сальмонеллалар, микробиологиялық диагностика, алдын-алу мен емдеу жолдары Презентация Климат и климатические ресурсы
Презентация Климат и климатические ресурсы Эволюционная теория Дарвина
Эволюционная теория Дарвина Монастыри, основанные учениками преподобного Сергия Радонежского
Монастыри, основанные учениками преподобного Сергия Радонежского Государственный историко-архитектурный и этнографический музей-заповедник Кижи
Государственный историко-архитектурный и этнографический музей-заповедник Кижи Оборудование по теме Порошки
Оборудование по теме Порошки Совершенствование законодательства в области гражданской обороны и защиты населения и территорий от чрезвычайных ситуаций
Совершенствование законодательства в области гражданской обороны и защиты населения и территорий от чрезвычайных ситуаций Презентация к открытому мероприятию для учащихся 1 класса по правилам дорожного движения. Путешествие в страну дорожных знаков.
Презентация к открытому мероприятию для учащихся 1 класса по правилам дорожного движения. Путешествие в страну дорожных знаков. Комплектация и коммутация щитов
Комплектация и коммутация щитов Проектная работа
Проектная работа Наша Фаня
Наша Фаня Жизнь первых людей на Земле
Жизнь первых людей на Земле Биологическая роль отдельных микро-и ультрамикроэлементов в организме животных
Биологическая роль отдельных микро-и ультрамикроэлементов в организме животных Экономико-математическое моделирование
Экономико-математическое моделирование Основы проектирования машин. Редукторы со сборочным узлом
Основы проектирования машин. Редукторы со сборочным узлом Победа или поражение. Сочинение по пьесе А.Н.Островского Гроза
Победа или поражение. Сочинение по пьесе А.Н.Островского Гроза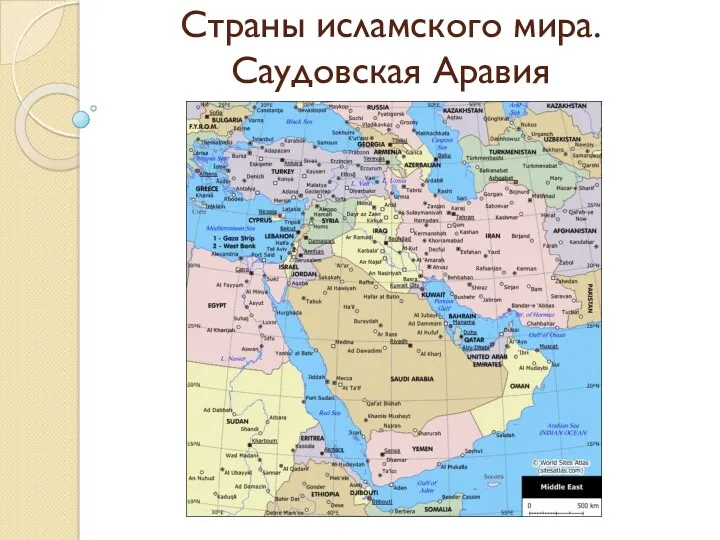 Страны исламского мира. Саудовская Аравия
Страны исламского мира. Саудовская Аравия