Слайд 2

Розчин йоду спиртовий 5%-ний
Solutio Iodi spirituosa 5%
Хімічна фомула : I2
Склад: йоду(I2)
-50г калію йодиду(KI) -20 г
Води( Н₂O.) і спирту 96%(C₂H₅OH) до 1 л
Добування :Джерелами для промислового добування йоду можуть бути морські водорості , залишки від добування чилійської селітри , нафтові бурові води .Вчені запропонували використовувати воду з свердловин нафтоносних районів.Вона є найпоширинішим джерелом йоду.
Властивості :Прозора рідина червоно-бурого кольору з характерним запахом
Слайд 3

Ідентифікація:
При додаванні до ЛЗ крохмалю утворюеться синьо-блакитне забарвлення
До ЛЗ додають
хлороформ (екстрагують йод)до знебарвлення водного шару , який ділиться на 2 частини :
В одній визначають йон калію з кислотою винною :
Слайд 4

У другій –йодид-іон за реакціею :з розчином калію дихромату в серидовищі
сульфатної розведенної у присутності хлороформу утворюєтся йод, який знебарвлює хлороформний шар у фіолетовий колір :
Реакція на етанол утворення йодоформу-жовтий осад з характерним запахом :
Слайд 5

Кількісне визначення:
Йодометрія:Вміст йоду визначають титруванням натрію тіосульфатом до знебарвлення розчину :S=1/2
Суму
калію йодиду натрію та натрію йодиду визначають аргентометрично за методом Фаянса у відтитрованному розчині :
Слайд 6
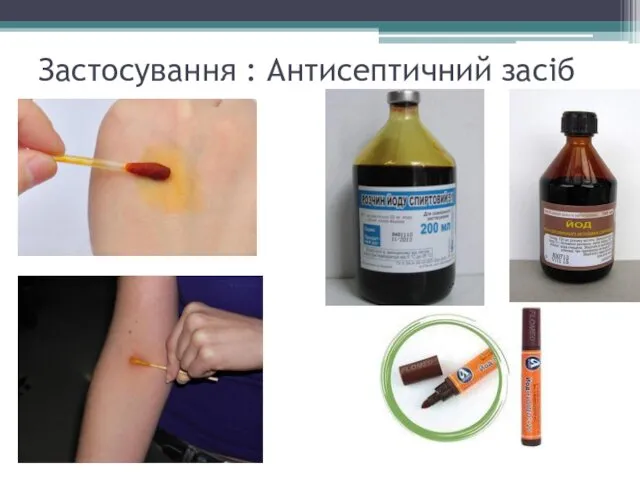
Застосування : Антисептичний засіб
Слайд 7

Зберігання:
У контейнері з темного скла ,у захищенному віж світла місці.Термін зберігання
6 місяців.
Слайд 8

Нітрогліцерин
Nitroglycerum
C3H5N3O9
Добування :синтезують при -15 С пропускаючи безводний гліцерин через суміш концентрованих
кислот сульфатної та нітратної.
Властивості: важка масляна рідина солодкого смаку .У воді не розчинний ,але добре розчинний в орг.розчинниках.Дуже отруйний.
Слайд 9

Ідентифікація:
Фізико-хімічними методами : ІЧ-спектоскопія ,тонкошарова хроматографія.
Субстанція дає реакції на нітрат-іони:
Реакція взаємодії
з сумішшю нітробензолу і кислоти сульфатної конц.,при подальшому додаванні до суміші розчину натрію гідроксиду і ацетону верхній шар набуває темно-фіолетового забарвлення
Субстанція не забарвлює роз-н калію перманганату,підкисленною сульфатною кислотою
Слайд 10

Не фармакопейні реакції:під час гідролізу гліцерину тринітрату в присутності лугу утворюється
гліцерин і сіль нітратної кислоти:
З розчином дифеніламіну в кислоті сульфатній конц.(залишки нітратної кислоти)
Слайд 11

Реакція на залишок гліцерину після лужного гідролізу лік. Р-ни – спирт
відганяють , залишок нагрівають з калію гідросульфатом-з'являтся запах акролеїну:
Слайд 12

Кількісне визначення:
Абсорбційна спектктрофотометрія у видимій області спектра (560 нм) .Метод базуеться
на вивчкнні оптичної густини забарвленного продукту ,який утворюеться після лужного гідролізу р-ни взаемо-дією з розчином кислоти сільфанілової у кислому серидовищі і розчином нафтилетиндіаміну дигідрохлориду
Слайд 13

Кислотно-основне титрування в присутності Н2О2 s=1\5
Надлишок натрію гідроксиду відтитровують розчином кислоти
хлористоводневої за фенолфталеїном. Паралельно проводять контрольний дослід
Слайд 14
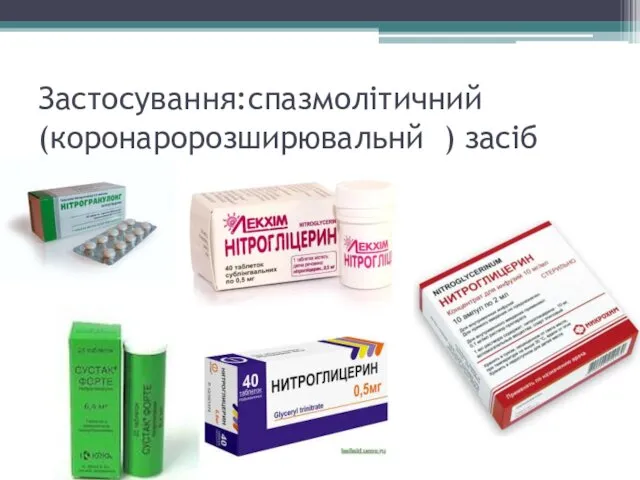
Застосування:спазмолітичний (коронаророзширювальнй ) засіб













 Совершенствование организации медицинской помощи населению
Совершенствование организации медицинской помощи населению Как родилась книга.
Как родилась книга. Первая медицинская помощь при различных травмах и поражениях
Первая медицинская помощь при различных травмах и поражениях Клаттеринг:симптоматика, коррекция
Клаттеринг:симптоматика, коррекция Капитальный ремонт скважин
Капитальный ремонт скважин Трудовые ресурсы. Планирование труда и его оплата на предприятии
Трудовые ресурсы. Планирование труда и его оплата на предприятии Гонорея. Возбудитель гонореи
Гонорея. Возбудитель гонореи Мышцы спины
Мышцы спины Современные решения оконных конструкций
Современные решения оконных конструкций Одномерные массивы и их обработка. Занятие 8-11
Одномерные массивы и их обработка. Занятие 8-11 Индивидуальная образовательная программа
Индивидуальная образовательная программа Жаңа дәуір философиясындағы сенсуалистік және рационалистік таным теорияларыны әлеуметтік-философиялық негіздері ретінде
Жаңа дәуір философиясындағы сенсуалистік және рационалистік таным теорияларыны әлеуметтік-философиялық негіздері ретінде Планируемые результаты обучения обществознанию в основной школе в соответствии с требованиями ФГОС
Планируемые результаты обучения обществознанию в основной школе в соответствии с требованиями ФГОС Производство и передача электроэнергии. Тест
Производство и передача электроэнергии. Тест Управление исполнителем Чертёжник
Управление исполнителем Чертёжник Обобщение педагогического опыта по теме Формирование действий самоконтроля и самооценки
Обобщение педагогического опыта по теме Формирование действий самоконтроля и самооценки Москва -Третий Рим
Москва -Третий Рим Творческая работа учеников 9 класса Желудок химический реактор
Творческая работа учеников 9 класса Желудок химический реактор Софисты. Концептуальные основы противостояния позиций Сократа и софистов
Софисты. Концептуальные основы противостояния позиций Сократа и софистов Классный час За здоровый образ жизни жителей Кубани в начальных классах
Классный час За здоровый образ жизни жителей Кубани в начальных классах Конкурс кабинетов информатики
Конкурс кабинетов информатики Адаптация организмов к окружающей среде
Адаптация организмов к окружающей среде Занятие 33
Занятие 33 Өкпе және плевра аурулары
Өкпе және плевра аурулары Газовый редуктор
Газовый редуктор Учебно-методическое пособиеКРАСНАЯ КНИГА
Учебно-методическое пособиеКРАСНАЯ КНИГА Diplom_1
Diplom_1 Электроизмерительные приборы
Электроизмерительные приборы