Содержание
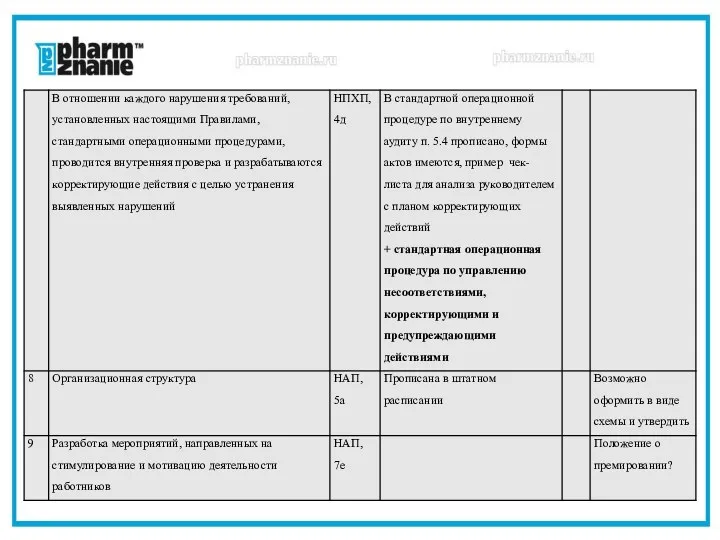
- 8. Корректирующие действия должны быть адекватными последствиям выявленных несоответствий Организация должна определить требования: к анализу несоответствий (включая
- 9. Внутренние проверки В аптечной организации должна быть создана система качества, о чем прописано в правилах надлежащих
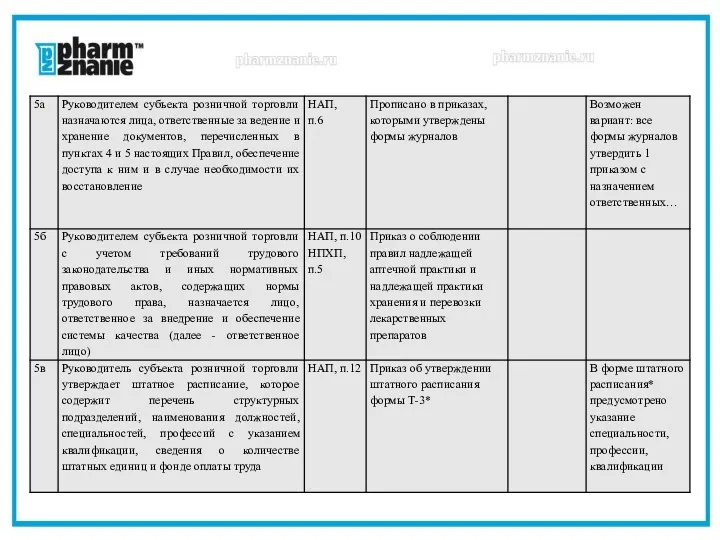
- 10. 4. Документация системы качества… включает в том числе: з) акты проверок субъекта розничной торговли должностными лицами
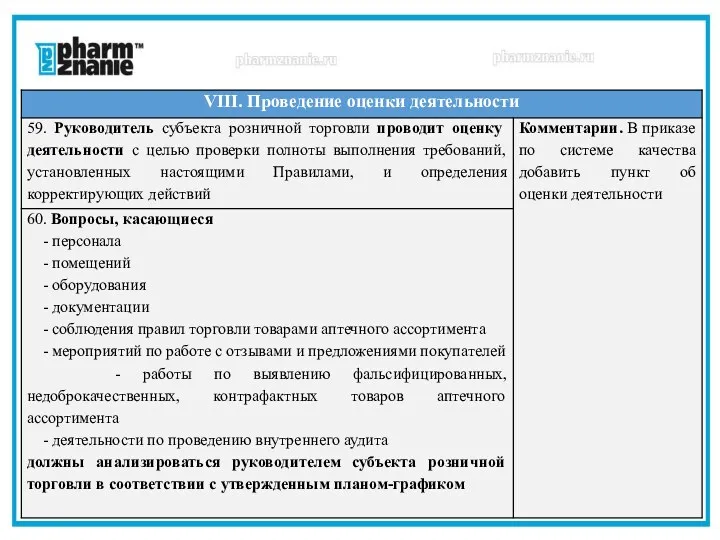
- 11. VIII. Проведение оценки деятельности 59. Руководитель субъекта розничной торговли проводит оценку деятельности с целью проверки полноты
- 12. 61. Внутренний аудит должен проводиться независимо и тщательно специально назначенными руководителем субъекта розничной торговли лицами, состоящими
- 13. 63. Внутренний аудит проводится также с целью выявления недостатков по выполнению требований законодательства Российской Федерации и
- 14. 67. Руководитель субъекта розничной торговли должен постоянно повышать результативность системы качества, используя в том числе результаты
- 15. Внутренний аудит проводится с целью выявления недостатков по выполнению требований законодательства Российской Федерации и несоблюдения внутренних
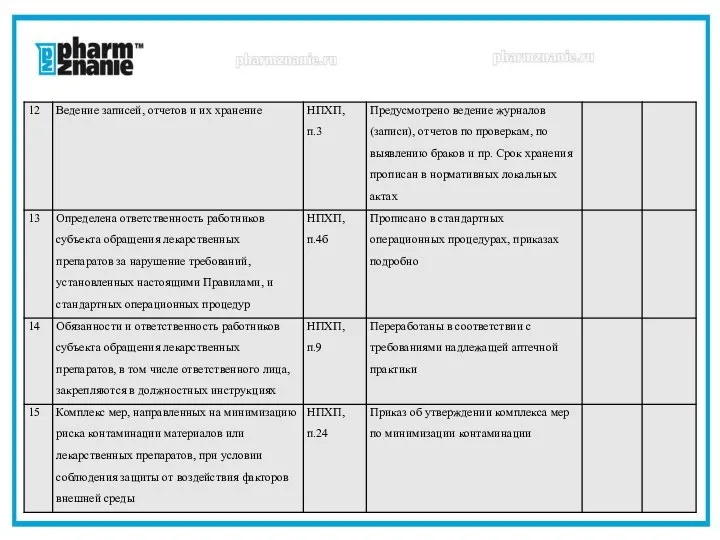
- 16. Уполномоченный по качеству (ответственное лицо за систему качества) несет ответственность, за разработку и своевременную актуализацию стандартных
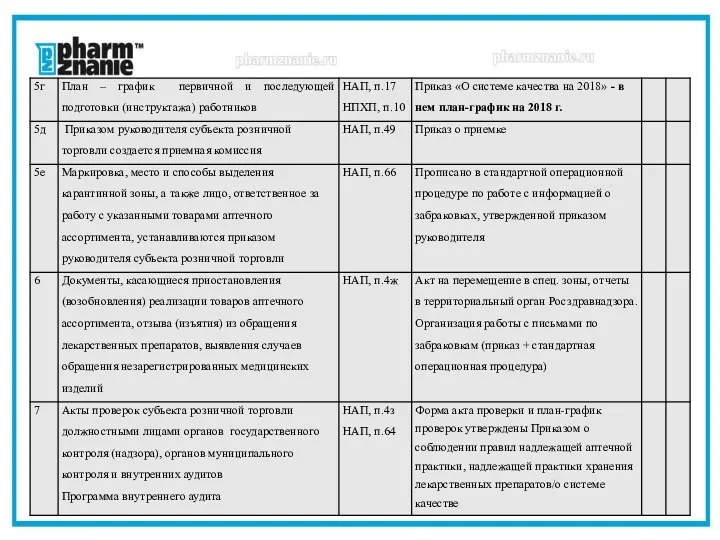
- 17. В начале календарного года утверждается план-график проведения внутренних проверок, устанавливается периодичность (частота и месяц проведения), тема
- 18. Если нет возможности независимой внутренней проверки уполномоченным по качеству (например, в аптеке заведующий является и уполномоченным
- 19. Как определиться с темами внутренних проверок? В связи с тем, что до 31 декабря ежегодно на
- 20. В случае, если ожидаются плановые проверки надзорных органов, в план-график внутренних проверок в обязательном порядке включаются
- 21. Кроме плана – графика необходимо составить т.н. «программу аудита» - Акт внутренней проверки Необходимо разработать и
- 22. В настоящее время действуют приказы Росздравнадзора № 9438 от 09.11.2017 г. «Об утверждении форм проверочных листов
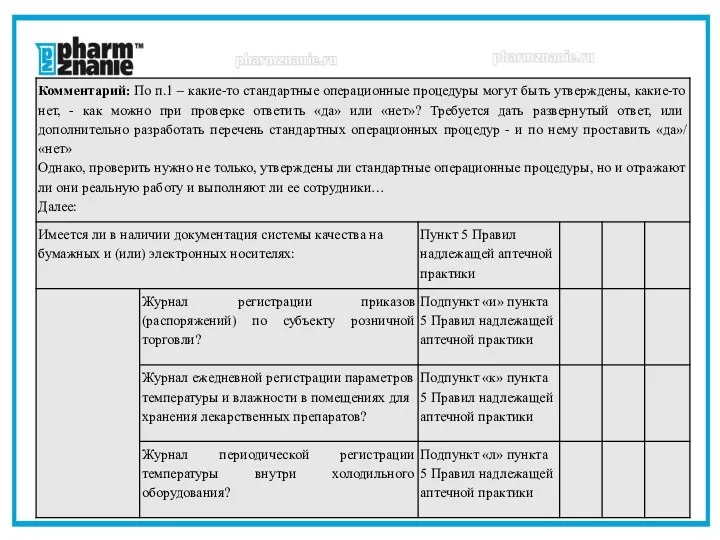
- 23. Например, в чек - листе по хранению лекарственных препаратов для аптеки:
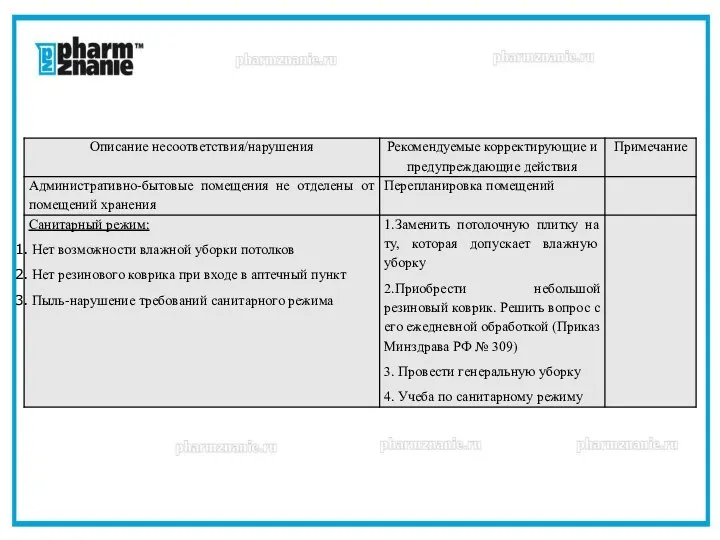
- 25. Если применить только чек-лист и отметить «есть», то где и как можно отразить замечания/нарушения по ведению
- 26. Помещения и оборудование - Административно-бытовые помещения не отделены от помещений хранения - Есть аптеки, где товар
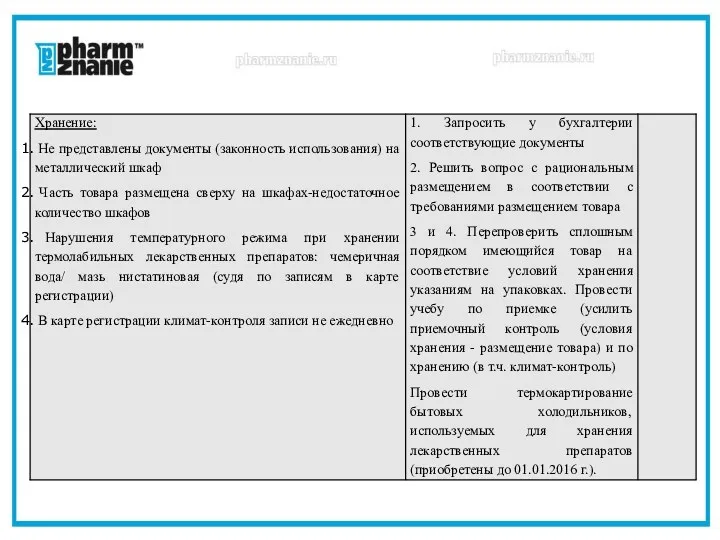
- 27. Климат-контроль - В журналах/картах регистрации учет ведется не ежедневно. В этом случае нужно приобретать терморегистраторы (логгеры)
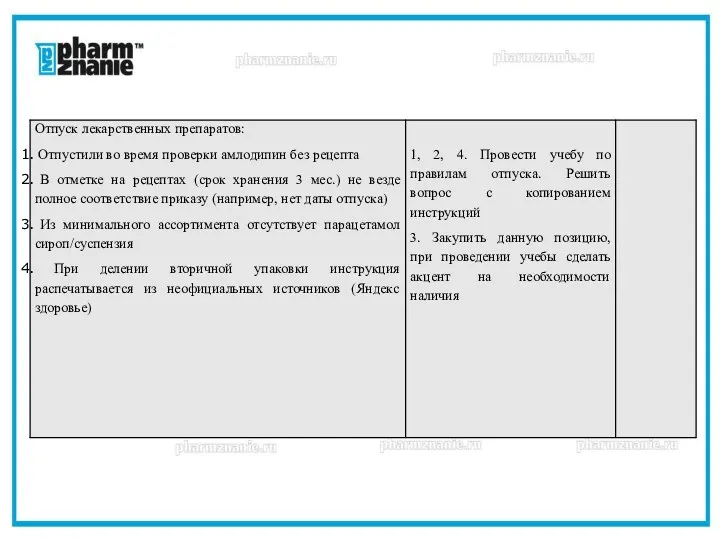
- 28. Отпуск лекарственных препаратов - При проверке рецептов, оставленных в аптеке (хранение 3 мес.) выявлены нарушения в
- 29. Предметно-количественный учет - Выявлены нарушения по заполнению журналов (например, в журнале учета прекурсоров в графа «фактический
- 30. Документы, составленные по результатам аудита, должны включать в себя всю полученную информацию и предложения по необходимым
- 31. Федеральный закон № 195-ФЗ от 30.12.2001 г. «Кодекс Российской Федерации об административных правонарушениях» Глава 14. АДМИНИСТРАТИВНЫЕ
- 32. 4. Осуществление предпринимательской деятельности с грубым нарушением требований и условий, предусмотренных специальным разрешением (лицензией), влечет наложение
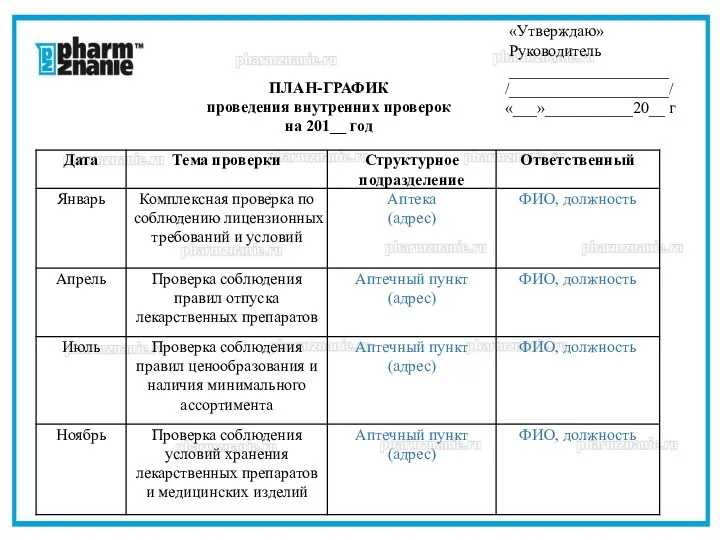
- 33. «Утверждаю» Руководитель ____________________ /____________________/ «___»___________20__ г ПЛАН-ГРАФИК проведения внутренних проверок на 201__ год
- 34. А К Т внутренней проверки Аптеки/аптечного пункта _______________________________________________ (наименование организации) расположен___ по адресу:_______________________________________________________________ «____»_________________20__ г. Цель:
- 35. Проверка соблюдения требований при обращении лекарственных препаратов Проверено по чек – листам: 1. Хранение лекарственных препаратов
- 36. При проверке _____________________________ лекарственных препаратов с истекшим сроком годности - выявлено/не выявлено При выборочной проверке нарушений
- 37. При выборочной проверке соблюдения правил ценообразования, оформления протоколов согласования цен на жизненно необходимые и важнейшие лекарственные
- 38. Проверена документация системы качества, в т.ч. наличие: - приказов по основной деятельности - стандартных операционных процедур
- 39. Отчет по результатам внутренней проверки Аптеки/ аптечного пункта _______________________________________________________, расположенного по адресу _______________________________________________________ Проверка проведена:_____________________________________________________________________ (должность,
- 40. Соблюдение сроков хранения документации________________________________________ ______________________________________________________________________________ Предлагаемые корректирующие действия __________________________________________ ____________________________________________________________________________________________________________________________________________________________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Предлагаемые предупреждающие мероприятия _____________________________________ ______________________________________________________________________________
- 41. Заключение по результатам проверки __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ С результатами проверки ознакомлены____________________________________________ ______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ «______»_____________20____г. _________________/______________/
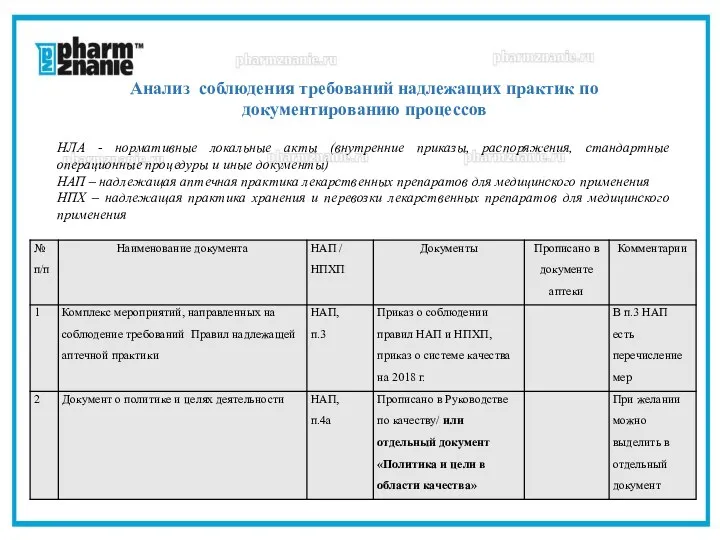
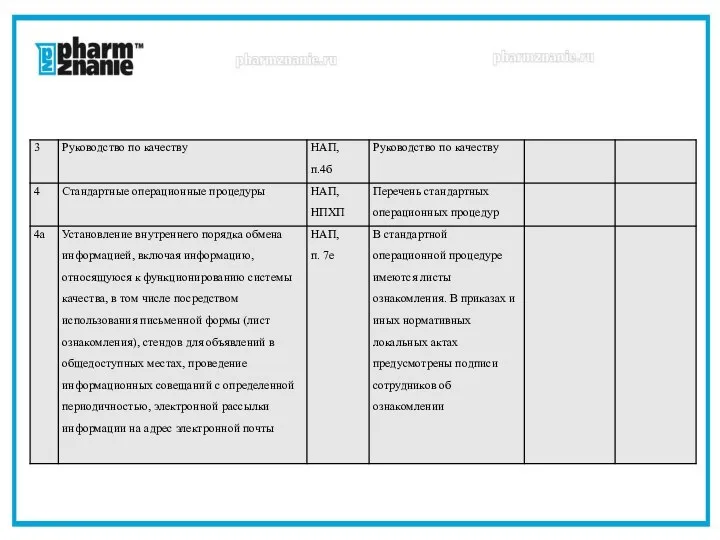
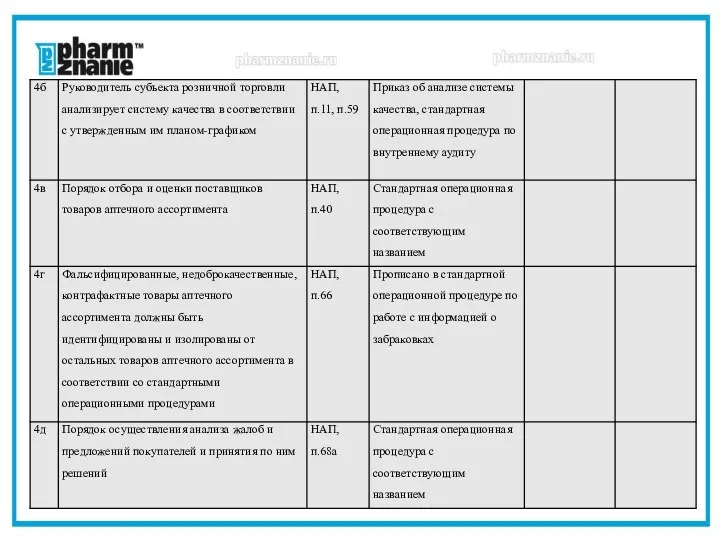
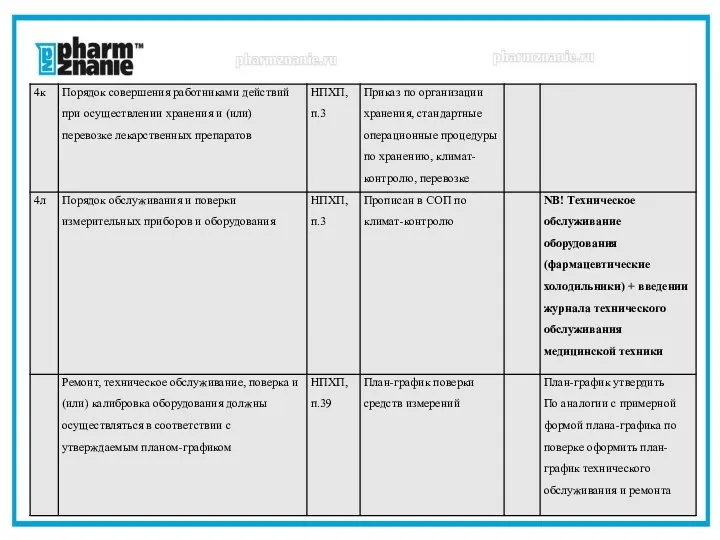
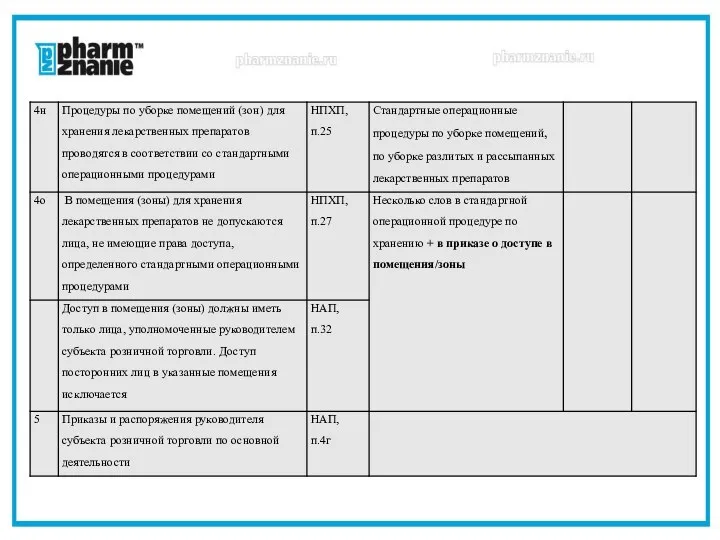
- 42. Анализ соблюдения требований надлежащих практик по документированию процессов НЛА - нормативные локальные акты (внутренние приказы, распоряжения,
- 53. Отчет по результатам внутренней проверки Аптеки/ аптечного пункта _______________________________________________ расположенного по адресу ______________________________________________ Проверка проведена ____________________________________________________
- 58. Заключение по результатам проверки: требования при осуществлении фармацевтической деятельности соблюдаются не в полной мере С результатами
- 60. Скачать презентацию










































 Местное самоуправление
Местное самоуправление Договор подряда
Договор подряда О мероприятиях по обеспечению избирательных прав граждан Российской Федерации, являющихся инвалидами, при проведении выборов
О мероприятиях по обеспечению избирательных прав граждан Российской Федерации, являющихся инвалидами, при проведении выборов Органы государственной власти РФ
Органы государственной власти РФ Сексуальная толерантность
Сексуальная толерантность Конституционное право
Конституционное право Президент Российской Федерации
Президент Российской Федерации Криминалистическое исследование документов. Почерк. Тема 13
Криминалистическое исследование документов. Почерк. Тема 13 ВКР: Институт условно - досрочного освобождения от отбывания наказания в уголовном праве
ВКР: Институт условно - досрочного освобождения от отбывания наказания в уголовном праве Система оценки соответствия продукции в Евразийском экономическом союзе. Технические регламенты
Система оценки соответствия продукции в Евразийском экономическом союзе. Технические регламенты Права и обязанности граждан
Права и обязанности граждан Розробка планів локалізації та ліквідації аварійних ситуацій і аварій
Розробка планів локалізації та ліквідації аварійних ситуацій і аварій Организационно-правовая основа управления дошкольной образовательной организацией
Организационно-правовая основа управления дошкольной образовательной организацией Международное частное право. Общие понятия: коллизионные нормы
Международное частное право. Общие понятия: коллизионные нормы Этика поведения оратора в судебном процессе. Диалогизация речи, общение со слушателями
Этика поведения оратора в судебном процессе. Диалогизация речи, общение со слушателями Федеральный закон от 28 декабря 2013 г. N 442-ФЗ Об основах социального обслуживания граждан в Российской Федерации
Федеральный закон от 28 декабря 2013 г. N 442-ФЗ Об основах социального обслуживания граждан в Российской Федерации Члены избирательных комиссий с правом совещательного голоса, наблюдатели на выборах, референдумах
Члены избирательных комиссий с правом совещательного голоса, наблюдатели на выборах, референдумах Нотариальное производство и его принципы. Общие правила нотариального производства
Нотариальное производство и его принципы. Общие правила нотариального производства Муниципальная реформа в Российской Федерации
Муниципальная реформа в Российской Федерации f2c593d1810b4241bab4ee136d2666de
f2c593d1810b4241bab4ee136d2666de Перечень документов, предоставляемых родителями
Перечень документов, предоставляемых родителями Прокурорский надзор за исполнением законодательства о труде
Прокурорский надзор за исполнением законодательства о труде Глобальная инициатива по отчетности (Global Reporting Initiative, GRI). Противоречия и проблемы КСО
Глобальная инициатива по отчетности (Global Reporting Initiative, GRI). Противоречия и проблемы КСО Конституционно-правовые основы организации судебной власти в Российской Федерации. Тема 16
Конституционно-правовые основы организации судебной власти в Российской Федерации. Тема 16 Защита прав потребителей
Защита прав потребителей Охрана труда
Охрана труда Конституционные основы судебной власти
Конституционные основы судебной власти Трудова дисципліна. Відповідальність за порушення трудового законодавства
Трудова дисципліна. Відповідальність за порушення трудового законодавства