Химические свойства. Аминокислоты проявляют свойства оснований за счет аминогруппы и свойства
кислот за счет карбоксильной группы, т.е. являются амфотерными соединениями. Подобно аминам, они реагируют с кислотами с образованием солей аммония:
H2N–CH2–COOH + HCl -> Cl- [H3N–CH2–COOH]+
Как карбоновые кислоты они образуют функциональные производные:
а) соли
H2N–CH2–COOH + NaOH -> H2N–CH2–COO- Na+ + H2O
б) сложные эфиры
Кроме того, возможно взаимодействие амино- и карбоксильной групп как внутри одной молекулы (внутримолекулярная реакция), так и принадлежащих разным молекулам (межмолекулярная реакция).
Межмолекулярное взаимодействие a-аминокислот приводит к образованию пептидов. При взаимодействии двух a-аминокислот образуется дипептид.
Межмолекулярное взаимодействие трех a-аминокислот приводит к образованию трипептида и т.д.
Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH - пептидной связью.
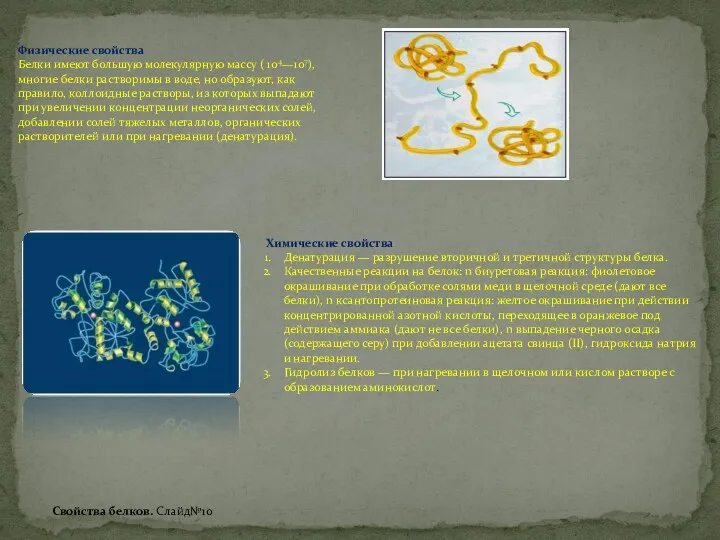
Физические свойства. Аминокислоты – твердые кристаллические вещества с высокой т.пл., при плавлении разлагаются. Хорошо растворимы в воде, водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе.
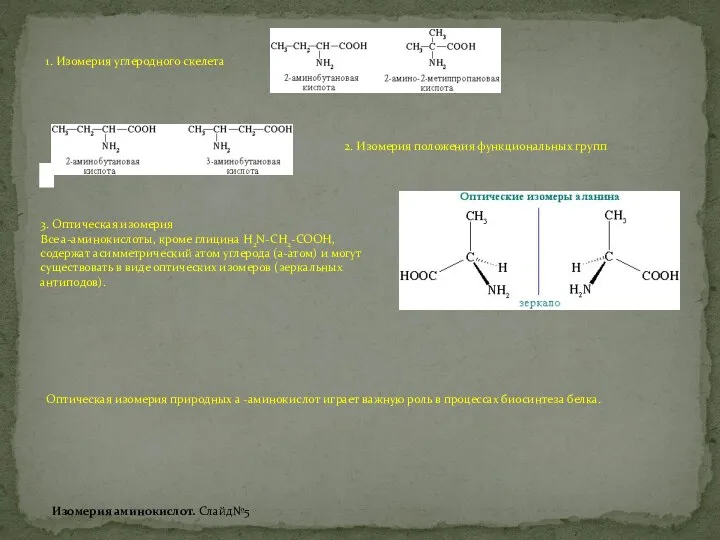
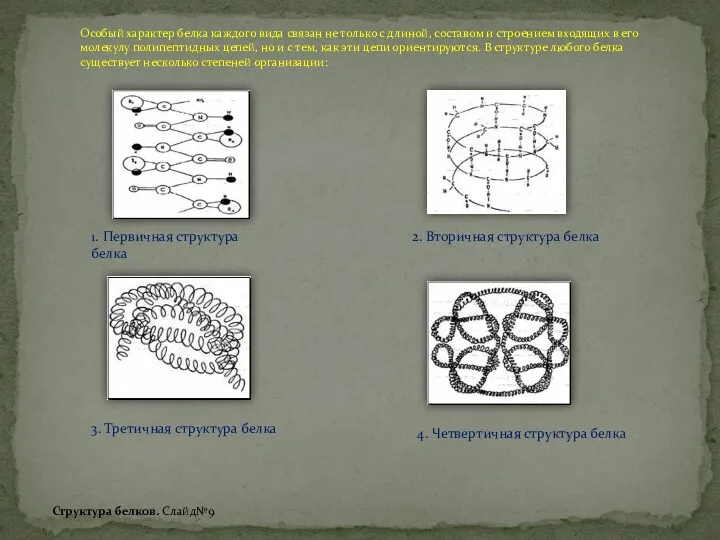
Свойства аминокислот. Слайд№6






 Половое размножение животных
Половое размножение животных Раздражимость. 6 класс
Раздражимость. 6 класс Бактерии. Группы бактерий. Размножение бактерий
Бактерии. Группы бактерий. Размножение бактерий Осінь. Осінні зміни в природі
Осінь. Осінні зміни в природі Тип хордовые
Тип хордовые Майстерність маскування
Майстерність маскування Человек, как биологический вид. Этапы антропогенеза
Человек, как биологический вид. Этапы антропогенеза Желілер типіне қысқаша сипаттама.Бассүйексіздер өкілдері
Желілер типіне қысқаша сипаттама.Бассүйексіздер өкілдері Презентация к уроку Класс Хрящевые рыбы
Презентация к уроку Класс Хрящевые рыбы Эндокринная система
Эндокринная система Животный мир Харьковской области
Животный мир Харьковской области Маленькие хитрости для улучшения умственной деятельности
Маленькие хитрости для улучшения умственной деятельности Биология. Классическая биология. Физико-химическая биология. Эволюционная биология
Биология. Классическая биология. Физико-химическая биология. Эволюционная биология Сравнение механизма действия некоторых популярных антацидных лекарственных препаратов. Кислотность
Сравнение механизма действия некоторых популярных антацидных лекарственных препаратов. Кислотность Зимующие птицы. Сбор информации
Зимующие птицы. Сбор информации Развитие скелета конечностей
Развитие скелета конечностей Размножение растений
Размножение растений Особливості будови грибів. Лабораторне дослідження №14
Особливості будови грибів. Лабораторне дослідження №14 Ткани растений
Ткани растений Альвеолата. Инфузории
Альвеолата. Инфузории Первичноназемные позвоночные амниоты. Класс рептилии
Первичноназемные позвоночные амниоты. Класс рептилии Человек и домашние животные
Человек и домашние животные АСҚ пайдаланылу жолдары
АСҚ пайдаланылу жолдары Урок - путешествие: Хрящевые морей и океанов
Урок - путешествие: Хрящевые морей и океанов Травмування та пошкодження хворобами і шкідниками насіннєвого матеріалу
Травмування та пошкодження хворобами і шкідниками насіннєвого матеріалу Қан туралы мәлімет
Қан туралы мәлімет Водоплавающие птицы
Водоплавающие птицы Музей естественной истории
Музей естественной истории