Содержание
- 2. СПб 2002 План лекции 1. Биохимический состав печени 2. Особенности обменных процессов в печени 3. Механизмы
- 3. СПб 2002 Участие печени во всех видах метаболизма делает этот орган уникальным. Постоянно меняющаяся концентрация поступающих
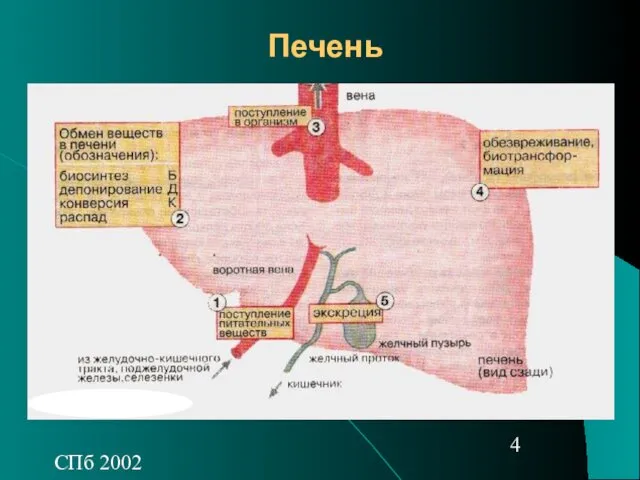
- 4. СПб 2002 Печень
- 5. СПб 2002 КЛЕТОЧНЫЙ СОСТАВ Гепатоциты 60% Купферовские клетки Эпителиальные клетки 40% Тканевые лимфоциты Жиросодержащие клетки
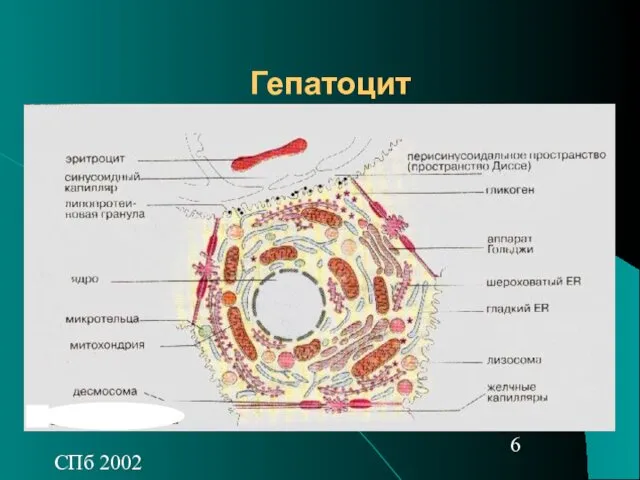
- 6. СПб 2002 Гепатоцит
- 7. СПб 2002 Гепатоциты содержат ядра, в которых 4 гр. ДНК Цитозоль 12 гр. РНК Митохондрии 18
- 8. СПб 2002 Химический состав печени Компонент % Вода 70-75 Сухой остаток 25-30 Белки 12-24 Углеводы 2-8
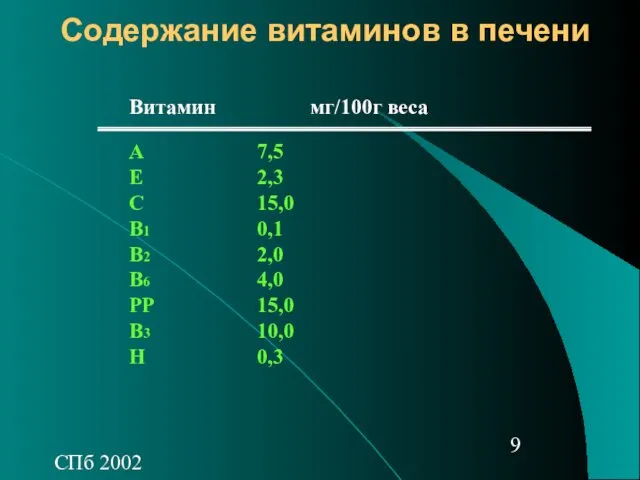
- 9. СПб 2002 Содержание витаминов в печени Витамин мг/100г веса А 7,5 Е 2,3 С 15,0 В1
- 10. СПб 2002 Минеральные компоненты печени Na, K, Ca, Mg, Fe, Cu
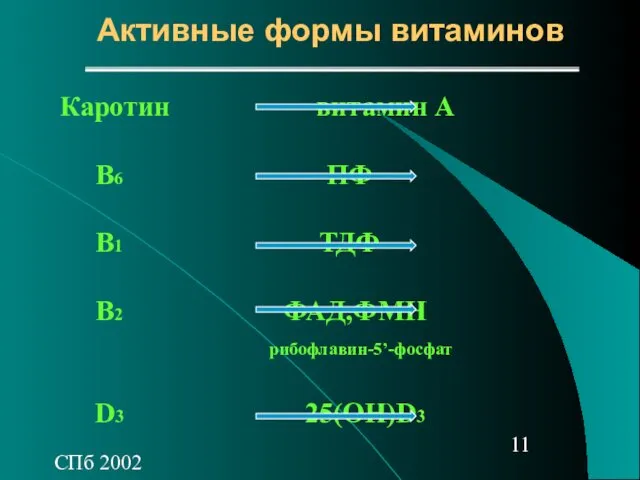
- 11. СПб 2002 Активные формы витаминов Каротин витамин А В6 ПФ В1 ТДФ В2 ФАД,ФМН рибофлавин-5’-фосфат D3
- 12. СПб 2002 ОСОБЕННОСТИ ХИМИЧЕСКОГО СОСТАВА ПЕЧЕНИ 1. По сравнению с другими органами в печени много углеводов
- 13. СПб 2002 Содержание отдельных компонентов в печени меняется при различной патологии. При отеках количество воды достигает
- 14. СПб 2002 РОЛЬ ПЕЧЕНИ В УГЛЕВОДНОМ ОБМЕНЕ Печень обеспечивает постоянную концентрацию глюкозы в крови 3.3-6.2 ммоль/л.
- 15. СПб 2002 Синтез гликогена Глюкоза Глюкозо-6-фосфат Глюкозо-1-фосфат УДФ-глюкоза УДФ УТФ Гликоген (С6Н10О5)n Гликоген (С6Н10О5)n+1 ПФ АТФ
- 16. СПб 2002 Синтез триглицеридов (при избытке глюкозы) Далее глюкоза включается в гликолитический путь 2ПВК аэр. усл.
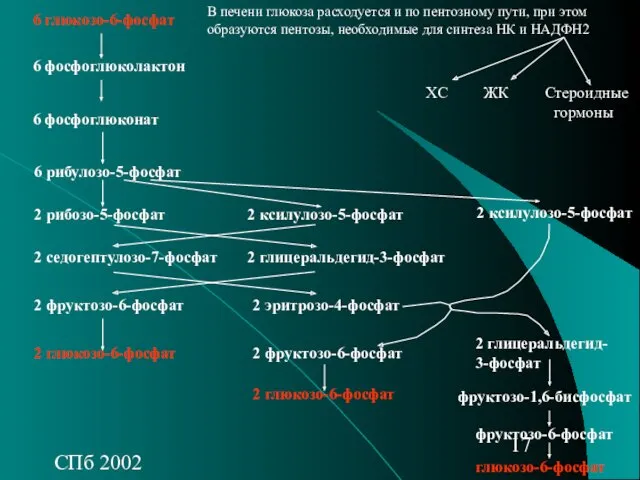
- 17. СПб 2002 В печени глюкоза расходуется и по пентозному пути, при этом образуются пентозы, необходимые для
- 18. СПб 2002 1. Распад гликогена Часть глюкозы в печени превращается в глюкуроновую кислоту, участвующую в обезвреживании
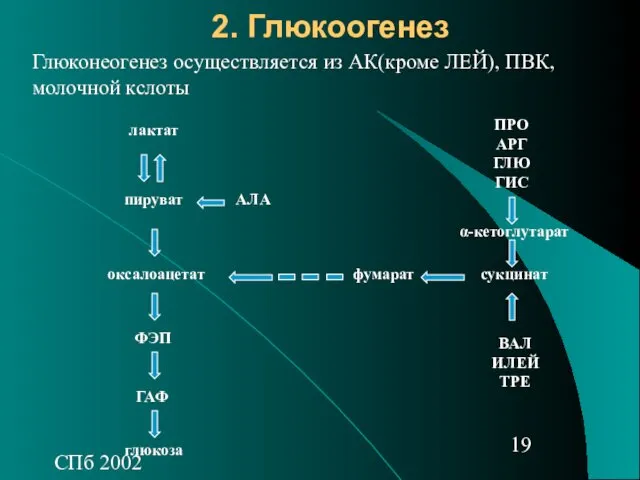
- 19. СПб 2002 2. Глюкоогенез Глюконеогенез осуществляется из АК(кроме ЛЕЙ), ПВК, молочной кслоты
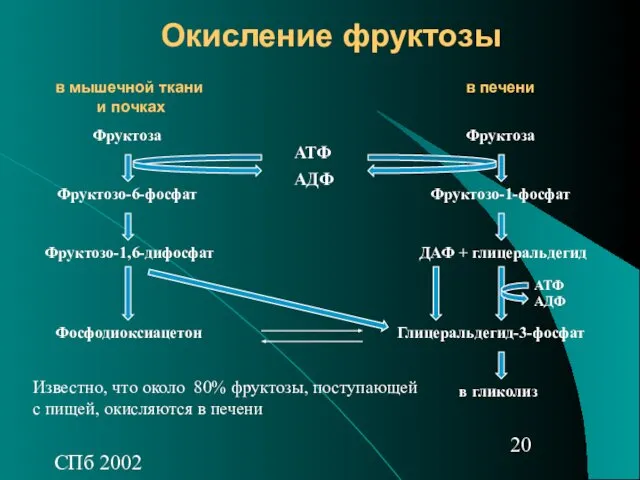
- 20. СПб 2002 Окисление фруктозы Фруктоза Фруктозо-6-фосфат Фруктозо-1,6-дифосфат Фруктоза Фруктозо-1-фосфат ДАФ + глицеральдегид в мышечной ткани и
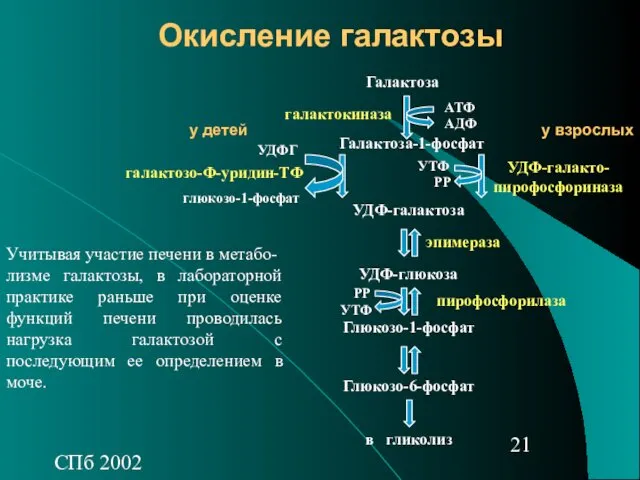
- 21. СПб 2002 Окисление галактозы Учитывая участие печени в метабо- лизме галактозы, в лабораторной практике раньше при
- 22. СПб 2002 Метаболизм глюкозы 3% глюкозы в гликоген 30% глюкозы в жирные кислоты 70% глюкозы окисляется
- 23. СПб 2002 Роль печени в липидном обмене
- 24. СПб 2002 Состав жёлчи Показатель % Жёлчные кислоты 50-70 ФЛ 20-25 ХС 5 Билирубин 2 Белки
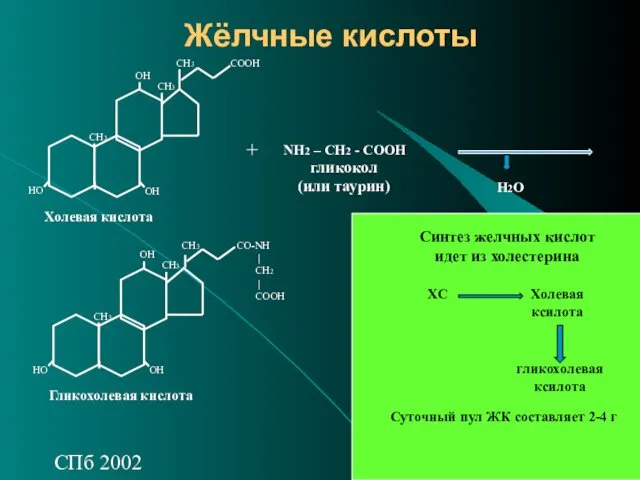
- 25. СПб 2002 Жёлчные кислоты ОН НО ОН СН3 СН3 СН3 СООН Холевая кислота NH2 – CH2
- 26. СПб 2002 Химический состав желчи Показатель Печеночная (г/л) Пузырная (г/л) Сухое вещество 23-33 180 Азот 0,8
- 27. СПб 2002 Роль желчных кислот Поступившие в кишечник ЖК: - эмульгируют жиры, облегчая действие липазы -
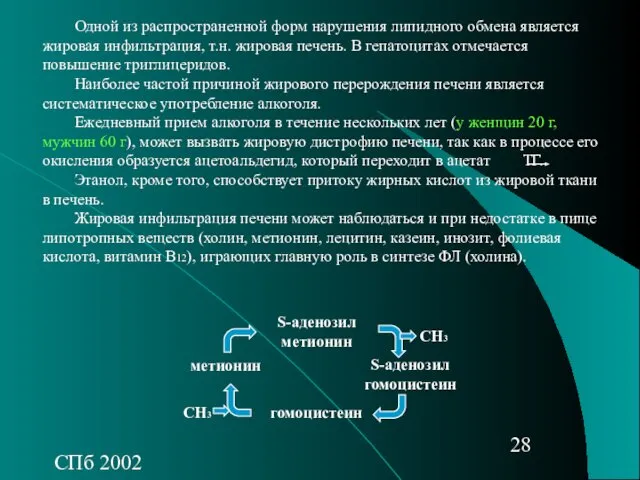
- 28. СПб 2002 Одной из распространенной форм нарушения липидного обмена является жировая инфильтрация, т.н. жировая печень. В
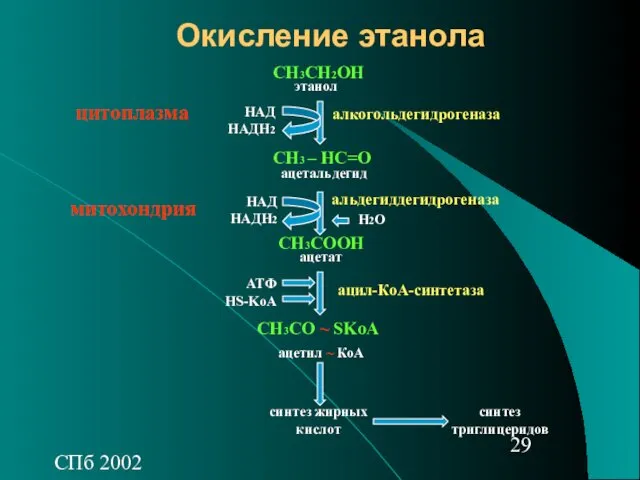
- 29. СПб 2002 Окисление этанола СН3СН2ОН СН3 – НС=О СН3СOОH СН3СO ~ SKoA АТФ HS-KoA НАД HАДН2
- 30. СПб 2002 Роль печени в белковом обмене В гепатоцитах печени синтезируются: весь альбумин факторы свертывания крови
- 31. СПб 2002 Ферменты печени АсАТ и АлАТ щелочная фосфатаза ЛДГ (4 и 5) изоцитрДГ ХЭ ЛАП
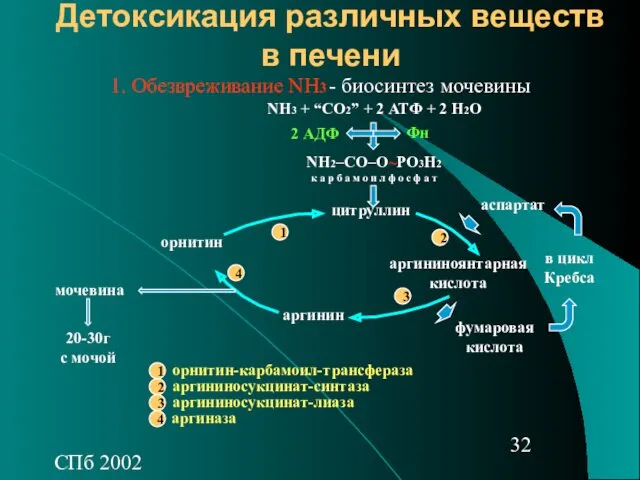
- 32. СПб 2002 Детоксикация различных веществ в печени - биосинтез мочевины NH3 + “CO2” + 2 АТФ
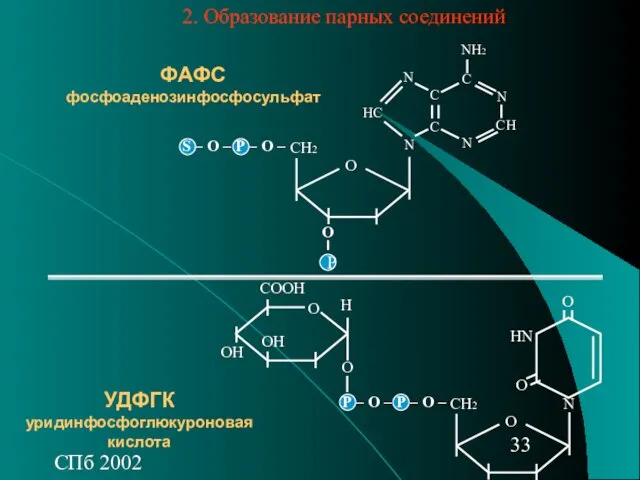
- 33. СПб 2002 О CH2 S – О – Р – O – N N HC C
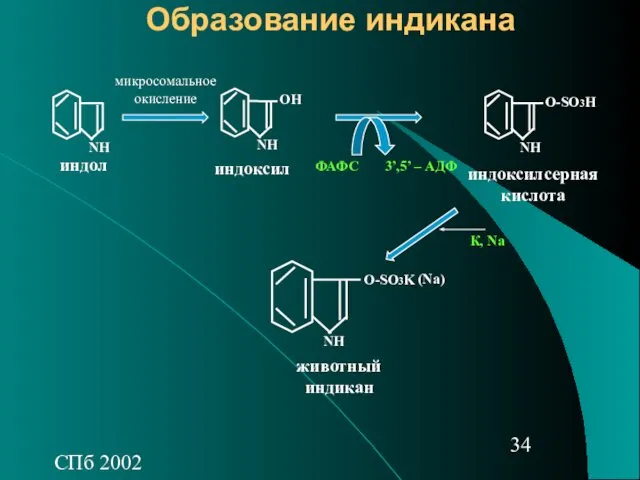
- 34. СПб 2002 Образование индикана индоксил индол индоксилсерная кислота NH О-SO3K животный индикан ФАФС 3’,5’ – АДФ
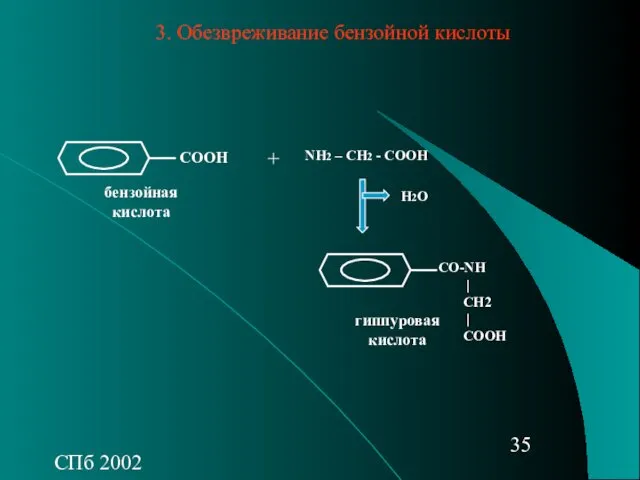
- 35. СПб 2002 СООН NH2 – CH2 - COOH + СО-NH | CH2 | СООH H2O бензойная
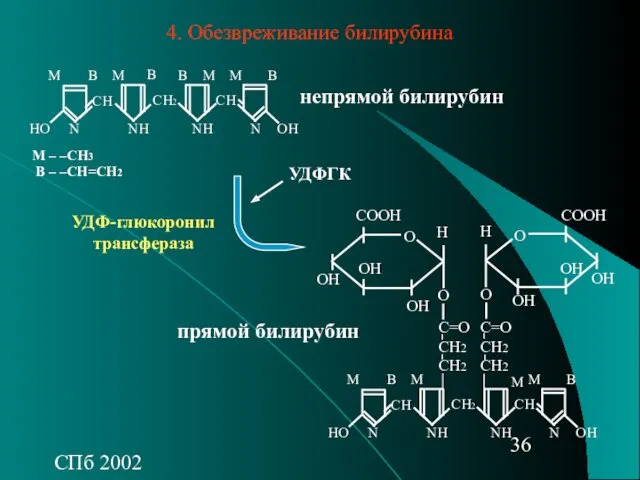
- 36. СПб 2002 СН СН2 СН ОН НО NН NН N N M – –CH3 B –
- 37. СПб 2002 5. Белковые гормоны инактивируются путем протеолиза 6. Гормоны щитовидной железы подвергаются дейодированию, дезаминированию, разрыву
- 38. СПб 2002 Гепатотоксические лекарственные вещества АНТИБИОТИКИ: - тетрациклины; - макролиды; - циклические полипептиды; - левомицетины; СУЛЬФАНИЛАМИДЫ:
- 39. СПб 2002 Учитывая, различие химической природы лекарственных веществ, невозможно представить какой-то единый метаболизм их обезвреживания. В
- 40. СПб 2002 Микросомальное окисление НАДФ-Н+Н+ НАДФ+ ФАД ФАД-Н2 Fe (II) белок Fe (III) белок Fe (III)
- 41. СПб 2002 Имеется точка зрения, что разная чувствительность людей к лекарственным препаратам определяется содержанием в печени
- 42. СПб 2002 Роль печени в пигментном обмене Печени принадлежит ведущая роль в распаде окрашенных сложных белков
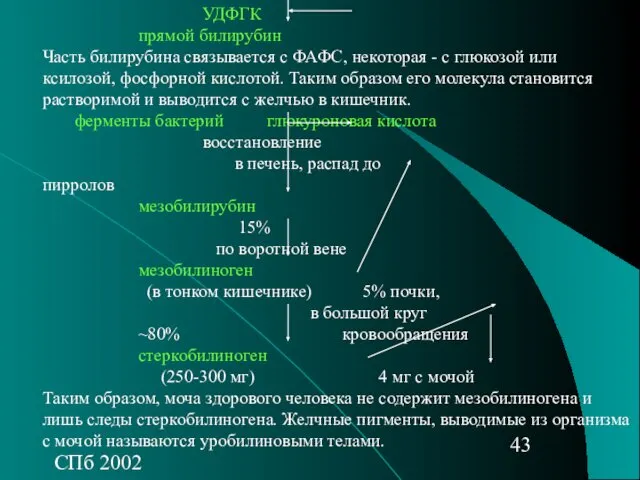
- 43. СПб 2002 УДФГК прямой билирубин Часть билирубина связывается с ФАФС, некоторая - с глюкозой или ксилозой,
- 44. СПб 2002 Основной источник желчных пигментов Hb эритроцитов 85% другие хромопротеиды 10% разрушение созревшие эритроциты 5%
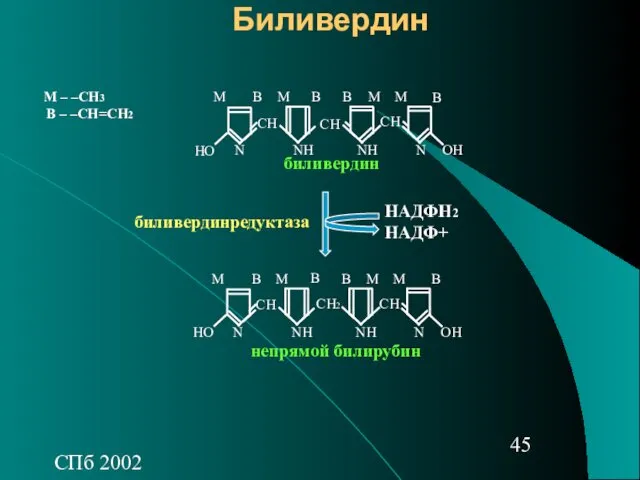
- 45. СПб 2002 Биливердин СН СН2 СН ОН НО NН NН N N M – –CH3 B
- 46. СПб 2002 Лабораторная диагностика желтух НАДПЕЧЕНОЧНАЯ (ГЕМОЛИТИЧЕСКАЯ) N ЩФ, АлАТ, АсАТ, ГГТФ; повышение в крови непрямого
- 48. Скачать презентацию



























 Человек как результат биологической и социокультурной эволюции. Обществознание. 10 класс
Человек как результат биологической и социокультурной эволюции. Обществознание. 10 класс Суцвіття
Суцвіття Морфология побега растений. Разнообразие побегов
Морфология побега растений. Разнообразие побегов Выращивание из семян растения мушмула
Выращивание из семян растения мушмула Своя игра. Мир растений
Своя игра. Мир растений Eukaryotic cell structure
Eukaryotic cell structure Экологическая характеристика организмов
Экологическая характеристика организмов Генная инженерия
Генная инженерия Фізіологія травлення
Фізіологія травлення Презентации к теме Химический состав клетки (5 класс)
Презентации к теме Химический состав клетки (5 класс) Биологическая игра Угадай растение
Биологическая игра Угадай растение Биотехнология, клеточная и генная инженерия. Клонирование
Биотехнология, клеточная и генная инженерия. Клонирование презентация к уроку Пищеварение в кишечнике
презентация к уроку Пищеварение в кишечнике Кинетика ферментативного катализа
Кинетика ферментативного катализа Домашний питомец, кот Мурзик
Домашний питомец, кот Мурзик Бесполое размножение клетки
Бесполое размножение клетки Строение и функции головного мозга человека
Строение и функции головного мозга человека Растениеводство. Клубнеплодные культуры
Растениеводство. Клубнеплодные культуры Миология. Мышечная ткань
Миология. Мышечная ткань Действие радиации на эмбрион и плод. Теоретические представления о механизме биологического действия ионизирующих излучений
Действие радиации на эмбрион и плод. Теоретические представления о механизме биологического действия ионизирующих излучений Основные понятия и законы генетики
Основные понятия и законы генетики Вторичный метаболизм растений
Вторичный метаболизм растений Продукты, полезные для глаз
Продукты, полезные для глаз Презентация Вирусы
Презентация Вирусы Викторина Анализаторы
Викторина Анализаторы Живые барометры, гигрометры и индикаторы
Живые барометры, гигрометры и индикаторы Размножение животных
Размножение животных Митоз — это деление клетки
Митоз — это деление клетки