Слайд 2

Биосинтез белка из 20 α-аминокислот происходит
в эндоплазматическом ретикулуме при помощи
сложной белок-синтезирующей системы:
рибосомы,
матричная («messenger» - посредник) РНК,
транспортные РНК,
белковые факторы трансляции,
ферменты трансляции,
макроэргические соединения (АТФ и ГТФ),
различные катионы.
Слайд 3

Биосинтез белка – это ферментативная полимеризация аминокислот, протекающая в следующей последовательности:
Активация
аминокислот.
Собственно трансляция включает этапы:
инициация трансляции;
элонгация трансляции;
терминация трансляции.
Слайд 4

Активация аминокислот.
Фермент: аминоацил-тРНК-синтетаза (АРСаза)
АК + тРНК + АТФ → АК-тРНК +
АМФ + ФФн
Аминокислота присоединяется
к концевой 3’-ОН транспортной тРНК (3’АСС…).
Для каждой из 20 аминокислот
существует специфическая
аминоацил-тРНК-синтетаза.
Слайд 5

2. Собственно трансляция
Инициация трансляции.
Синтез белка осуществляется на рибосомах (рибонуклеопротеины, надмолекулярные белковые
комплексы), которые:
- удерживают всю белок-синтезирующую систему,
- обеспечивают точность считывания (трансляции),
- катализируют образование пептидной связи.
Слайд 6
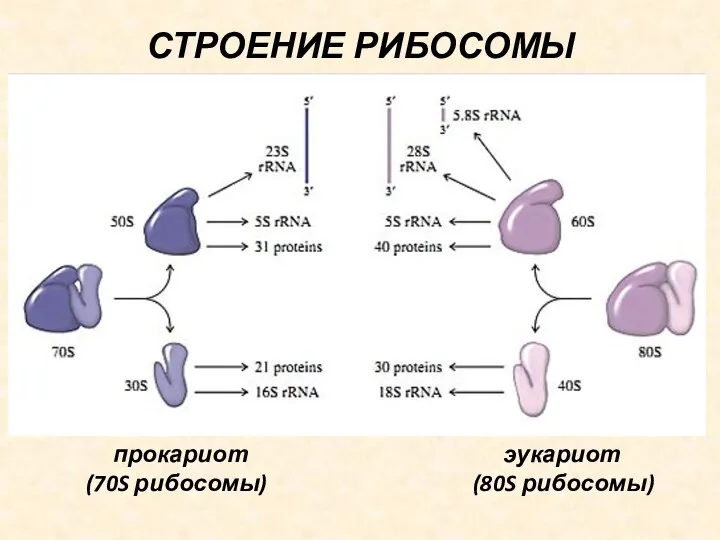
СТРОЕНИЕ РИБОСОМЫ
прокариот эукариот
(70S рибосомы) (80S рибосомы)
Слайд 7

Слайд 8

Инициация трансляции –
сборка всего комплекса белкового синтеза.
До начала трансляции субъединицы
рибосом находятся в диссоциированном состоянии.
Ассоциация малой и большой субъединицы происходят в присутствии мРНК.
Для инициации необходимо присутствие белковых факторов инициации IF.
Слайд 9
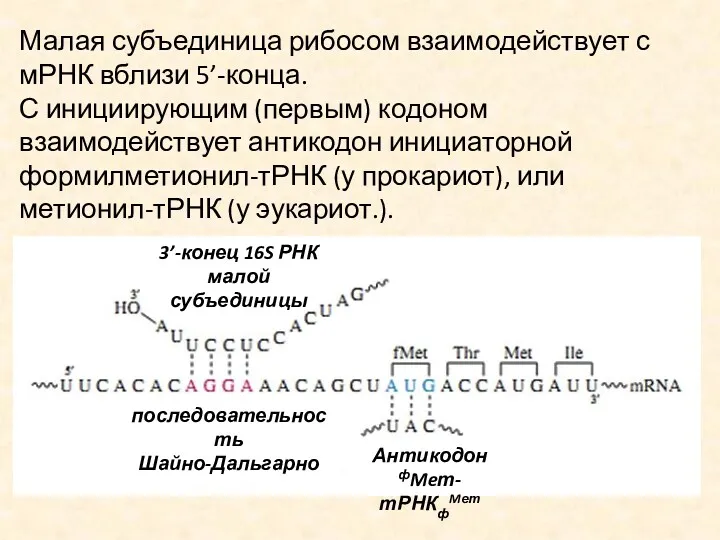
Малая субъединица рибосом взаимодействует с мРНК вблизи 5’-конца.
С инициирующим (первым) кодоном
взаимодействует антикодон инициаторной формилметионил-тРНК (у прокариот), или метионил-тРНК (у эукариот.).
Слайд 10
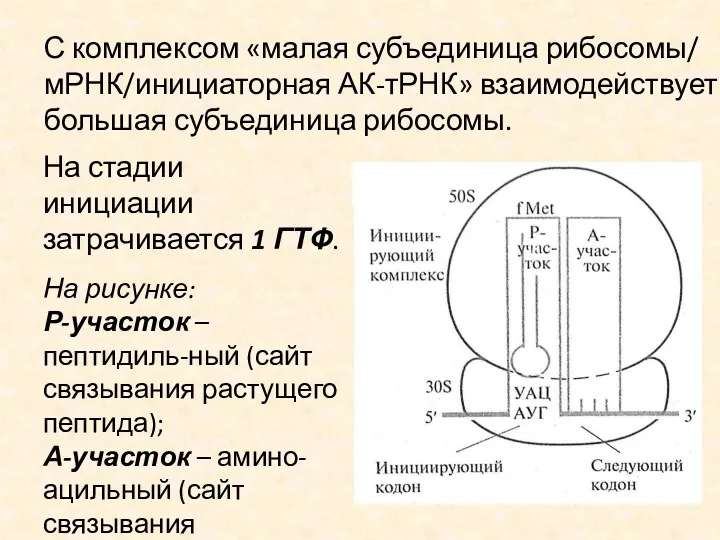
С комплексом «малая субъединица рибосомы/ мРНК/инициаторная АК-тРНК» взаимодействует большая субъединица рибосомы.
На
стадии инициации
затрачивается 1 ГТФ.
На рисунке:
Р-участок – пептидиль-ный (сайт связывания растущего пептида);
А-участок – амино-ацильный (сайт связывания следующей АК-тРНК).
Слайд 11

ЭЛОНГАЦИЯ ТРАНСЛЯЦИИ
Элонгация трансляции – удлинение цепи полипептида.
В элонгации принимают участие 3
белковых фактора элонгации EF (eEF).
Направление считывания информации с мРНК (направление движения рибосомы по мРНК)– 5’→3’.
Направление роста полипептидной цепи от N-конца к С-концу.
Слайд 12
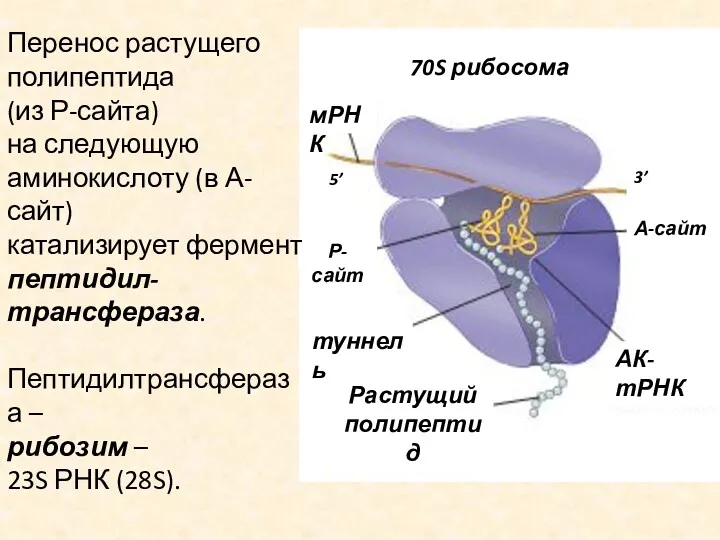
Растущий полипептид
АК-тРНК
3’
А-сайт
мРНК
5’
Р-сайт
туннель
70S рибосома
Перенос растущего
полипептида
(из Р-сайта)
на следующую
аминокислоту (в А-сайт)
катализирует
фермент
пептидил-
трансфераза.
Пептидилтрансфераза –
рибозим –
23S РНК (28S).
Слайд 13

После образования пептидной связи в А-сайте находится пептидил-тРНК, Р-сайт свободен.
Рибосома сдвигается
на 3 нуклеотида (кодон) в сторону 3’-конца – шаг рибосомы.
При этом пептидил-тРНК из А-сайта переносится
в Р-сайт – транслокация.
В А-сайте размещается новый кодон мРНК.
Энергетические затраты в процессе элонгации:
для удлинения цепи на 1 аминокислотный остаток требуется 2ГТФ.
Слайд 14

ТЕРМИНАЦИЯ ТРАНСЛЯЦИИ
Белковые факторы терминации RF.
Терминирующие кодоны: УАГ, УАА, УГА
После последнего шага
рибосомы в А-центр не поступает (не становится) АК-тРНК.
В результате транспептидазной реакции полипептид переносится на воду и освобождается из Р-сайта.
Рибосома диссоциирует на субъединицы.
Энергетические затраты – 1 ГТФ.
Слайд 15

nАК +nАТФ (активация) + ГТФ(инициация) +
+ ГТФ (терминация) + 2(n-1)
ГТФ (элонгация) →
→ полипептид + nАМФ + nФФн + 2nГДФ + 2nФн
Слайд 16

После синтеза полипептидная цепь подвергается фолдингу, в процессе которого белок приобретает
нативную конформацию, и посттрансляционной модификации (фосфорилированию, аденилирования, гликозилированию и др.) и транспортируется к месту функционирования.















 Nucleic acids
Nucleic acids Развитие органического мира на Земле
Развитие органического мира на Земле Эволюция опорно- двигательной системы у животных
Эволюция опорно- двигательной системы у животных Апаптоз кезіндегі молекулалық оқиғалардың жалпы сипаттамасы
Апаптоз кезіндегі молекулалық оқиғалардың жалпы сипаттамасы Минирующие насекомые. (Лекция 8)
Минирующие насекомые. (Лекция 8) Фотосинтез
Фотосинтез Уголок живой природы как средство формирования исследовательских способностей обучающихся по биологии
Уголок живой природы как средство формирования исследовательских способностей обучающихся по биологии Индивидуальное развитие организмов
Индивидуальное развитие организмов Информация и ее роль в обществе
Информация и ее роль в обществе Структура и содержание курса общей биологии. 10 класс
Структура и содержание курса общей биологии. 10 класс Бактериалық жасушаның химиялық құрамы
Бактериалық жасушаның химиялық құрамы Class ear
Class ear Среда обитания
Среда обитания Цветы. Уход за цветами
Цветы. Уход за цветами Цветочная карусель
Цветочная карусель Стадии онтогенеза почв
Стадии онтогенеза почв Дыхательная система
Дыхательная система Wild and domestic animals
Wild and domestic animals Лимфатическая система
Лимфатическая система Учебный проект Экспериментальное определение качества молочной продукции
Учебный проект Экспериментальное определение качества молочной продукции Животные Севера
Животные Севера Cад (окружающий мир, 1 класс)
Cад (окружающий мир, 1 класс) Эндокринная система человека
Эндокринная система человека Первоцветы. Биологические особенности раннецветущих растений
Первоцветы. Биологические особенности раннецветущих растений Дикая природа России
Дикая природа России Водоросли. Общая характеристика
Водоросли. Общая характеристика Сторінками Червоної книги України
Сторінками Червоної книги України Основные загрязнители почвы
Основные загрязнители почвы