Содержание
- 3. 1. Колориметрический способ основан на использовании кислотно-основных индикаторов, которые представляют собой слабые кислоты или основания, изменяющие
- 4. рН = 2 окраска красная рН = 3 окраска красно-оранжевая рН = 4 окраска оранжевая рН
- 5. 2. Электрометрический способ основан на измерении электродвижущей силы в гальваническом элементе, составленном из водородселективного электрода (обычно
- 6. В результате жизнедеятельности в организме ежесуточно образуется большое количество кислот. Во-первых, при усвоении белков, жиров и
- 7. Образование кислот характерно для некоторых патологических процессов. При диабетическом кетозе образуется до 1 моль эквивалента ацетоуксусной
- 8. Все выделяющиеся кислоты утилизируются тем или иным способом: кислотные остатки фосфорной кислоты образуют органические фосфаты и
- 9. Физико-химические расчеты показывают, что 0,15 моль СО2 достаточно для того, чтобы нарушить кислотно-основное равновесие организма человека
- 10. Буферной системой называют равновесную систему, способную поддерживать примерно на постоянном уровне какой-либо параметр при незначительных внешних
- 11. Важным является то, что концентрация этих кислот на несколько порядков превышает концентрацию Н3О+ и ОН-. 1-ый
- 12. 2-ой тип Раствор, содержащий одну или несколько буферных систем, называется буферным раствором.
- 13. Буферные растворы можно приготовить двумя способами: 1. Частичной нейтрализацией слабого электролита сильным СН3СООНизбыток + NaOH или
- 14. Буферные растворы можно приготовить двумя способами: 2. Смешивание растворов слабых электролитов с их солями (или двух
- 15. Чтобы понять механизм буферного действия рассмотрим равновесие – ионизацию слабой кислоты в водном растворе: НВ +
- 16. В соответствии с принципом смещения химического равновесия добавление в эту систему сильной кислоты или соли, содержащей
- 17. Если рассмотреть другое изолированное равновесие – гидролиз соли по аниону: В- + Н2О ↔ НВ +
- 18. При совмещении этих двух изолированных равновесий оказывается, что процессы, которые в них будут протекать при воздействии
- 19. Уравнение буферной системы – уравнение, выражающее зависимость рН буферного раствора от состава буферной системы.
- 20. Как видно из приведенного уравнения, рН буферного раствора зависит от: - природы слабого электролита; - температуры
- 21. Буферное действие сохраняется в определенном интервале значений рН (зона буферного действия) и зависит от соотношения концентраций
- 22. т.е. рН = рКа±1 Иначе, имея в распоряжении кислоту с рКа, можно приготовить буферные растворы, поддерживающие
- 23. Количественно буферное действие характеризуется буферной емкостью. Буферная емкость (В) равна количеству вещества эквивалента сильной кислоты или
- 24. Экспериментально буферную емкость можно определить титрованием буферной системы с последующим расчетом по уравнению: , где -
- 25. Буферная емкость будет тем больше, чем больше суммарная концентрация компонентов буферного раствора при постоянном соотношении их
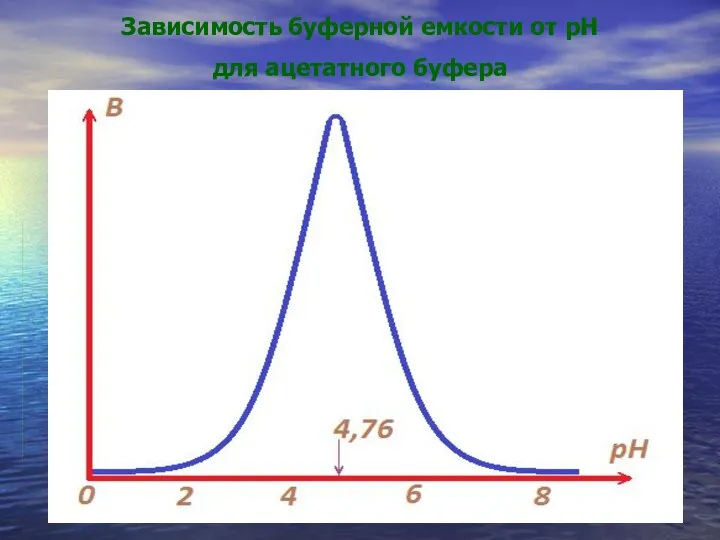
- 26. Зависимость буферной емкости от рН для ацетатного буфера
- 27. Значение рН различных систем
- 28. Значение рН, благоприятные для развития патогенных бактерий
- 29. В организме человека присутствуют различные буферные системы. Из них наиболее важными являются: гидрокарбонатная, гемоглобиновая, Фосфатная, белковая.
- 30. Гидрокарбонатная система образована оксидом углерода (IV) (как кислота) и гидрокарбонат-ионом (как сопряженное основание). Для гидрокарбонатного буфера
- 31. Гидрокарбонатный буфер является основной буферной системой плазмы крови и является системой быстрого реагирования, т.к. продукт его
- 32. Гемоглобиновая буферная система представлена двумя слабыми кислотами – гемоглобином и оксигемоглобином – и сопряженными им основаниями,
- 33. Фосфатная буферная система функционирует в основном в плазме. Она представлена ионами Н2РО (кислота) и НРО (основание).
- 34. В организме также функционируют и другие буферные системы: - белковая или протеиновая; - аминокислотная; - аммиачная
- 37. Скачать презентацию

































 Структурно-функциональная организация клетки
Структурно-функциональная организация клетки Улюблена домашня тварина
Улюблена домашня тварина Весна
Весна Статическая биохимия. Строение, свойства, биологическая роль углеводов и липидов
Статическая биохимия. Строение, свойства, биологическая роль углеводов и липидов Обмен веществ и превращение энергии в клетке
Обмен веществ и превращение энергии в клетке Приспособленность организмов к определенной среде обитания
Приспособленность организмов к определенной среде обитания Презентация Организация исследовательской работы
Презентация Организация исследовательской работы Вид и видообразование. (лекция 9-10)
Вид и видообразование. (лекция 9-10) Общие свойства живых организмов
Общие свойства живых организмов Тип Хордовые. Ланцетник 7 класс
Тип Хордовые. Ланцетник 7 класс Презентация Класс Млекопитающие
Презентация Класс Млекопитающие Пряно-вкусовые растения. Специи
Пряно-вкусовые растения. Специи Витамины
Витамины презентация к уроку Ветер
презентация к уроку Ветер Общие вопросы миологии. Мышцы головы и шеи
Общие вопросы миологии. Мышцы головы и шеи Овощеводство. Размножение овощных растений
Овощеводство. Размножение овощных растений Клетка. 10 класс
Клетка. 10 класс Мониторинг и профилактика здоровья старших школьников в средней школе №5
Мониторинг и профилактика здоровья старших школьников в средней школе №5 Контейнерное озеленение
Контейнерное озеленение Общие вопросы миологии мышцы головы и шеи
Общие вопросы миологии мышцы головы и шеи Эволюционная иммунология. Защитные системы прокариот
Эволюционная иммунология. Защитные системы прокариот Основные этапы антропогенеза
Основные этапы антропогенеза урок путешествие Многообразие Амфибий
урок путешествие Многообразие Амфибий Презентация Реализация принципа связи с жизнью в преподавании биологии в старшем звене
Презентация Реализация принципа связи с жизнью в преподавании биологии в старшем звене Мои дельфиниумы
Мои дельфиниумы Анатомо-физиологические особенности системы органов дыхания
Анатомо-физиологические особенности системы органов дыхания Селекция животных
Селекция животных Питательные вещества и природные пищевые компоненты-важный экологический фактор
Питательные вещества и природные пищевые компоненты-важный экологический фактор