Содержание
- 2. План лекции История учения о биологическом окислении. Современные представления о биологическом окислении. Тканевое дыхание, определение, этапы,
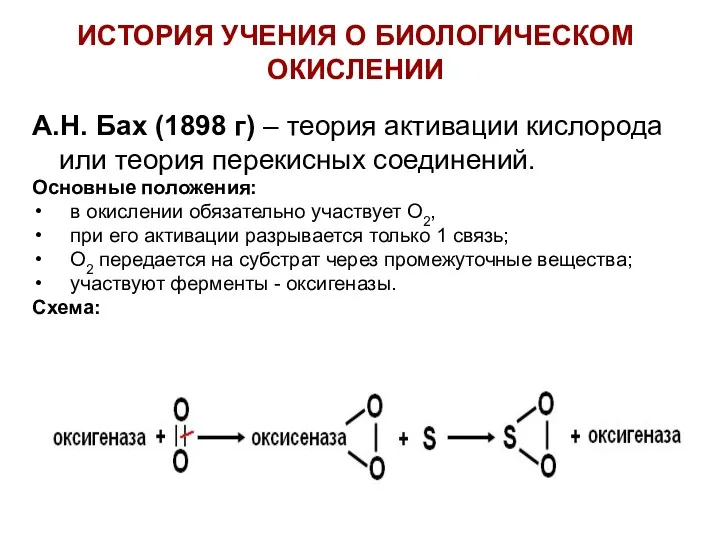
- 3. ИСТОРИЯ УЧЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ А.Н. Бах (1898 г) – теория активации кислорода или теория перекисных
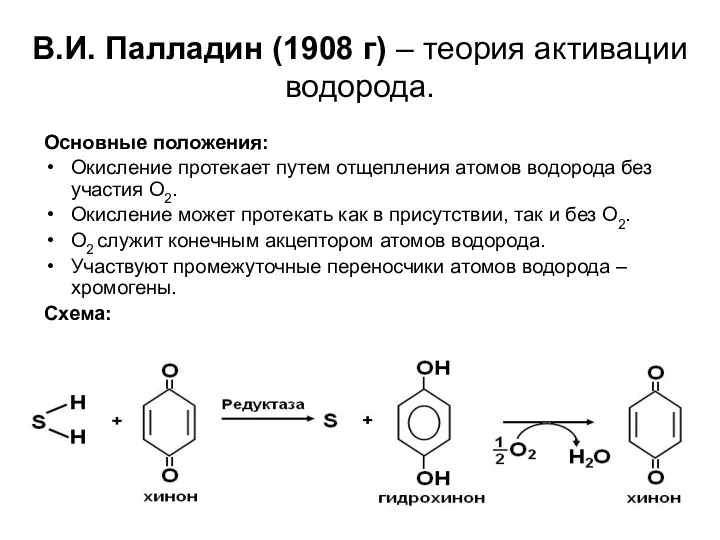
- 4. В.И. Палладин (1908 г) – теория активации водорода. Основные положения: Окисление протекает путем отщепления атомов водорода
- 5. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ И ТКАНЕВОМ ДЫХАНИИ. БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ – совокупность всех ОВР в живых
- 6. Тканевое дыхание комплекс аэробных окислительно-восстановительных реакций распада субстратов, сопровождающийся передачей протонов и электронов через дыхательную цепь
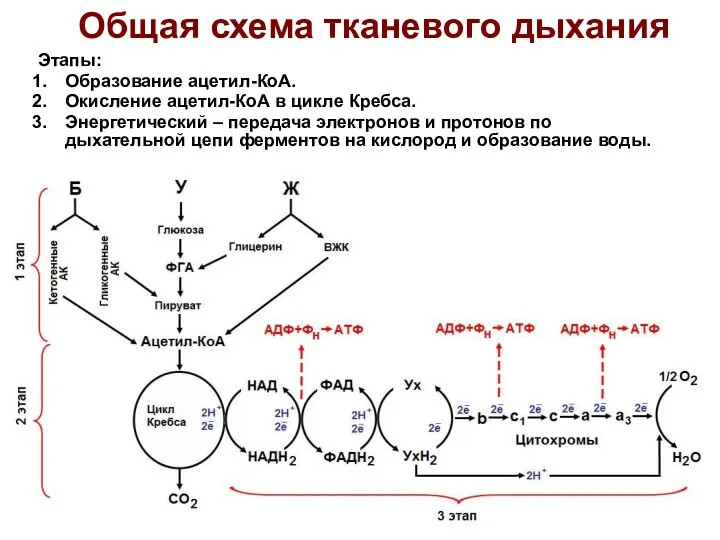
- 7. Общая схема тканевого дыхания Этапы: Образование ацетил-КоА. Окисление ацетил-КоА в цикле Кребса. Энергетический – передача электронов
- 8. Редокс-система Окисленная и восстановленная форма одного вещества. Примеры: НАД/НАДН2 ФАД/ФАДН2 Ух/УхН2
- 9. - это химическая характеристика способности вещества принимать и удерживать электроны. Выражается в вольтах (В). Самый низкий
- 10. Характеристика дыхательной цепи Состоит из 3 групп ферментов и низкомолекулярного витаминоподобного вещества – убихинона. Локализована на
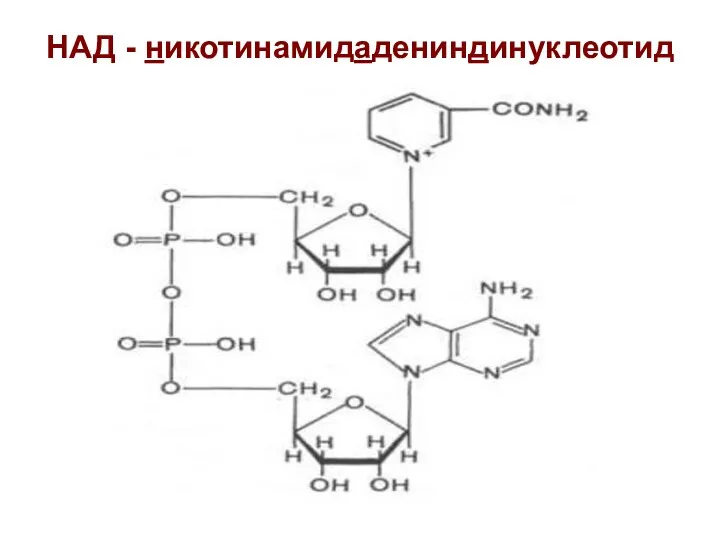
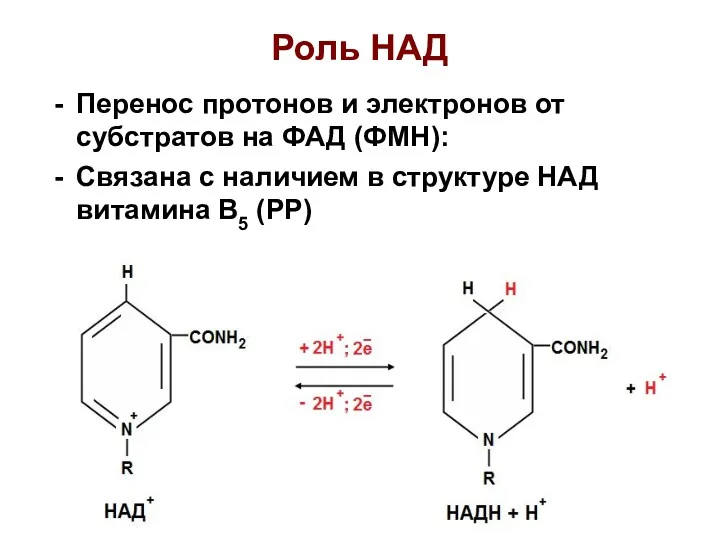
- 11. НАД - никотинамидадениндинуклеотид
- 12. Роль НАД Перенос протонов и электронов от субстратов на ФАД (ФМН): Связана с наличием в структуре
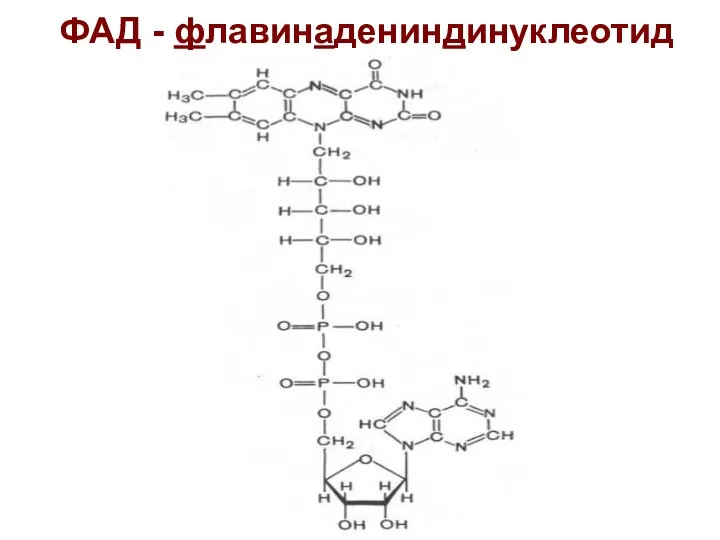
- 13. ФАД - флавинадениндинуклеотид
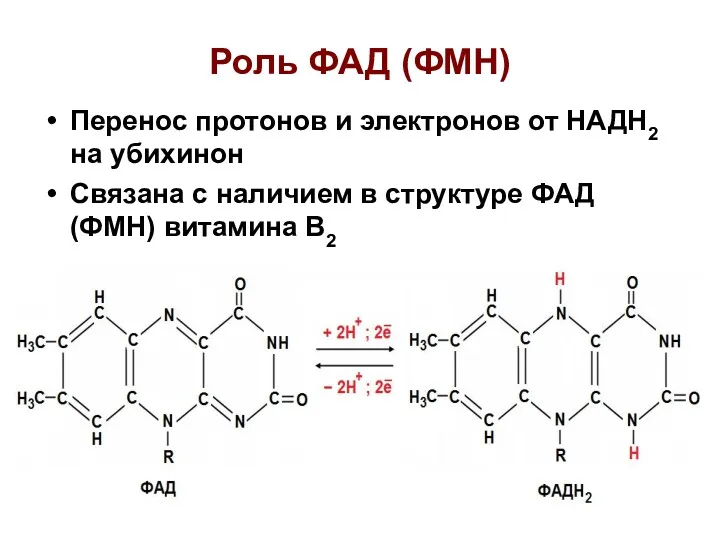
- 14. Роль ФАД (ФМН) Перенос протонов и электронов от НАДН2 на убихинон Связана с наличием в структуре
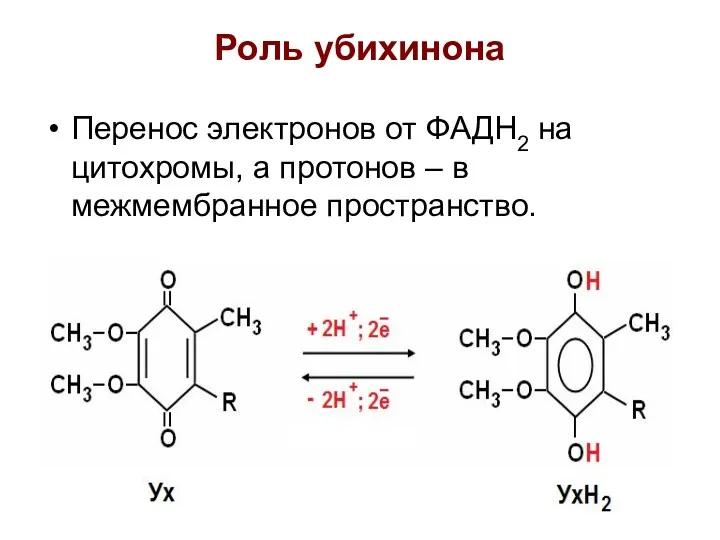
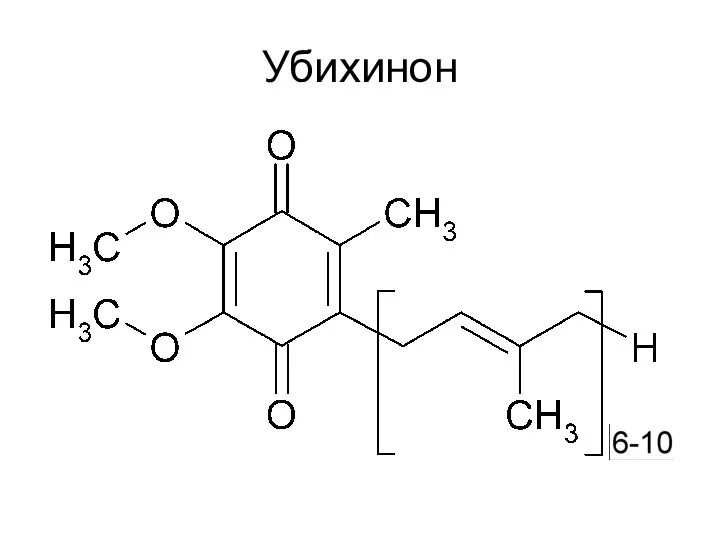
- 15. Роль убихинона Перенос электронов от ФАДН2 на цитохромы, а протонов – в межмембранное пространство.
- 16. Цитохромы (Цх) - гемсодержащие ферменты, осуществляют перенос электронов за счет изменения степени окисления атома железа в
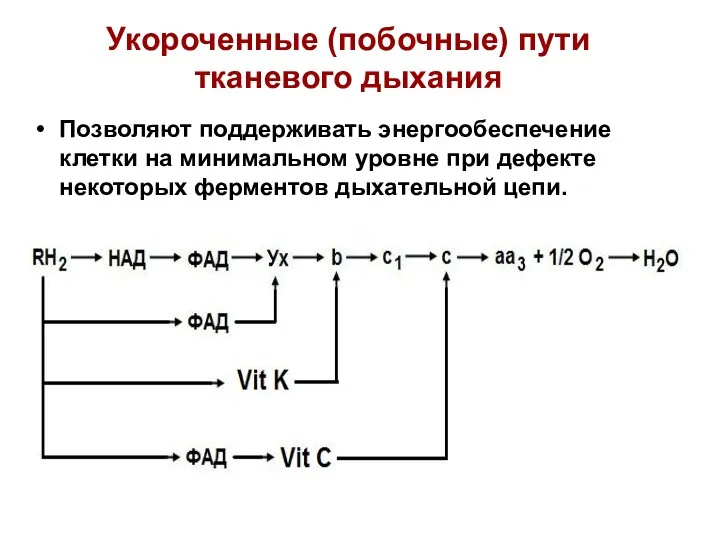
- 17. Укороченные (побочные) пути тканевого дыхания Позволяют поддерживать энергообеспечение клетки на минимальном уровне при дефекте некоторых ферментов
- 18. Дыхательный коэффициент отношение объема СО2, выделенного из легких, к объему поглощенного О2. RQ = CO2/O2 Для
- 19. Окислительное фосфорилирование - синтез АТФ из АДФ и Н3РО4 с затратой энергии тканевого дыхания.
- 20. - это внутренняя митохондриальная мембрана, т.к. благодаря её работе происходит сопряжение тканевого дыхания и окислительного фосфорилирования.
- 21. Пункты сопряжения ТД и ОФ в дыхательной цепи Между НАД и ФАД Между цитохромами b и
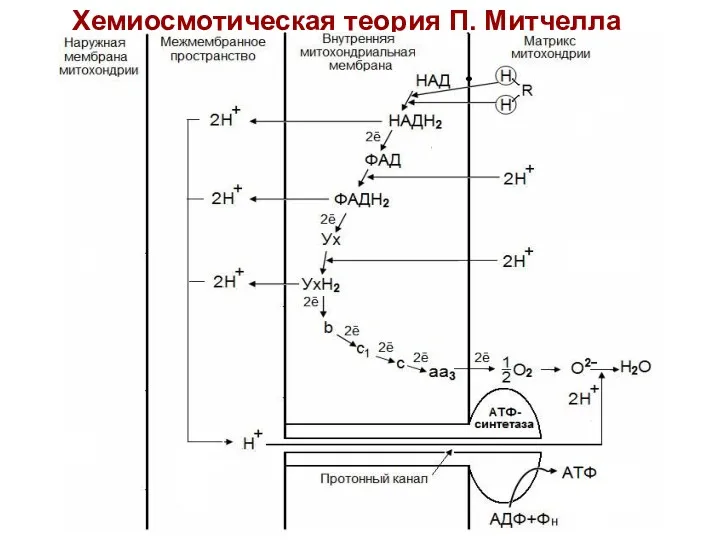
- 22. Хемиосмотическая теория П. Митчелла (1961-1966 гг) Дыхание и фосфорилирование связаны между собой через электрохимический потенциал Н+
- 24. ДГГ НАДН2 отдает пару ē на ДГГ ФАД, что позволяет ФАД принять пару протонов (Н+) из
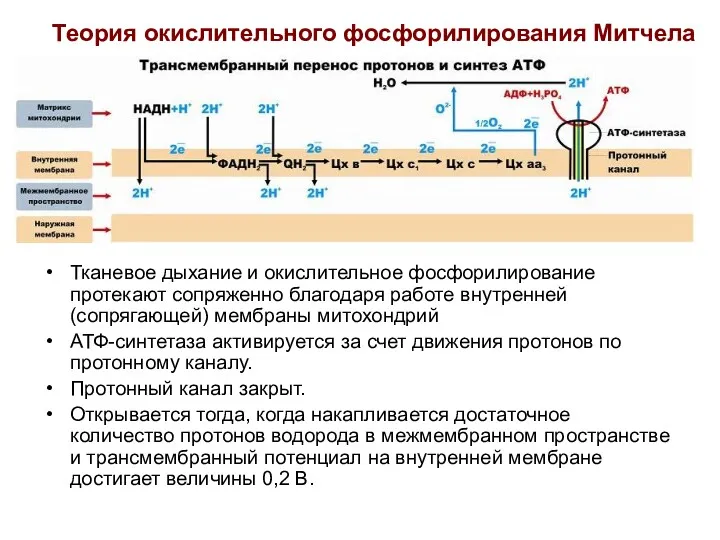
- 25. Разница потенциалов и разница рН обеспечивает движение протонов через протонный канал в матрикс. Протонный канал открывается,
- 26. Таким образом, тканевое дыхание заряжает митохондриальную мембрану, а окислительное фосфорилирование разряжает ее, используя энергию мембранного потенциала
- 27. Хемиосмотическая теория П. Митчелла
- 28. Коэффициент окислительного фосфорилирования (Р/О) - отношение количества связанной Н3РО4 к количеству поглощенного атомарного кислорода. Р/О для
- 29. Дыхательный контроль - усиление дыхания и фосфорилирования в митохондриях при увеличении концентрации АДФ
- 30. Виды фосфорилирования: Окислительное За счет энергии тканевого дыхания Субстратное 2 реакции в гликолизе Транс- (перефосфорилирование) Креатин
- 31. Роль АТФ: Энергия АТФ тратится на работу Механическую (мышечное сокращение) Химическую (анаболические процессы - синтез веществ)
- 32. соединения, при гидролизе которых высвобождается более 30 кДж/моль энергии. АТФ, ГТФ, ЦТФ и т.д., АДФ Креатинфосфат
- 33. Гипоэнергетические состояния - снижение синтеза АТФ. Причины: Гипоксия тканей (недостаток О2); Гиповитаминозы (образуется мало коферментов); Голодание
- 34. Разобщение тканевого дыхания и окислительного фосфорилирования - состояние, при котором потребление кислорода и окисление субстратов продолжаются,
- 35. Виды разобщения 1) физиологическое (холод, тироксин, кортикостероиды, женские половые гормоны) 2) медикаментозное (дикумарин) 3) токсическое (динитрофенол)
- 36. Ингибиторы ТД и ОФ а) ингибиторы электронного транспорта – это вещества, которые взаимодействуют с ферментами дыхательной
- 37. Микросомальное окисление Протекает в мембранах ЭПР (микросомах) клеток печени и коры надпочечников. Не дает клетке энергии
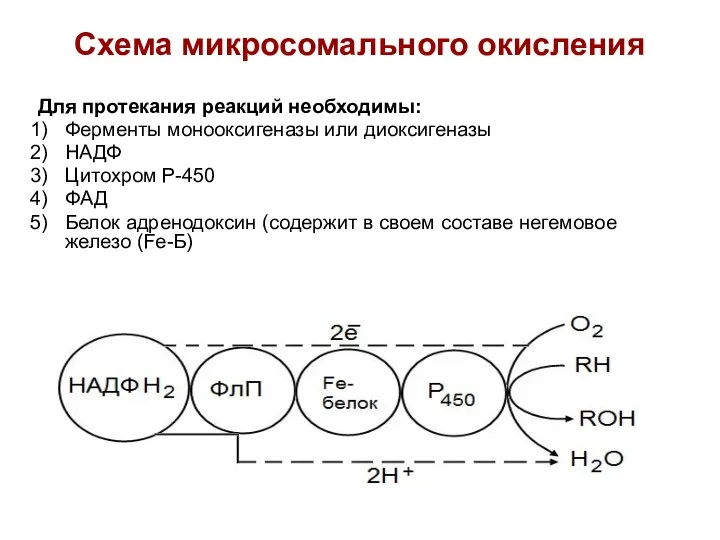
- 38. Схема микросомального окисления Для протекания реакций необходимы: Ферменты монооксигеназы или диоксигеназы НАДФ Цитохром Р-450 ФАД Белок
- 39. Активные формы кислорода (АФК) Это продукты неполного восстановления кислорода, содержащие неспаренные электроны. АФК являются свободными радикалами.
- 40. Вспомогательные ферменты тканевого дыхания 1) Супероксиддисмутаза (превращает супероксидные радикалы в менее токсичную перекись водорода); 2О2- +
- 41. Владимир Петрович Скулачев (род. 21 февраля 1935, Москва) Направление научной деятельности Механизмы биологического окисления: трансформации химической
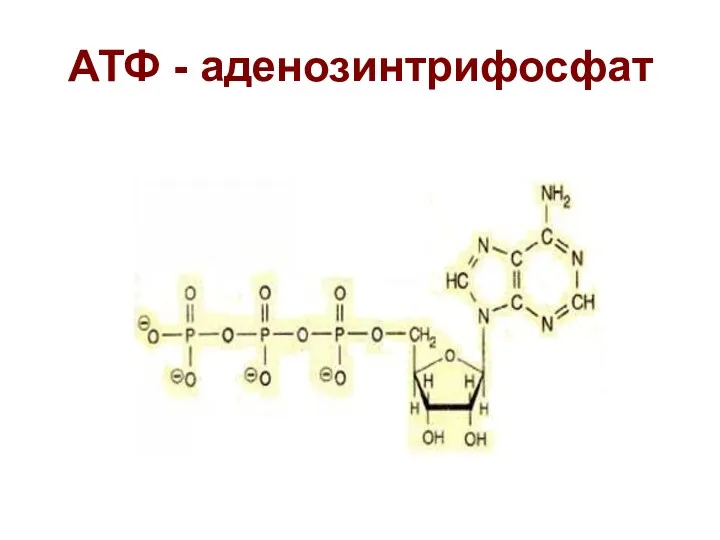
- 42. АТФ - аденозинтрифосфат
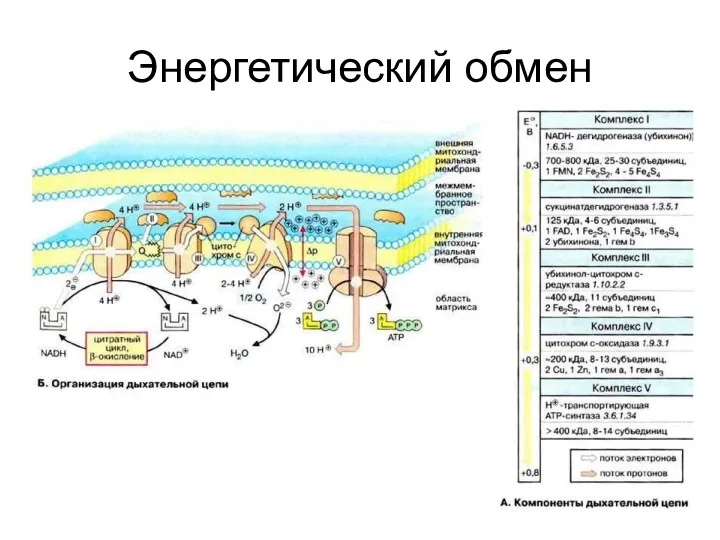
- 43. Энергетический обмен
- 44. Теория окислительного фосфорилирования Митчела Тканевое дыхание и окислительное фосфорилирование протекают сопряженно благодаря работе внутренней (сопрягающей) мембраны
- 45. Убихинон
- 46. Биохимические процессы протекающие в матриксе митохондрий и передающие водород в дыхательную цепь Цикл Кребса. Бета-окисление ВЖК.
- 48. Гипоэнергетические состояния Причины: алиментарные (голодание, гиповитаминозы РР, В2); гипоксические (нарушения доставки О2 в клетки); митохондриальные (действие
- 49. В живых клетках АФК образуются: в реакциях окисления гемоглобина в метгемоглобин; в реакциях, катализируемых оксидазами (пероксид
- 50. Негативное воздействие свободных радикалов на организм действуют на SH – группы белков, что ведет к их
- 51. Положительное воздействие свободных радикалов на организм: Обновление липидного состава мембран; Из арахидоновой кислоты образуются простагландины (ПГ)
- 52. Антиоксидантная защита Неферментативная защита. Важнейшим компонентом является витамин Е (токоферол), витамин размножения. Токоферол защищает ненасыщенные жирные
- 53. ФЕРМЕНТАТИВНАЯ АНТИОКСИДАНТНАЯ ЗАЩИТА КЛЕТКИ ОТ АФК Супероксиддисмутаза (превращает супероксидные радикалы в менее токсичную перекись водорода); Каталаза
- 55. Скачать презентацию





































 Методы исследования биологии
Методы исследования биологии Ферменты в генетической инженерии. Тема 2
Ферменты в генетической инженерии. Тема 2 Внешнее строение листа
Внешнее строение листа Клиническая физиология КЩС
Клиническая физиология КЩС Происхождение человека
Происхождение человека Цветок – орган генеративного размножения
Цветок – орган генеративного размножения General Musculoskeletal Screening: Upper Extremities
General Musculoskeletal Screening: Upper Extremities Эволюционные теории и взгляды
Эволюционные теории и взгляды Систематика растений
Систематика растений Дуб - царь деревьев
Дуб - царь деревьев Эпизоотологическое и эпидемиологическое значение грызунов. Дератизация
Эпизоотологическое и эпидемиологическое значение грызунов. Дератизация Значение водорослей в природе и жизни человека
Значение водорослей в природе и жизни человека презентация к уроку по теме: Цветок. Строение и значение цветка
презентация к уроку по теме: Цветок. Строение и значение цветка Антропогенез. Гипотезы возникновения человека. Сходство и различия человека и животных. Часть 4
Антропогенез. Гипотезы возникновения человека. Сходство и различия человека и животных. Часть 4 Живі фільтри
Живі фільтри Слух. Среднее и внутреннее ухо. Функции среднего уха. Строение улитки
Слух. Среднее и внутреннее ухо. Функции среднего уха. Строение улитки Анатомия и физиология ЦНС. Свойства и принципы функционирования нервных центров. Строение СМ. Цереброспинальная жидкость
Анатомия и физиология ЦНС. Свойства и принципы функционирования нервных центров. Строение СМ. Цереброспинальная жидкость Ферменты,структура и механизм действия. Классификация и номенклатура. (Лекция 4)
Ферменты,структура и механизм действия. Классификация и номенклатура. (Лекция 4) Практика по общей биологии
Практика по общей биологии Простейшие – эукариотические одноклеточные микроорганизмы
Простейшие – эукариотические одноклеточные микроорганизмы Главные направления эволюции органического мира
Главные направления эволюции органического мира Желудочная секреция
Желудочная секреция Строение, химический состав и жизнедеятельность растительной клетки
Строение, химический состав и жизнедеятельность растительной клетки презентация по биологии Экологическая задача Ч.Дарвина
презентация по биологии Экологическая задача Ч.Дарвина Nervové mechanismy regulace dýchání
Nervové mechanismy regulace dýchání Минеральные вещества
Минеральные вещества Что такое хвоинки
Что такое хвоинки Глюконеогенез. Регуляция гликолиза и глюконеогенеза. Цикл кори. Пентозофосфатный путь превращения глюкозы. Спиртовое брожение
Глюконеогенез. Регуляция гликолиза и глюконеогенеза. Цикл кори. Пентозофосфатный путь превращения глюкозы. Спиртовое брожение